El tratamiento del cáncer de recto por laparoscopia es controvertido por su complejidad técnica. Estudios prospectivos aleatorizados han demostrado claras ventajas para el paciente, con resultados oncológicos equiparables a la cirugía abierta, aunque durante el aprendizaje de esta cirugía puede existir un aumento de las complicaciones y peor pronóstico.
ObjetivoNuestro objetivo es analizar cómo influye la curva de aprendizaje del cáncer de recto por vía laparoscópica en los resultados intra y postoperatorios, así como en los marcadores oncológicos.
Pacientes y métodosSe realizó una revisión retrospectiva de los 120 primeros pacientes intervenidos de neoplasia de recto por vía laparoscópica. La población a estudio se ordenó cronológicamente por fecha de intervención y se dividió en un primer grupo que contenía las 40 primeras intervenciones, y un segundo grupo que contenía las 80 siguientes. Las intervenciones fueron realizadas por el mismo equipo quirúrgico con una amplia experiencia en el tratamiento del cáncer colorrectal abierto, además de estar capacitados para realizar cirugía laparoscópica avanzada. Se analizaron sexo, ASA, localización del tumor, neoadyuvancia, técnica quirúrgica, tiempo operatorio, conversión, complicaciones postoperatorias, estancia hospitalaria, número de ganglios, estadio y afectación de márgenes.
ResultadosSe observaron diferencias significativas en cuanto a tiempo quirúrgico (224min en el primer grupo, 204min en el segundo grupo), con una mayor tasa de conversión en el primer grupo (22,5%) frente al segundo (11,3%). No se apreciaron diferencias significativas en cuanto a la tasa de cirugía conservadora de esfínteres, estancia hospitalaria, complicaciones posquirúrgicas, número de ganglios afectos/aislados ni márgenes circunferencial y distal afectos.
ConclusiónEs posible realizar el aprendizaje de esta compleja cirugía sin comprometer la seguridad y resultado oncológico del paciente.
The treatment of rectal cancer via laparoscopy is controversial due to its technical complexity. Several randomized prospective studies have demonstrated clear advantages for the patient with similar oncological results to those of open surgery, although during the learning of this surgical technique there may be an increase in complications and a worse prognosis.
ObjectiveOur aim is to analyze how the learning curve for rectal cancer via laparoscopy influences intra- and postoperative results and oncological markers. A retrospective review was conducted of the first 120 patients undergoing laparoscopic surgery for rectal neoplasia. The operations were performed by the same surgical team with a wide experience in the treatment of open colorectal cancer and qualified to perform advanced laparoscopic surgery. We analyzed sex, ASA, tumour location, neoadjuvant treatment, surgical technique, operating time, conversion, postoperative complications, length of hospital stay, number of lymph nodes, stage and involvement of margins.
ResultsSignificant differences were observed with regard to surgical time (224min in the first group, 204min in the second group), with a higher rate of conversion in the first group (22.5%) than in the second (11.3%). No significant differences were noted for rate of conservative sphincter surgery, length of hospital stay, post-surgical complications, number of affected/isolated lymph nodes or affected circumferential and distal margins.
ConclusionsIt is possible to learn this complex surgical technique without compromising the patient's safety and oncological outcome.
Diversos estudios han demostrado que el tratamiento del cáncer de colon por vía laparoscópica tiene resultados oncológicos similares a la cirugía abierta, sin aumentar la morbimortalidad y ofreciendo al paciente las ventajas de la cirugía laparoscópica1–4.
Sin embargo, la cirugía laparoscópica en el cáncer de recto es más controvertida por su complejidad técnica, debido a su localización anatómica, necesidad de realizar una escisión total mesorrectal (ETM) con márgenes adecuados, la continuidad con el aparato esfinteriano y su vecindad con el plexo hipogástrico. Aun así, cada vez son más los estudios que demuestran que la cirugía laparoscópica en el cáncer de recto tiene unos resultados oncológicos y funcionales similares a los de la cirugía abierta5–9.
El aprendizaje de esta cirugía es técnicamente más complejo que la cirugía de resección colónica, y el adquirir la capacitación en la cirugía laparoscópica avanzada sigue siendo uno de los obstáculos para la aplicación generalizada de la cirugía laparoscópica colorrectal. Esta cirugía requiere la identificación de planos tisulares, sin lesionar las estructuras vecinas, como la próstata, la vagina y el plexo nervioso hipogástrico, entre otras, además de restaurar, en la gran mayoría de las ocasiones, el tránsito intestinal con anastomosis colorrectal, a veces de gran complejidad. Es necesario un período de formación inicial y poder alcanzar, mediante la repetición continua del proceso, la experiencia necesaria para realizar estos procedimientos complejos con seguridad, sin aumentar la morbimortalidad de esta cirugía ni comprometer los resultados oncológicos a largo plazo. Así, se ha descrito una mayor positividad del margen circunferencial10 y un aumento de fugas anastomóticas11 cuando se utiliza la cirugía laparoscópica para la resección de recto.
En este estudio presentamos los resultados a corto plazo del aprendizaje de la resección del cáncer de recto por vía laparoscópica y las consecuencias que ha tenido para el paciente la curva de aprendizaje del cirujano.
Pacientes y métodoSe realizó revisión retrospectiva de los 120 primeros pacientes intervenidos de neoplasia de recto por vía laparoscópica en nuestro hospital con histología de adenocarcinoma. La población a estudio se ordenó cronológicamente por fecha de intervención, y se dividió en un primer grupo que contenía las 40 primeras intervenciones y un segundo grupo que contenía las 80 siguientes. Fueron excluidos al inicio de la serie aquellos pacientes con índice de masa corporal (IMC) superior a 35 y los pacientes con cáncer de recto en su tercio inferior; conforme el cirujano fue adquiriendo experiencia estos pacientes se fueron incluyendo. Todos los pacientes fueron estudiados mediante exploración física, tacto rectal, colonoscopia total más biopsia, rectoscopia rígida, ecografía anorrectal, tomografía computarizada torácica y abdominal, resonancia magnética nuclear de recto y enema opaco en los pacientes sin colonoscopia completa. El anestesista valoró de forma preoperatoria a todos los pacientes y se determinó el score de la American Society of Anestesiologist (ASA).
Los pacientes con adenocarcinoma en estadio ii o iii (The International Union Against Cancer/American Joint Committee on Cancer [UICC/AJCC] colorectal cancer staging system) recibieron tratamiento neoadyuvante con quimiorradioterapia (QTRT) con la siguiente pauta: radioterapia (RT) pélvica 3 campos con 50-54Gy, 5 días a la semana, 1,8Gy/día, junto con capecitabina oral a la dosis de 1.000-1.500mg/m2/día durante todo el tiempo que duró la RT.
La intervención quirúrgica se realiza entre 6 y 8 semanas tras finalizar el tratamiento neoadyuvante. Los pacientes con metástasis a distancia resecables fueron intervenidos de forma metacrónica tras la recuperación de la cirugía del recto. En los pacientes con estadios iii y iv se administró quimioterapia adyuvante.
Las intervenciones fueron realizadas por el mismo equipo quirúrgico (L.J., H.Q.) con una amplia experiencia en el tratamiento del cáncer colorrectal abierto, además de estar capacitados para realizar cirugía laparoscópica avanzada. En todos los casos se realizó lavado anterógrado de colon con polietilenglicol, profilaxis antitrombótica con heparina de bajo peso molecular y profilaxis antibiótica con amoxicilina-clavulánico o metronidazol más gentamicina en alérgicos a los β-lactámicos.
En todos los pacientes se practicó una ETM con preservación de los nervios hipogástricos. En los casos en que el tumor infiltraba el músculo elevador del ano o no fuese posible obtener un margen distal mayor de 1cm se realizó una amputación abdominoperineal (AAP). Cuando se realizó una resección anterior (RA), las anastomosis fueron colorrectal lateroterminal mecánica o coloanal manual. Se asoció una ileostomía de protección en las resecciones anteriores, a criterio del cirujano, principalmente en los casos con tratamiento neoadyuvante, cuando la anastomosis fue laboriosa y en todas las anastomosis coloanales.
Técnica quirúrgicaSe crea el neumoperitoneo con una presión de 12-15mmHg, colocando los siguientes puertos de trabajo: uno supraumbilical de 11mm, 2 en la fosa ilíaca derecha de 5 y 12mm y otro en la fosa ilíaca izquierda de 5mm. Cuando fue preciso se colocó un quinto puerto de 10mm en la región suprapúbica para separar al nivel del fondo de saco de Douglas y ocasionalmente un puerto accesorio en el hemiabdomen superior derecho para el descenso del ángulo esplénico En los pacientes con resección anterior y anastomosis mecánica se realizó una mini laparotomía, habitualmente horizontal, para la extracción de la pieza y la colocación del cabezal de la grapadora de autosutura; la anastomosis se realizó intracorpórea. En las amputaciones abdominoperineales y en las resecciones anteriores con anastomosis coloanal manual, la pieza fue extraída por el periné, sin precisar incisión abdominal. Se realizó una conversión a laparotomía cuando no fue posible realizar la extirpación total del mesorrecto por laparoscopia debido a problemas técnicos o incidencias durante la disección.
El tratamiento de la herida del periné en todos los pacientes a los que se les realizó una AAP fue con drenaje-lavado postoperatorio12.
Todos los especímenes fueron analizados por el mismo patólogo experto, evaluando la afectación del margen circunferencial (distancia ≤1mm desde el tumor a la fascia mesorrectal), afectación del margen distal (tumor que alcanza la sección distal) y el número de ganglios aislados.
Se consideró fuga anastomótica clínica cuando se detectó la dehiscencia mediante examen digital o endoscopia y el paciente presentó peritonitis, salida de gas o material fecaloideo por el drenaje o absceso pélvico.
Se consideran complicaciones postoperatorias las que se producen durante el ingreso o condicionan el reingreso en los primeros 30 días postoperatorios.
Se analizaron el sexo, la edad, el IMC, el ASA, la localización del tumor, la técnica quirúrgica, el tiempo operatorio, la conversión y las complicaciones postoperatorias, la estancia, el número de ganglios y la afectación de márgenes.
Análisis estadísticoLos datos fueron procesados con el paquete estadístico SPSS 13.0 para Windows. Las comparaciones de 2 medias se realizaron con el test «t» de Student combinado con el test de Behrens-Fisher, según hubiera o no homogeneidad de varianzas entre las 2 muestras, o con el test no paramétrico de Mann-Whitney cuando los datos se distribuían claramente de manera no normal aun después de realizar la transformación logarítmica, como por ejemplo, los días de estancia.
Para el estudio de la relación entre variables cualitativas y la comparación de proporciones en muestras independientes se realizó un análisis de tablas de contingencia mediante el test Chi-cuadrado de Pearson y el subsiguiente análisis de residuos, o mediante el test exacto de Fisher.
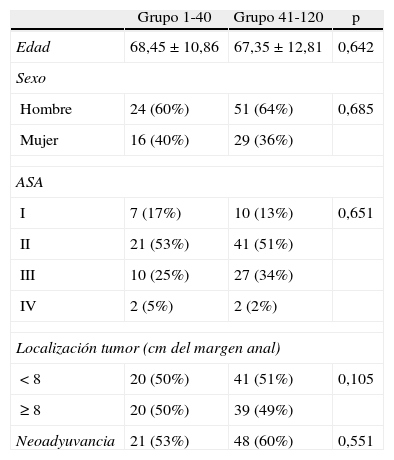
ResultadosLos 2 grupos eran homogéneos sin observar diferencias significativas (tabla 1).
Características de los 2 grupos de pacientes
| Grupo 1-40 | Grupo 41-120 | p | |
| Edad | 68,45±10,86 | 67,35±12,81 | 0,642 |
| Sexo | |||
| Hombre | 24 (60%) | 51 (64%) | 0,685 |
| Mujer | 16 (40%) | 29 (36%) | |
| ASA | |||
| I | 7 (17%) | 10 (13%) | 0,651 |
| II | 21 (53%) | 41 (51%) | |
| III | 10 (25%) | 27 (34%) | |
| IV | 2 (5%) | 2 (2%) | |
| Localización tumor (cm del margen anal) | |||
| <8 | 20 (50%) | 41 (51%) | 0,105 |
| ≥8 | 20 (50%) | 39 (49%) | |
| Neoadyuvancia | 21 (53%) | 48 (60%) | 0,551 |
ASA: American Society of Anesthesiologists.
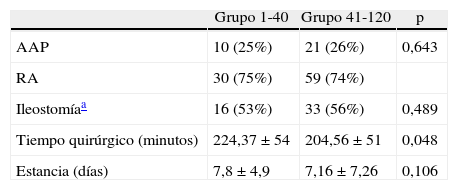
La tasa global de cirugía conservadora de esfínteres fue del 74% sin diferencias entre los 2 grupos. Se realizó ileostomía de protección en el 48% de los pacientes con cirugía conservadora de esfínteres, sin diferencias entre los grupos. El tiempo quirúrgico fue de 224, 37min en el grupo 1-40 y de 204,56min en el grupo 41-120, con diferencias significativas. La estancia fue similar en ambos grupos (tabla 2).
Resultados en los 2 grupos de pacientes
| Grupo 1-40 | Grupo 41-120 | p | |
| AAP | 10 (25%) | 21 (26%) | 0,643 |
| RA | 30 (75%) | 59 (74%) | |
| Ileostomíaa | 16 (53%) | 33 (56%) | 0,489 |
| Tiempo quirúrgico (minutos) | 224,37±54 | 204,56±51 | 0,048 |
| Estancia (días) | 7,8±4,9 | 7,16±7,26 | 0,106 |
AAP: amputación abdominoperineal; RA: resección anterior.
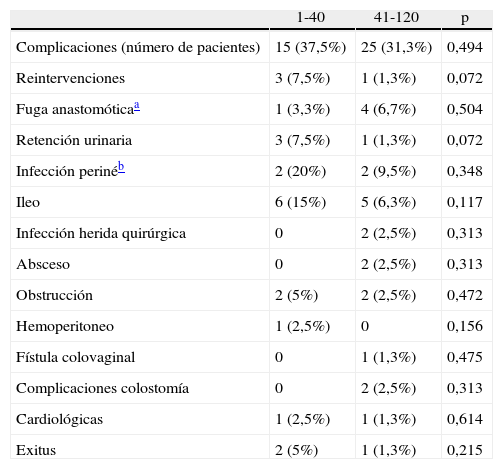
En el grupo 1-40 se realizó conversión a cirugía abierta en 9 pacientes (22,5%) y en el grupo 41-120 en 9 pacientes (11,3%). Estas diferencias no son significativas probablemente debido a un error estadístico tipo ii. Se produjeron complicaciones en 15 pacientes (37,5%) del grupo 1-40 y en 25 pacientes (31,3%) del grupo 41-120 sin diferencias entre grupos. Tampoco hay diferencias al analizar las complicaciones una a una. Se produjeron 2 exitus (5%) en el grupo 1-40 y uno (1,3%) en el grupo 41-120 sin diferencias significativas (tabla 3). Los 3 exitus que se han producido han sido por causas ajenas a la cirugía. Dos de ellos por problemas cardiológicos y otro de ellos por problemas respiratorios.
Complicaciones postoperatorias y distribución
| 1-40 | 41-120 | p | |
| Complicaciones (número de pacientes) | 15 (37,5%) | 25 (31,3%) | 0,494 |
| Reintervenciones | 3 (7,5%) | 1 (1,3%) | 0,072 |
| Fuga anastomóticaa | 1 (3,3%) | 4 (6,7%) | 0,504 |
| Retención urinaria | 3 (7,5%) | 1 (1,3%) | 0,072 |
| Infección perinéb | 2 (20%) | 2 (9,5%) | 0,348 |
| Ileo | 6 (15%) | 5 (6,3%) | 0,117 |
| Infección herida quirúrgica | 0 | 2 (2,5%) | 0,313 |
| Absceso | 0 | 2 (2,5%) | 0,313 |
| Obstrucción | 2 (5%) | 2 (2,5%) | 0,472 |
| Hemoperitoneo | 1 (2,5%) | 0 | 0,156 |
| Fístula colovaginal | 0 | 1 (1,3%) | 0,475 |
| Complicaciones colostomía | 0 | 2 (2,5%) | 0,313 |
| Cardiológicas | 1 (2,5%) | 1 (1,3%) | 0,614 |
| Exitus | 2 (5%) | 1 (1,3%) | 0,215 |
El examen anatomopatológico del espécimen fue similar en el número de ganglios aislados y en la afectación del margen circunferencial y radial, sin diferencias significativas (tabla 4).
DiscusiónLa cirugía laparoscópica colorrectal requiere un alto grado de destreza y habilidades técnicas, aún más en el cáncer de recto, ya que es técnicamente muy demandante por la complejidad que supone por un lado el realizar una escisión total mesorrectal, por otro la sección distal mecánica del recto bajo, para realizar una anastomosis coloanal o en caso contrario una amputación abdominoperineal, y el realizar una identificación y preservación de los nervios autonómicos, todo ello cumpliendo los principios oncológicos de adecuados márgenes (circunferencial y distal) y ligadura proximal de la arteria que nutre al tumor. Esto hace imprescindible, para la mayoría de los cirujanos, un periodo de formación inicial, con una continua repetición del procedimiento, para llegar a ser técnicamente competentes en la cirugía laparoscópica del cáncer de recto. Conseguir adquirir la destreza necesaria para realizar esta cirugía laparoscópica avanzada, sin comprometer la seguridad del paciente, sigue siendo uno de los obstáculos más importantes para su generalización.
En nuestra unidad hemos seguido un protocolo para el aprendizaje de la cirugía del cáncer de recto por laparoscopia. Los cirujanos que la realizan deben tener una amplia experiencia en el tratamiento del cáncer colorrectal abierto, además de estar capacitados para realizar cirugía laparoscópica avanzada. Otros estudios han demostrado que puede iniciarse el aprendizaje de la cirugía laparoscópica de cáncer de recto sin necesidad de tener experiencia en cirugía abierta del colon13. Pensamos que actualmente es difícil llevar a cabo estos programas de formación de forma generalizada, debido a que no está totalmente extendida la cirugía laparoscópica del colon y menos la del recto. Los cirujanos que deben enseñarla aún están en periodo de formación, o ni siquiera la han iniciado. Nosotros, previa a esta cirugía, habíamos iniciado las resecciones de colon derecho e izquierdo por vía laparoscópica. Durante el aprendizaje solo 2 cirujanos realizaban las intervenciones quirúrgicas de cáncer de recto (L.J. y H.Q.), ya que como es un procedimiento técnicamente exigente, complejo, que requiere un alto grado de destreza y habilidades técnicas, los cirujanos se compenetran durante la cirugía y tienen la oportunidad de compartir experiencias y aprender entre sí.
En nuestro protocolo otro factor importante ha sido la selección del paciente. Para obtener unos buenos resultados en el aprendizaje de la cirugía colorrectal es imprescindible la selección de los pacientes al inicio del aprendizaje, como sugieren diferentes autores14 que excluyen a pacientes complejos y de alto riesgo. Debemos evitar al principio del aprendizaje pacientes obesos y grandes tumores que son factores que van a influir en la complejidad de la cirugía y consiguientemente en la conversión a cirugía abierta15,16. Con el aumento de la experiencia se pueden ir incrementando las indicaciones de cirugía laparoscópica en cáncer de recto. En nuestra serie al principio éramos muy selectivos a la hora de seleccionar los pacientes, y progresivamente el criterio no fue tan estricto, sin aumentar las complicaciones y disminuyendo el número de conversiones.
La incidencia de conversión a cirugía abierta varía enormemente entre el 5-20% según las series publicadas17–20. La conversión en sí no es una complicación, aunque se ha relacionado con un mayor número de complicaciones21,22. Este aumento de conversiones a cirugía abierta puede ser debido a una mayor complejidad de los pacientes que precisan conversión, y esto no compromete los resultados oncológicos de la cirugía22. Durante la curva de aprendizaje está relacionada con la selección de los pacientes, la habilidad y experiencia del cirujano, y no se puede considerar como un fallo del procedimiento laparoscópico, sino más bien como una apelación al sentido común del cirujano; de hecho, cuanto más alto es el umbral para la conversión mayores pueden ser las complicaciones. Así, Bege et al.23 no observan una variación significativa de la incidencia de conversión (16% durante el aprendizaje y 14% una vez superado este), aunque el número de complicaciones fue del 52% en el periodo de aprendizaje y del 32% una vez finalizado este, a pesar de que la complejidad de los pacientes aumentó. En nuestra serie al principio el umbral de conversión era muy bajo, y cuando ocurría alguna complicación que no se podía solucionar fácilmente por laparoscopia, por pequeña que fuera, o existía dificultad en el avance de la cirugía de escisión mesorrectal o movilización del ángulo esplénico, o había imposibilidad de introducir bien la endocortadora para la sección del margen distal o cualquier otra incidencia que podría comprometer la seguridad de la cirugía y del paciente, se realizaba conversión a cirugía abierta.
El tiempo quirúrgico es un parámetro que juega en contra de la cirugía laparoscópica, debido a que en la mayoría de las series es mayor por cirugía laparoscópica que en abierta. Muchos estudios limitan el aprendizaje de la cirugía laparoscópica colorrectal al tiempo quirúrgico, y utilizar este único indicador para juzgar la competencia quirúrgica tal vez no sea del todo correcto24. Cuando el cirujano inicia el aprendizaje de esta cirugía laparoscópica o cualquier otra cirugía no debe entrar al quirófano con el cronómetro en la mano. Debe estar libre de todo tipo de presiones como la programación quirúrgica, el servicio de anestesia o el personal del quirófano. Lo más importante es saber que se está realizando la intervención de forma correcta y que se avanza lento pero seguro. Conforme vaya aumentando la experiencia del equipo quirúrgico el tiempo será menor, con la misma seguridad para el paciente.
En nuestro estudio la tasa de complicaciones postoperatorias se ha mantenido estable dentro de los límites publicados en la literatura sin diferencias significativas entre ambos grupos. Ello ha sido debido probablemente a la experiencia en cirugía colorrectal y laparoscopia avanzada de los cirujanos y a la selección de los pacientes al inicio de la serie. Puede ser que con el aumento de la experiencia y el incremento de las indicaciones ocurra un aumento de complicaciones como ha sucedido en otras series25. Así, Ito et al.26 hallan mayores tasas de fugas de la anastomosis y reoperaciones en la fase donde los cirujanos tenían más experiencia que en la fase inicial, debido a que incluyeron más pacientes con cáncer del tercio medio y bajo en la fase final del aprendizaje.
Algunas publicaciones han demostrado que la supervivencia no solo está ligada a la metástasis en los ganglios linfáticos, sino también al número de ganglios aislados27. Por ello, se ha sugerido que un mínimo número de ganglios linfáticos deben ser examinados para proporcionar el estadio adecuado del cáncer y poder aplicar el correcto tratamiento adyuvante28. La recidiva local en algunos casos fue mayor durante el aprendizaje25, y ello puede ser debido a la falta de habilidad en la manipulación del mesorrecto con las pinzas que puede dar lugar a rotura de la fascia mesorrectal y la apertura del recto, y con ello mayores tasas de recidiva local. No ha habido diferencias estadísticamente significativas en ambos grupos con respecto a la supervivencia, los ganglios y el número de recidivas, probablemente debido a la experiencia previa en escisión total mesorrectal por cirugía abierta y a que, para nosotros, la cirugía laparoscópica es un medio, no un fin, con un bajo umbral para la conversión a cirugía abierta.
ConclusiónPara el correcto aprendizaje de la cirugía laparoscópica del cáncer de recto es necesario tener una adecuada formación en la escisión mesorrectal abierta y cirugía laparoscópica avanzada, seleccionar a los pacientes al inicio del aprendizaje y tener un umbral bajo para la conversión a cirugía abierta. De esta forma es posible realizar el aprendizaje de esta compleja cirugía sin comprometer la seguridad y el resultado oncológico del paciente.
Conflicto de interesesLos autores declaran no que no existe conflicto de intereses.