Determinar la seguridad de la traqueotomía percutánea por dilatación (TPD) en los pacientes receptores de un trasplante hepático.
Pacientes y métodoSe revisaron las historias de los pacientes ingresados para control postoperatorio de trasplante hepático (n=291) entre octubre de 2007 y abril de 2013. En este periodo 25 pacientes trasplantados hepáticos requirieron la realización de una TPD. Se analizaron entre otros: índices de gravedad (APACHE II y SAPS II), número de días desde la intubación, razón PO2/FiO2, estudios de coagulación y complicaciones. Se compararon los resultados con la población general de pacientes críticos y las publicaciones similares en la literatura.
ResultadosLa mediana de edad fue 58 años (RIC 47-65) y el 64% de los pacientes eran varones. La mediana desde la intubación hasta la TPD fue 11 días (RIC 6,5-15,5) y desde el trasplante hasta la TPD, 12 días. La mediana de la PO2/FiO2 fue de 212 (RIC 177-259). El recuento de plaquetas mostró valores menores en los pacientes trasplantados 89 (RIC 37-149) vs. 272 (RIC 186-381), p=0,001.
Las complicaciones incluyeron: sangrado clínicamente significativo, 8 frente al 0,3% de los pacientes críticos no trasplantados (p=0,005), infección del estoma en el 4% y neumonía asociada a ventilación mecánica en el 16% (frente al 2,8% del resto de pacientes críticos, p=0,007). No hubo muertes relacionadas con el procedimiento.
ConclusionesLa TPD es bien tolerada en los pacientes ingresados en UCI para el control postoperatorio de trasplante hepático y presenta una tasa relativamente baja de complicaciones graves y mortalidad relacionada con el procedimiento.
To determinate the safety of percutaneous dilatational tracheostomy (PDT) on hepatic allograft recipients.
Patients and methodsWe reviewed the records of patients who underwent liver transplantation between October 2007 and April 2013, followed by PDT. In this time period, 25 liver recipients underwent PDT in our intensive care unit. We recorded severity index scores such as APACHE II and SAPS II, number of days since intubation, ratios of PaO2/FiO2 (arterial oxygen pressure to fraction of inspired oxygen), coagulation study findings, complications, and procedure-related mortality rates. We compared these records with the general ICU population and literature reports.
ResultsThe median age was 58 (IC range 47-65) and 64% were men. The median time since intubation to PDT was 11 days (IC range 6.5-15.5) and from transplant to PDT 12 days. The median ratio of PaO2/FiO2 was 212 (IC range 177-259). The median platelet count was 89 (IC range 37-149), significantly lower than the general ICU population (272 (IC range 186-381) P=.001).
Complications were infrequent and included clinically remarkable major bleeding 8% (vs. 0,3% in general ICU population; P=.005), peristomal infection (4%) and ventilator-associated pneumonia 16% (vs. 2,8% in general ICU population; P=.007). There were no deaths associated with the procedures.
ConclusionPDT was tolerated well in recipients of liver allografts and had a relatively low risk of major complications and a low procedure-related mortality rate.
Los pacientes operados mediante trasplante ortotópico hepático (TOH) presentan algunas peculiaridades en sus requerimientos de monitorización y tratamiento, incluida la inmunosupresión, por lo que es habitual su ubicación en un área específica para una mejor adhesión a los protocolos de actuación1, de modo que el cuidado del postoperatorio, especialmente en los primeros días, se ha consolidado como una de las competencias de las unidades de cuidados intensivos (UCI). Tanto el procedimiento quirúrgico como el postoperatorio del TOH son procesos con una relativa baja morbimortalidad en manos de equipos experimentados, aunque no exentos de posibles complicaciones graves. Entre las complicaciones más habituales en el postoperatorio del TOH habría que incluir tanto las ligadas a la disfunción del órgano implantado (disfunción primaria del injerto, rechazo agudo, trombosis arterial, etc.), como las infecciones favorecidas por el tratamiento inmunosupresor, siendo, especialmente, la neumonía y la insuficiencia respiratoria asociada las que obligan a perpetuar la ventilación mecánica2–5. Ante la necesidad de esta ventilación mecánica prolongada, la evidencia reciente indica que la realización de una traqueotomía antes de transcurrida la primera semana tras el inicio de la ventilación mecánica podría presentar algunos potenciales beneficios respecto a la intubación orotraqueal6–8. Ejemplo de ello sería la reducción del tiempo de ventilación mecánica y de estancia en UCI, así como la disminución de la incidencia de neumonía asociada al ventilador, si bien, estos efectos beneficiosos no son constantes en la literatura9,10.
A pesar de las ventajas documentadas11–13 a favor de la traqueotomía percutánea por dilatación (TPD), existen pocos estudios en los que se haya evaluado su eficacia-conveniencia y comprobado su seguridad en los pacientes ingresados en UCI para control postoperatorio de TOH14,15.
Con estas consideraciones, el objetivo del presente estudio fue evaluar los resultados y seguridad de la TPD en un grupo de pacientes operados con TOH, mediante la comparación con el resto de procedimientos de TPD realizados en los pacientes críticos ingresados en nuestra Unidad por motivos diferentes al TOH.
Material y métodosEl presente estudio se realizó en una Unidad de Medicina Intensiva polivalente de 32 camas, 6 de las cuales están destinadas a los pacientes operados mediante TOH o trasplante de otro órgano sólido. El cuidado postoperatorio inmediato se realiza en estrecha colaboración entre los miembros de la Unidad asignados a esta área y el Servicio de Cirugía General y de Aparato Digestivo responsable de esta actividad. Las 6 camas disponen de la monitorización electrocardiográfica y hemodinámica habitual con un sistema computarizado (ICIP®). Los pacientes ingresados para el control postoperatorio de TOH son atendidos bajo un protocolo específico que contempla, además de los controles habituales, la medición de los débitos de los diferentes sistemas de drenado emplazados durante la cirugía, la evaluación seriada de las pruebas de la función hepática, de coagulación y de la posible respuesta inflamatoria. La población del presente estudio la constituyó aquellos pacientes operados de TOH ingresados en nuestra unidad durante el periodo comprendido entre octubre de 2007 y abril de 2013 y que precisaron TPD (25 pacientes). En todos los casos la TPD se realizó, in situ «a pie de cama» y se efectuó por al menos 2 facultativos especialistas en Medicina Intensiva o por residentes de dicha especialidad. La supervisión del procedimiento se verificó en todos los casos por un especialista en Medicina Intensiva.
La indicación de la TPD se estableció por criterios clínicos habituales de los médicos responsables, apoyados en escores de propensión que intenten anticipar la eventual necesidad de ventilación mecánica prolongada (incluyendo entre otros: insuficiencia respiratoria con infiltrados radiológicos pulmonares, bajo nivel de conciencia de origen estructural, disfunción multiorgánica, desnutrición severa).
La técnica de TPD utilizada es una variante menor del procedimiento descrito por Ciaglia en 198516. La mayor parte de los pacientes fueron sedados con sedoanalgesia intravenosa profunda, mediante midazolan más fentanilo y atracurio de forma facultativa; posteriormente, se procedió a la realización de la técnica siguiendo los pasos habituales16.
Tras concluir el procedimiento, se obtuvo una gasometría arterial y una radiografía de tórax17.
Para todos los procedimientos se utilizó el kit de traqueotomía percutánea: Portex ULTRAperc® (Smiths Medical).
Se recogieron prospectivamente variables relativas a la situación basal del paciente (edad, sexo, comorbilidades); aquellas con relación a los índices de gravedad al ingreso (APACHE II, SAPS II y SAPS III), parámetros de coagulación (ttpa, recuento de plaquetas y actividad de protrombina), y situación ventilatoria previa (presión parcial de oxígeno entre fracción inspirada de oxígeno [PO2/FiO2]). Adicionalmente, se recogieron, entre otras variables, el número de días de ventilación mecánica previos y posteriores a la TPD y el motivo para su indicación. Respecto a las complicaciones, se contemplaron tanto aquellas relacionadas con el procedimiento (tales como la ocurrencia de hemorragia, infección local del estoma, atelectasia, lesiones esofágicas, neumotórax, o muerte) como aquellas potencialmente atribuibles (aparición de neumonía, sangrado diferido del estoma, etc.).
Respecto a las complicaciones hemorrágicas y con objeto de minimizar la subjetividad del observador se aplicó la siguiente consideración:
- -
Sangrado mayor: se consideró todo aquel que precisó revisión quirúrgica o caída del hematocrito>8 puntos.
- -
Sangrado menor: se consideró todo aquel sangrado de escasa cuantía al que se hacía cualquier referencia en al menos 4 de las siguientes 6 notas de evolución de enfermería posteriores al procedimiento de la TPD.
Respecto a las complicaciones infecciosas se consideró como infección de la traqueotomía la presencia de signos inflamatorios en los labios del estoma. Se realizó radiografía simple de tórax para el diagnóstico posprocedimiento de atelectasia o de neumotórax. Para el resto de complicaciones se utilizaron los criterios diagnósticos habituales.
A efectos del estudio y respecto al desenlace final de los pacientes al alta de la UCI contemplamos 3 posibilidades: muerte durante su ingreso en UCI por cualquier causa; alta desde la UCI a planta de hospitalización con mantenimiento de la cánula de traqueotomía y alta desde la UCI a planta tras la retirada bien tolerada de la cánula.
En todos los procedimientos electivos se cumplimentó el consentimiento informado por parte del paciente o su representante legal.
Análisis estadísticoLos resultados de la TPD en el grupo de 25 pacientes con TOH (TOH) fueron comparados con los de los 781 pacientes operados mediante TPD cuyo motivo de ingreso en UCI no fue por control postoperatorio de TOH (no-TOH). Las variables fueron consideradas en función de su distribución. Para aquellas variables categóricas se utilizó el test de chi cuadrado. Las variables con distribución no normal fueron comparadas mediante la U de Mann-Whitnney.
El soporte para el tratamiento de los datos se realizó con el paquete estadístico Statistical Package for the Social Sciences (SPSS) en su versión 20.0.
ResultadosDurante el periodo del estudio fueron atendidos en nuestra unidad 291 pacientes para control postoperatorio de trasplante TOH. De entre ellos, 25 pacientes (8,6%) presentaron complicaciones que obligaron a prolongar la ventilación mecánica y se indicó la traqueotomía, realizada en todos los casos mediante TPD. Durante el periodo mencionado ningún paciente con TOH fue operado por traqueotomía quirúrgica convencional. Durante ese mismo periodo, se realizaron otras 781 TPD en los pacientes ingresados en nuestra Unidad por motivos diferentes al cuidado postoperatorio del TOH. Las causas últimas que motivaron la indicación de la TPD por orden de frecuencia fueron la insuficiencia respiratoria en 16 casos, el coma en 5 casos y el fracaso multiorgánico en los 4 casos restantes.
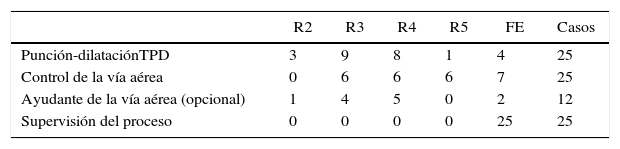
Respecto a las diferentes responsabilidades en la realización del procedimiento, en todos los casos la supervisión directa corrió a cargo de un especialista en Medicina Intensiva. La punción percutánea y subsiguiente dilatación la realizó un facultativo especialista o un residente mayor excepto en 3 casos en que la realizó un residente menor de tercer año (tabla 1).
Responsabilidades en la realización de los 25 casos de TPD
| R2 | R3 | R4 | R5 | FE | Casos | |
|---|---|---|---|---|---|---|
| Punción-dilataciónTPD | 3 | 9 | 8 | 1 | 4 | 25 |
| Control de la vía aérea | 0 | 6 | 6 | 6 | 7 | 25 |
| Ayudante de la vía aérea (opcional) | 1 | 4 | 5 | 0 | 2 | 12 |
| Supervisión del proceso | 0 | 0 | 0 | 0 | 25 | 25 |
FE: facultativo especialista; R2: residente de segundo año; R3 residente de tercer año; R4: residente de cuarto año; R5: residente de quinto año; TPD: traqueotomía percutánea por dilatación.
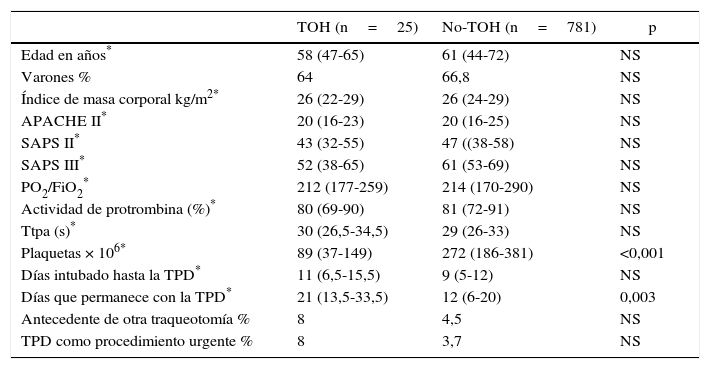
Las características basales de los pacientes con TOH y los no-TOH se reflejan en la (tabla 2). Respecto a los pacientes no-TOH, los TOH presentaron como única diferencia estadísticamente significativa un menor recuento de plaquetas y un mayor número de días portando la cánula de traqueotomía durante su estancia en la UCI. Asimismo, existió una tendencia que no fue estadísticamente significativa a realizar la TPD más precozmente en los pacientes del grupo no-TOH respecto a los del TOH.
Características de los pacientes
| TOH (n=25) | No-TOH (n=781) | p | |
|---|---|---|---|
| Edad en años* | 58 (47-65) | 61 (44-72) | NS |
| Varones % | 64 | 66,8 | NS |
| Índice de masa corporal kg/m2* | 26 (22-29) | 26 (24-29) | NS |
| APACHE II* | 20 (16-23) | 20 (16-25) | NS |
| SAPS II* | 43 (32-55) | 47 ((38-58) | NS |
| SAPS III* | 52 (38-65) | 61 (53-69) | NS |
| PO2/FiO2* | 212 (177-259) | 214 (170-290) | NS |
| Actividad de protrombina (%)* | 80 (69-90) | 81 (72-91) | NS |
| Ttpa (s)* | 30 (26,5-34,5) | 29 (26-33) | NS |
| Plaquetas × 106* | 89 (37-149) | 272 (186-381) | <0,001 |
| Días intubado hasta la TPD* | 11 (6,5-15,5) | 9 (5-12) | NS |
| Días que permanece con la TPD* | 21 (13,5-33,5) | 12 (6-20) | 0,003 |
| Antecedente de otra traqueotomía % | 8 | 4,5 | NS |
| TPD como procedimiento urgente % | 8 | 3,7 | NS |
NS: no significativo; TOH: trasplante ortotópico hepático; TPD: traqueotomía percutánea por dilatación; TTPA: tiempo de tromboplastina parcial activada.
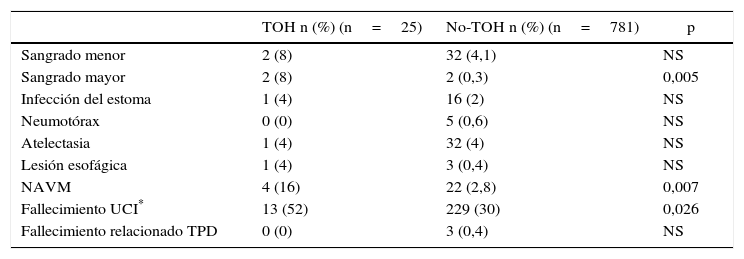
En cuanto a la incidencia de las complicaciones (tabla 3) en relación con la TDP, el sangrado mayor se evidenció más frecuentemente en el grupo TOH, aunque se limitó a 2 pacientes, si bien en ambos casos la hemorragia se controló en la UCI con medidas de compresión y sutura simple de un vaso sin necesidad de reconvertir a un procedimiento quirúrgico abierto, y sin comportar complicaciones graves que hicieran peligrar la vida del paciente. Con respecto a la incidencia de neumonía asociada a ventilación mecánica (NAVM), apreciamos una tasa significativamente mayor en el grupo TOH respecto al control (no-TOH).
Complicaciones asociadas a la TPD
| TOH n (%) (n=25) | No-TOH n (%) (n=781) | p | |
|---|---|---|---|
| Sangrado menor | 2 (8) | 32 (4,1) | NS |
| Sangrado mayor | 2 (8) | 2 (0,3) | 0,005 |
| Infección del estoma | 1 (4) | 16 (2) | NS |
| Neumotórax | 0 (0) | 5 (0,6) | NS |
| Atelectasia | 1 (4) | 32 (4) | NS |
| Lesión esofágica | 1 (4) | 3 (0,4) | NS |
| NAVM | 4 (16) | 22 (2,8) | 0,007 |
| Fallecimiento UCI* | 13 (52) | 229 (30) | 0,026 |
| Fallecimiento relacionado TPD | 0 (0) | 3 (0,4) | NS |
Expresado como número de casos (porcentaje).
NAVM: neumonía asociada a ventilación mecánica; TOH: trasplante ortotópico hepático; TPD: traqueotomía percutánea por dilatación; UCI: unidad de cuidados intensivos.
En lo relativo al desenlace final de los pacientes al alta de la UCI, los del grupo TOH presentaron una mayor mortalidad en la Unidad frente al grupo de pacientes no-TOH (52 vs. 30%; p=0,026). También existió una mayor proporción de pacientes a los que se les consiguió retirar la cánula de traqueotomía antes de ser dados de alta a la planta, a favor de los pacientes no-TOH respecto a los TOH (25 vs. 8%; p=0,007).
Respecto al porcentaje de complicaciones totales, en nuestra serie, no hemos encontrado diferencias significativas en función de que el procedimiento fuera realizado por un R3 de UCI (13,9%), un R4 (12,4%), un R5 (11,6%) o un adjunto (13,5%).
DiscusiónLa TPD descrita por Ciaglia en 198516 ha ganado una amplia aceptación respecto a la traqueotomía quirúrgica convencional. Incluye entre las principales ventajas la TPD su fácil realización a la cabecera del paciente por facultativos no entrenados específicamente en el campo quirúrgico, la rapidez de su realización y su coste económico reducido. Adicionalmente, la TPD parece acompañarse de menos complicaciones18. Probablemente por todas estas razones, se ha convertido en muchos casos en la técnica de elección a la hora de realizar una traqueotomía al paciente crítico19–22.
La práctica de la TPD en el postoperatorio inmediato de los pacientes operados mediante TOH se muestra como una técnica segura, comparable a la realizada en otros pacientes. Esta afirmación hay que ponderarla con el hecho de que la evidencia de sangrado mayor, en nuestra serie, fue más frecuente en los pacientes TOH. Si bien este hecho puede ser atribuible al azar, puesto que se dio en solo 2 casos dentro de un relativo reducido número de pacientes, no es descartable que una mayor propensión a la hemorragia en los pacientes con TOH sea atribuible al menor número de plaquetas asociado a este grupo y a la posible disfunción plaquetaria. Nuestros resultados coinciden con la serie de Andrew et al.14 en la que también evidencian 2 complicaciones hemorrágicas mayores en la mayor serie publicada de pacientes operados mediante TPD en el postoperatorio del trasplante de órganos sólidos. Igualmente, el mencionado trabajo hace referencia a las condiciones de comorbilidad en el momento de la TPD pero no aporta la evaluación de las escalas de severidad pronóstica habituales (APACHE, SAPS).
A pesar de estas consideraciones, a la vista de nuestros datos, en la práctica de cualquier procedimiento invasivo, incluida la TPD, es obligado ser especialmente cauto y tener en cuenta que los pacientes operados mediante TOH presentan frecuentemente alteraciones severas de la coagulación, reciben gran cantidad de hemoderivados, incluidos los concentrados de plaquetas, potencialmente disfuncionantes, que los hacen potencialmente un grupo con alto riesgo de complicaciones hemorrágicas23.
Respecto a las complicaciones infecciosas, solo un paciente del grupo TOH presentó infección del estoma de traqueotomía, lo que supone un 4% de incidencia, similar a la comunicada habitualmente en la literatura24. Aunque en el referido estudio de Andrew et al. no se menciona la incidencia de la NAVM, en nuestro caso la presentaron 4 pacientes (16%) del grupo TOH. Esta complicación supone 6 casos de neumonía por cada 1.000 días de ventilador (6/1.000), tasa más de 3 veces superior al del grupo no-TOH (1,7/1.000 días). Es probable que esta mayor incidencia de NAVM en el grupo de TOH resida en la utilización de inmunosupresión, que si bien es necesaria para el tratamiento de estos pacientes, los convierte en especialmente vulnerables a la adquisición de infecciones.
Respecto a las complicaciones fatales relacionadas con el procedimiento de la TPD no encontramos ningún caso en el grupo TOH ni existieron diferencias significativas como era de esperar, dado que solo existieron 3 casos fatales en el grupo no-TOH (0,38%). Los 3 pacientes fallecidos durante la TDP en el grupo no-TOH fueron por pérdida de la vía aérea durante el procedimiento, con imposibilidad para la reintubación, seguida de desaturación extrema y parada cardiaca. Los 3 casos descritos presentaban valores medios similares al resto de los pacientes en cuanto al APACHE II (19 vs. 20), SAPS II (37 vs. 48), índice de masa corporal (30 vs. 28), edad (49 vs. 56) y relación PO2/FiO2 (192 vs. 232).
En lo que se refiere a la mortalidad global por otras causas no relacionadas con la TPD, en nuestros resultados la mortalidad intra-UCI de los pacientes trasplantados hepáticos operados mediante TPD fue del 52%, significativamente más elevada que en el resto de pacientes no trasplantados que precisó una TPD durante su ingreso en UCI (30%). Como es lógico, la mortalidad de los pacientes operados mediante TOH25, no objeto de nuestro estudio, depende de numerosos factores relacionados con las causas de la insuficiencia respiratoria o del deterioro de conciencia que obliguen a la ventilación mecánica prolongada en un paciente postoperado, inmunodeprimido y con un postoperatorio complicado. En el trabajo, Andrew et al. describen una mortalidad global intrahospitalaria por cualquier causa del 55% en los pacientes con trasplante de órgano sólido que han precisado una TPD; desenlace que resulta similar a los resultados de nuestra serie14.
Existen otras series en la literatura con escaso número de pacientes, como la de Pirat et al.15, que recoge datos de 5 pacientes trasplantados operados mediante TPD (2 hepáticos, 2 renales y uno cardiaco) por lo que sus resultados son difícilmente comparables.
Una particularidad en nuestro estudio, a diferencia del de Andrew et al., es que la TPD en TOH fue comparada con el resto de las TPD realizadas. En este sentido, nuestra tasa de hemorragias (4,4%) en los pacientes críticos no trasplantados arroja resultados similares a los descritos en otras series26.
Adicionalmente, hemos de destacar que no ha sido posible comparar los resultados de la TPD con un grupo control de traqueotomías quirúrgicas abiertas, puesto que en nuestro centro, desde hace más de 10 años, la totalidad de las traqueotomías en los pacientes críticos se realizan por el método de la TPD.
Siempre con las consideraciones de la mayor propensión a la hemorragia y la obligada utilización de la inmunosupresión, la TPD es hoy en día un procedimiento seguro en el paciente trasplantado hepático, con un número relativamente bajo de complicaciones similar al de la población general en pacientes críticos de UCI.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.