La prevención de la enfermedad cardiovascular se fundamenta en la detección y control de los factores de riesgo cardiovascular (FRCV). En España existen importantes diferencias territoriales tanto en la prevalencia como en el grado de control de los FRCV. En la última década ha habido una mejora del control de la hipertensión y la dislipidemia, pero un empeoramiento de los factores de riesgo cardiometabólicos relacionados con la obesidad y la diabetes.
El estudio SIMETAP es un estudio observacional descriptivo transversal realizado en 64 centros de atención primaria de la Comunidad de Madrid. El objetivo principal es determinar las tasas de prevalencia de FRCV, de las enfermedades cardiovasculares y de las enfermedades metabólicas relacionadas con el riesgo cardiovascular. El presente artículo informa sobre las características basales de la población, la metodología del estudio, y las definiciones de los parámetros y enfermedades en estudio. Se seleccionaron 6.631 sujetos de estudio mediante una muestra aleatoria base poblacional. Se determinaron variables antropométricas, estilos de vida, presión arterial, parámetros bioquímicos, y tratamientos farmacológicos.
Las prevalencias crudas más elevadas se detectaron en tabaquismo, inactividad física, obesidad, prediabetes, diabetes, hipertensión, dislipidemias y síndrome metabólico. Para valorar la verdadera dimensión epidemiológica de estas enfermedades y FRCV, es necesario realizar un análisis pormenorizado de tasas de prevalencia estratificadas por grupos etarios y de las tasas de prevalencia ajustadas por edad y sexo.
The prevention of cardiovascular disease is based on the detection and control of cardiovascular risk factors (CVRF). In Spain there are important geographical differences both in the prevalence and in the level of control of the CVRF. In the last decade there has been an improvement in the control of hypertension and dyslipidaemia, but a worsening of cardio-metabolic risk factors related to obesity and diabetes.
The SIMETAP study is a cross-sectional descriptive, observational study being conducted in 64 Primary Care Centres located at the Community of Madrid. The main objective is to determine the prevalence rates of CVRF, cardiovascular diseases, and metabolic diseases related to cardiovascular risk. A report is presented on the baseline characteristics of the population, the study methodology, and the definitions of the parameters and diseases under study. A total of 6,631 study subjects were selected using a population-based random sample. The anthropometric variables, lifestyles, blood pressure, biochemical parameters, and pharmacological treatments were determined.
The highest crude prevalences were detected in smoking, physical inactivity, obesity, prediabetes, diabetes, hypertension, dyslipidaemias, and metabolic syndrome. A detailed analysis needs to be performed on the prevalence rates, stratified by age groups, and prevalence rates adjusted for age and sex to assess the true epidemiological dimension of these CVRF and diseases.
La enfermedad cardiovascular (ECV) aterosclerótica se puede considerar como el resultado de un continuum patogénico en el que intervienen estilos de vida no saludables y múltiples factores de riesgo cardiovascular (FRCV). Las manifestaciones clínicas de la ECV constituyen la principal causa de muerte en el mundo occidental, por lo que es prioritario implementar intervenciones sanitarias de alto impacto que disminuyan el riesgo cardiovascular (RCV) de padecerlas.
La adaptación española1 de la guía europea de prevención de la ECV en la práctica clínica2 recomienda la valoración previa del RCV, fomentar estilos de vida saludables e intervenir sobre los FRCV, síndromes y enfermedades relacionadas con la ECV con una intensidad proporcional al RCV preestablecido.
De manera similar, estas consideraciones también se pueden aplicar en entidades clínicas relacionadas con la insulinorresistencia (IR) como la prediabetes, la diabetes mellitus (DM), la enfermedad renal crónica (ERC), la hiperlipidemia familiar combinada, el síndrome metabólico (SM) o la obesidad. Las guías europeas2,3 insisten en el mensaje de que los pacientes con DM padecen un RCV alto o muy alto, e incluso el consenso de las asociaciones de endocrinología americanas4 considera el RCV extremo si la ECV se asocia a DM o ERC.
La acción continuada de los FRCV más importantes, como el tabaquismo, la hipertensión arterial (HTA) y la hipercolesterolemia, consigue deteriorar el endotelio vascular, favoreciendo la formación, oxidación y vulnerabilidad de la placa arteriosclerótica, hasta manifestarse clínicamente la ECV en forma de enfermedad coronaria (EC), de ictus o accidentes cerebrovasculares (ACV), o de enfermedad arterial periférica (EAP).
Por otra parte, los pacientes con procesos relacionados con IR tienen un RCV especialmente elevado debido a que padecen un característico perfil lipídico que acelera el proceso de arteriosclerosis denominado dislipidemia aterogénica. Este fenotipo lipídico se caracteriza por unos niveles bajos de colesterol unido a lipoproteína de alta densidad (C-HDL), hipertrigliceridemia (HTG), y unos niveles no elevados de colesterol unido a lipoproteínas de baja densidad (C-LDL) aunque con elevada concentración de partículas LDL con apolipoproteína B caracterizadas por ser pequeñas y densas5. Dada su importancia etiopatogénica, es importante evaluar en la población las diversas expresiones fenotípicas de los perfiles lipídicos y de IR de los pacientes que padecen manifestaciones clínicas o metabólicas de la ECV o de la DM.
El concepto de SM6 surgió hace casi 40 años para definir una agrupación no casual de factores asociados a IR observados en la práctica clínica: obesidad central, dislipidemia, anomalías en el metabolismo de la glucosa e HTA. Su importancia se fundamenta en que incrementa el riesgo de padecer DM7,8, ECV8, y ERC9. El SM aumenta la mortalidad por todas las causas y duplica el riesgo de padecer ECV8. Incluso si las definiciones más frecuentemente utilizadas de SM10–13 excluyeran a la DM entre sus criterios diagnósticos, se mantendría el riesgo incrementado de padecer ECV.
Probablemente lo más prudente sea aceptar que el SM engloba a un conjunto de individuos en los que cualquier criterio puede estar ausente pero que tienen un RCV elevado que no se detectaría si no se tomara en cuenta este enfoque global. Es aquí donde radica la doble relevancia del SM. Por un lado, sirve para alertar al clínico para investigar la presencia de otros FRCV en pacientes con algún factor de riesgo cardiometabólico. Por otro lado, permite identificar a un gran número de sujetos con RCV alto sobre los que se debe intervenir, tanto con estrategias clínicas como de salud pública. Los expertos de la OMS14 consideran que la actuación primordial sobre el SM debe centrarse en las políticas sanitarias basadas en la atención primaria.
Sin embargo, los estudios sobre prevalencia se han encontrado con varias dificultades conceptuales. Una de ellas es comprender que el SM es un clúster de factores que se relacionan con FRCV, con la ECV y con la morbilidad relacionada de la IR. Otro inconveniente es la existencia de varias definiciones de SM que incluyen FRCV clásicos y otros factores de riesgo cardiometabólicos que se consideran de forma distinta según sean referenciados por unas u otras sociedades10–13. Por otra parte, dado que las definiciones de SM no figuran en la actualidad en la codificación de episodios de la Clasificación Internacional de Atención Primaria15 (CIAP2) o en la Clasificación Internacional de Enfermedades16 (CIE9), no es fácil el registro del episodio de SM en las historias clínicas de los pacientes. Los códigos de la CIAP2 (K22) o de la CIE9 (277.7; 277.9) no se refieren específicamente a ninguna de las definiciones existentes de SM. Esto dificulta la detección de SM, la valoración del RCV global del paciente y la intervención integral sobre todos los FRCV y cardiometabólicos relacionados con el SM.
La prevención de la ECV necesita una valoración previa de la situación epidemiológica de todos los factores que influyen en el problema que se pretende evaluar. A su vez, la realización de un diagnóstico de salud adecuado precisa valorar la prevalencia en todos los tramos etarios de la población de estudio. Siguiendo esta estrategia de actuación, el objetivo el estudio SIMETAP fue determinar en la población adulta de la Comunidad de Madrid las tasas de prevalencia ajustadas por edad y sexo de los FRCV, de la ERC, de las enfermedades cardiovasculares y de las enfermedades metabólicas relacionadas con la ECV.
Material y métodosDiseño y población de estudioEl estudio SIMETAP es un estudio observacional, descriptivo y transversal realizado por 121 médicos de familia de 64 centros de atención primaria del Servicio de Salud Pública de la Comunidad de Madrid (SERMAS). Se realizó de acuerdo con los principios establecidos por la 18.a Asamblea Médica Mundial (Helsinki, 1964) y sus enmiendas, y por la Conferencia Internacional sobre armonización y directrices para una buena práctica clínica. La Comisión de Investigación de la Gerencia Adjunta de Planificación y Calidad de la Gerencia de Atención Primaria de la Comunidad de Madrid emitió el informe favorable para su realización.
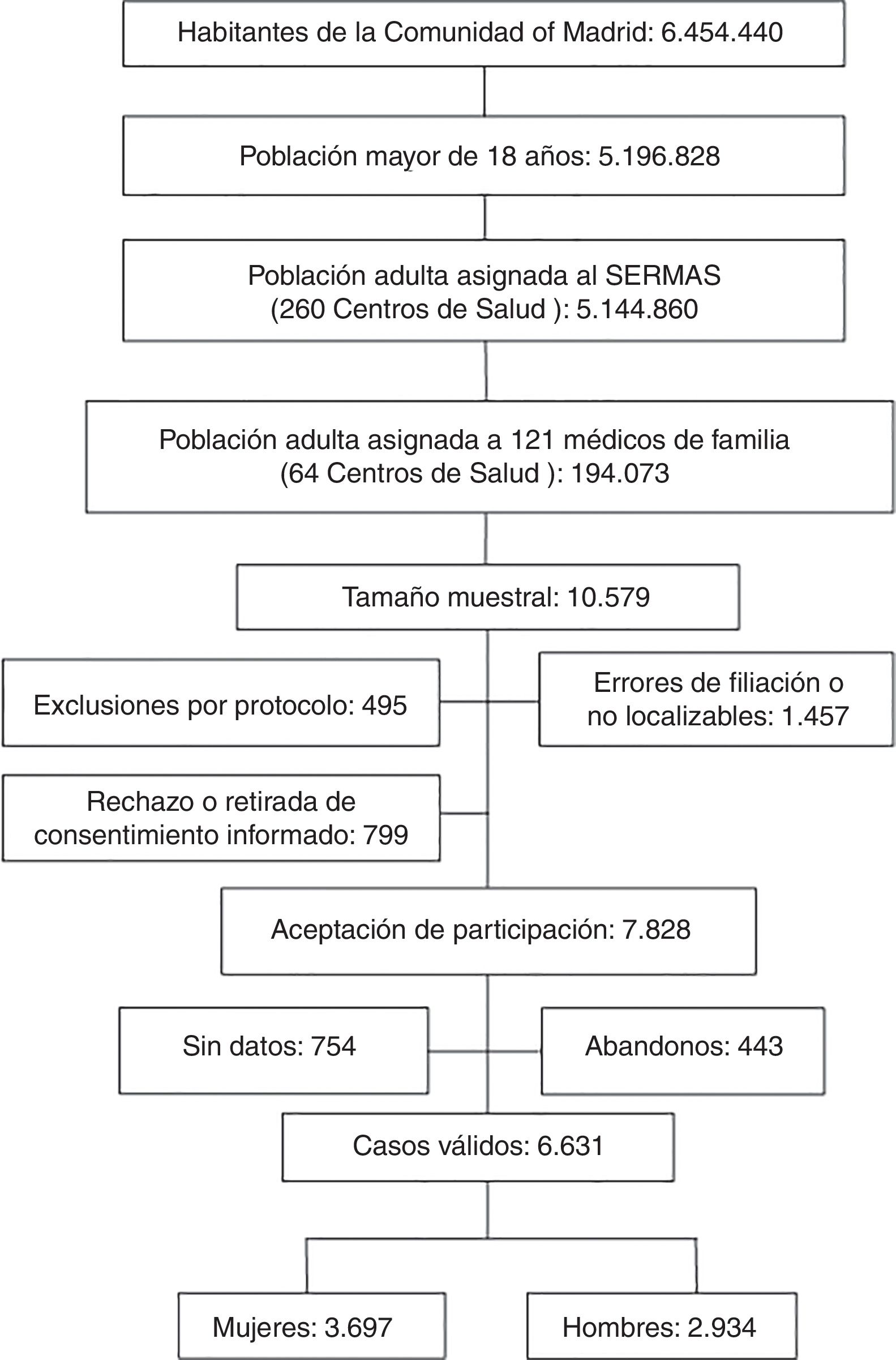
La población adscrita al SERMAS fue de 5.144.860 adultos (el 99% del censo poblacional), cuya asistencia sanitaria se prestaba en 260 centros de atención primaria. Se obtuvo una muestra representativa (10.579 adultos) basada en la población asignada a los médicos de familia con 18 o más años y sin límite de edad (194.073 adultos). El tamaño muestral se calculó con esta población finita para un nivel de confianza del 95% (error α), 0,024 para el intervalo de confianza (margen de error del 1,2%), p=0,5 para la proporción esperada, y considerando un 25% por falta de respuesta y un 14% por pérdidas y abandonos.
Para obtener la población muestral, se utilizaron tablas de números aleatorios generadas por el programa Microsoft© Excel© 2013, que se aplicaron para ordenar aleatoriamente los listados de los pacientes asignados a los médicos de familia y seleccionar a los sujetos del estudio.
Se excluyeron del estudio por protocolo a pacientes terminales, institucionalizados, con deterioro cognitivo y a mujeres en periodo de gestación. Mediante una búsqueda activa de los sujetos de la muestra resultante, los investigadores realizaron hasta 5 llamadas telefónicas para contactar e invitarles a participar en el estudio.
Recogida de datosTras obtener el consentimiento firmado, los investigadores realizaron una entrevista clínica a los sujetos de estudio para obtener información sobre edad, sexo, estilos saludables de vida, medidas antropométricas, presión arterial sistólica y diastólica, FRCV, antecedentes de enfermedades metabólicas, enfermedad pulmonar obstructiva crónica, enfermedades cardiovasculares (EC, ACV, EAP, insuficiencia cardiaca, fibrilación auricular), disfunción eréctil, ERC, albuminuria, tratamientos farmacológicos y parámetros bioquímicos más recientes determinados en análisis de sangre y orina durante el último año. Los investigadores recopilaron los datos del estudio entre enero y diciembre de 2015. La doble entrada de datos garantizó el registro en la base de datos.
Definición de variablesA efectos del presente estudio se consideró que los pacientes padecían los síndromes y enfermedades objeto de estudio si sus respectivos diagnósticos o sus códigos relacionados de la CIAP215 o de la CIE916 estaban registrados en sus historias clínicas, considerando las siguientes definiciones y criterios diagnósticos:
Tabaquismo: Consumo de cualquier cantidad de cigarrillos o tabaco durante el último mes.
Exfumador: Paciente que se ha abstenido de fumar durante más de un año.
Etilismo: Consumo habitual de alcohol>21 unidades (210g) semanales en los hombres y >14 unidades (140g) semanales en las mujeres.
Inactividad física: Actividad física menor de 150min a la semana.
Presión arterial elevada (CIAP2: K85): Presión arterial sistólica≥130mmHg y/o presión arterial diastólica≥85mmHg sin diagnóstico de HTA17.
HTA (CIAP2: K86, K87. CIE9: 401-404): Presión arterial sistólica≥140mmHg y/o presión arterial diastólica≥90mmHg17, o si el paciente estaba tomando fármacos para reducir la presión arterial.
HTA marcada: Presión arterial≥180/110mmHg.
Prediabetes ADA (American Diabetes Association)18 (CIAP2: A91. CIE9: 271.3): Sin criterios de DM, niveles de glucemia plasmática en ayunas (GPA) entre 100mg/dL (5,6mmol/L) y 125mg/dL (6,9mmol/L) ambos niveles incluidos, o niveles de glucohemoglobina A1c (HbA1c) entre el 5,7% (39mmol/mol) y el 6,4% (47mmol/mol), ambos niveles incluidos.
Prediabetes CDA (Canadian Diabetes Association)19 (CIAP2: A91. CIE9: 271.3): Sin criterios de DM, niveles de GPA entre 110mg/dL (6,1mmol/L) y 125mg/dL (6,9mmol/L) ambos niveles incluidos, o niveles de HbA1c entre el 6% (42mmol/mol) y el 6,4% (47mmol/mol), ambos niveles incluidos.
DM tipo 1 (CIAP2: T89. CIE9: 250.01). Criterios ADA18 o CDA19.
DM tipo 2 (CIAP2: T90. CIE9: 249; 250.02): Criterios ADA18 o CDA19. Niveles de GPA≥126mg/dL (7mmol/L) o niveles de HbA1c≥6,5% (48mmol/mol).
Hipercolesterolemia (CIAP2: T93. CIE9: 272.0; 272.2; 272.4): Nivel sérico de colesterol-total (CT)≥200mg/dL (5,17mmol/L), o si el paciente estaba tomando fármacos para reducir el colesterol.
Hipercolesterolemia marcada: Nivel sérico de CT≥300mg/dL (7,76mmol/L), o C-LDL≥190mg/dL (4,91mmol/L), o si los diagnósticos de hipercolesterolemia familiar o de hiperlipidemia familiar combinada estaban registrados en la historia clínica de los pacientes.
HTG10 (CIE9: 272.1; 272.3): Nivel sérico de triglicéridos (TG)≥150mg/dL (1,69mmol/L), o si el paciente estaba tomando fármacos para reducir los TG.
C-HDL elevado: Nivel sérico≥60mg/dL (1,55mmol/L).
C-HDL bajo: Nivel sérico<40mg/dL (1,03mmol/L) en hombres o<45mg/dL (1,16mmol/L) en mujeres5. También se consideró el nivel de C-HDL<50mg/dL (1,29mmol/L) en mujeres10–13.
Colesterol-no-HDL: Diferencia de los niveles séricos entre CT y C-HDL.
C-LDL: Se determinó con la fórmula de Friedewald (C-LDL=CT−[C-HDL]-TG/5) si los niveles de TG eran<400mg/dL (<4,52mmol/L)20.
Colesterol unido a lipoproteínas de muy baja densidad: CT−(C-HDL)−(C-LDL).
Dislipidemia aterogénica5: HTG con C-HDL bajo.
Índice Castelli-I21: CT/C-HDL.
Índice Castelli-II21: C-LDL/C-HDL.
Coeficiente aterogénico colesterol-no-HDL/C-HDL.
Índice TG/C-HDL.
Índice aterogénico de plasma22: log (TG/C-HDL).
Índice TG y glucosa23: Ln [TG (mg/dL)×GPA (mg/dL)/2]
Sobrepeso24 (CIAP2: T83. CIE9: 278.02): índice de masa corporal (IMC) entre 25,0 y 29,9kg/m2.
Obesidad24 (CIAP2: T82; CIE9: 278.00; 278.01): IMC (peso/talla2)≥30kg/m2.
Obesidad abdominal o central: Perímetro de cintura≥102cm en hombres o≥88cm en mujeres13, o≥94cm en hombres o≥80cm en mujeres12, determinado con el sujeto en bipedestación mediante cinta métrica flexible ajustada sin comprimir la piel, al final de una espiración normal, localizando el borde superior de las crestas ilíacas y por encima de ese punto rodeando la cintura paralela al suelo24.
Índice cintura-talla25 (ICT): Perímetro de cintura/talla (cm/cm).
Hipotiroidismo (CIAP2: T86; CIE9: 244.9) en tratamiento sustitutivo.
Esteatosis hepática (CIE9: 571.8) registrado en historia clínica.
EC (CIAP2: K74, K75, K76. CIE9: 410-414): Incluye cardiopatía isquémica, infarto agudo de miocardio previo, síndromes coronarios agudos, revascularización coronaria y otros procedimientos de revascularización arterial.
ACV (CIAP2: K89, K90; K91. CIE9: 430; 431-436): Incluye accidente cerebrovascular, isquemia cerebral o hemorragias intracraneales y ataque isquémico transitorio.
EAP (CIAP2: K92. CIE9: 440; 443.9; 444): También incluye claudicación intermitente o un índice tobillo-brazo≤0,9.
ECV: Incluye EC, ACV y EAP.
Insuficiencia cardiaca (CIAP2: K77. CIE9: 428).
Fibrilación auricular (CIAP2: K78. CIE9: 427.3).
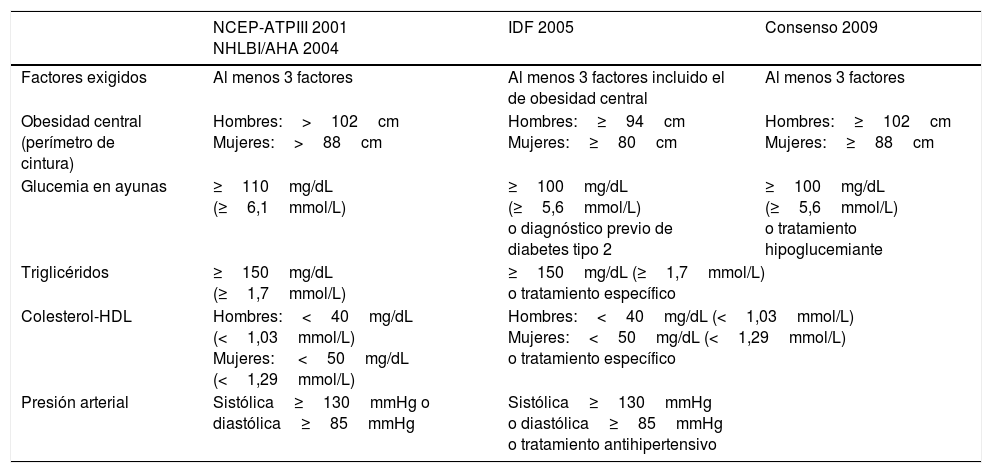
SM (CIAP2: K22. CIE9: 277.7; 277.9): Se consideraron 3 conceptos: La definición del National Cholesterol Education Program-Adult Treatment Panel III10 (NCEP-ATPIII) y mantenida por la National Heart, Lung, and Blood Institute/American Heart Association11 (NHLBI/AHA); la definición de la International Diabetes Federation12 (IDF) para la población europea; y la definición del consenso armonizado13 de SM para la población europea establecido por las siguientes sociedades científicas: IDF, Task Force on Epidemiology and Prevention; NHLBI; AHA; World Heart Federation; International Atherosclerosis Society; e International Association for the Study of Obesity (tabla 1).
Definiciones de síndrome metabólico para la población europea
| NCEP-ATPIII 2001 NHLBI/AHA 2004 | IDF 2005 | Consenso 2009 | |
|---|---|---|---|
| Factores exigidos | Al menos 3 factores | Al menos 3 factores incluido el de obesidad central | Al menos 3 factores |
| Obesidad central (perímetro de cintura) | Hombres:>102cm Mujeres:>88cm | Hombres:≥94cm Mujeres:≥80cm | Hombres:≥102cm Mujeres:≥88cm |
| Glucemia en ayunas | ≥110mg/dL (≥6,1mmol/L) | ≥100mg/dL (≥5,6mmol/L) o diagnóstico previo de diabetes tipo 2 | ≥100mg/dL (≥5,6mmol/L) o tratamiento hipoglucemiante |
| Triglicéridos | ≥150mg/dL (≥1,7mmol/L) | ≥150mg/dL (≥1,7mmol/L) o tratamiento específico | |
| Colesterol-HDL | Hombres:<40mg/dL (<1,03mmol/L) Mujeres: <50mg/dL (<1,29mmol/L) | Hombres:<40mg/dL (<1,03mmol/L) Mujeres:<50mg/dL (<1,29mmol/L) o tratamiento específico | |
| Presión arterial | Sistólica≥130mmHg o diastólica≥85mmHg | Sistólica≥130mmHg o diastólica≥85mmHg o tratamiento antihipertensivo | |
IDF: International Diabetes Federation; NCEP-ATPIII: National Cholesterol Education Program-Adult Treatment Panel III; NHLBI/AHA: National Heart, Lung, and Blood Institute/American Heart Association.
SM mórbido: SM con DM o con ECV.
SM premórbido: SM sin DM ni ECV.
Enfermedad pulmonar obstructiva crónica (CIAP2: R95. CIE9: 491.2; 492; 496): Criterios de la guía GOLD26.
Excreción urinaria de albúmina y cociente albúmina-creatinina (CIAP2: U90; U98. CIE9: 593.6; 791): Criterios de la guía KDIGO27.
Albuminuria: cociente albúmina-creatinina≥30mg/g.
Tasa de filtración glomerular estimada (FGe): Se utilizaron las siguientes ecuaciones Chronic Kidney Disease EPIdemiology collaboration (CKD-EPI)28 expresadas en mL/min/1,73m2: Mujeres con creatinina≤0,7mg/dL=144×(creatinina)-0,329×(0,993)edad; Mujeres con creatinina>0,7mg/dL=144×(creatinina)-1,209×(0,993)edad; Hombres con creatinina≤0,9mg/dL=141×(creatinina)-0,411×(0,993)edad; Hombres con creatinina>0,9mg/dL=141×(creatinina)-1,209×(0,993)edad.
ERC (CIAP2: U99. CIE9: 585): FGe<60mL/min/1,73m2 o cociente albúmina-creatinina≥30mg/g (KDIGO)27.
Disfunción eréctil: Incapacidad para lograr o mantener una erección suficiente para conseguir una relación sexual satisfactoria29.
FRCV: Factor de riesgo que predice la probabilidad de desarrollar una ECV: Edad (>55 años en hombres; >65 en mujeres), HTA, hipercolesterolemia, tabaquismo.
FRCV muy elevado: Hipercolesterolemia marcada o HTA marcada.
Modificador de RCV: Factor con posible potencial de reclasificación del RCV cuando la puntuación SCORE (systematic coronary risk evaluation)2 se encuentra cerca del umbral de decisión. Inactividad física, antecedente de ECV prematura (hombres<55 años o mujeres<65 años) en familiar de primer grado, C-HDL bajo, obesidad.
RCV: Riesgo de mortalidad por patología cardiovascular a 10 años. Para la población entre 40 y 65 años, se asignaron las categorías de RCV utilizando el sistema SCORE2 para los países europeos de bajo riesgo. RCV bajo: Población<40 años sin 2 o más FRCV; SCORE=0%. RCV moderado: Población<40 años con 2 o más FRCV; DM<40 años; SM; SCORE entre el 1 y 4%. RCV alto: FRCV muy elevado; DM sin FRCV; ERC moderada (FGe 30-59mL/min/1,73m2); SCORE entre el 5 y 9%. RCV muy alto: ECV clínica o documentada por imagen; DM con lesión en órganos diana o con FRCV; ERC grave (FGe<30mL/min/1,73m2); SCORE≥10%. RCV extremo4: ECV asociada a DM o ERC. La asignación del RCV en la población>65 años fue determinada con los criterios SCORE OP30.
Análisis estadísticoSe realizó utilizando el programa Statistical Package for the Social Sciences (IBM® SPSS® Statistical release 20.0, Armonk, NY, EE. UU.). Se determinó el rango, mediana y rango intercuartílico (RIC) (percentil 25; percentil 75) de la variable edad. El análisis estadístico descriptivo se realizó determinando la media y la desviación estándar (±DE). Las variables cuantitativas se compararon mediante la realización de las pruebas Levene y t de Student de 2 colas para comparar 2 variables o usando el análisis de varianza ANOVA de una vía para comparar más de 2 variables. Las variables analizadas mostraron una distribución normal (asimetría y curtosis entre −2 y +2). Las variables cualitativas se analizaron mediante tasas de prevalencia y porcentajes en cada categoría, presentadas con límites inferior y superior del intervalo de confianza (IC) del 95%. El análisis inferencial de los datos cualitativos se realizó mediante la prueba de Chi-cuadrado, y mediante la prueba de Fisher para los datos cuantitativos. Los odds-ratios se determinaron con IC del 95%. Todas las pruebas se consideraron estadísticamente significativas si las estimaciones con odds-ratio eran superiores a 1 o el valor de p de 2 colas era inferior a 0,05. Las prevalencias se determinaron como tasas brutas y ajustadas por edad y sexo. El ajuste de tasas se realizó mediante el método directo31 utilizando como poblaciones estándares las distribuciones por tramos etarios quinquenales y decenales de las poblaciones masculina y femenina de la Comunidad de Madrid y de España, información obtenida de la base de datos del Instituto Nacional de Estadística32 de enero de 2015.
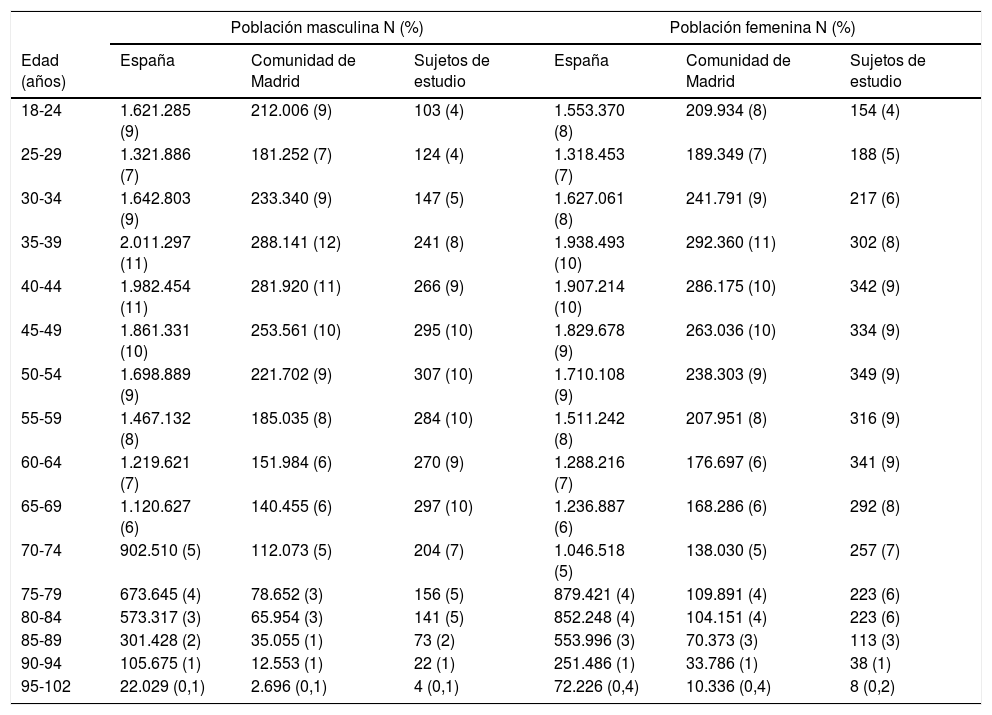
ResultadosLos habitantes mayores de 18 años de la Comunidad de Madrid y de España fueron 5.196.828 y 38.102.546 adultos respectivamente. La distribución por tramos etarios quinquenales de las poblaciones de estudio y de referencia se muestran en la tabla 2. La distribución del origen étnico de los habitantes de la Comunidad de Madrid32 era la siguiente: españoles (88,9%), del resto de Europa (4,9%), de América Central y del Sur (3,4%), norteamericanos (0,2%), africanos (1,5%), asiáticos (1,1%) y de Oceanía (0,01%).
Distribución etaria de las poblaciones de estudio y de referencia
| Población masculina N (%) | Población femenina N (%) | |||||
|---|---|---|---|---|---|---|
| Edad (años) | España | Comunidad de Madrid | Sujetos de estudio | España | Comunidad de Madrid | Sujetos de estudio |
| 18-24 | 1.621.285 (9) | 212.006 (9) | 103 (4) | 1.553.370 (8) | 209.934 (8) | 154 (4) |
| 25-29 | 1.321.886 (7) | 181.252 (7) | 124 (4) | 1.318.453 (7) | 189.349 (7) | 188 (5) |
| 30-34 | 1.642.803 (9) | 233.340 (9) | 147 (5) | 1.627.061 (8) | 241.791 (9) | 217 (6) |
| 35-39 | 2.011.297 (11) | 288.141 (12) | 241 (8) | 1.938.493 (10) | 292.360 (11) | 302 (8) |
| 40-44 | 1.982.454 (11) | 281.920 (11) | 266 (9) | 1.907.214 (10) | 286.175 (10) | 342 (9) |
| 45-49 | 1.861.331 (10) | 253.561 (10) | 295 (10) | 1.829.678 (9) | 263.036 (10) | 334 (9) |
| 50-54 | 1.698.889 (9) | 221.702 (9) | 307 (10) | 1.710.108 (9) | 238.303 (9) | 349 (9) |
| 55-59 | 1.467.132 (8) | 185.035 (8) | 284 (10) | 1.511.242 (8) | 207.951 (8) | 316 (9) |
| 60-64 | 1.219.621 (7) | 151.984 (6) | 270 (9) | 1.288.216 (7) | 176.697 (6) | 341 (9) |
| 65-69 | 1.120.627 (6) | 140.455 (6) | 297 (10) | 1.236.887 (6) | 168.286 (6) | 292 (8) |
| 70-74 | 902.510 (5) | 112.073 (5) | 204 (7) | 1.046.518 (5) | 138.030 (5) | 257 (7) |
| 75-79 | 673.645 (4) | 78.652 (3) | 156 (5) | 879.421 (4) | 109.891 (4) | 223 (6) |
| 80-84 | 573.317 (3) | 65.954 (3) | 141 (5) | 852.248 (4) | 104.151 (4) | 223 (6) |
| 85-89 | 301.428 (2) | 35.055 (1) | 73 (2) | 553.996 (3) | 70.373 (3) | 113 (3) |
| 90-94 | 105.675 (1) | 12.553 (1) | 22 (1) | 251.486 (1) | 33.786 (1) | 38 (1) |
| 95-102 | 22.029 (0,1) | 2.696 (0,1) | 4 (0,1) | 72.226 (0,4) | 10.336 (0,4) | 8 (0,2) |
N: tamaños poblacionales; (%): porcentaje respecto al total.
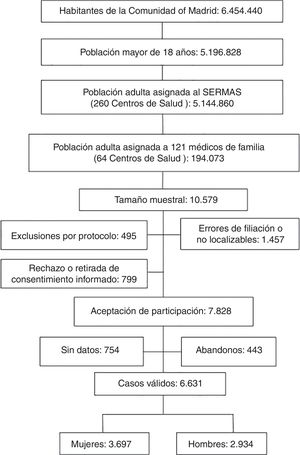
El 7,6% de la muestra inicial rechazó participar en el estudio o no firmó el consentimiento informado. El 13,8% de los sujetos de la muestra tenía errores de filiación o no se pudo contactar tras realizar una búsqueda activa. El 4,7% de los sujetos de la muestra cumplían criterios de exclusión. El 7,1% de los sujetos del estudio sin datos clínicos o con registros médicos sin información clínica relevante fueron excluidos. La tasa de respuesta fue el 74%. Las pérdidas, abandonos o sujetos del estudio que no acudieron a la entrevista clínica fue el 4,2% (fig. 1).
La población del estudio fue de 6.631 sujetos, siendo masculina el 44,25% (IC: 43,05; 45,45) (tabla 1). La media de edad (±DE) de la población de estudio fue de 55,03 (±17,54) años, la mediana de edad fue de 54,56 años, y el rango de edad (RIC) estuvo entre 18,01 y 102,80 (41,55; 67,98) años.
La media de edad (±DE) de la población masculina fue de 55,06 (±16,90) años, la mediana fue de 54,75 años, y el rango de edad (RIC) entre 18,01 y 102,12 (42,01; 67,35) años. La media de edad (±DE) de la población femenina fue de 55,01 (±18,04) años, la mediana fue de 54,36 años, y el rango de edad (RIC) entre 18,01 y 102,80 (40,94; 68,77) años. La diferencia de las medias de edad (0,05 [IC: −0,80; 0,90] años) entre las poblaciones masculina y femenina no fue significativa (p=0,908).
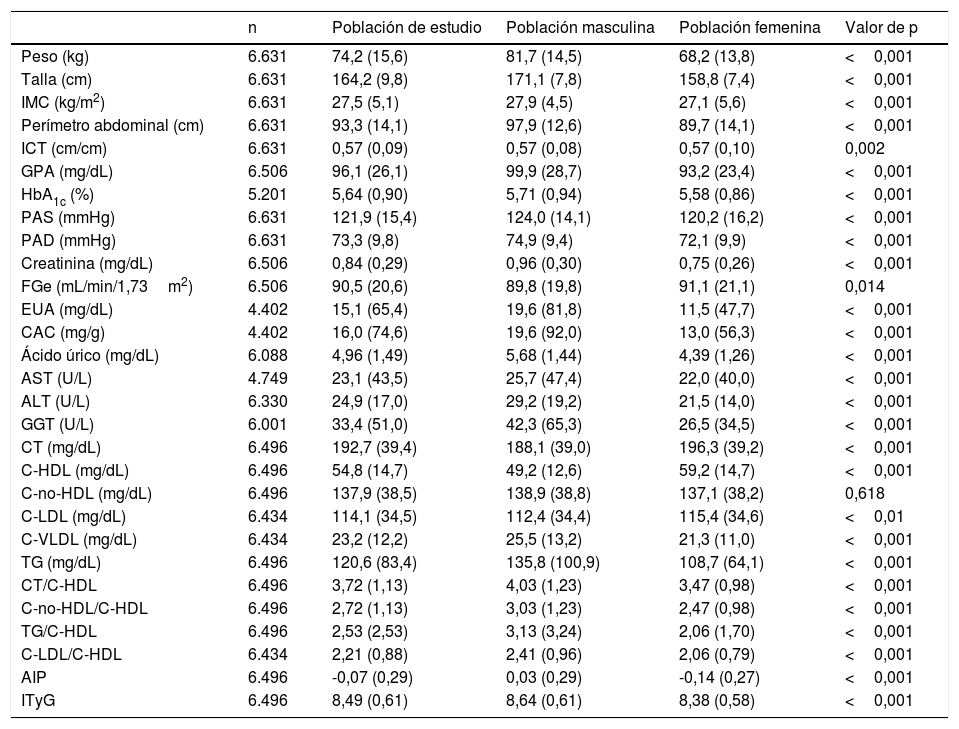
Las medias (±DE) de las variables antropométricas, de presión arterial y bioquímicas de la población de estudio y la significación de las diferencias entre las poblaciones masculina y femenina se muestran en la tabla 3. Las medias de los parámetros más elevados fueron: el sobrepeso (IMC: 27,5kg/m2), los perímetros de cintura (97,9cm en hombres y 89,7cm en mujeres), el ICT (0,57), y la HbA1c (5,6%). Todos los parámetros mencionados eran significativamente mayores en la población masculina, excepto la FGe, el CT, el C-LDL y el C-HDL que eran significativamente mayores en la población femenina.
Características cuantitativasa de la población de estudio
| n | Población de estudio | Población masculina | Población femenina | Valor de p | |
|---|---|---|---|---|---|
| Peso (kg) | 6.631 | 74,2 (15,6) | 81,7 (14,5) | 68,2 (13,8) | <0,001 |
| Talla (cm) | 6.631 | 164,2 (9,8) | 171,1 (7,8) | 158,8 (7,4) | <0,001 |
| IMC (kg/m2) | 6.631 | 27,5 (5,1) | 27,9 (4,5) | 27,1 (5,6) | <0,001 |
| Perímetro abdominal (cm) | 6.631 | 93,3 (14,1) | 97,9 (12,6) | 89,7 (14,1) | <0,001 |
| ICT (cm/cm) | 6.631 | 0,57 (0,09) | 0,57 (0,08) | 0,57 (0,10) | 0,002 |
| GPA (mg/dL) | 6.506 | 96,1 (26,1) | 99,9 (28,7) | 93,2 (23,4) | <0,001 |
| HbA1c (%) | 5.201 | 5,64 (0,90) | 5,71 (0,94) | 5,58 (0,86) | <0,001 |
| PAS (mmHg) | 6.631 | 121,9 (15,4) | 124,0 (14,1) | 120,2 (16,2) | <0,001 |
| PAD (mmHg) | 6.631 | 73,3 (9,8) | 74,9 (9,4) | 72,1 (9,9) | <0,001 |
| Creatinina (mg/dL) | 6.506 | 0,84 (0,29) | 0,96 (0,30) | 0,75 (0,26) | <0,001 |
| FGe (mL/min/1,73m2) | 6.506 | 90,5 (20,6) | 89,8 (19,8) | 91,1 (21,1) | 0,014 |
| EUA (mg/dL) | 4.402 | 15,1 (65,4) | 19,6 (81,8) | 11,5 (47,7) | <0,001 |
| CAC (mg/g) | 4.402 | 16,0 (74,6) | 19,6 (92,0) | 13,0 (56,3) | <0,001 |
| Ácido úrico (mg/dL) | 6.088 | 4,96 (1,49) | 5,68 (1,44) | 4,39 (1,26) | <0,001 |
| AST (U/L) | 4.749 | 23,1 (43,5) | 25,7 (47,4) | 22,0 (40,0) | <0,001 |
| ALT (U/L) | 6.330 | 24,9 (17,0) | 29,2 (19,2) | 21,5 (14,0) | <0,001 |
| GGT (U/L) | 6.001 | 33,4 (51,0) | 42,3 (65,3) | 26,5 (34,5) | <0,001 |
| CT (mg/dL) | 6.496 | 192,7 (39,4) | 188,1 (39,0) | 196,3 (39,2) | <0,001 |
| C-HDL (mg/dL) | 6.496 | 54,8 (14,7) | 49,2 (12,6) | 59,2 (14,7) | <0,001 |
| C-no-HDL (mg/dL) | 6.496 | 137,9 (38,5) | 138,9 (38,8) | 137,1 (38,2) | 0,618 |
| C-LDL (mg/dL) | 6.434 | 114,1 (34,5) | 112,4 (34,4) | 115,4 (34,6) | <0,01 |
| C-VLDL (mg/dL) | 6.434 | 23,2 (12,2) | 25,5 (13,2) | 21,3 (11,0) | <0,001 |
| TG (mg/dL) | 6.496 | 120,6 (83,4) | 135,8 (100,9) | 108,7 (64,1) | <0,001 |
| CT/C-HDL | 6.496 | 3,72 (1,13) | 4,03 (1,23) | 3,47 (0,98) | <0,001 |
| C-no-HDL/C-HDL | 6.496 | 2,72 (1,13) | 3,03 (1,23) | 2,47 (0,98) | <0,001 |
| TG/C-HDL | 6.496 | 2,53 (2,53) | 3,13 (3,24) | 2,06 (1,70) | <0,001 |
| C-LDL/C-HDL | 6.434 | 2,21 (0,88) | 2,41 (0,96) | 2,06 (0,79) | <0,001 |
| AIP | 6.496 | -0,07 (0,29) | 0,03 (0,29) | -0,14 (0,27) | <0,001 |
| ITyG | 6.496 | 8,49 (0,61) | 8,64 (0,61) | 8,38 (0,58) | <0,001 |
AIP: índice aterogénico de plasma; ALT: alanina aminotransferasa; AST: aspartato aminotransferasa; C-HDL: colesterol unido a lipoproteínas de alta densidad; C-LDL: colesterol unido a lipoproteínas de baja densidad; C-VLDL: colesterol unido a lipoproteínas de muy baja densidad; CAC: cociente albúmina-creatinina; CT: colesterolemia total; EUA: excreción urinaria de albúmina; FGe: tasa de filtrado glomerular estimada según CKD-EPI (Chronic Kidney Disease EPIdemiology collaboration); GGT: gamma-glutamil transferasa; GPA: glucemia plasmática en ayunas; HbA1c: glucohemoglobina A1c; ICT: índice cintura-talla; IMC: índice de masa corporal (peso/talla2); ITyG: índice TG y glucosa; n: número de° de casos; PAD: presión arterial diastólica; PAS: presión arterial sistólica; TG: trigliceridemia; Valor de p: de la diferencia de medias entre las poblaciones masculina y femenina.
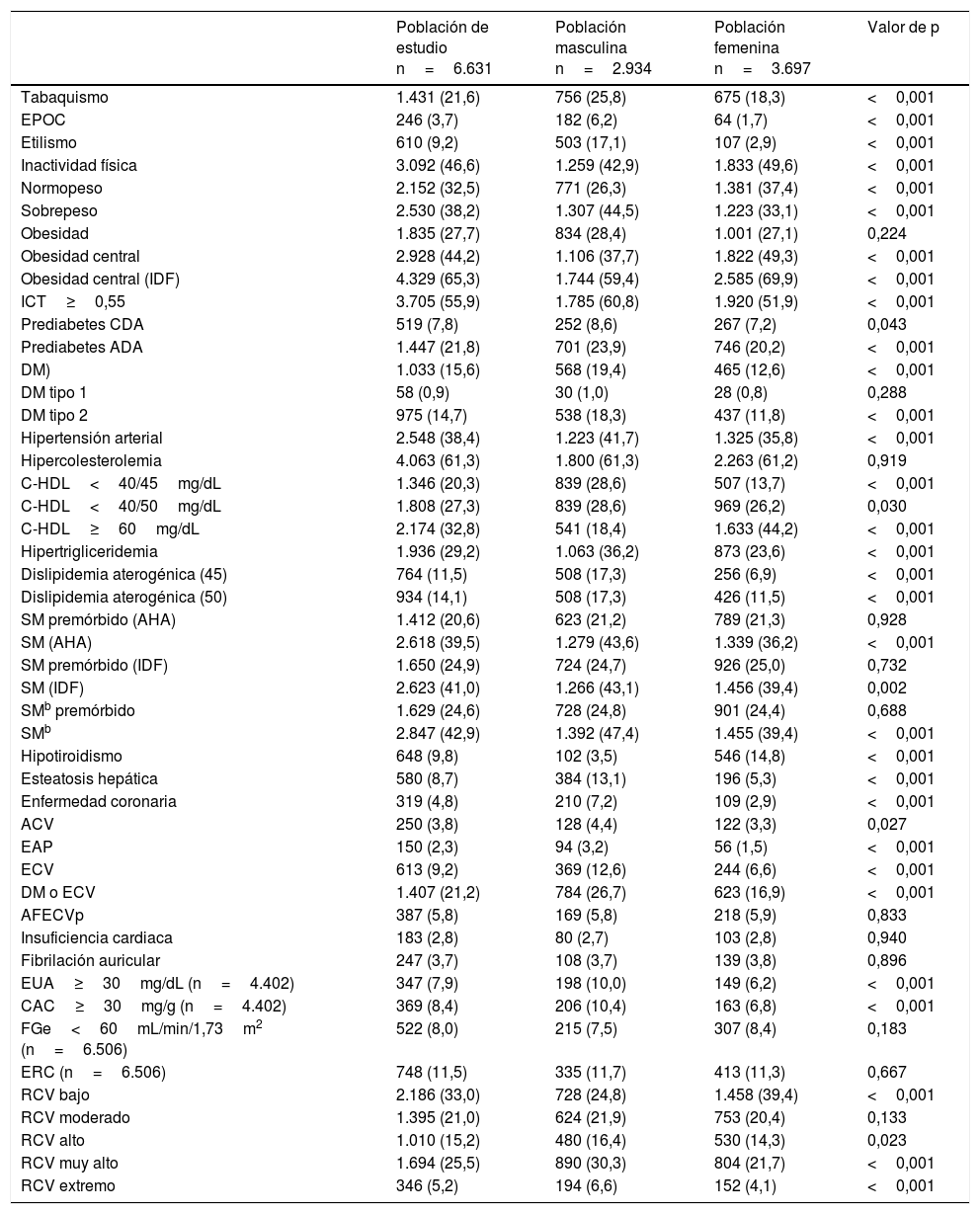
Las prevalencias crudas de las características cualitativas y morbilidad de la población de estudio y la significación de las diferencias entre las poblaciones masculina y femenina se muestran en la tabla 4. Las prevalencias crudas globales más elevadas fueron: Tabaquismo (22%), inactividad física (47%), sobrepeso (38%), obesidad (28%), obesidad abdominal (65%), ICT≥0,55 (56%), prediabetes (22%), DM (16%), HTA (38%), hipercolesterolemia (61%), HTG (29%), dislipidemia aterogénica (14%), SM (43%), y SM premórbido (25%). No existían diferencias de las prevalencias crudas entre las poblaciones masculina y femenina, en los siguientes FRCV y enfermedades: antecedente de ECV prematura en familiar de primer grado, obesidad, DM tipo 1, hipercolesterolemia, SM premórbido, insuficiencia cardiaca, fibrilación auricular y ERC. El resto de las prevalencias crudas eran significativamente mayores en la población masculina, excepto la inactividad física, la obesidad abdominal, el hipotiroidismo, y el C-HDL≥60mg/dL que eran significativamente mayores en la población femenina.
Características cualitativasa de la población de estudio
| Población de estudio n=6.631 | Población masculina n=2.934 | Población femenina n=3.697 | Valor de p | |
|---|---|---|---|---|
| Tabaquismo | 1.431 (21,6) | 756 (25,8) | 675 (18,3) | <0,001 |
| EPOC | 246 (3,7) | 182 (6,2) | 64 (1,7) | <0,001 |
| Etilismo | 610 (9,2) | 503 (17,1) | 107 (2,9) | <0,001 |
| Inactividad física | 3.092 (46,6) | 1.259 (42,9) | 1.833 (49,6) | <0,001 |
| Normopeso | 2.152 (32,5) | 771 (26,3) | 1.381 (37,4) | <0,001 |
| Sobrepeso | 2.530 (38,2) | 1.307 (44,5) | 1.223 (33,1) | <0,001 |
| Obesidad | 1.835 (27,7) | 834 (28,4) | 1.001 (27,1) | 0,224 |
| Obesidad central | 2.928 (44,2) | 1.106 (37,7) | 1.822 (49,3) | <0,001 |
| Obesidad central (IDF) | 4.329 (65,3) | 1.744 (59,4) | 2.585 (69,9) | <0,001 |
| ICT≥0,55 | 3.705 (55,9) | 1.785 (60,8) | 1.920 (51,9) | <0,001 |
| Prediabetes CDA | 519 (7,8) | 252 (8,6) | 267 (7,2) | 0,043 |
| Prediabetes ADA | 1.447 (21,8) | 701 (23,9) | 746 (20,2) | <0,001 |
| DM) | 1.033 (15,6) | 568 (19,4) | 465 (12,6) | <0,001 |
| DM tipo 1 | 58 (0,9) | 30 (1,0) | 28 (0,8) | 0,288 |
| DM tipo 2 | 975 (14,7) | 538 (18,3) | 437 (11,8) | <0,001 |
| Hipertensión arterial | 2.548 (38,4) | 1.223 (41,7) | 1.325 (35,8) | <0,001 |
| Hipercolesterolemia | 4.063 (61,3) | 1.800 (61,3) | 2.263 (61,2) | 0,919 |
| C-HDL<40/45mg/dL | 1.346 (20,3) | 839 (28,6) | 507 (13,7) | <0,001 |
| C-HDL<40/50mg/dL | 1.808 (27,3) | 839 (28,6) | 969 (26,2) | 0,030 |
| C-HDL≥60mg/dL | 2.174 (32,8) | 541 (18,4) | 1.633 (44,2) | <0,001 |
| Hipertrigliceridemia | 1.936 (29,2) | 1.063 (36,2) | 873 (23,6) | <0,001 |
| Dislipidemia aterogénica (45) | 764 (11,5) | 508 (17,3) | 256 (6,9) | <0,001 |
| Dislipidemia aterogénica (50) | 934 (14,1) | 508 (17,3) | 426 (11,5) | <0,001 |
| SM premórbido (AHA) | 1.412 (20,6) | 623 (21,2) | 789 (21,3) | 0,928 |
| SM (AHA) | 2.618 (39,5) | 1.279 (43,6) | 1.339 (36,2) | <0,001 |
| SM premórbido (IDF) | 1.650 (24,9) | 724 (24,7) | 926 (25,0) | 0,732 |
| SM (IDF) | 2.623 (41,0) | 1.266 (43,1) | 1.456 (39,4) | 0,002 |
| SMb premórbido | 1.629 (24,6) | 728 (24,8) | 901 (24,4) | 0,688 |
| SMb | 2.847 (42,9) | 1.392 (47,4) | 1.455 (39,4) | <0,001 |
| Hipotiroidismo | 648 (9,8) | 102 (3,5) | 546 (14,8) | <0,001 |
| Esteatosis hepática | 580 (8,7) | 384 (13,1) | 196 (5,3) | <0,001 |
| Enfermedad coronaria | 319 (4,8) | 210 (7,2) | 109 (2,9) | <0,001 |
| ACV | 250 (3,8) | 128 (4,4) | 122 (3,3) | 0,027 |
| EAP | 150 (2,3) | 94 (3,2) | 56 (1,5) | <0,001 |
| ECV | 613 (9,2) | 369 (12,6) | 244 (6,6) | <0,001 |
| DM o ECV | 1.407 (21,2) | 784 (26,7) | 623 (16,9) | <0,001 |
| AFECVp | 387 (5,8) | 169 (5,8) | 218 (5,9) | 0,833 |
| Insuficiencia cardiaca | 183 (2,8) | 80 (2,7) | 103 (2,8) | 0,940 |
| Fibrilación auricular | 247 (3,7) | 108 (3,7) | 139 (3,8) | 0,896 |
| EUA≥30mg/dL (n=4.402) | 347 (7,9) | 198 (10,0) | 149 (6,2) | <0,001 |
| CAC≥30mg/g (n=4.402) | 369 (8,4) | 206 (10,4) | 163 (6,8) | <0,001 |
| FGe<60mL/min/1,73m2 (n=6.506) | 522 (8,0) | 215 (7,5) | 307 (8,4) | 0,183 |
| ERC (n=6.506) | 748 (11,5) | 335 (11,7) | 413 (11,3) | 0,667 |
| RCV bajo | 2.186 (33,0) | 728 (24,8) | 1.458 (39,4) | <0,001 |
| RCV moderado | 1.395 (21,0) | 624 (21,9) | 753 (20,4) | 0,133 |
| RCV alto | 1.010 (15,2) | 480 (16,4) | 530 (14,3) | 0,023 |
| RCV muy alto | 1.694 (25,5) | 890 (30,3) | 804 (21,7) | <0,001 |
| RCV extremo | 346 (5,2) | 194 (6,6) | 152 (4,1) | <0,001 |
ACV: enfermedad cerebrovascular o ictus; ADA: American Diabetes Association; AFECVp: antecedente de ECV prematura en familiar de primer grado; AHA: American Heart Association; ATPIII: Adult Treatment Panel III; CAC: cociente albúmina-creatinina; C-HDL: colesterol unido a lipoproteínas de alta densidad; CDA: Canadian Diabetes Association; EAP: enfermedad arterial periférica; ECV: enfermedad cardiovascular; ERC: enfermedad renal crónica; DM: diabetes mellitus; EPOC: enfermedad pulmonar obstructiva crónica; EUA: excreción urinaria de albúmina; FGe: tasa de filtrado glomerular estimada según CKD-EPI (Chronic Kidney Disease EPIdemiology collaboration); ICT: índice cintura-talla; IDF: International Diabetes Federation; IMC: índice de masa corporal (peso/talla2); NCEP-ATPIII: National Cholesterol Education Program-Adult Treatment Panel III; NHLBI: National Heart, Lung, and Blood Institute; RCV: riesgo cardiovascular; SM: síndrome metabólico; Valor de p: de la diferencia de medias entre las poblaciones masculina y femenina.
Normopeso24: IMC entre 18,5 y 24,9kg/m2. Sobrepeso24: IMC entre 25,0 y 29,9kg/m2. Obesidad24: IMC≥30kg/m2. Obesidad central13: Perímetro abdominal≥102cm (hombres) o≥88cm (mujeres). Obesidad central (IDF)12: ≥94cm (hombres) o≥80cm (mujeres). Prediabetes CDA19: glucemia entre 110 y 125mg/dL, o HbA1c entre el 6% y el 6,4%. Prediabetes ADA18: glucemia entre 100 y 125mg/dL, o HbA1c entre el 5,7% y el 6,4%. C-HDL<40/45: colesterol unido a lipoproteínas de alta densidad<40mg/dL (hombres) o<45mg/dL (mujeres). C-HDL<40/50: ídem<50mg/dL (mujeres). Dislipidemia aterogénica (45): hipertrigliceridemia y C-HDL<45mg/dL (mujeres). Dislipidemia aterogénica (50): hipertrigliceridemia y C-HDL<50mg/dL (mujeres). SM (AHA)10,11: síndrome metabólico según NCEP-ATPIII/NHLBI/AHA. SM (IDF)12: Síndrome metabólico según IDF. FGe: Tasa de filtrado glomerular estimada según CKD-EPI28.
La ECV originó 119.778 defunciones en 2016, siendo la primera causa de muerte (30%) en la población española33. Durante los últimos años la mortalidad cardiovascular se ha reducido gracias a la intervención sobre FRCV como el tabaquismo, la HTA y la hipercolesterolemia. Sin embargo, la intervención no ha sido tan beneficiosa34 sobre los hábitos alimentarios, la inactividad física, la obesidad y la DM. La información preliminar que se ofrece en el presente artículo describe la situación epidemiológica de una población en la que se mantiene una elevada prevalencia de los FRCV relacionados con los estilos de vida y de la morbilidad relacionada con el metabolismo. La población de estudio presentaba unas características antropométricas y metabólicas cuantitativas que predisponen al diagnóstico de SM. La media de IMC indicaba sobrepeso grado ii o preobesidad; los perímetros de cintura superaban los límites establecidos por la IDF12, y la HbA1c rozaba el nivel límite inferior de prediabetes según la IDF12. Sin embargo, la población tenía unas medias de buen control de presión arterial, FGe, GPA y perfil lipídico.
De forma similar, las prevalencias crudas globales más elevadas fueron FRCV cardiometabólicos: Tabaquismo, inactividad física, sobrepeso, obesidad, obesidad abdominal, ICT aumentado, prediabetes, DM, HTA, hipercolesterolemia, HTG, dislipidemia aterogénica, SM, y SM premórbido. La alta prevalencia de FRCV cardiometabólicos favorece que el 21% de la población padeciera ECV o DM, y que el 31% tuviera un RCV muy alto o extremo.
Sin embargo, para valorar la verdadera magnitud epidemiológica y para comparar tasas de prevalencia entre distintas poblaciones es importante considerar que la edad y el sexo son factores que están directamente relacionados con los FRCV, las enfermedades cardiovasculares y morbilidad cardiometabólica. Por ello es necesario analizar no solo las prevalencias crudas sino las tasas de prevalencia específicas estratificadas por grupos etarios, y las tasas de prevalencias globales ajustadas por edad y sexo.
En España existen importantes diferencias territoriales tanto en la prevalencia como en el grado de control de los FRCV35. Se ha demostrado que las estrategias de prevención poblacionales son muy beneficiosas1, por lo que es fundamental determinar un diagnóstico de salud de la población que incluya todos los factores relacionados con la patología cardiovascular.
El estudio SIMETAP pretende ofrecer una actualización de la dimensión epidemiológica de los FRCV, ECV, SM y morbilidad metabólica relacionada. Esta actualización facilitaría la comparación entre distintas poblaciones, podría estimular la intervención sanitaria y animar a las autoridades sanitarias a intensificar estrategias de prevención poblacionales aplicando más eficientemente los recursos disponibles .El presente artículo es el preámbulo de posteriores análisis más detallados de tasas de prevalencia tanto estratificadas por grupos etarios como ajustadas por edad y sexo con poblaciones de referencia de la Comunidad de Madrid y de España.
ConclusionesEl presente estudio muestra una población con unas medias de buen control de presión arterial, FGe, GPA y perfil lipídico. Sin embargo, sus características antropométricas de sobrepeso, obesidad central (según los criterios de la IDF), y una media de HbA1c (5,6%) sugieren favorecer el diagnóstico de prediabetes o SM.
Las prevalencias crudas globales más elevadas se registraron en estilos de vida inadecuados (tabaquismo, inactividad física, obesidad) y morbilidad cardiometabólica (prediabetes, DM, HTA, dislipidemias y SM). Esta alta prevalencia puede favorecer que un elevado porcentaje de la población tenga un RCV alto o muy alto.
Para precisar la verdadera dimensión epidemiológica y poder comparar entre poblaciones es necesario realizar el análisis de las tasas de prevalencia estratificadas por grupos etarios y ajustadas por edad y sexo.
FinanciaciónLa Agencia «Pedro Laín Entralgo» de Formación, Investigación y Estudios Sanitarios de la Comunidad de Madrid (n.o beca: RS05/2010) proporcionó financiación económica para la realización del presente estudio. La Comisión de Investigación de la Gerencia Adjunta de Planificación y Calidad de la Gerencia de Atención Primaria de la Comunidad de Madrid emitió el informe favorable para su realización.
Conflicto de interesesCon relación a este estudio, los autores declaran que no ha habido ninguna influencia en los resultados ni en la interpretación de los mismos, por lo que no tienen ningún conflicto de intereses.
Agradecemos la asistencia y colaboración de los siguientes médicos que han participado en el Grupo de investigación del Estudio SIMETAP:
Abad Schilling C., Adrián Sanz M., Aguilera Reija P., Alcaraz Bethencourt A., Alonso Roca R., Álvarez Benedicto R., Arranz Martínez E., Arribas Álvaro P., Baltuille Aller M.C., Barrios Rueda E., Benito Alonso E., Berbil Bautista M.L., Blanco Canseco J.M., Caballero Ramírez N., Cabello Igual P., Cabrera Vélez R., Calderín Morales M.P., Capitán Caldas M., Casaseca Calvo T.F., Cique Herráinz J.A., Ciria de Pablo C., Chao Escuer P., Dávila Blázquez G., de la Peña Antón N., de Prado Prieto L., del Villar Redondo M.J., Delgado Rodríguez S., Díez Pérez M.C., Durán Tejada M.R., Escamilla Guijarro N., Escrivá Ferrairó R.A., Fernández Vicente T., Fernández-Pacheco Vila D., Frías Vargas M.J., García Álvarez J.C., García Fernández M.E., García García Alcañiz M.P., García Granado M.D., García Pliego R.A., García Redondo M.R., García Villasur M.P., Gómez Díaz E., Gómez Fernández O., González Escobar P., González-Posada Delgado J.A., Gutiérrez Sánchez I. Hernández Beltrán M.I., Hernández de Luna M.C., Hernández López R.M., Hidalgo Calleja Y., Holgado Catalán M.S., Hombrados Gonzalo M.P., Hueso Quesada R., Ibarra Sánchez A.M., Iglesias Quintana J.R., Íscar Valenzuela I., Iturmendi Martínez N., Javierre Miranda A.P., López Uriarte B., Lorenzo Borda M.S., Luna Ramírez S., Macho del Barrio A.I., Magán Tapia P., Marañón Henrich N., Mariño Suárez J.E., Martín Calle M.C., Martín Fernández A.I., Martínez Cid de Rivera E., Martínez Irazusta J., Migueláñez Valero A., Minguela Puras M.E., Montero Costa A., Mora Casado C., Morales Cobos L.E., Morales Chico M.R., Moreno Fernández J.C., Moreno Muñoz M.S., Palacios Martínez D., Pascual Val T., Pérez Fernández M., Pérez Muñoz R., Plata Barajas M.T., Pleite Raposo R., Prieto Marcos M., Quintana Gómez J.L., Redondo de Pedro S., Redondo Sánchez M., Reguillo Díaz J., Remón Pérez B., Revilla Pascual E., Rey López A.M., Ribot Catalá C., Rico Pérez M.R., Rivera Teijido M., Rodríguez Cabanillas R., Rodríguez de Cossío A., Rodríguez de Mingo E., Rodríguez Rodríguez A.O., Rosillo González A., Rubio Villar M., Ruiz Díaz L., Ruiz García A., Sánchez Calso A., Sánchez Herráiz M., Sánchez Ramos M.C., Sanchidrián Fernández P.L., Sandín de Vega E., Sanz Pozo B., Sanz Velasco C., Sarriá Sánchez M.T., Simonaggio Stancampiano P., Tello Meco I., Vargas-Machuca Cabañero C., Velazco Zumarrán J.L., Vieira Pascual M.C., Zafra Urango C., Zamora Gómez M.M., Zarzuelo Martín N.