El lupus eritematoso sistémico (LES) es una enfermedad crónica autoinmune que potencialmente causa inflamación y daño en cualquier órgano y/o sistema. Presentamos el caso de un paciente varón de 18 años de edad, que acude al servicio de nefrología por presentar en estudio de rutina elevación de creatinina sérica negando cualquier tipo de sintomatología; encontrando como hallazgo sérico indirecto únicamente C3 disminuido durante el estudio inicial. Se realiza una revisión de la literatura describiendo las características de esta enfermedad.
Systemic Lupus Erythematosus (SLE) is an autoimmune chronic disease that causes potentially systemic injury or/and inflammation. We report a case of a 18 year old Mexican man; presenting with serum creatinine elevation in a routine laboratories without any symptoms. We only found C3 alterations at the initial study. We provide a review of the literature describing Systemic lupus erythematosus characteristics.
La nefritis lúpica afecta del 30 al 50% de los pacientes con lupus eritematoso sistémico (LES). El compromiso renal se manifiesta con la presencia de proteinuria, sedimento activo con eritrocitos dismórficos, cilindros eritrocitarios y otros elementos formes, puede presentar deterioro en la tasa de filtración glomerular, aunque la expresión clínica e histológica es extremadamente variable. Entre los factores de mal pronóstico se encuentran sexo varón, esclerosis glomerular, depósitos subendoteliales, presencia de ANCA, atrofia tubular, fibrosis intersticial, deterioro de la tasa de filtrado glomerular, complemento (C3-C4) y hematocrito bajo.
Reporte de casoPaciente varón de 18 años de edad quien acude a consulta por presentar en química sanguínea de control, elevación de creatinina sérica; negando sintomatología agregada. Sin antecedentes de importancia que comentar. Se inicia protocolo de estudio y se realiza biopsia renal (tabla 1).
Laboratorios y gabinete de admisión
| Laboratorio y gabinete de admisión | Valor |
|---|---|
| Hb | 14g/dl |
| Hct | 45% |
| Leucocitos | 5,6×103μl |
| Plaquetas | 157mil |
| Creatinina | 3,7mg/dl |
| BUN | 34mg/dl |
| Proteínas totales | 4,7g/dl |
| Albúmina | 1,8g/dl |
| Triglicéridos | 130mg/dl |
| Colesterol total | 249mg/dl |
| VSG | 40mm/h |
| PCR | 206mg/dl |
| Proteínas en orina 24h | 5,24g/dl |
| Depuración de creatinina en orina en 24h | 44,9ml/min |
| Panel viral (VH, VHB, VHC) | No reactivo |
| Inmunoglobulinas IgA, IgM, IgG | Normales |
| Complemento C3 | Disminuido 49,7mg/dl (87-200) |
| Complemento C4 | Normal 21mg/dl (19-52) |
| Sedimento urinario | Cilindros hialinos, 5 eritrocitos por campo isomórficos, lipiduria |
| Anticuerpos anti-PR3 | Ausentes |
| Anticuerpos anti-SSA | Ausentes |
| ANA | Ausentes |
| Anti-DNAdc | Ausentes |
| Anticuerpos anti-MPO | Ausentes |
| Anticardiolipinas IgM e IgG | Ausentes |
| Anticoagulante lúpico | Ausente |
| Anti-Sm | Ausente |
| Anti-RNP | Ausente |
| Ultrasonido renal | RD: 10,2×7,4×4,5cm relación corteza-médula conservada, sin alteración estructuralRI: 10,2×5,7×4,2cm relación corteza-médula conservada, sin alteración estructural |
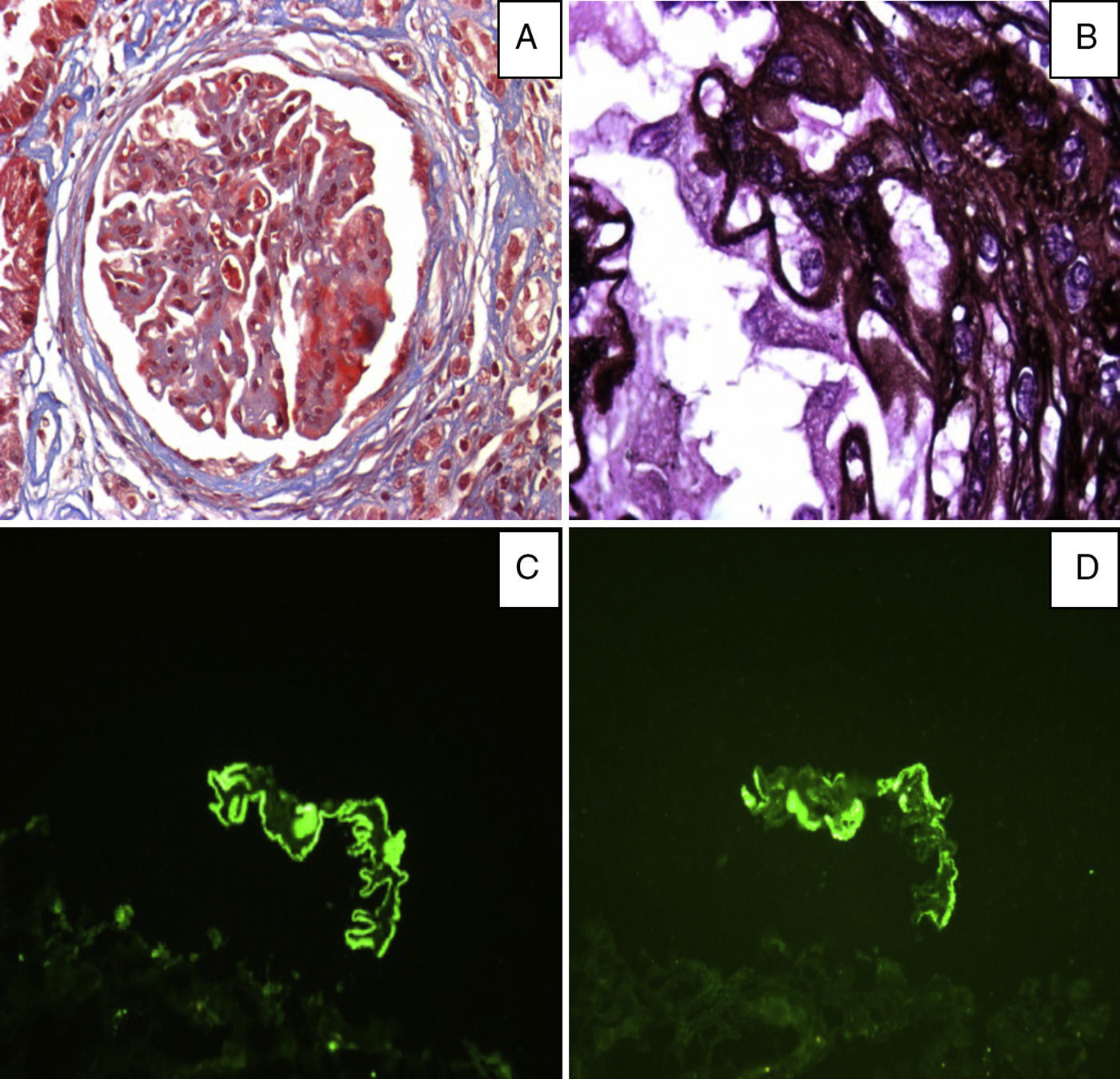
La microscopia de luz mostró 14 glomérulos, 6 con esclerosis global, 8 con proliferación del endotelio mesangial, daño acentuado de las membranas basales glomerulares con defectos de llenado y espículas, depósitos subepiteliales y escasos subendoteliales, con fibrosis difusa >40% (grado III) y atrofia tubular. La inmunofluorescencia directa resultó positiva con patrón granular en membranas basales glomerulares para IgG, C1q, C3c, kappa y lambda.
La microscopia electrónica mostró datos de cicatrización avanzada y membranas basales con depósito de complejos inmunes (fig. 1).
A) Tricrómico de Masson (×40) Se observa ensanchamiento y proliferación mesangial, así como proliferación endocapilar segmentaria, con algunos depósitos fuschinofílicos subendoteliales. B) Metamina de Jones (×100) Se pueden observar defectos de llenado y pequeñas espículas. Los podocitos están prominentes. C) Microscopia por inmunofluoresencia: IgG con patrón granular fino en las membranas basales glomerulares, D) C1q con algunos depósitos subendoteliales.
Solicitamos nuevamente inmunológicos obteniendo los siguientes resultados: anti-PR3 5,9U/ml (<3,5), anti-SSA 734U/ml (<9), ANA+1:1.200; anti-Sm 10U/ml (<7,6), anti-DNAdc 50U/ml (<9,6) resto de autoanticuerpos ausentes, complemento disminuido C3 30,7mg/dl y C4 5,2mg/dl; desarrollándose posteriormente artritis (hipersensibilidad e inflamación en dedos índices, muñecas), fotosensibilidad severa y úlceras orales.
DiscusiónEl término lupus eritematoso fue introducido por los médicos del siglo XIX para describir lesiones de piel, requiriendo aproximadamente 100 años para descubrir que la enfermedad es sistémica y que está causada por una respuesta autoinmune alterada. La heterogeneidad de la enfermedad forzó a establecer el diagnóstico con 11 criterios, requiriendo 4 para un diagnóstico formal de LES1.
La nefritis lúpica permanece como una de las manifestaciones más graves del LES, la cual se asocia con mayor morbimortalidad de los pacientes2.
En años recientes, algunos nuevos marcadores han sido identificados, por ejemplo, el ligando sérico de inducción de proliferación (APRIL, por sus siglas en ingles), con el potencial para pronosticar los casos de poca respuesta al tratamiento en la nefritis lúpica entre otros3.
El papel del complemento en la patogénesis del LES es paradójico. Por una parte, el sistema del complemento parece tener efectos de protección; ya que un riesgo aumentado para desarrollar lupus se asocia con las deficiencias hereditarias de la vía clásica; por otra parte, la activación de complejos inmunes mediados por el complemento en tejidos afectados es evidente en los pacientes con lupus4.
Existen datos contradictorios en cuanto al uso del complemento C3 y C4 y su consumo en el diagnóstico de LES; reportándose baja sensibilidad y especificidad para ambos, mencionándose cierto beneficio en la detección de las recaídas con consumo de C4 y relacionando el consumo de C3 con la afección predominante e importante a tejidos5–8.
Algunos pacientes se presentan con alteraciones clínicas sugerentes de enfermedad autoinmune con autoanticuerpos negativos, denominándose enfermedad autoinmune seronegativa, considerando la probabilidad de autoinmunidad latente, pre-clínica o pos-clínica.
Por lo anterior debemos tener en cuenta la posibilidad de que los anticuerpos no sean el único factor patógeno, y que existe alteración en el método de detección o alteración inmunológica.
Ante anticuerpos negativos se deben verificar como posibilidades su ausencia real, dificultad para la detección de algunas especificidades, exceso de antígenos circulantes (fenómeno prozone) o niveles bajos de inmunoglobulinas asociados con proteinuria masiva9,10.
En la década de los 70, el LES ANA negativo se presentaba únicamente en el 5% de los casos; con ausencia generalmente de anti-Sm y anti-DNA de forma concomitante con ANA negativo.
Los casos ANA negativo se correlacionan con presencia de autoanticuerpos SSA/Ro, siendo percibidos como parte del espectro clínico de LES, añadiendo peso específico a su diagnóstico; caracterizándose por fotosensibilidad severa y en raras ocasiones nefritis lúpica.
Actualmente con los avances que se han logrado en la medición de los anticuerpos se considera extremadamente rara la ausencia de este anticuerpo y en pocas ocasiones (como en este caso) de primera instancia los anticuerpos son negativos para posteriormente volverse positivos11–13.
En nuestro paciente el único marcador serológico inicial evidente fue el consumo de C3, correlacionándose con el extenso daño en tejidos (esclerosis importante en la biopsia renal) y la pobre respuesta al tratamiento.
Como tratamiento se indica esquema de remisión para nefritis lúpica, 3 pulsos de metilprednisolona 1g intravenoso, prednisona 30mg/24h, micofenolato de mofetilo 3g/24h, hidroxicloroquina 400mg/24h, losartan 50mg/12h, atorvastatina 40mg/24h14–16; sin respuesta adecuada hasta el momento.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses