Modern society depends on non-renewable energy sources like petroleum hydrocarbons for transportation fuel. There is currently a great interest in developing new sources and processes for biofuels. Ethanol is a promising biofuel obtained from carbohydrate fermentation by baker’s yeast (Sac-charomyces cerevisiae). In this work, we present a set of teaching lab sessions where students prepare fermentations and produce first (free sugars and starch) and second (cellulose) generation bioethanol. Several carbohydrate sources produced in the tropical regions of Mexico and the Americas were tested, for example, juice (pineapple, sugarcane, grape and apple), tuberous crops (cassava, potato and sweet potato) and cellulose (sugarcane leaves and recycled paper). Sessions were developed as supervised research projects and students learnt and discussed the principles and challenges of ethanol biofuel production.
La sociedad moderna depende del petróleo —una fuente no renovable— para obtener el combustible necesario para trasladar personas y productos. Actualmente existe el interés de desarrollar fuentes renovables y procesos de producción de biocombustibles. Entre las más importantes está el bioetanol que se produce a partir de fuentes de carbohidratos mediante la fermentación microbiana, especialmente por la levadura del pan (Saccharomyces cerevisiae). En este trabajo se presenta una serie de prácticas de laboratorio en las que los estudiantes desarrollan fermentaciones para producir bioetanol de primera (azúcares libres y almidón) y segunda generación (celulosa). Debido a que las zonas tropicales de México y de otros países americanos se están considerando como las más propicias para el cultivo de las materias primas vegetales, se probaron fuentes de carbohidratos de estas regiones tales como jugos (piña, caña de azúcar, uva y manzana), almidón de tubérculos (camote, papa y malanga) y celulosa (hojas de caña y papel reciclado). Las prácticas se desarrollaron como investigación dirigida y con ellas se aprenden y discuten los principios y los retos de la producción de etanol como biocombustible.
Para movilizar a las personas y a los productos, la sociedad moderna depende de las máquinas de combustión interna que usan gasolina. Este combustible se produce por medio de refinación del petróleo, una fuente natural no renovable. A pesar de que México es el séptimo productor volumétrico de petróleo en el mundo, es un país importador de gasolina. El 50% de los 135 millones de litros diarios de gasolina que se consumen en México son importados, mayoritariamente de Estados Unidos. Este escenario de fuentes energéticas convencionales es más desalentador si se toma en cuenta que los expertos calculan que México se convertirá en un importador neto de petróleo en el año 2020 (USEIA, 2011).
Esta problemática no solo es de México, sino también internacional. Ante esto, los científicos están explorando alternativas de combustibles que se puedan producir de forma masiva como la gasolina pero que, a diferencia de ésta, se puedan obtener de fuentes renovables, como las plantas de cultivo tropicales (SE, 2006; USDE, 2006; EPE, 2009).
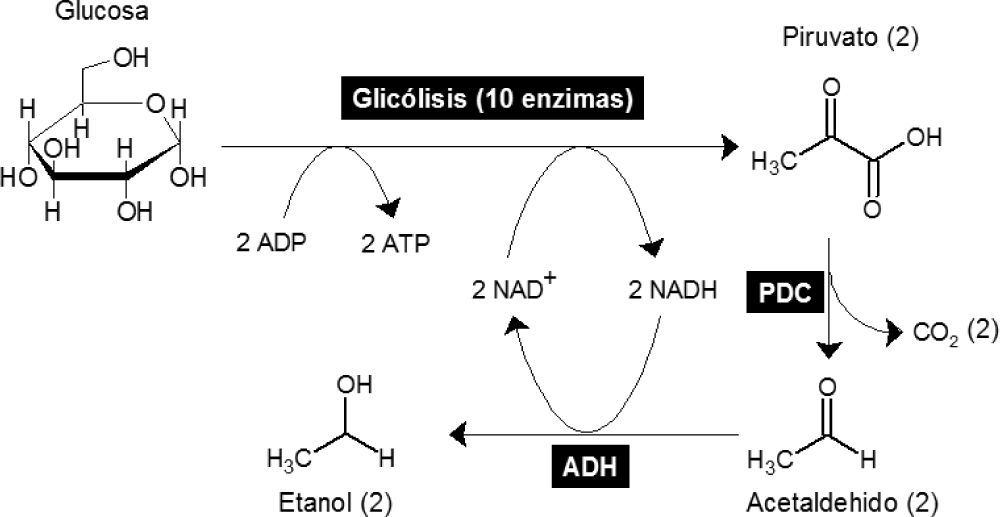
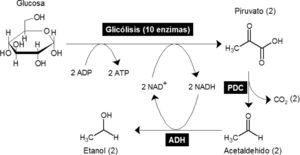
El combustible que cumple con estas características y que parece ser el más prometedor es el bioetanol (USDE, 2006). El bioetanol se sintetiza bioquímicamente por las levaduras como el producto final de la glucólisis y de la regeneración anaerobia de NAD+ (figura 1). De esta forma, cualquier fuente de carbohidratos tiene el potencial de transformarse en etanol. Si esta fuente de carbohidratos es de origen vegetal, se recupera de forma indirecta la energía luminosa captada durante la fotosíntesis (figura 2; USDE, 2006).
La glicólisis y la fermentación son las rutas metabólicas por las que se sintetiza etanol en la levadura del pan Saccharomyces cerevisae.
Mediante una ruta bioquímica de 10 reacciones enzimáticas diferentes conocida como la glicólisis, una molécula de glucosa se oxida para producir dos moléculas de piruvato. En el proceso, también se sintetizan dos moléculas de Adenosin Trifosfato (ATP) a partir de Adenosin Difosfato (ADP) y dos de Dinucleótido de Adenina y Nicotinamida reducido (NADH) a partir de NAD+ también llamado NAD oxidado. El ATP es una molécula de alta energía que se utiliza en la célula para transportar la energía extraída de la glucosa, y el NADH es un acarreador de electrones. Para que la glicó-lisis continúe funcionando, el NAD+ necesita ser regenerado a partir de NADH; esto se logra gracias a la fermentación. La fermentación consiste en la conversión de piruvato en etanol gracias a la catálisis de las enzimas piruvato descarboxilasa (PDC) y de la alcohol deshidrogenasa (ADH). Así, se puede considerar que el etanol es el residuo metabólico de la extracción de energía de la glucosa.
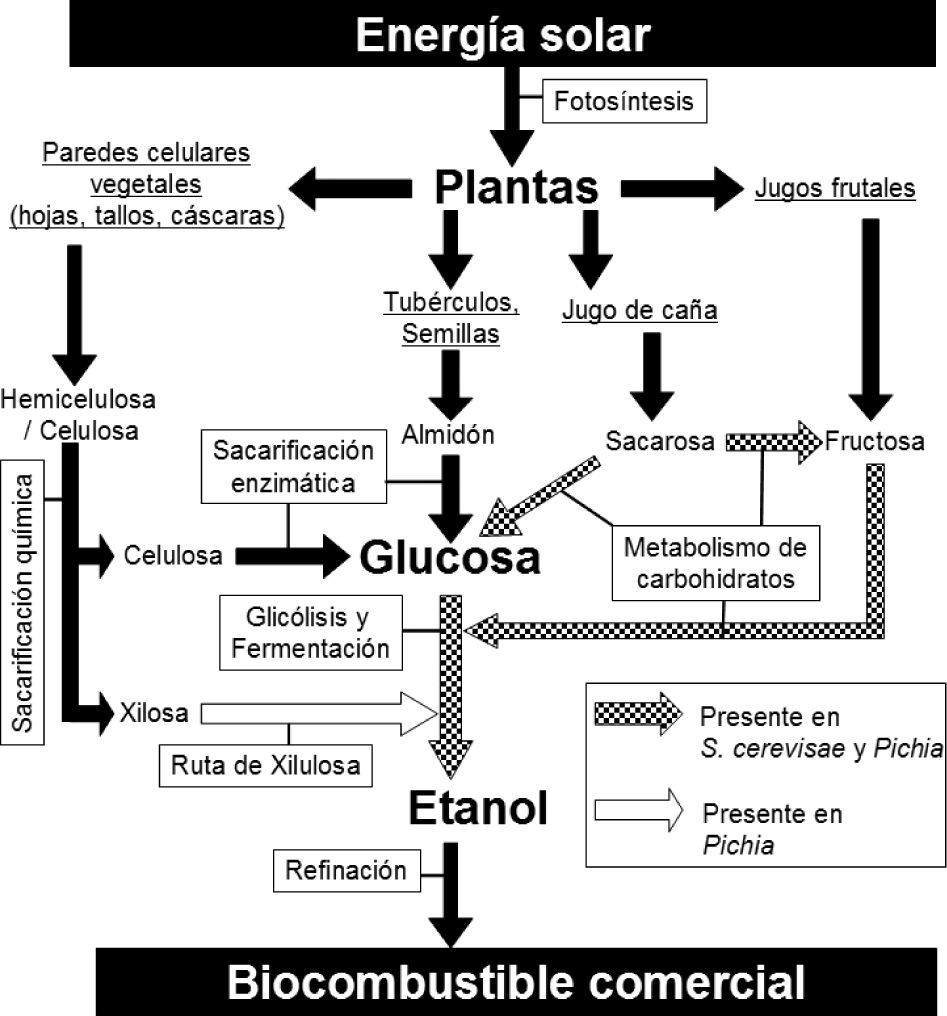
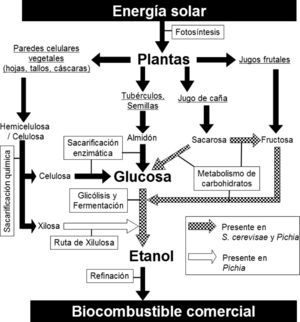
Materias primas, rutas metabólicas y procesos para la producción de bioetanol.
Las plantas utilizan la energía solar capturada durante la fotosíntesis para producir moléculas de carbono que funcionan como soportes estructurales (hemicelulosa y celulosa), reservas energéticas (almidón) y fuente de nutrientes (sacarosa y fructosa). Las moléculas más complejas como la celulosa y la hemicelulosa se pueden procesar química y enzimáticamente para producir sus monómeros, que son glucosa (seis carbonos) y xilosa (cinco carbonos), respectivamente. La glucosa se puede utilizar por la levadura del pan (Saccharomyces cerevisiae) durante la glicólisis y la fermentación para sintetizar etanol de manera anaerobia. La xilosa no puede ser utilizada por cepas silvestres de S. cerevisiae, pero sí por otras levaduras como las del género Pichia o por cepas transgénicas de S. cerevisiae. El polímero llamado almidón se puede tratar química o enzimáticamente para liberar sus monómeros de glucosa e incorporarlos a la glicólisis y fermentación. Las moléculas más sencillas como la sacarosa y fructosa se pueden incorporar mediante rutas metabólicas convergentes a la glicólisis y a la fermentación para sintetizar etanol. Sin importar la materia prima, el bioetanol se tiene que someter a un proceso de refinación donde se separa, purifica y deshidrata para usarse como biocombustible.
Cuando la obtención de etanol es a partir de carbohidratos solubles de origen vegetal —por ejemplo, la sacarosa— o de polímeros simples como el almidón, se la denomina producción de primera generación; cuando se obtiene de polímeros de carbohidratos complejos como la hemicelulosa y la celulosa se le denomina de segunda generación (GFM, 2010). Mientras que los procesos de primera generación son relativamente simples, sus materias primas (frutos, tubérculos, jugos) no son abundantes, con la notoria excepción de la caña de azúcar. Por otro lado, los procesos de segunda generación son complejos pero sus fuentes son abundantes (ej. hojas, aserrín, pastos y residuos agrícolas; USDE, 2006).
Las materias primas vegetales para la producción de etanol se pueden colocar en cuatro grupos (figura 2): jugos frutales, biomasa de pastos, tubérculos y residuos agroindus triales. Los jugos de frutas son simples de usar para producir etanol, de hecho, el proceso milenario de hacer vino es similar salvo que no existe un paso de purificación del etanol por medio de la destilación fraccionada (Epstein, et al., 2010). Las fuentes no frutales de jugos vegetales no son tan variadas, pero sí son abundantes; tales son los casos de la caña de azúcar (cultivo tropical) y la remolacha (cultivo de zonas frías), y ambos son fácilmente fermentables (BDB, 2008). Los tubérculos se han propuesto recientemente como cultivos para bioetanol y su preprocesamiento es sencillo (Purohit y Mishra, 2012); sin embargo, su productividad en campo es menor a la de la caña de azúcar, y al igual que las semillas de los pastos (ej. maíz), son fuente de alimentación humana, teniendo su uso el riesgo de causar desabasto alimentario. Finalmente, los residuos agroindustriales si bien son abundantes, su uso es complejo pues primero se necesita sacarificar la materia prima, es decir, liberar carbohidratos simples como la glucosa de estructuras complejas como la lignocelulosa (USDE, 2006; Jutakanoke, et al., 2012).
La optimización de estos procesos, su estudio bioquímico y su implementación biotecnológica están actualmente en la frontera de la investigación moderna. Dos casos de éxito de esto último son Brasil, donde el bioetanol que se obtiene de la caña de azúcar ha sustituido en un 40% a la gasolina (BDB, 2008; EPE, 2009), y EUA, donde el bioetanol que se obtiene del almidón de maíz se usa rutinariamente en mezcla con gasolina (USDE, 2006).
En la actualidad existen grandes expectativas globales de usar tierras agrícolas ociosas o marginales en los trópicos para sembrar y expandir los cultivos útiles para la producción de biocombustibles (USDE, 2006). En México, los estados adyacentes al Golfo de México y al Océano Pacífico son candidatos ideales para la producción de bioetanol debido a sus condiciones climáticas y a la tradición centenaria de cultivo de caña de azúcar y pastos para ganadería (SE, 2006).
Debido a la imperante necesidad de desarrollar tecnologías que provean a la sociedad moderna de nuevas fuentes de combustibles, es necesario familiarizar desde temprano a los estudiantes de las carreras químicas y biotecnológicas de nivel medio y superior con los procesos de obtención de bioetanol y con los retos de su producción. Adicionalmente, también se debe promover en los estudiantes la capacidad de reconocer en su entorno las materias primas disponibles para el proceso.
De esta forma, en este trabajo presentamos una serie de demostraciones prácticas que pueden implementarse en cursos de bioquímica, biotecnología y bioprocesos, que ayudan a explicar los fundamentos y los retos de la producción de bioetanol.
2Materiales y métodos2.1Dinámica de trabajoLa estrategia de trabajo consistió en realizar las prácticas como proyecto de investigación dirigido. A los estudiantes se les presentó la idea del proyecto por el instructor y ellos decidieron qué materias primas utilizar (tabla 1). En cada práctica (ver secciones 2.4, 2.5 y 2.6) se dirigió a los estudiantes a resolver las preguntas que se detallan en la sección de Resultados y Discusión y a presentar estrategias alternativas a las usadas en la práctica. Finalmente, se les pidió un reporte grupal de sus resultados.
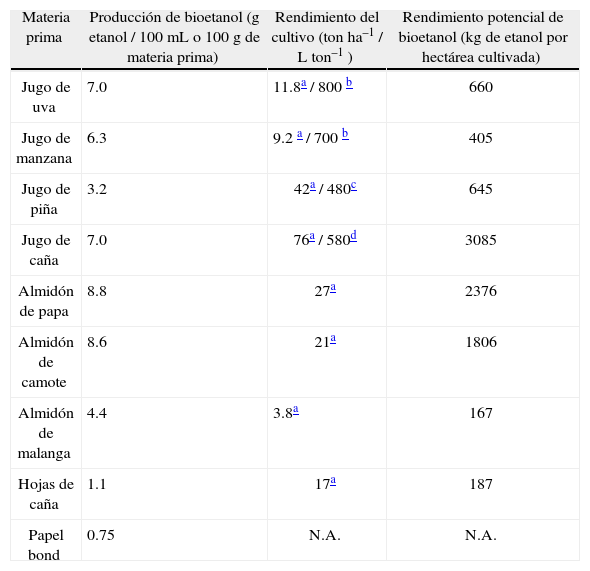
Cálculos de rendimiento potencial de bioetanol por hectárea cultivada de diversas materias primas seleccionadas y procesadas por los estudiantes. La densidad utilizada para convertir mililitros de etanol a gramos fue de 0.789g/cm3.
| Materia prima | Producción de bioetanol (g etanol / 100mL o 100 g de materia prima) | Rendimiento del cultivo (ton ha–1 / L ton–1 ) | Rendimiento potencial de bioetanol (kg de etanol por hectárea cultivada) |
| Jugo de uva | 7.0 | 11.8a / 800 b | 660 |
| Jugo de manzana | 6.3 | 9.2 a / 700 b | 405 |
| Jugo de piña | 3.2 | 42a / 480c | 645 |
| Jugo de caña | 7.0 | 76a / 580d | 3085 |
| Almidón de papa | 8.8 | 27a | 2376 |
| Almidón de camote | 8.6 | 21a | 1806 |
| Almidón de malanga | 4.4 | 3.8a | 167 |
| Hojas de caña | 1.1 | 17a | 187 |
| Papel bond | 0.75 | N.A. | N.A. |
N.A. No aplica pues es un deshecho ya procesado.
El organismo que se utilizó en todos los experimentos fue la levadura del pan Saccharomyces cerevisiae en forma de la presentación comercial liofilizada “La Pastora” en una relación 1.2% W/V. Las fermentaciones se llevaron a cabo por 24 horas a temperatura ambiente (28 °C) y sin agitación, a menos que se indique lo contrario. Como contenedor, se usaron matraces de 500 mL con un volumen máximo de sustrato de 250 mL. Los matraces se sellaron con tapones de goma y Parafilm. Los tapones tenían un orificio donde se introdujo un vidrio en forma de U con un extremo largo y uno corto. El extremo corto se colocó dentro del matraz y el largo se ubicó hacia afuera, de tal forma que pudiera sumergirse en una trampa de CO2 de 200 mL (Ca(OH)2, 1.5% W/V) para mantener un ambiente anaeróbico (Epstein et al., 2010).
2.3Métodos analíticosEl contenido de carbohidratos en las muestras clarificadas por centrifugación (4,000 g por 2 min), antes y después de la fermentación, se midió con un refractómetro digital portátil (Atago, EUA) y se expresó en grados Brix (porcentaje W/V de azúcares libres). De ser necesario, una vez clarificadas, las muestras se pueden guardar a 4 °C. El crecimiento de la levadura se midió por peso seco (24h a 70 °C) del sedimento centrifugado (2000 g por 2 min). El rendimiento de bioetanol se determinó mediante destilación fraccionada a 75 °C con un kit educativo (SEV, México). La pureza del destilado se verificó en diluciones con un alcoholímetro graduado en unidades Gay-Lussac (Mantey, México), oscilando entre 93-96%.
2.4Producción de etanol de primera generación a partir de jugos frutales, jugo de caña de azúcar y tubérculosLos jugos de uva y manzana se adquirieron de marcas comerciales como Jumex y Boing, mientras que el de piña se compró en mercados locales. El jugo de caña se obtuvo por prensado de cañas maduras (7 meses) recién cortadas. Todos se utilizaron en las fermentaciones directamente sin otro procesamiento. Para demostrar el crecimiento de la levadura y la cinética de producción de bioetanol, se montaron fermentaciones exclusivas para el muestreo en cada intervalo de tiempo, con lo que se evitó abrir y cerrar de los matraces, asegurando el mantenimiento de las condiciones anaeróbicas. Los ejemplos aquí presentados se hicieron con fermentaciones de 24 horas, pero las fermentaciones pueden ser estables hasta por 10 días, para el caso que se tengan sesiones de laboratorio semanales.
Las papas y los camotes se adquirieron en mercados locales. La malanga se obtuvo de la asociación Taro Gourmet. En todos los casos, los tubérculos sin cáscara se cortaron en cubos de 3 cm3 aproximadamente y se licuaron (70 g en 100 mL de H2O). Posteriormente y sin filtrarse, 100 mL del homogenizado se hidrolizaron agregando 25 mL de HCl 6N por 1h a 90 °C. Después se ajustó el pH a 6.0 con NaOH y se procedió a fermentar (Hoseinpour et al., 2010; Purohit y Mishra, 2012).
2.5Producción de etanol de segunda generación a partir de hojas de caña y de papel recicladoLas hojas de una planta de caña de azúcar de 3 meses de edad se cortaron en pequeñas tiras de aproximadamente 2 cm de ancho y se secaron durante 24h a 70°C. Después del secado, las tiras se pulverizaron en seco con una licuadora industrial (Waring, EUA). Para sacarificar la hemicelulosa y liberar la celulosa, se probaron dos tipos diferentes de hidrólisis: ácida y básica. Para realizar la hidrólisis ácida se pesaron 22 g de polvo de hojas y se agregaron 360 mL de H2SO4 (1.5% V/V) en un vaso de precipitados. Para realizar la hidrólisis alcalina se pesaron 22 g de polvo de hojas y se agregaron a 222 mL de NaOH (2% W/V) en un vaso de precipitados. Ambos recipientes se colocaron en autoclave a 15 psi durante 1h. Posteriormente, se dejaron atemperar, se filtraron al vacío y se separaron los líquidos de los sólidos.
Los líquidos se llevaron a pH 6.0 con H2SO4 o NaOH y se fermentaron (Sección 2.2) (Hernández-Salas, et al., 2009; Jutakanoke, et al., 2012). Los sólidos se filtraron a través de una malla cielo y se lavaron dos veces con agua estéril para posteriormente suspenderse en 360 mL de búffer de acetatos pH 5.0 (0.216g/L de ácido acético, 0.871g/L de acetato de sodio). Para lograr la sacarificación de la celulosa, al búffer se le agregaron 4 mL de la preparación enzimática (xilanasa, celulasa y hemicelulasa) comercial Viscozyme L (Sigma, EUA) y se incubaron a 50 °C por 24 horas en agitación constante (100 rpm). Finalmente, se filtró al vacío y se realizaron las fermentaciones con las siguientes modificaciones: se incubaron a 30 °C por 48 horas en agitación constante (180 rpm) y se enriquecieron con medio mínimo (KH2PO4 1.0g/L, CaCl2 0.1g/L, MgSO4 0.5g/L, NaCl 0.1g/L, peptona 5g/L). La sacarificación de hojas de papel se realizó de esta misma manera.
2.6Cuidados y seguridadSe debe tener cuidado con las soluciones concentradas de ácidos. Se recomienda que si se desean implementar a nivel de bachillerato, sea el instructor el encargado de pipetear y manejar el material de vidrio que estuvo en contacto con los ácidos. El etanol destilado es altamente infiamable, por lo que las destilaciones deben ser realizadas con mantas de calentamiento eléctricas.
Para demostrar la transformación de los carbohidratos en etanol y su uso como combustible, el instructor puede quemar cuidadosamente el etanol producido por los estudiantes en torundas o mechas para elevar un globo de plástico como se demuestra en el siguiente enlace de YouTube (http://bit.ly/Qo64MO).
3Resultados y discusiónLas demostraciones prácticas aquí reportadas se aplicaron para enseñar los fundamentos y los retos de la producción de bioetanol durante cursos de bioquímica en la licenciatura de Ingeniería Biotecnológica y en la Semana Nacional de Ciencia y Tecnología para bachillerato. Sin embargo, creemos que la facilidad de estas prácticas hace que sean también adecuadas para prácticas de secundaria.
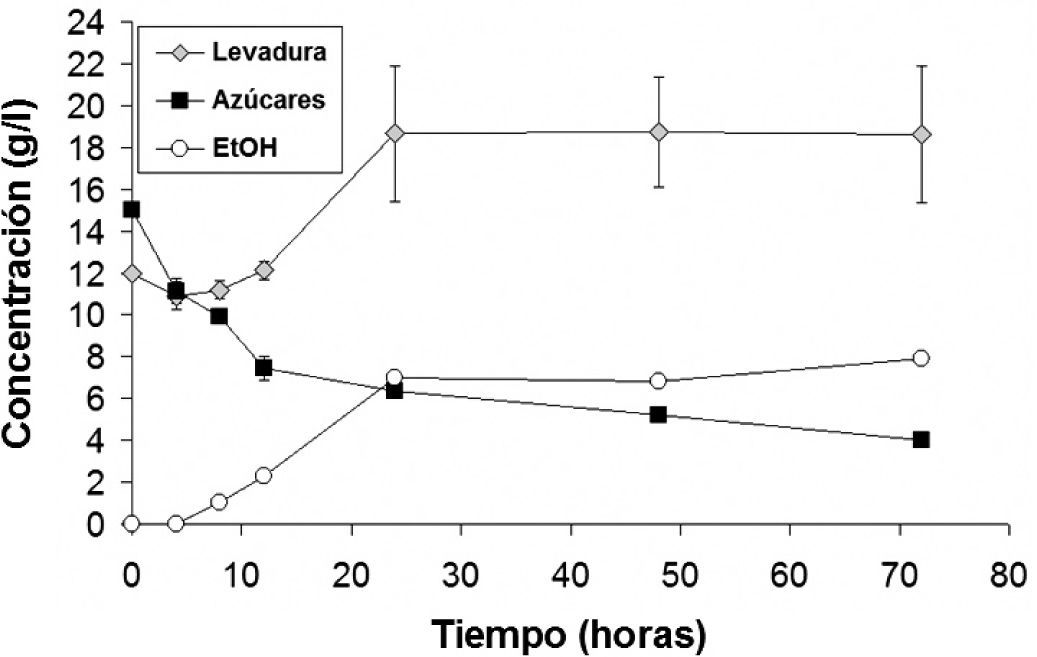
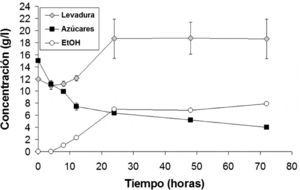
3.1Bioetanol a partir de jugos frutales y cinéticas de crecimientoCon el uso de jugos frutales se demostró a los estudiantes una cinética de producción de bioetanol, consumo de carbohidratos y aumento de biomasa. En la figura 3 se observa una cinética obtenida por los estudiantes. En ella se puede observar la relación inversa que hay entre la disminución de los carbohidratos solubles y el aumento de la biomasa con la producción de etanol durante las primeras 24h. Si la fermentación se deja avanzar más de 24h, se puede observar cómo, a pesar de que todavía hay carbohidratos solubles, tanto el crecimiento de la levadura como la producción de etanol se estacionan por efecto de inhibición del cultivo por etanol.
Demostración de la producción de bioetanol con jugo de uva y levadura del pan (S. cerevisiae).
Se presenta una cinética de crecimiento de levadura (rombos grises), consumo de carbohidratos (cuadros negros) y producción de bioetanol (círculos abiertos). Las barras de error indican desviación estándar.
Los estudiantes pueden realizar fácilmente el muestreo pues las fermentaciones de jugos son sencillas de hacer y no necesitan nutrientes extras. No obstante lo anterior, permiten observar signos de actividad biológica como el burbujeo, el cambio de color de la muestra y el olor del etanol. Durante este sencillo experimento, los estudiantes pueden resolver las siguientes preguntas:
- —
¿Cuál es el proceso de transformación que lleva a cabo la levadura (figura 1)?
- —
¿Cuál es el biocatalizador en la fermentación (figura 2)?
- —
¿Por qué se detuvo la fermentación cuando el etanol alcanzó el 7% de concentración (inhibición por producto, figura 3)?
- —
¿Cuál es el principio de separación del etanol en la destilación?
- —
¿Qué se puede hacer con los residuos de la fermentación (abono, levadura)?
Los estudiantes pueden investigar la productividad en peso de los cultivos ensayados y calcular rendimientos potenciales de cada uno de los jugos (tabla 1). De esta forma, se observará que el rendimiento final no solo depende del proceso de producción de bioetanol, sino también de la productividad de la materia prima en el campo. En este contraste los estudiantes observan que el jugo de caña de azúcar es el que más potencial tiene como fuente de materia prima para la obtención de bioetanol con un rendimiento teórico de hasta tres toneladas de etanol por hectárea sembrada. En los trópicos, los estudiantes pueden observar la potencialidad económica de sus regiones (generalmente subdesarrolladas y con pocas perspectivas de crecimiento social) y diseñar planes y estrategias para lograr una industrialización agrícola sustentable.
3.2Bioetanol a partir de hidrolizados de almidonesLos almidones se utilizaron para mostrar el potencial de fuentes más complejas de carbohidratos, así como la implementación de un pretratamiento químico para adecuar una materia prima a la producción de bioetanol. La producción de bioetanol a partir de tubérculos fue similar a la de jugos (tabla 1); sin embargo, al ser cultivos con menor rendimiento en el campo, quedaron atrás de la caña de azúcar en rendimiento potencial desde un 23% (papa), 40% (camote) y 90% (malanga) menos. Los tubérculos utilizados son los que se producen tradicionalmente (camote y papa) y otro de reciente introducción (malanga), es decir, unos con conocimiento agrícola fuerte y buena productividad, contra otro con conocimiento incipiente y por ende baja productividad.
En esta sección el estudiante aprende a realizar un método de sacarificación sencilla (hidrólisis ácida) y discute las ventajas (conocimiento agrícola, líneas de comercialización) y desventajas (aumento de precios, competición de mercados) de utilizar almidones que también sean comestibles. Durante este experimento el estudiante puede resolver las siguientes preguntas:
- —
¿Qué es la sacarificación?
- —
¿Puede haber un proceso donde haya una sacarificación enzimática de almidón?
- —
¿Puede haber problemas sociales si se usan fuentes de alimentos para producir bioetanol?
- —
¿Cómo se podría aumentar el área de cultivo de tubérculos sin afectar selvas o bosques?
Las prácticas de las secciones anteriores son sencillas y baratas de realizar. Por el contrario, las de esta sección son más laboriosas y requieren materiales como la mezcla enzimática Viscozyme L ($115 USD por 100 mL, suficiente para 25 demostraciones). Por otra parte, también es la sección donde el estudiante aprenderá los temas más avanzados de la producción de bioetanol como la sacarificación enzimática, las preferencias metabólicas de los microorganismos y el uso de cultivos no convencionales o residuos para la producción de bioetanol.
El estudiante observará que la levadura del pan no puede fermentar los hidrolizados (ácido y básico) de hojas de caña a pesar de tener un contenido de carbohidratos libres de hasta 12g/L, muy similar al de un jugo de frutas. Lo anterior se debe a que los hidrolizados están compuestos mayoritariamente de xilosa (Jutakanoke, et al., 2012), un carbohidrato de cinco carbonos que compone a la hemicelulosa y que no puede ser metabolizado por S. cerevisiae (figura 2). Se le puede enseñar al estudiante que mediante métodos avanzados de biología molecular se están incorporando en S. cerevisiae las rutas enzimáticas de otras levaduras que sí pueden fermentar a la xilosa, ej. Pichia, para que pueda asimilar este carbohidrato tan abundante (Ha, et al., 2010).
A primera vista el estudiante observa que sacarificar y producir bioetanol a partir de la celulosa es un trabajo laborioso y aparentemente de baja producción con solo un 15% de lo que se produce del jugo de caña. Sin embargo, cuando se compara el cálculo de rendimiento neto por hectárea (tabla 1), los estudiantes observan que es el proceso que mayor potencial tiene de producción pues es un material que se quema en el campo sin que su energía sea aprovechada. El estudiante podrá ver que al final del proceso tendrá mucho residuo sólido que todavía puede sacarificarse, siempre y cuando avance la investigación para aumentar la actividad de las enzimas celulolíticas, para desarrollar métodos de cultivo de pastos, para fermentar la xilosa y para aprovechar a otras fuentes residuales de celulosa, como los olotes del maíz, por ejemplo.
Por otra parte, el empleo de fuentes alternativas a la caña de azúcar podría ser una buena opción si se logra aumentar los rendimientos de estos nuevos cultivos (ej. malanga), o si se asegura que los costos de producción de biomasa fermentable, así como otros factores de importancia económica (ej. la eficiencia de uso de agua), sean comparables a los de la caña de azúcar. El desarrollo de métodos más económicos y eficientes para obtener bioetanol a partir de fuentes de carbono económicas y accesibles será crucial para asegurar el éxito de las nuevas tecnologías de producción.
Existe un proceso totalmente químico para lograr la sacarificación de celulosa; sin embargo, es un proceso que no recomendamos intentar pues es muy peligroso para realizar en el laboratorio de docencia ya que se utilizan cantidades abundantes de ácidos y bases concentrados (Camacho, et al., 1996), además de que el líquido que se obtiene no es susceptible a fermentación por la cantidad de sales producto de la neutralización.
Durante este experimento el estudiante puede resolver las siguientes preguntas:
- —
¿Cómo se podría emplear íntegramente a todas las fracciones de la materia vegetal para producir bioetanol?
- —
¿Qué estrategia se puede proponer para resolver los retos de la producción de bioetanol de segunda generación?
- —
¿Qué otros materiales celulósicos se pueden emplear para obtener bioetanol (agave, pastos, olotes)?
- —
¿Qué se puede hacer con los residuos de lignina del proceso (combustión, electricidad)?
Las prácticas anteriores conforman un tren metodológico que se puede usar como investigación guiada con el fin de demostrar los conceptos, fundamentos, retos y procesos de la producción de bioetanol. Se han propuesto prácticas de un nivel muy sencillo, tales como las cinéticas de producción de bioetanol con jugos, hasta más avanzadas como la sacarificación de celulosa. Se lograron realizar con materiales baratos y estándar en laboratorios de docencia, así como con materias primas regionales. Se demostró a los estudiantes que la caña de azúcar es el cultivo que tiene mayor rendimiento de bioetanol y que también es el que mayor potencial tiene para ser aumentado si se logra optimizar la sacarificación de su biomasa celulósica.
A la Asociación Taro Gourmet por la donación de la malanga. A los técnicos IBQ Luz Quevedo, QFB Leticia Saldaña e IQ Juan Hernández por su asistencia. La investigación de los autores es apoyada por los proyectos SEP-CONACyT (152643, 169619), SEP-PROMEP (103.5/11/6720) y Repatriación (146633).