Aunque las recomendaciones actuales sugieren el empleo de fórmulas específicas en nutrición enteral en personas con diabetes, hay poca evidencia de su efectividad a largo plazo en el control glucémico. El objetivo principal de este estudio es evaluar la eficacia a largo plazo (24 semanas) de una fórmula de nutrición enteral hipercalórica hiperproteica específica para personas con diabetes en control glucémico y mejora del estado nutricional.
MetodologíaEstudio multicéntrico observacional prospectivo en vida real de pacientes con prescripción de nutrición enteral de larga duración a través de sonda de gastrostomía o nasogástrica que recibieron una fórmula hipercalórica hiperproteica específica para diabetes. Una vez obtenido el consentimiento informado del participante y comprobados los criterios de inclusión y exclusión, se recogieron datos relativos a control glucémico, parámetros de inflamación, bioquímicos, situación nutricional y tolerancia gastrointestinal a 0, 12 y 24 semanas.
ResultadosSe reclutó a 112 pacientes, 44,6% mujeres, edad 75,0 (12,0) años y tiempo medio de evolución de la diabetes 18,1 (9,5) años. El porcentaje de pacientes con desnutrición según la valoración global subjetiva descendió a lo largo del tratamiento del 78,6% al 29,9% (p<0,001). Los niveles de glucemia y de HbA1c se redujeron significativamente a las 12 y 24 semanas (glucemia 155,9-139,0-133,9mg/dl, p<0,001; HbA1c 7,7-7,3-7,1%, p<0,001), mientras que no se observaron cambios significativos en colesterol, triglicéridos, creatinina ni filtrado glomerular. Se observó un aumento significativo de las variables relacionadas con la situación nutricional (peso, IMC, albúmina, prealbúmina y transferrina), se redujeron significativamente los niveles de PCR y disminuyó el cociente PCR/albúmina. La tolerancia gastrointestinal fue buena, siendo escaso el número de pacientes con síntomas moderados-graves y no se modificó a lo largo del seguimiento.
ConclusiónNuestro estudio en vida real apoya que el empleo de una fórmula hipercalórica hiperproteica específica para diabetes durante un tratamiento nutricional a 6 meses permite un adecuado control glucémico y evolución nutricional, con una buena tolerancia gastrointestinal.
Although current recommendations suggest the use of specific formulas in enteral nutrition in people with diabetes, there is little evidence of their long-term effectiveness in glycemic control. The main objective of this study is to evaluate the long-term efficacy (24 weeks) of a specific high-protein hypercaloric enteral nutrition formula for people with diabetes in glycemic control and in their improvement in nutritional status.
MethodologyThis was a multicenter, prospective, observational, real-life study of patients with long-term enteral nutrition prescription through gastrostomy or nasogastric tube who received a high protein hypercaloric formula specific for diabetes. Once the participant's informed consent was obtained and the inclusion and exclusion criteria were verified, data relating to glycemic control, inflammation parameters, biochemical data, nutritional status and gastrointestinal tolerance at 0, 12 and 24 weeks were collected.
Results112 patients were recruited, 44.6% women, age 75.0 (12.0) years and a mean time of evolution of diabetes of 18.1 (9.5) years. The percentage of patients with malnutrition according to VGS decreased throughout the treatment from 78.6% to 29.9% (P<.001). Glycemic and HbA1c levels were significantly reduced at 12 and 24 weeks (Blood glucose 155.9-139.0-133.9mg/dl, P<.001; HbA1c 7.7-7.3-7.1%, P<.001) while no significant changes were observed in cholesterol, triglycerides, creatinine, or glomerular filtration. A significant increase in variables related to nutritional status was observed: weight, the BMI, albumin, prealbumin and transferrin, and CRP levels were significantly reduced and the CRP / Albumin ratio decreased. Gastrointestinal tolerance was good, the number of patients with moderate-severe symptoms was small, and did not change throughout the follow-up.
ConclusionOur real-life study suggests that the use of a specific hyperprotein hypercaloric formula for diabetes during a 6-month nutritional treatment allows adequate glycemic control and nutritional evolution, with good gastrointestinal tolerance.
La hiperglucemia es un problema asociado a la diabetes mellitus (DM) tipo 1 y 2. A corto plazo, la hiperglucemia prolongada puede provocar poliuria, aumento de la sed, deshidratación, pérdida involuntaria de peso y astenia, y puede conllevar la aparición de complicaciones agudas severas, como una cetoacidosis o un estado hiperosmolar. A largo plazo, las complicaciones derivadas pueden ser más graves, como lesiones microvasculares (retinopatía, polineuropatía o nefropatías diabéticas) o macrovasculares (accidentes cerebrovasculares, infarto agudo de miocardio, enfermedad vascular periférica y otros). Además, niveles altos de glucemia en sangre por largos períodos se han asociado con un mayor riesgo de infección y un mayor tiempo de cicatrización de las heridas. Además de las concentraciones de glucosa en ayunas, también es importante controlar las glucemias posprandiales para mejorar este control glucémico. Por esta razón, mantener unos niveles de glucosa normales es uno de los principales objetivos de cualquier terapia en pacientes con diabetes. En estos pacientes, la alimentación y la nutrición desempeñan un papel fundamental.
Para los pacientes con diabetes que deben permanecer largos períodos alimentándose mediante nutrición enteral (NE), se debería valorar la prescripción de una fórmula de NE hipercalórica hiperproteica específica para el control metabólico de la diabetes1. Diversos estudios han demostrado la efectividad de estas formulaciones en el control de la glucemia basal en períodos cortos y medios (< 12 semanas) en pacientes con DM2,3. Sin embargo, hay poca evidencia de la efectividad de estas formulaciones a largo plazo (> 6 meses) en el control glucémico basal y posprandial, en la mejora o el mantenimiento del estado nutricional y en la evolución de los parámetros bioquímicos de inflamación. Por ello, el objetivo principal de este estudio es evaluar la eficacia a largo plazo (24 semanas) de una fórmula de NE hipercalórica hiperproteica específica para personas con diabetes en control glucémico, evaluado mediante hemoglobina glucosilada (HbA1c), parámetros bioquímicos de inflamación y evolución del estado nutricional durante un período de 6 meses. Además, como objetivo secundario se planteó analizar el grado de tolerancia digestiva de la fórmula de NE administrada.
MetodologíaEstudio multicéntrico observacional prospectivo en vida real de pacientes con prescripción de NE de larga duración en domicilio, ya sea a través de sonda de gastrostomía o sonda nasogástrica. El estudio fue aprobado por el Comité Ético de Investigación clínica del Complejo Asistencial Universitario de León (estudio 1629, fecha de aprobación 29 de marzo del 2016) y se llevó a cabo cumpliendo los estándares éticos y legales exigibles a la investigación biomédica según la Declaración de Helsinki. Todos los pacientes incluidos otorgaron por escrito su consentimiento informado.
Los centros participantes en el estudio recibieron una invitación a participar por parte de la investigadora principal pero no se siguió ningún método de aleatorización al tratarse de un estudio observacional en vida real. A los investigadores colaboradores se les solicitó la inclusión en el estudio de forma consecutiva de todos aquellos pacientes que cumplieran los criterios de inclusión durante el período de estudio (desde el 9 de mayo del 2016 hasta el 31 de diciembre del 2019): mayores de 40 años y antecedentes de diabetes tipo 2 diagnosticada previamente al episodio actual, con niveles de HbA1c ≥ 7,0% y <10%, a los que se prescriba una alimentación vía enteral (a través de sonda nasogástrica o gastrostomía) y con una previsión de duración igual o superior a 24 semanas. El paciente o su cuidador principal debía ser capaz de comprender el estudio y tener plena libertad para la participación en este, así como firmar el consentimiento informado. Se excluyó a pacientes con alergia manifestada para algunos de los ingredientes del producto, enfermedad renal o hepática grave (filtrado glomerular menor de 30ml/min, elevación de transaminasas×3 valor superior de la normalidad), insuficiencia cardiaca grado iv NYHA, tratamiento con corticoides (2 semanas antes y en cualquier momento durante el período de estudio), enfermedad gastrointestinal en las 2semanas anteriores al inicio del estudio o activa, contraindicación al empleo de fibra, mal control glucémico (HbA1c> 10%), ingreso hospitalario, embarazo o lactancia. Al tratarse de un estudio observacional en condiciones de práctica clínica real, los pacientes siguieron la pauta de NE recomendada por su médico responsable para cubrir sus necesidades energéticas y de macronutrientes según la práctica clínica habitual de los centros participantes. El tratamiento específico de la diabetes también quedó a criterio de los médicos investigadores. La fórmula hipercalórica hiperproteica empleada para cubrir estas necesidades tenía una densidad calórica de 1,5 Kcal/ml y estaba compuesta por 20% de proteínas (7,5g/100ml), 35% de hidratos de carbono (13,1g/100ml, dextrinomaltosa, dextrina de tapioca, isomaltulosa y fructosa), 3% de fibra (2,3g/100ml, 78% soluble) y 42% de grasas (7g/100ml, aceites vegetales de colza, girasol y soja, MCT y aceite de pescado).
Se realizó una predeterminación del tamaño muestral, empleando el cambio en la HbA1c en los pacientes que consumen la fórmula de NE administrada durante 24 semanas. Teniendo en cuenta que estimamos una mejora de los niveles del porcentaje de HbA1c de un 0,8%, asumiendo en un contraste bilateral, un error alfa (tipo i) de un 5%, un error beta de un 20% y unas pérdidas de seguimiento del 15%, se calculó una muestra total de 44 pacientes para llevar a cabo el estudio. Posteriormente, se decidió ampliar la muestra para poder tener también poder estadístico suficiente para valorar los objetivos secundarios. Se realizó un cuaderno de recogida de datos (CRD) en papel para el registro de los datos. Una vez obtenido el consentimiento informado del participante y comprobados los criterios de inclusión y exclusión, se recogieron en la visita de reclutamiento en el CRD de forma disociada los datos de filiación (edad y sexo), enfermedades y tratamientos concomitantes, lugar de residencia (domicilio o institucionalizado), datos sobre la diabetes (tiempo de evolución, complicaciones, tratamiento y episodios de hipoglucemia), motivo de prescripción de NE y dosis y vía de administración, características antropométricas iniciales (talla, peso) y valoración global subjetiva (VGS). Se recogieron determinaciones analíticas de glucemia basal, HbA1c, colesterol total, triglicéridos, creatinina y filtrado glomerular, albúmina, prealbúmina, transferrina y proteína C reactiva (PCR).
Las visitas sucesivas se llevaron a cabo en condiciones de práctica clínica habitual a las 12 y 24 semanas del inicio del tratamiento. Se recogieron en dichas visitas los mismos datos antropométricos, VGS y bioquímicos, así como cambios en enfermedades y tratamientos concomitantes, y episodios de hipoglucemias al mes. La tolerancia gastrointestinal se evaluó considerando el porcentaje de pacientes que presentaron los siguientes síntomas: náuseas, vómitos, regurgitación, estreñimiento, diarrea, flatulencia, distensión abdominal y dolor abdominal. Se consideraron leves si el síntoma estaba presente pero no era molesto; moderado si el síntoma era frecuentemente molesto, pero no interfería con las actividades cotidianas o el sueño; severo cuando era suficientemente molesto para interferir con las actividades cotidianas o el sueño y muy severo cuando requería atención médica.
Todos los datos se registraron en una base de datos creada únicamente para el estudio en Microsoft Excel 97-2003 (© Microsoft). Todos los análisis se han llevado a cabo mediante el programa estadístico SPSS versión 24 (IBM Corp©). El análisis de datos solo se ha realizado para los datos existentes, sin realizar ninguna sustitución de datos faltantes. Para llevar a cabo los análisis estadísticos, se ha utilizado los estadísticos de tendencia central para describir las variables (media [desviación típica]) ya que las pruebas de normalidad han indicado que los datos se distribuyen según una distribución normal (pruebas de Kolmogorov-Smirnov y Shapiro Wilk). En el caso de variables de tipo cualitativo, se han descrito a través de la frecuencia y el porcentaje. Para evaluar si existían diferencias significativas durante el período de tratamiento (visita basal, 12 y 24 semanas) se ha utilizado un modelo lineal general para medidas repetidas (ANOVA de medidas repetidas) para las variables cuantitativas (peso, IMC y datos bioquímicos) y la prueba de comparación de proporciones emparejadas (test de McNemar) para las variables de tipo cualitativo (cambio de estado nutricional). El nivel de significación utilizado ha sido del 5% (p valor <0,05).
ResultadosSe reclutó para el estudio a 112 pacientes, 50 mujeres (44,6%) y 62 varones (55,4%). Todos los pacientes que cumplían criterios de inclusión durante el período de seguimiento en los centros participantes aceptaron participar y todos finalizaron las 24 semanas de seguimiento. La edad media fue 75,0 (12,0) años. Un 41,2% vivía en su propio domicilio y 58,8% estaba institucionalizado. El tiempo medio de evolución de la diabetes fue 18,1 (9,5) años. Como complicaciones asociadas a la diabetes, presentaba retinopatía el 43,8%, polineuropatía el 26,8%, nefropatía el 25% y enfermedad cardiovascular el 25%. El porcentaje de pacientes con desnutrición según la VGS descendió a lo largo del tratamiento de forma significativa (tabla 1). Los pacientes con desnutrición grave (VGS C) disminuyeron del 30,4% al inicio (34 pacientes) a solo el 3% (2 pacientes) a las 24 semanas.
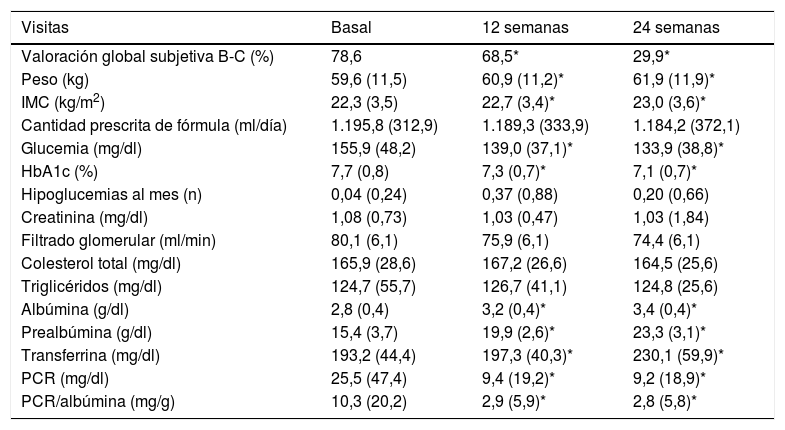
Características basales y evolución a 12 y 24 semanas
| Visitas | Basal | 12 semanas | 24 semanas |
|---|---|---|---|
| Valoración global subjetiva B-C (%) | 78,6 | 68,5* | 29,9* |
| Peso (kg) | 59,6 (11,5) | 60,9 (11,2)* | 61,9 (11,9)* |
| IMC (kg/m2) | 22,3 (3,5) | 22,7 (3,4)* | 23,0 (3,6)* |
| Cantidad prescrita de fórmula (ml/día) | 1.195,8 (312,9) | 1.189,3 (333,9) | 1.184,2 (372,1) |
| Glucemia (mg/dl) | 155,9 (48,2) | 139,0 (37,1)* | 133,9 (38,8)* |
| HbA1c (%) | 7,7 (0,8) | 7,3 (0,7)* | 7,1 (0,7)* |
| Hipoglucemias al mes (n) | 0,04 (0,24) | 0,37 (0,88) | 0,20 (0,66) |
| Creatinina (mg/dl) | 1,08 (0,73) | 1,03 (0,47) | 1,03 (1,84) |
| Filtrado glomerular (ml/min) | 80,1 (6,1) | 75,9 (6,1) | 74,4 (6,1) |
| Colesterol total (mg/dl) | 165,9 (28,6) | 167,2 (26,6) | 164,5 (25,6) |
| Triglicéridos (mg/dl) | 124,7 (55,7) | 126,7 (41,1) | 124,8 (25,6) |
| Albúmina (g/dl) | 2,8 (0,4) | 3,2 (0,4)* | 3,4 (0,4)* |
| Prealbúmina (g/dl) | 15,4 (3,7) | 19,9 (2,6)* | 23,3 (3,1)* |
| Transferrina (mg/dl) | 193,2 (44,4) | 197,3 (40,3)* | 230,1 (59,9)* |
| PCR (mg/dl) | 25,5 (47,4) | 9,4 (19,2)* | 9,2 (18,9)* |
| PCR/albúmina (mg/g) | 10,3 (20,2) | 2,9 (5,9)* | 2,8 (5,8)* |
HbA1c: hemoglobina glucosilada; IMC: índice de masa corporal; PCR: proteína C reactiva.
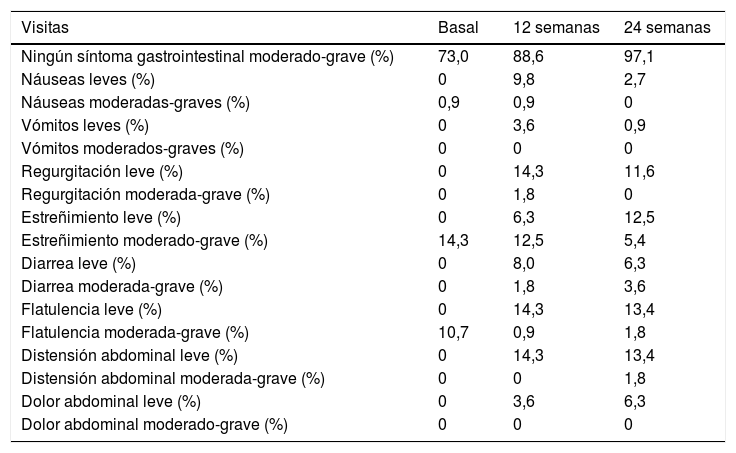
Los niveles de glucemia y de HbA1c se redujeron significativamente a las 12 y las 24 semanas, mientras que no se observaron cambios estadísticamente significativos en colesterol, triglicéridos, creatinina ni filtrado glomerular. Se observó un aumento significativo de las variables relacionadas con la situación nutricional: peso, IMC, albúmina, prealbúmina y transferrina. Durante el seguimiento se redujeron significativamente los niveles de PCR y disminuyó el cociente PCR/albúmina (tabla 1). No hubo diferencias significativas en relación con el lugar de residencia del paciente (propio domicilio o institucionalizado). Respecto a la tolerancia gastrointestinal, fue escaso el número de pacientes con síntomas moderados-graves y no se modificó a lo largo del seguimiento. El porcentaje de pacientes sin sintomatología gastrointestinal se incrementó del 73% inicial al 88,6% a 12 semanas y al 97,1% a 24 semanas (p <0,001). La complicación gastrointestinal más frecuente fue el estreñimiento, sin cambios significativos a lo largo del seguimiento (tabla 2).
Síntomas gastrointestinales basales y evolución a 12 y 24 semanas
| Visitas | Basal | 12 semanas | 24 semanas |
|---|---|---|---|
| Ningún síntoma gastrointestinal moderado-grave (%) | 73,0 | 88,6 | 97,1 |
| Náuseas leves (%) | 0 | 9,8 | 2,7 |
| Náuseas moderadas-graves (%) | 0,9 | 0,9 | 0 |
| Vómitos leves (%) | 0 | 3,6 | 0,9 |
| Vómitos moderados-graves (%) | 0 | 0 | 0 |
| Regurgitación leve (%) | 0 | 14,3 | 11,6 |
| Regurgitación moderada-grave (%) | 0 | 1,8 | 0 |
| Estreñimiento leve (%) | 0 | 6,3 | 12,5 |
| Estreñimiento moderado-grave (%) | 14,3 | 12,5 | 5,4 |
| Diarrea leve (%) | 0 | 8,0 | 6,3 |
| Diarrea moderada-grave (%) | 0 | 1,8 | 3,6 |
| Flatulencia leve (%) | 0 | 14,3 | 13,4 |
| Flatulencia moderada-grave (%) | 10,7 | 0,9 | 1,8 |
| Distensión abdominal leve (%) | 0 | 14,3 | 13,4 |
| Distensión abdominal moderada-grave (%) | 0 | 0 | 1,8 |
| Dolor abdominal leve (%) | 0 | 3,6 | 6,3 |
| Dolor abdominal moderado-grave (%) | 0 | 0 | 0 |
La diabetes es una enfermedad cada vez más frecuente en el mundo occidental. En España, los datos de estudio Di@bet.es han estimado que un 13,8% de la población española tiene diabetes y hasta un 30% puede presentar alguna alteración del metabolismo hidrocarbonado4. La desnutrición se asocia con frecuencia a diabetes5. En un estudio reciente, la prevalencia de la DM en pacientes que recibían NE fue del 31,8% y más del 85% de los pacientes recibieron una fórmula específica para diabetes6. Diversos estudios han demostrado la efectividad de estas formulaciones en el control de la glucemia basal en períodos cortos y medios (< 12 semanas) en pacientes diabéticos2,3,7,8. Además, su empleo se ha asociado con una importante reducción de gastos sanitarios9. Los metaanálisis publicados10-12 han podido valorar, sin embargo, solo un escaso número de estudios, con pocos pacientes y siempre a corto plazo (menos de 3meses), por lo que concluyen que son necesarios más estudios en este tema.
En el metaanálisis más reciente de Sanz-París et al.12 solo pudieron incluirse 18 estudios que empleaban fórmulas ricas en grasa monoinsaturadas (MUFA), definidas como aquellas que aportan> 20% de su valor calórico total como MUFA, como es el caso de la fórmula empleada en nuestro estudio. Solo 3 estudios valoraron a pacientes a más de un mes, pero aun así el tiempo de seguimiento fue corto, 703 y 84 días7,8, respectivamente. Nuestro estudio tiene la limitación de no ser un ensayo clínico de intervención comparando una fórmula específica, sino observacional en vida real sin grupo control. Sin embargo, nuestra fortaleza es precisamente esa, ser un estudio en práctica clínica real y además ser multicéntrico y haber incluido un número importante de personas con diabetes de larga evolución y durante un período largo de 24 semanas. Además, todos los pacientes completaron el tiempo de seguimiento. En nuestro conocimiento, ningún estudio de fórmulas específicas en diabetes ha tenido un seguimiento a tan largo plazo.
El metaanálisis de Sanz-París et al.12 demostró que las fórmulas ricas en MUFA suponían una reducción en HbA1c de –0,63% (IC del 95% –1,21 a –0,05) frente a fórmulas estándar, aunque existía una gran heterogeneidad entre los estudios valorados, entre otras cosas porque se refieren a pacientes tanto con NE por sonda como con suplementación oral. Nuestros datos, solo en pacientes con sonda, reflejan también un buen control glucémico cuando se valora por HbA1c, que fue del 7,1% al final del seguimiento, evidenciando además una reducción significativa a lo largo del seguimiento en –0,6%, similar a lo comunicado en el metaanálisis de Sanz-París et al.12. Si consideramos la edad media de 75 años, el largo tiempo de evolución de la DM y la frecuencia de complicaciones crónicas en nuestra serie podemos considerar el grado de control conseguido como muy bueno. Por ello, podemos decir que, en un contexto de vida real, nuestros datos confirman el efecto favorable de las fórmulas específicas en conseguir un buen control glucémico.
El perfil lipídico no se modificó en nuestro estudio a lo largo de 24 semanas, con niveles que pueden considerarse adecuados ya desde la visita inicial. Aunque se ha relacionado el empleo de fórmulas específicas con menores niveles de triglicéridos respecto a la estándar12,13, en nuestro caso no era esperable un cambio en los parámetros lipídicos. Tampoco se evidenciaron cambios significativos en la función renal. El hecho de que la fórmula haya sido hipercalórica e hiperproteica podría despertar reticencias sobre su efecto en la hidratación que podría repercutir en un empeoramiento de función renal, pero ya nuestro grupo ha demostrado la seguridad de las fórmulas concentradas14.
El porcentaje de pacientes con desnutrición según la VGS descendió a lo largo del tratamiento de forma significativa, como era esperable con el tratamiento médico nutricional. Los pacientes con desnutrición grave disminuyeron del 30,4% al inicio a solo el 3% a 24 semanas y cualquier grado de desnutrición del 78,6 al 29,9%, lo que confirma la efectividad de la fórmula, según lo que era esperable. Esta mejora en la situación nutricional es paralela a un aumento de peso superior a 2kg y a una mejoría en los niveles de proteínas plasmáticas y del cociente PCR/albúmina, que se ha propuesto como un marcador de morbimortalidad15. Por último, queremos reseñar la buena tolerancia a la fórmula, con un progresivo aumento en el porcentaje de pacientes sin ninguna sintomatología gastrointestinal. También el hecho de no haber registrado ninguna pérdida de pacientes por discontinuación de la fórmula nos orienta a que la tolerancia global a lo largo de los 6 meses de seguimiento ha tenido que ser necesariamente buena.
En conclusión, nuestro estudio en vida real apoya que el empleo de una fórmula hipercalórica hiperproteica específica para diabetes durante un tratamiento nutricional a 6 meses permite un adecuado control glucémico y mejoría nutricional, con una buena tolerancia gastrointestinal.
FinanciaciónEl presente estudio ha sido financiado por Fresenius Kabi España exclusivamente para el análisis estadístico de los datos.
Conflicto de interesesMaría D. Ballesteros Pomar ha recibido honorarios por conferencias, consultoría o estudios de investigación de Fresenius Kabi, Nestlé Health Science, Abbott Nutrition, Nutricia, Vegenat y Novo Nordisk.
Beatriz Lardiés Sánchez ha recibido honorarios por conferencias, consultoría o estudios de investigación de Fresenius Kabi, Nestlé Health Science, Abbott Nutrición, Nutricia, Persan, Novo Nordisk, Lilly, Boerhinguer, Sanofi, AstraZeneca, Gebro Pharma y Mylan.
María Argente Pla ha recibido honorarios por conferencias o estudios de investigación de Fresenius Kabi, Nestlé Health Science y Abbott Nutrition.
Araceli Ramos Carrasco ha recibido honorarios por estudios de investigación de Fresenius Kabi, Nestlé Health Science, Abbott Nutrition, Nutricia y Vegenat.
Lorena Suárez Gutiérrez ha recibido honorarios por conferencias, consultoría o estudios de investigación de Fresenius Kabi, Nestlé Health Science, Abbott Nutrition, Vegenat, Novo Nordisk, Amgen,Sanofi, Jamsen, AstraZeneca, Takeda, MSD y Novartis.
Alfredo Yoldi Arrieta ha recibido honorarios por conferencias de Astra y Novo Nordisk.
Patricia Sorribes Carreras ha recibido honorarios por ponencias de Fresenius Fabi en el área de disfagia.
Sonsoles Gutiérrez Medina ha recibido honorarios de Fresenius Kabi, Nutricia, Novonordisk, Lilly, Sanofi y AstraZeneca.
Juan Bautista Molina Soria ha recibido honorarios por conferencias, consultoría o estudios de investigación de Fresenius Kabi, Nestlé Health Science, Abbott Nutrition, Nutricia, Vegenat y Persan.
María Berrio Miranda ha recibido honorarios por conferencias, o estudios de investigación de Fresenius Kabi, Abbott Nutrition, Nutricia y Lilly.
M. Socorro Leyva Martínez ha recibido honorarios por conferencias o estudios de investigación de Fresenius Kabi, Abbott Nutrition, Nutricia y Lilly.
Oscar Torregrosa Suau no tiene conflicto de intereses.
M. Teresa Oliván Usieto no tiene conflicto de intereses.
Francisco Villazón González ha recibido honorarios por conferencias de Amgen, Fresenius Kabi, Nutricia y Abbott Nutrition.
Jimena Abilés Osinaga no tiene conflicto de intereses.
Esteban Martín Echevarría ha recibido honorarios por conferencias o estudios de investigación de Fresenius Kabi, Nestlé Health Science, Novonordisk, Nutricia y Persan farma.
Katherine García-Malpartida ha recibido honorarios por conferencias o consultoría de Fresenius-Kabi, Nestlé Health Science, Abbott Nutrition, Nutricia y Persan Farma.