La hormona de crecimiento recombinante humana (rhGH) se utiliza en niños con crecimiento intrauterino retardado sin recuperación posnatal de talla. En 2010 se inició el Comité Asesor de Castilla y León para aplicar de forma homogénea los criterios de utilización de la rhGH. El objetivo es valorar la evolución antropométrica y clínica de niños sometidos a tratamiento.
Pacientes y métodosEstudio retrospectivo, longitudinal, con pacientes de Castilla y León diagnosticados de crecimiento intrauterino retardado sin crecimiento recuperador a partir del año 2010, con al menos 3 años de tratamiento. Se evaluaron las modificaciones en diferentes parámetros antropométricos, clínicos y analíticos.
ResultadosSe incluyeron 43 niños con una edad media de 6,06 años (58,14%<5 años), tratados con una dosis media de 0,038mg/kg/día. Se observó un aumento significativo en la talla (−3,05 hasta −1,58DE). El peso se incrementó durante todo el estudio, así como el IMC (14,51 hasta 15,80kg/m2). La velocidad de crecimiento alcanzó su pico máximo durante el primer año de tratamiento (0,74DE). Los valores de IGF-1 se incrementaron durante todo el estudio (99,96 hasta 392,88ng/ml). Se observaron incrementos significativos de la glucohemoglobina en el primer año y de la glucemia y de la insulinemia basal durante el segundo año, así como un descenso en el cociente LDL/HDL (1,70 hasta 1,50).
ConclusiónEl tratamiento con hormona de crecimiento favorece el crecimiento de niños con crecimiento intrauterino retardado, observándose su máximo efecto en los primeros 12 meses, siendo mayor si la edad de comienzo es anterior a los 5 años de edad.
Growth hormone (rhGH) is used in children with intrauterine growth retardation without catch-up growth. The Advisory Committee of Castilla y León was implemented in 2010 to watch for consistent application of the criteria for using rhGH. The aim is to assess anthropometric and clinical changes in children treated with growth hormone.
Patients and methodsA retrospective, longitudinal study of patients diagnosed with intrauterine growth retardation without catch-up growth in Castilla y León since 2010 who have received treatment for at least 3 years. Changes in anthropometric, clinical, and laboratory parameters were assessed.
ResultsForty-three children with a mean age of 6.06 years (58.14%<5 years) were enrolled and treated with a mean dose of 0.038mg/kg/day. A significant increase was seen in height (−3.05 to −1.58SD). Both weight and BMI (14.51 to 15.80kg/m2) increased throughout the study. Growth rate peaked during the first year of treatment (0.74SD). IGF-1 levels increased throughout the study (99.96 to 392.88ng/mL). There were significant increases in glycosylated hemoglobin levels in the first year, and in basal blood glucose and insulin levels during the second year. The LDL/HDL ratio decreased during the study period (1.70 to 1.50).
ConclusionTreatment with rhGH promotes growth in children with intrauterine growth retardation. Peak effect occurs in the first 12 months of treatment, and is greater when growth hormone is started before the age of 5 years.
El término pequeño para la edad gestacional fue definido en el año 2001 por el International Small for Gestational Age Advisory Board Consensus Development Conference, como aquel recién nacido con un peso y/o longitud al menos 2 desviaciones estándar (DE) por debajo de la media para la edad gestacional, ya sea a término o pretérmino, según datos de su población de referencia1.
Los casos de recién nacidos pequeños para la edad gestacional (PEG) o con crecimiento intrauterino retardado (CIR) pueden tener diferentes orígenes: fetales, maternos, placentarios y, en al menos un 40% de los casos, idiopáticos2.
Se estima que aproximadamente el 85-90% de estos niños efectúan un crecimiento recuperador (catch-up growth) de forma espontánea, recuperando valores normales de longitud y peso durante los primeros 2-3 años de edad1. Las razones por las que el restante 10-15% no experimentan ese crecimiento espontáneo son desconocidas, y es muy poco probable que suceda después de los 4 primeros años de vida3,4.
Para este grupo de niños, se realiza tratamiento con hormona de crecimiento recombinante humana (rhGH), que fue aprobada para esta indicación en el año 2003 por la Food and Drug Administration y por la European Agency for the Evaluation of Medical Products5.
Los estudios demuestran que en un 85% de los casos se alcanza una talla adulta normal superior a −2DE, y en un 98% una talla dentro del rango de su talla genética. Además del efecto sobre el crecimiento lineal, la rhGH muestra un efecto normalizador sobre el índice de masa corporal (IMC), se asocia con el descenso de la presión arterial y con una mejoría en el perfil lipídico al disminuir los niveles de colesterol total y del colesterol ligado a proteínas de baja densidad (c-LDL)6,7.
Diferentes estudios postautorización muestran la eficacia y la seguridad del tratamiento con rhGH cuando es utilizado para las indicaciones autorizadas por los distintos organismos reguladores8.
Con el fin de que los criterios para el diagnóstico de las enfermedades susceptibles de ser tratadas con rhGH, y los criterios de selección de los pacientes para el tratamiento se apliquen de forma homogénea, resulta de interés contar con un Comité Asesor para la utilización de la rhGH. Además, la actuación de dicho Comité garantiza la equidad en el acceso a la rhGH y sustancias relacionadas, así como el uso racional y eficiente de los recursos en el Sistema Nacional de Salud. En la comunidad autónoma de Castilla y León se creó el Comité Asesor para la utilización terapéutica de la hormona de crecimiento y sustancias relacionadas en diciembre del año 20079, siendo su implantación efectiva en enero de 2010.
Los objetivos de este estudio son:
- •
Cuantificar el número de niños con CIR, en Castilla y León, que hayan sido tratados al menos durante 3 años con rhGH, así como analizar las variaciones antropométricas y analíticas que se han producido durante dicho período.
- •
Evaluar la influencia de diferentes variables (condición de prematuro, sexo y edad de comienzo del tratamiento) sobre la ganancia de talla en los pacientes sometidos a tratamiento con rhGH.
Se trata de un estudio retrospectivo y longitudinal, con pacientes de la Comunidad Autónoma de Castilla y León que hayan sido diagnosticados de CIR a partir del año 2010, y con al menos 3 años de tratamiento continuado con rhGH. Toda la información ha sido extraída de los documentos de solicitud de inicio y renovación de tratamiento con rhGH, remitidos al Comité Asesor de Hormona de Crecimiento de Castilla y León. Los pacientes incluidos en el estudio tenían que cumplir los siguientes criterios requeridos por el citado Comité para niños con CIR:
- •
Longitud y/o peso al nacimiento menor de −2DE, utilizando para ello las tablas de referencia de los estándares auxológicos integrados españoles10.
- •
No haber tenido a los 4 años de vida recuperación de crecimiento.
- •
En el momento de la solicitud, la talla deberá ser inferior a −2,5DE (según los estándares auxológicos integrados españoles10), y menor de −1DE ajustada a la talla media parental (salvo excepciones).
Los criterios de exclusión para este estudio han sido los siguientes:
- •
Inicio de pubertad.
- •
Intolerancia hidrocarbonada.
- •
Diabetes mellitus.
Se ha recogido y analizado la evolución de diferentes parámetros clínicos, auxológicos y analíticos:
Clínicos y auxológicos:
- •
Al nacimiento: peso, longitud, talla de los progenitores y edad gestacional. Como parámetro adicional se ha calculado la talla genética de cada niño, mediante las siguiente fórmulas:
- o
Niños: (talla del padre+talla de la madre+13)/2
- o
Niñas: (talla del padre+talla de la madre−13)/2
- •
Antes del inicio y en cada revisión anual de tratamiento: edad cronológica, edad ósea, peso, talla, velocidad de crecimiento según la edad cronológica, presión arterial sistólica y diastólica y talla diana. Como parámetros adicionales, se han calculado el cociente edad cronológica/edad ósea y el IMC.
Analíticos:
Antes de iniciar el tratamiento y en cada revisión anual, se analizaron en ayunas los siguientes parámetros analíticos: IGF-1, IGFBP3, glucemia basal, insulina basal, glucohemoglobina, colesterol total, colesterol ligado a proteínas de alta densidad (c-HDL), c-LDL y triglicéridos. Como parámetros adicionales, se han calculado los cocientes IGF-1/IGFBP3, colesterol total/c-HDL y c-LDL/c-HDL.
Por otra parte, se ha realizado un seguimiento de las dosis de rhGH pautada en cada uno de los años de estudio.
Análisis estadísticoPara la descripción de las diferentes características basales de la muestra se ha realizado un estudio de las variables cuantitativas (media, DE, mediana, mínimo, máximo y rango intercuartílico).
Todos los contrastes de hipótesis se han realizado mediante técnicas paramétricas, ya que la muestra cumple los criterios de normalidad de Kolmogorov-Smirnov y Shapiro-Wilk. La efectividad del tratamiento con rhGH se ha determinado mediante la comparación de la media de la talla en cada año de tratamiento con el resultado de la medición anterior mediante la prueba t de muestras relacionadas.
La comparación de los valores medios de las diferentes variables entre condición de prematuro, sexos y grupos de edad al inicio del tratamiento con rhGH se ha realizado mediante el test de t de Student para muestras independientes. Para variables categóricas se ha utilizado el test de Chi cuadrado de Pearson. En cuanto a la edad al inicio del tratamiento, se han establecido 2 grupos diferentes: menores de 5 años y mayores o con una edad igual a 5 años.
Se ha considerado que los resultados eran estadísticamente significativos cuando el valor de p<0,05. Para la realización del análisis estadístico se utilizó el programa estadístico SPSS® 20.
ResultadosCaracterísticas basalesEl estudio está compuesto por 43 pacientes, de los cuales 25 eran niños (58,14%) y 18 niñas (41,86%). Del total de los pacientes se observó que un 7% correspondían a embarazos múltiples, mientras que un 51,16% nació de forma prematura, siendo mayor el número de niños prematuros que de niñas (68,18 frente a 31,82%), no siendo esta diferencia estadísticamente significativa.
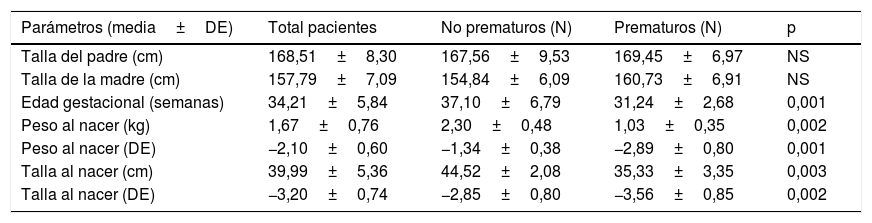
Tras el nacimiento (tabla 1), la edad gestacional media fue de 34,21±5,84 semanas (37,1±6,79 en no prematuros y 31,24±2,68 en prematuros, p<0,05), con una longitud media al nacimiento de 39,99±5,36cm (−3,2±0,7DE), siendo mayor en no prematuros, 44,52±2,08cm (−2,85±0,8DE), que en prematuros, 35,33±3,35cm (−3,56±0,85DE) (p<0,05). El peso medio fue de 1,67±0,76kg (−2,1±0,6DE), siendo mayor en no prematuros, 2,30±0,48kg (−1,34±0,38DE), que en prematuros, 1,03±0,35kg (−2,89±0,8DE) (p<0,05). No se encontraron diferencias en ninguna de estas variables en función del sexo del paciente. La talla diana de los varones fue de 169,4±5,6cm (−1,26±0,35DE) y la de las mujeres, de 156,4±3,8cm (−1,33±0,42DE), sin que se demuestren diferencias en la talla en DE.
Datos al nacimiento según los pacientes sean prematuros o no
| Parámetros (media±DE) | Total pacientes | No prematuros (N) | Prematuros (N) | p |
|---|---|---|---|---|
| Talla del padre (cm) | 168,51±8,30 | 167,56±9,53 | 169,45±6,97 | NS |
| Talla de la madre (cm) | 157,79±7,09 | 154,84±6,09 | 160,73±6,91 | NS |
| Edad gestacional (semanas) | 34,21±5,84 | 37,10±6,79 | 31,24±2,68 | 0,001 |
| Peso al nacer (kg) | 1,67±0,76 | 2,30±0,48 | 1,03±0,35 | 0,002 |
| Peso al nacer (DE) | −2,10±0,60 | −1,34±0,38 | −2,89±0,80 | 0,001 |
| Talla al nacer (cm) | 39,99±5,36 | 44,52±2,08 | 35,33±3,35 | 0,003 |
| Talla al nacer (DE) | −3,20±0,74 | −2,85±0,80 | −3,56±0,85 | 0,002 |
DE: desviación estándar.
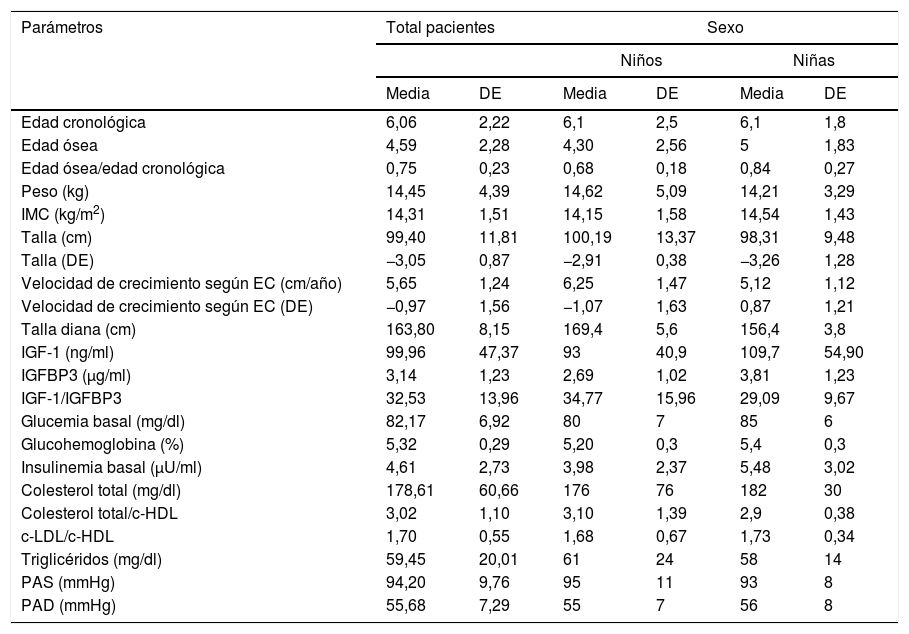
La edad media al inicio del tratamiento (tabla 2) fue de 6,06±2,22 años. En cuanto a la distribución por edades, 25 pacientes (58,14%), de los cuales el 60% eran niños y el 40% niñas, presentaban una edad inferior a 5 años, mientras que 18 pacientes (41,86%), de los cuales el 55,56% eran niños y el 44,44% eran niñas, presentaban una edad igual o superior a 5 años. La talla media observada al inicio del tratamiento fue de 99,40±11,81cm, lo que equivale a −3,05±0,87DE.
Datos auxológicos y analíticos al inicio del tratamiento
| Parámetros | Total pacientes | Sexo | ||||
|---|---|---|---|---|---|---|
| Niños | Niñas | |||||
| Media | DE | Media | DE | Media | DE | |
| Edad cronológica | 6,06 | 2,22 | 6,1 | 2,5 | 6,1 | 1,8 |
| Edad ósea | 4,59 | 2,28 | 4,30 | 2,56 | 5 | 1,83 |
| Edad ósea/edad cronológica | 0,75 | 0,23 | 0,68 | 0,18 | 0,84 | 0,27 |
| Peso (kg) | 14,45 | 4,39 | 14,62 | 5,09 | 14,21 | 3,29 |
| IMC (kg/m2) | 14,31 | 1,51 | 14,15 | 1,58 | 14,54 | 1,43 |
| Talla (cm) | 99,40 | 11,81 | 100,19 | 13,37 | 98,31 | 9,48 |
| Talla (DE) | −3,05 | 0,87 | −2,91 | 0,38 | −3,26 | 1,28 |
| Velocidad de crecimiento según EC (cm/año) | 5,65 | 1,24 | 6,25 | 1,47 | 5,12 | 1,12 |
| Velocidad de crecimiento según EC (DE) | −0,97 | 1,56 | −1,07 | 1,63 | 0,87 | 1,21 |
| Talla diana (cm) | 163,80 | 8,15 | 169,4 | 5,6 | 156,4 | 3,8 |
| IGF-1 (ng/ml) | 99,96 | 47,37 | 93 | 40,9 | 109,7 | 54,90 |
| IGFBP3 (μg/ml) | 3,14 | 1,23 | 2,69 | 1,02 | 3,81 | 1,23 |
| IGF-1/IGFBP3 | 32,53 | 13,96 | 34,77 | 15,96 | 29,09 | 9,67 |
| Glucemia basal (mg/dl) | 82,17 | 6,92 | 80 | 7 | 85 | 6 |
| Glucohemoglobina (%) | 5,32 | 0,29 | 5,20 | 0,3 | 5,4 | 0,3 |
| Insulinemia basal (μU/ml) | 4,61 | 2,73 | 3,98 | 2,37 | 5,48 | 3,02 |
| Colesterol total (mg/dl) | 178,61 | 60,66 | 176 | 76 | 182 | 30 |
| Colesterol total/c-HDL | 3,02 | 1,10 | 3,10 | 1,39 | 2,9 | 0,38 |
| c-LDL/c-HDL | 1,70 | 0,55 | 1,68 | 0,67 | 1,73 | 0,34 |
| Triglicéridos (mg/dl) | 59,45 | 20,01 | 61 | 24 | 58 | 14 |
| PAS (mmHg) | 94,20 | 9,76 | 95 | 11 | 93 | 8 |
| PAD (mmHg) | 55,68 | 7,29 | 55 | 7 | 56 | 8 |
c-HDL: colesterol ligado a proteínas de alta densidad; c-LDL: colesterol ligado a proteínas de baja densidad; DE: desviación estándar; EC: edad cronológica; IGF-1: factor de crecimiento análogo a insulina tipo 1; IGFBP3: proteína transportadora 3 del factor de crecimiento análogo a la insulina; IMC: índice de masa corporal; PAD: presión arterial diastólica; PAS: presión arterial sistólica.
Tanto los datos clínicos de presión arterial como los datos analíticos pretratamiento se encuentran dentro del rango de la normalidad. Se observaron cifras más elevadas en niñas que en niños para los parámetros de la IGFBP3 (3,81±1,23μg/ml vs. 2,69±1,02μg/ml, p<0,05), la glucemia basal (84,94±6,16mg/dl vs. 80,28±6,89mg/dl, p<0,05) y la glucohemoglobina (5,45±0,30 vs. 5,24±0,26%, p<0,05). No se encontraron diferencias en función de la condición de prematuro de los pacientes.
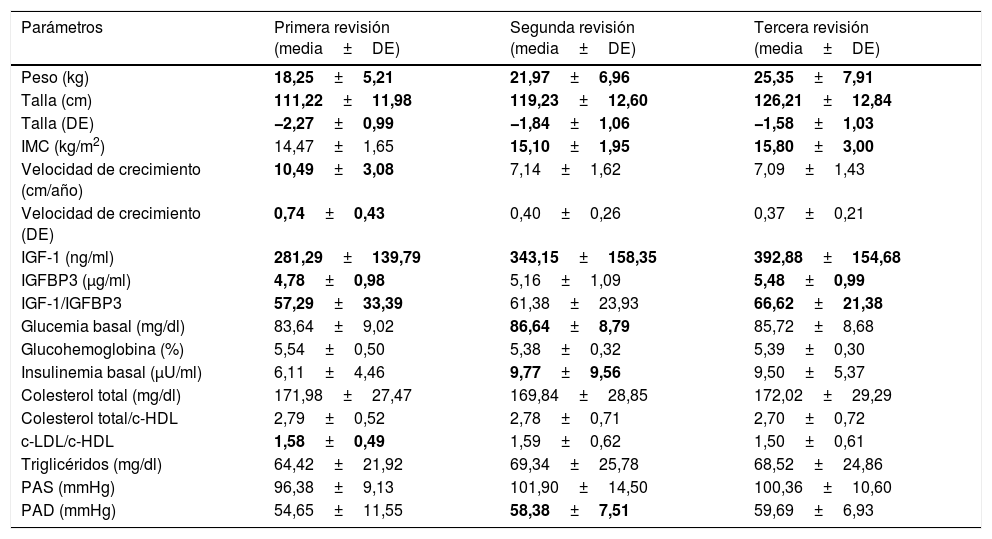
Evolución de los datos auxológicosLa evolución de los datos auxológicos a lo largo de todo el período de estudio se muestra en la tabla 3.
Evolución de parámetros auxológicos y analíticos a lo largo del estudio
| Parámetros | Primera revisión (media±DE) | Segunda revisión (media±DE) | Tercera revisión (media±DE) |
|---|---|---|---|
| Peso (kg) | 18,25±5,21 | 21,97±6,96 | 25,35±7,91 |
| Talla (cm) | 111,22±11,98 | 119,23±12,60 | 126,21±12,84 |
| Talla (DE) | −2,27±0,99 | −1,84±1,06 | −1,58±1,03 |
| IMC (kg/m2) | 14,47±1,65 | 15,10±1,95 | 15,80±3,00 |
| Velocidad de crecimiento (cm/año) | 10,49±3,08 | 7,14±1,62 | 7,09±1,43 |
| Velocidad de crecimiento (DE) | 0,74±0,43 | 0,40±0,26 | 0,37±0,21 |
| IGF-1 (ng/ml) | 281,29±139,79 | 343,15±158,35 | 392,88±154,68 |
| IGFBP3 (μg/ml) | 4,78±0,98 | 5,16±1,09 | 5,48±0,99 |
| IGF-1/IGFBP3 | 57,29±33,39 | 61,38±23,93 | 66,62±21,38 |
| Glucemia basal (mg/dl) | 83,64±9,02 | 86,64±8,79 | 85,72±8,68 |
| Glucohemoglobina (%) | 5,54±0,50 | 5,38±0,32 | 5,39±0,30 |
| Insulinemia basal (μU/ml) | 6,11±4,46 | 9,77±9,56 | 9,50±5,37 |
| Colesterol total (mg/dl) | 171,98±27,47 | 169,84±28,85 | 172,02±29,29 |
| Colesterol total/c-HDL | 2,79±0,52 | 2,78±0,71 | 2,70±0,72 |
| c-LDL/c-HDL | 1,58±0,49 | 1,59±0,62 | 1,50±0,61 |
| Triglicéridos (mg/dl) | 64,42±21,92 | 69,34±25,78 | 68,52±24,86 |
| PAS (mmHg) | 96,38±9,13 | 101,90±14,50 | 100,36±10,60 |
| PAD (mmHg) | 54,65±11,55 | 58,38±7,51 | 59,69±6,93 |
c-HDL: colesterol ligado a proteínas de alta densidad; c-LDL: colesterol ligado a proteínas de baja densidad; DE: desviación estándar; EC: edad cronológica; IGF-1: factor de crecimiento análogo a insulina tipo 1; IGFBP3: proteína transportadora 3 del factor de crecimiento análogo a la insulina; IMC: índice de masa corporal; PAD: presión arterial diastólica; PAS: presión arterial sistólica.
p<0,05.
Datos antropométricos: se incrementaron los valores de la talla desde −3,05±0,87 hasta −1,58±1,03DE (p<0,05), encontrando diferencias en los 3 años, produciéndose la máxima ganancia durante el primer año del tratamiento con rhGH. La ganancia media de talla a lo largo del estudio fue de 1,47±0,67DE. Se observa una mayor ganancia de talla en el grupo de edad de menores de 5 años al comienzo del tratamiento, 1,50±0,73 frente a 1,43±0,6DE (p < 0,05) correspondiente a los de 5 o más años. No se observaron diferencias en cuanto a la condición de prematuro y al sexo del paciente.
El peso se incrementó desde los 14,45±4,39 hasta los 25,35±7,91kg (p<0,05), encontrando diferencias en los 3 años de estudio. El IMC se vio incrementado a lo largo del período de estudio, mostrando diferencias a lo largo del segundo y tercer año de tratamiento (p<0,05), pasando de 14,51±1,31 al inicio hasta 15,80±3 en el tercer año.
La velocidad de crecimiento observada durante el tratamiento fue superior a la del período previo a la utilización del medicamento. La velocidad de crecimiento presentó un pico máximo en el primer año de uso: 0,74±0,43DE (p<0,05) en el primer año, 0,40±0,26DE en el segundo año y 0,37±0,21DE en el tercer año. No se han observado diferencias en estos parámetros con respecto a la condición de prematuro, al sexo ni al grupo de edad de inicio del tratamiento de los pacientes.
Datos clínicos: la presión arterial de los pacientes mantiene unos valores estables dentro de la normalidad a lo largo del período de estudio. No obstante, se ha detectado un incremento de la presión arterial diastólica entre el primer y el segundo año de tratamiento (54,65±11,55 vs. 58,38±7,51mmHg; p<0,05). No se han observado diferencias en estos parámetros con respecto a la condición de prematuro, al sexo ni al grupo de edad de inicio del tratamiento de los pacientes.
Datos analíticos: los valores de IGF-1 se incrementaron (p<0,05) a lo largo de los 3 años de estudio, mientras que la IGFBP3 y el cociente IGF-1/IGFBP3 aumentaron (p<0,05) en el primer y tercer año de tratamiento.
Los valores de glucohemoglobina se incrementaron durante el primer año. Por otro lado, los valores correspondientes a la glucemia e insulinemia basal se incrementaron (p<0,05) durante el segundo año de tratamiento. En cuanto al perfil lipídico, la única variación significativa a lo largo del período de estudio es la disminución del cociente c-LDL/c-HDL en el primer año de tratamiento. No se han observado diferencias en estos parámetros con respecto a la condición de prematuro, al sexo ni al grupo de edad de inicio del tratamiento de los pacientes.
La dosis media de rhGH pautada al inicio del tratamiento de los pacientes en estudio fue de 0,038±0,005mg/kg/día, y no se observaron variaciones significativas a lo largo de todo el período de estudio, ni tampoco con respecto a la condición de prematuro, al sexo ni al grupo de edad de inicio del tratamiento de los pacientes.
DiscusiónEl presente estudio describe los resultados obtenidos a lo largo de 3 años de tratamiento con rhGH en niños diagnosticados de CIR y que cumplen todos los requisitos establecidos por el Comité Asesor de Castilla y León para la utilización terapéutica de la rhGH y sustancias relacionadas. Los resultados del estudio muestran una ganancia paulatina de talla a lo largo de los 3 años de tratamiento con rhGH. La dosis media de rhGh utilizada fue de 0,038±0,005mg/kg/día, y se observó un crecimiento total de 1,47±0,67DE. Este resultado estaría en consonancia con otros estudios publicados1,5.
Teniendo en cuenta los resultados obtenidos en este estudio, los diferentes factores que influyen en la respuesta inicial a la rhGH son la edad de comienzo del tratamiento y la talla de partida de los pacientes, tal y como ha sido descrito previamente por otros autores11,12. Los resultados de este estudio indican que se produce una mayor ganancia de talla en el grupo de pacientes que comienzan con el tratamiento antes de los 5 años de edad. Este hallazgo coincide con lo observado en diferentes estudios realizados5,13.
Varios autores han descrito un aumento total de la talla durante el tratamiento con rhGH equivalente a +2DE cuando se inicia antes de los 8 años de edad, pero que puede llegar a disminuir hasta las 0,6DE si la edad de inicio del tratamiento con rhGH se retrasa hasta en torno a los 11 años de edad7,14. Estos datos, junto con lo observado en este estudio, parecen indicar la importancia de comenzar el tratamiento a una edad temprana.
En este estudio, el 51,16% de los casos, siendo el doble de frecuente en niños que en niñas, fueron recién nacidos prematuros. Este dato supone una representación muy elevada de la muestra, ya que los datos de niños nacidos prematuramente en Europa se encuentran en torno al 5-9% del total de nacimientos15. El número de recién nacidos prematuros es superior al observado en otros estudios similares realizados en España, que presentan unas cifras de en torno a un 20% de los casos16,17. En estos pacientes prematuros también se ha observado una mejoría significativa en cuanto a la ganancia de talla y peso, siendo similar a la de los nacidos a término18.
La edad de inicio del tratamiento con rhGH autorizada por las diferentes agencias reguladoras es a partir de los 4 años de edad, sin embargo, la edad media de comienzo del tratamiento de los pacientes de este estudio se sitúa en torno a los 6,06 años. No obstante, esta edad de inicio está en consonancia con otros estudios similares realizados en España13,16,17.
Tal y como han reflejado diferentes autores19,20, la velocidad de crecimiento se incrementa de forma significativa durante el período de estudio, produciéndose un pico durante el primer año, lo que determinará un incremento de la talla final, aproximándose a la talla genética de los pacientes. En el segundo y tercer año de seguimiento se observa una velocidad de crecimiento menor que la del primer año, aunque superior a la de la etapa pretratamiento, lo que conlleva una ganancia de talla menos pronunciada.
Al inicio de este estudio, los pacientes con CIR de Castilla y León se encontraban en unos valores de IMC en el límite inferior de los valores normales correspondientes a su edad. Tras el comienzo del tratamiento con rhGH, esos valores de peso se incrementan y se van normalizando a lo largo del período de estudio, tal y como se describe en la bibliografía1,5.
La dosis de rhGH media utilizada por los pacientes a lo largo de todo el período de estudio fue de 0,038±0,005mg/kg/día, por lo que se sitúa en el límite inferior del rango terapéutico recomendado para pacientes con CIR (0,035-0,060mg/kg/día). El rango de dosis de los tratamientos pautados en este estudio está en consonancia con lo descrito en la bibliografía5,21,22.
En cuanto a los diferentes parámetros analíticos sometidos a estudio, queda patente en la bibliografía7 que el tratamiento con rhGH produce una respuesta dependiente de la dosis sobre los niveles de IGF-1 e IGFBP3. Los resultados de este estudio muestran que los valores de IGF-1 se incrementaron de forma significativa a lo largo de los 3 años de seguimiento, mientras que los valores de IGFBP3 aumentaron de forma significativa en el primer y tercer año de estudio. El mayor incremento de estos 2 parámetros se produjo durante el primer año de tratamiento. Debido a ello, también se produce ese mismo aumento significativo en el cociente IGF-1/IGFBP3 durante el primer y tercer año de tratamiento. No obstante, los valores de la IGF-1 se mantuvieron en rangos de normalidad a lo largo del período de estudio sin superar las 1,5 y 2DE23. En la literatura se encuentran referencias que indican que pacientes con CIR tratados a dosis de entre 0,066 y 0,1mg/kg/día pueden experimentar incrementos en los valores de la IGF-1 que se eleven por encima del rango normal para su edad24.
El incremento en la talla de los pacientes del estudio se acompañó de un aumento sostenido de los valores de glucemia y de insulinemia basal, que fueron significativos en el segundo año de estudio, así como de los valores de glucohemoglobina, que aumentaron de forma significativa en el primer año de tratamiento; sin embargo, no parece que este incremento tenga un impacto clínico relevante. En otros estudios publicados se registraron incrementos de dichos valores sobre todo durante el primer año de tratamiento, llegando a indicar cierta resistencia insulínica25,26. Dichos valores tienden a normalizarse una vez que el tratamiento con rhGH se suspende7,26.
El perfil lipídico de los pacientes no se vio modificado a lo largo del período de seguimiento, a excepción de una disminución estadísticamente significativa en el primer año de seguimiento del cociente c-LDL/c-HDL, lo que puede implicar una posible mejoría en el perfil aterogénico de estos pacientes.
Por último, en cuanto a los parámetros clínicos, la presión arterial de los pacientes se mantuvo estable durante el tratamiento, detectándose únicamente un incremento estadísticamente significativo en la presión arterial diastólica entre el primer y el segundo año de estudio.
Aunque en este estudio no disponemos de la talla adulta de los pacientes al finalizar el tratamiento, se podría decir que el tratamiento con rhGH a las dosis utilizadas es eficaz y segura en niños con CIR sin recuperación de talla posnatal, consiguiendo un incremento en la talla de estos de la misma forma que ha quedado demostrado en otras publicaciones27–30.
En cuanto a los criterios de inclusión, en este estudio se ha realizado una excepción, incluyendo a un paciente de 3,9 años de edad al inicio del tratamiento y con una talla en ese momento de −2,11DE, ya que sus características clínicas así lo aconsejaban y, por lo tanto, el Comité lo autorizó.
Una de las limitaciones más importantes que tiene nuestro estudio está en relación con la fuente de información de donde se han recopilado los datos, ya que no recoge datos que habrían resultado de utilidad a la hora de realizar el estudio, como son los efectos secundarios o la adherencia de los pacientes al tratamiento. La obtención y el análisis de dichos datos podría ser un buen punto de partida para continuar con el estudio en el futuro.
En conclusión, los resultados de este estudio muestran que el tratamiento con rhGH favorece el crecimiento en los niños con CIR, observándose su máximo efecto en los primeros 12 meses, siendo mayor si la edad de comienzo se sitúa antes de los 5 años de edad.
AutoríaTodos los autores han contribuido intelectualmente al trabajo, reúnen las condiciones de autoría y han aprobado la versión final del mismo.
Diseño del estudio y recopilación, análisis e interpretación de los datos: Eduardo Gutiérrez Abejón, Eva Pilar Campo Ortega y Pablo Prieto Matos.
Borrador del artículo: Eduardo Gutiérrez Abejón, María Pilar Bahíllo Curieses y María Teresa Breñas Villalón.
Revisión del artículo: Eva Pilar Campo Ortega, Pablo Prieto Matos, María Teresa Breñas Villalón y Nieves Martín Sobrino.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.