Los tumores testiculares de restos adrenales (TTRA) son neoplasias infrecuentes que se han descrito, sobre todo, asociadas a la hiperplasia suprarrenal congénita en su forma clásica, con prevalencias de hasta un 40% de los pacientes, especialmente en aquellos con un control inadecuado de su enfermedad1. De forma excepcional, aparecen en otras enfermedades asociadas a unas elevadas concentraciones de ACTH2-5.
Son lesiones que podrían confundirse con tumores de células de Leydig y, por ello, los pacientes pueden llegar a ser intervenidos mediante gonadectomía. Por este motivo, debemos tener presente esta entidad, ya que su tratamiento debe ser conservador y su objetivo, preservar la fertilidad.
Presentamos, este caso, segundo recogido en la literatura, de TTRA en un paciente con enfermedad de Addison.
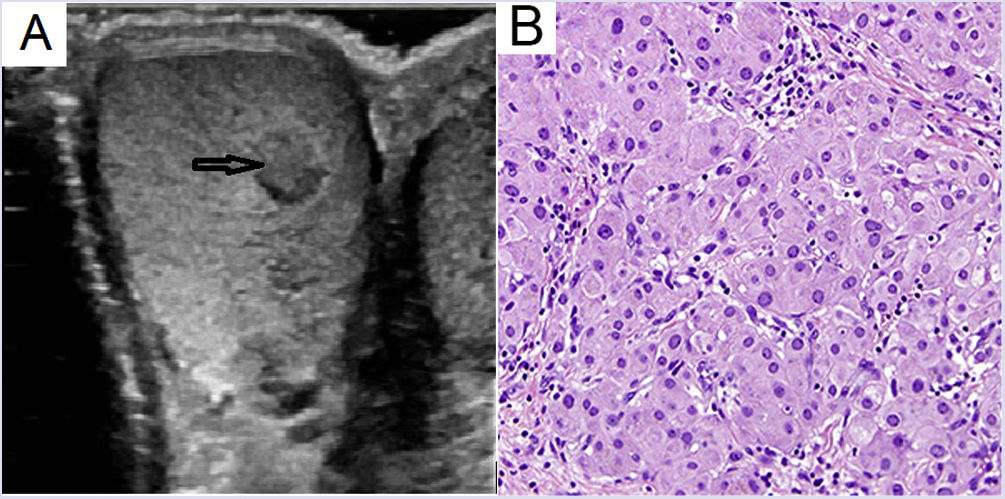
CasoSe trata de un varón de 36 años con enfermedad de Addison diagnosticado a los 21 años y en tratamiento con 20mg/día de hidrocortisona (15mg a las 9h y 5mg a las 16h) y 0,1mg/día de fludrocortisona. Fue remitido a Urología tras autopalparse una pequeña masa en ambos testículos. En la exploración presentaba una tumoración sólida y móvil en ambos testes. Se observaron mediante ecografía varias lesiones focales hipoecogénicas en el parénquima testicular, la de mayor tamaño de 6×6mm en el teste derecho (fig. 1A) que, además, presentaba aumento de la vascularización y ectasia de la rete testis. Se realizó exéresis de dicha lesión mediante epididimectomía derecha.
El estudio anatomopatológico reveló una masa de 2cm, bien definida, firme y amarillenta. Al microscopio, la masa estaba claramente demarcada del epidídimo y no presentaba características histológicas de malignidad. Estaba compuesta por células poligonales con abundante citoplasma eosinofílico y núcleos redondos (fig. 1B). Destacaba la presencia de lipofuscina en algunas células y ausencia de cristales de Reinke. La imunohistoquímica fue positiva para vimentina, inhibina A, calretina y CD56; débilmente positiva para pancitoqueratina, sinaptofisina y receptor de andrógenos y negativa para S100 y cromogranina A.
El diagnóstico de TTRA, difícil de diferenciar de los tumores de células de Leydig, se estableció en nuestro caso por los datos histopatológicos, por lo que no se realizó la orquiectomía. Fueron determinantes la multifocalidad y bilateralidad de las lesiones junto con los antecedentes de enfermedad de Addison, que condiciona una exposición crónica a elevadas concentraciones de ACTH.
DiscusiónLos tumores testiculares de restos adrenales son tumores benignos que aparecen como consecuencia de la estimulación crónica de altas concentraciones plasmáticas de ACTH sobre células pluripotenciales adrenales presentes en el testículo. Se han descrito sobre todo en pacientes con hiperplasia suprarrenal congénita, sin embargo, podrían teóricamente aparecer en otras enfermedades que cursen con elevación persistente de la ACTH1,2. De esta manera, han sido descritos, aunque de forma excepcional, en 5pacientes con síndrome de Nelson3, recientemente en 2pacientes con insuficiencia adrenal primaria asociada a adrenoleucodistrofia ligada al cromosoma X4 y en un paciente con enfermedad de Addison de origen autoinmune5. El caso que describimos es el segundo publicado asociado a enfermedad de Addison.
Los TTRA expresan genes específicos de las glándulas adrenales, como ACTH-MCR2, y genes propios gonadales, como LH-CGR, HSD17B3 e INSL36. Los marcadores rutinariamente investigados en los tumores del estroma de los cordones sexuales, como los tumores de células de Leydig, están ausentes en los TTRA. Sin embargo, marcadores específicos de células productoras de andrógenos, así como marcadores adrenocorticales, incluyendo proteínas de la esteroidogénesis adrenal, están presentes en los TTRA7.
Se ha propuesto que el origen de los TTRA son células pluripotenciales del primordio adrenogonadal o anillo urogenital, donde la ACTH es su principal estímulo7. Por este motivo, los pacientes con mayor nivel de ACTH y con una exposición temprana presentarían una mayor probabilidad para su desarrollo. No se ha estudiado el mecanismo por el que las células de los restos adrenales podrían no estar expuestas a los anticuerpos presentes en la enfermedad de Addison.
La cirugía conservadora ha sido descrita en pequeñas cohortes de pacientes, sin mejorías significativas en la función gonadal1. La terapia de elección es la intensificación del tratamiento glucocorticoideo para suprimir, en la medida de lo posible, la exposición a elevadas concentraciones de ACTH y evitar la sobredosificación esteroidea. Todo ello basado en la reducción del tamaño tumoral y en la mejora de la función testicular conseguida en algunos pacientes8. En este sentido, se podrían utilizar corticoides de vida media más larga, como prednisona o dexametasona a bajas dosis. En nuestro paciente añadimos prednisona nocturna a bajas dosis y conseguimos una importante frenación de la ACTH, como cabría esperar, pasando de una cifra inicial de 1.208 pg/ml a 291,7 pg/ml tras un mes de tratamiento.
En el foco del tratamiento farmacológico se requieren pautas más fisiológicas de liberación de glucocorticoides para mantener la ACTH controlada, junto con el desarrollo de fármacos antagonistas del receptor de ACTH, o del receptor CRF-1, que ya se están investigando en el tratamiento de la hiperplasia suprarrenal congénita9.
ConclusionesPresentamos este caso, dada su excepcionalidad. Ante la aparición de la masa testicular en un paciente con enfermedad de Addison, la posibilidad de TTRA debe tenerse en cuenta. El objetivo final del tratamiento es preservar la fertilidad, evitar gonadectomías innecesarias y ofrecer la criopreservación, en su caso.
Responsabilidades éticasPara la redacción de este artículo se han seguido los protocolos de nuestro centro de trabajo sobre la publicación de datos de pacientes, que cuentan con el consentimiento del paciente para su publicación y se ha respetado la privacidad de los sujetos.
FinanciaciónNo se ha recibido financiación.
Conflicto de interesesNinguno.