La vitamina B7, H o biotina es una vitamina hidrosoluble del grupo B que actúa como cofactor de enzimas carboxilasas esenciales en diferentes rutas metabólicas (acetil-CoA carboxilasa, piruvato carboxilasa, propionil-CoA carboxilasa y metilcrotonil-CoA carboxilasa) del ciclo del ácido tricarboxílico, la gluconeogénesis y el metabolismo de la leucina. Considerada un nutriente esencial, está presente, en pequeñas cantidades, en numerosos alimentos vegetales y animales, facilitando su ingesta diaria recomendada. También está presente en numerosos productos farmacéuticos (complejos multivitamínicos), habiéndose popularizado como suplemento de belleza, para la piel, el crecimiento de las uñas, la dermatitis seborreica y la alopecia, pudiendo adquirirse, sin receta, como producto de parafarmacia (over the counter).
Existen suplementos comercializados para el tratamiento de enfermedades desmielinizantes (esclerosis múltiple [EM] y adrenomieloneuropatía)1–3, pues a dosis elevadas (300mg/día) la biotina juega un papel esencial en la estimulación directa de la guanilato ciclasa soluble, así como del efecto antiinflamatorio y neuroprotector de la guanosín monofostato cíclico sobre la microvasculatura cerebral1,4,5. Por ello, la terapia biotínica constituye un tratamiento prometedor de la EM1,4,5, cuya alta prevalencia (33 casos/100.000 habitantes)1 constituye un problema creciente, incrementando los casos de interferencia2,3, como advierte la U. S.Food and Drug Administration (safety communication: noviembre de 2017), pudiendo afectar a diferentes pruebas de laboratorio, como la troponina-T (disminución por debajo del percentil 99), ocasionando diagnósticos potencialmente erróneos1,6.
Además de su función biológica, la biotina presenta características fisicoquímicas especiales, como su capacidad de reconocimiento y unión específica a la estreptavidina, que han propiciado su incorporación en el diseño de inmunoanálisis7–9. La ingesta de dosis altas de biotina puede interferir en los resultados de aquellos inmunoanálisis que utilizan el sistema biotina-estreptavidina entre sus componentes1. La interferencia puede ser positiva o negativa según el diseño del ensayo. Así, los inmunoanálisis no competitivos o tipo sándwich (como los diseñados para la determinación de TSH) suelen afectarse mostrando resultados falsamente disminuidos, mientras que en los competitivos (determinación de T4L, T3L y TSHR-Ab) el exceso de biotina compite con el análogo biotinilado por los sitios de unión de la estreptavidina, generando resultados falsamente elevados1,7.
Aunque la interferencia de la biotina en el resultado de algunos inmunoanálisis es conocida, su incidencia era muy poco frecuente, pues los tratamientos con dosis altas de esta se limitaban a pacientes con errores congénitos del metabolismo (déficit de biotinidasa o de carboxilasa4,5).
Presentamos un caso clínico ilustrativo de diagnóstico erróneo de hipertiroidismo en una paciente afecta de EM en tratamiento suplementario multivitamínico con biotina a altas dosis.
Se trata de una mujer de 57 años con antecedentes de EM remitente-recurrente e hipotiroidismo primario autoinmune en tratamiento sustitutivo y seguimiento endocrinológico, con adecuado control (TSH normal). Las últimas revisiones mostraron valores contradictorios compatibles con hipertiroidismo secundario: TSH 3,70μU/ml (0,30-5,0), T4L 2,07ng/dl (0,93-1,78) y anticuerpos anti-TPO 44,5UI/ml (0-34), en ausencia de clínica de hipertiroidismo y exploración física normal. Se decide, por tanto, realizar una nueva determinación tiroidea, con los siguientes resultados: TSH 1,50μU/ml y T4L 2,10ng/dl, y determinación de TSHR-Ab<1U/l.
Ante la discordancia clinicobioquímica se reinterroga a la paciente, que confirma seguir tratamiento a base de megadosis de biotina de 300mg/día (10.000 veces la dosis diaria recomendada) por su potencial utilidad neuroprotectora, al lograr un efecto estabilizador en la progresión de la EM, que mejora los síntomas y la calidad de vida de la paciente1,4,5.
Ese fue el caso de los resultados de TSH y T4L obtenidos con reactivos de Roche Diagnostics® en la plataforma analítica Modular E170 (electroquimioluminiscencia) con estreptavidina y anticuerpos biotilinados/rutenilados. Por este motivo, se decidió repetir el estudio tiroideo con otro inmunoanálisis alternativo (inmunoanálisis quimioluminiscente con partículas paramagnéticas) de Abbott Diagnostics® (Architect i4000SR), que utiliza éster de acridinio como marcaje de la reacción. Los resultados obtenidos, T4L 1,4ng/dl (0,8-2,0) y TSH 2,8μU/ml (0,5-4,0), descartan hipertiroidismo y confirman interferencia analítica.
La discordancia analítica entre el diagnóstico previo de tiroiditis de Hashimoto y el hipertiroidismo bioquímico observado en los últimos estudios señalan, únicamente, a la biotina como factor precipitante. Es importante valorar la posibilidad de interferencia con biotina, particularmente cuando los resultados no presenten correlación clínica. Ante la posibilidad de interferencia, los resultados analíticos deben obtenerse o verificarse con ensayos no afectados por la presencia de biotina. Si bien se considera una situación excepcional, cada vez se informan más casos, siendo necesario concienciar al clínico de la existencia de interferencias frecuentes y relevantes por consumo de biotina a través de suplementos alimentarios, así como de la necesidad de confrontar los resultados con la clínica antes de iniciar intervenciones o tratamientos innecesarios.
La dosis diaria de biotina recomendada en adultos es de 30μg/día, aconsejándose suplementación en estados carenciales y durante la gestación. Sin embargo, personas en tratamiento suplementario biotínico presentan ingestas mucho más elevadas (≥40mg/día). La biotina, incluso en grandes dosis, no presenta toxicidad. Sería necesario conocer el tiempo requerido antes de la extracción y la determinación1, recomendándose un período mínimo de 8h para aquellos tratamientos de biotina>5mg/día1. Recientes estudios indican, para concentraciones de 100-300mg, una vida media entre 7,8 y 18,8h3; por tanto, considerando la semivida de la biotina, serían necesarias 5 vidas medias para reducir su concentración por debajo de la tolerancia analítica de TSH, T4L, T3L y anticuerpos antitiroideos (estos últimos pueden requerir períodos más prolongados)1. Aquellos ensayos menos sensibles requerirán un menor número de vidas medias para situarse dentro de la tolerancia del ensayo, en comparación con aquellos altamente sensibles. Recientemente, la American Thyroid Association recomendaba suspender la terapia biotínica mínimo 2 días antes de evaluar la función tiroidea10 como forma de evitar falsos hipertiroidismos, precisando un período mayor1 (7 días4) para invertir la positividad de los TSHR-Ab a valores normales. Dado que su eliminación es casi exclusivamente renal, situaciones de insuficiencia renal producirán una significativa acumulación de biotina y metabolitos.
Aunque los marcadores tumorales son menos susceptibles, la biotina puede simular respuestas favorables y enmascarar recidivas de la enfermedad. Mención especial requiere la tiroglobulina, que puede presentar disminuciones≥10% en pacientes con cáncer diferenciado de tiroides1 (tabla 1).
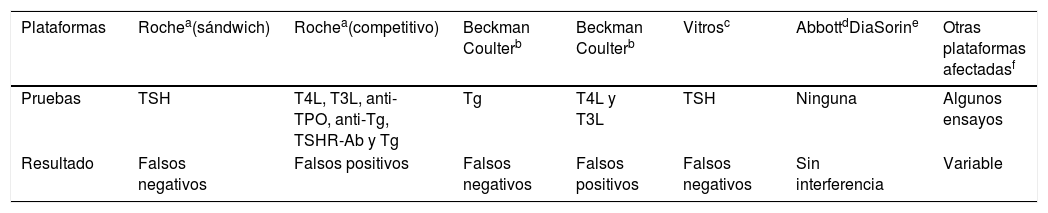
Efecto de la biotina sobre las pruebas de función tiroidea en diferentes plataformas analíticas
| Plataformas | Rochea(sándwich) | Rochea(competitivo) | Beckman Coulterb | Beckman Coulterb | Vitrosc | AbbottdDiaSorine | Otras plataformas afectadasf |
|---|---|---|---|---|---|---|---|
| Pruebas | TSH | T4L, T3L, anti-TPO, anti-Tg, TSHR-Ab y Tg | Tg | T4L y T3L | TSH | Ninguna | Algunos ensayos |
| Resultado | Falsos negativos | Falsos positivos | Falsos negativos | Falsos positivos | Falsos negativos | Sin interferencia | Variable |
Anti-Tg: anticuerpos antitiroglobulina; Anti-TPO: anticuerpos antiperoxidasa; Tg: tiroglobulina; TSH: tirotropina; TSHR-Ab: anticuerpos antirreceptor de TSH; T4L: tiroxina libre; T3L: triyodotironina libre.
La tecnología biotina-estreptavidina se usa ampliamente en múltiples plataformas susceptibles de interferencia.
Roche: la mayoría de los inmunoensayos (sándwich y competitivos) se ven afectados. Sándwich (sesgo negativo): TSH, LH, FSH, prolactina, SHBG, PTH, ACTH, insulina, péptido C, pro-BNP, troponina T, PSA total y libre, β-hCG, AFP, CEA, CA19-9 y CA15-3. Competitivos (sesgo positivo): ácido fólico, vitamina B12, cortisol, testosterona, estradiol, DHEA-S, T4L, T3L y Tg. La digoxina y los anticuerpos antitiroideos (anti-TPO, anti-Tg y anti-TSHR) son extremadamente susceptibles.
Otras plataformas afectadas: Immunodiagnostic Systems iSYS y Siemens (ADVIA Centaur, Immulite, Dimension Vista LOCI): troponina I ultra, para la cual Siemens, recientemente, emitió una nota de advertencia sobre la interferencia de biotina (falsos positivos).
Fuente: Trambas et al.1.
El laboratorio clínico debe valorar el tipo de plataforma analítica y establecer medidas adecuadas para evaluar y responder a esta amenaza creciente, requiriendo de más estudios e innovaciones analíticas para prevenir posibles consecuencias secundarias a la interferencia por biotina.