El hiperparatiroidismo normocalcémico posparatiroidectomía (HPPTNCPP) es una situación frecuente de la que no tenemos información de nuestro país. El objetivo es conocer nuestra prevalencia del HPPTNCPP, los factores etiológicos asociados, los marcadores predictivos, el tratamiento administrado y la evolución.
Pacientes y métodoEstudio retrospectivo observacional transversal sobre 42 pacientes. Se comparan 12 pacientes con HPPTNCPP y 30 sin HPPTNCPP.
ResultadosPrevalencia del HPPTNCPP: 28,6%. Factores etiológicos: déficit de vitamina D: 75%; remineralización ósea: 16,7%; insuficiencia renal: 16,7%; hipercalciuria: 8,3%. No se observó cambio en el punto de regulación de la secreción de parathormona (PTH) mediada por la calcemia, pero sí un aumento del cociente PTH/calcio corregido por albúmina (CCA) preoperatorio. Marcadores predictivos: cociente PTH/CCA (AUC 0,947; sensibilidad 100%, especificidad 78,9%) y PTH (AUC 0,914; sensibilidad 100%, especificidad 73,7%) una semana posparatiroidectomía. Evolución: en el seguimiento de 30±16,3 meses el 50% normalizó PTH y el 8,3% tuvo recurrencia del hiperparatiroidismo. Los pacientes con HPPTNCPP recibieron con menor frecuencia tratamiento preoperatorio con bifosfonatos y postoperatorio con sales de calcio.
ConclusionesEs el primer estudio en nuestro país que demuestra una prevalencia media del HPPTNCPP, relacionado principalmente con un déficit de vitamina D y con una probable resistencia a la acción de la PTH, que puede ser predicho mediante el cociente PTH/CCA y la PTH a la semana postintervención, que con frecuencia evoluciona normalizando la PTH. Disentimos del efecto etiológico de la hipercalciuria y del cambio en el punto de regulación PTH/calcemia, y reconocemos el escaso tratamiento administrado con sales de calcio en el postoperatorio.
Postparathyroidectomy normocalcemic hyperparathyroidism (PPNCHPPT) is a frequent situation for which we have no information in our country. The objective is to know our prevalence of PPNCHPPT, the associated etiological factors, the predictive markers, the treatment administered and the evolution.
Patients and methodRetrospective observational cross-sectional study on 42 patients. Twelve patients with PPNCHPPT and 30 without PPNCHPPT are compared.
ResultsHPPTNCPP prevalence: 28.6%. Etiological factors: vitamin D deficiency: 75%; bone remineralization: 16.7%; renal failure: 16.7%; hypercalciruria: 8.3%. No change in the set point of calcium-mediated parathormone (PTH) secretion was observed, but an increase in the preoperative PTH/albumin-corrected calcium (ACC) ratio was observed. Predictive markers: PTH/ACC ratio (AUC 0.947; sensitivity 100%, specificity 78.9%) and PTH (AUC 0.914; sensitivity 100%, specificity 73.7%) one week postparathyroidectomy. Evolution: follow-up 30±16.3 months: 50% normalized PTH and 8.3% had recurrence of hyperparathyroidism. Patients with PPNCHPPT less frequently received preoperative treatment with bisphosphonates and postoperative treatment with calcium salts.
ConclusionsThis is the first study in our country that demonstrates a mean prevalence of PPNCHPPT, mainly related to a vitamin D deficiency and a probable resistance to the action of PTH, which can be predicted by the PTH/ACC ratio and PTH a week post-intervention and often evolves normalizing the PTH. We disagree with the etiological effect of hypercalciuria and the change in the PTH/calcemia regulation set point, and we acknowledge the scant treatment administered with calcium salts in the postoperative period.
La curación bioquímica del hiperparatiroidismo (HPPT) tras su tratamiento quirúrgico se confirma cuando los niveles de parathormona (PTH) y de calcemia corregida por albúmina (CCA) son normales durante al menos 6 meses después de la intervención. La hipercalcemia con elevación de la PTH en este período de tiempo indica HPPT persistente, y la hipercalcemia observada más allá de los 6 meses después de un período de normocalcemia se considera HPPT recurrente. Una situación intermedia entre la curación y la persistencia del HPPT resulta de la elevación de la PTH con normocalcemia, después de la resección quirúrgica curativa de un HPPT primario (HPPTNCPP o hiperparatiroidismo normocalcémico posparatiroidectomía). Esta alteración tiene, en promedio, una prevalencia fuera de nuestro entorno del 30%1–3.
El HPPTNCPP representa una situación clínica compleja, cuyo significado patológico no está suficientemente definido y sobre el cual tampoco existe un consenso para su seguimiento y tratamiento1,2,4,5. Por el momento no hay evidencia de que el HPPTNCPP sea una consecuencia del fracaso quirúrgico1,2. En un 30-60% de estos pacientes la PTH se normalizará en los siguientes 12 a 18 meses de la intervención, y en el resto puede significar una autonomización de su secreción que debería ser monitorizada para valorar una recurrencia del HPPT1,2,6-9.
Se han descrito algunos marcadores predictivos del HPPTNCPP, aunque no de forma unánime1,2,8,10–15, y una serie de causas potencialmente responsables como son el déficit de vitamina D, el síndrome de remineralización ósea, la inadecuada ingesta o absorción de calcio, la enfermedad renal crónica y la hipercalciuria. También se han propuesto 2 mecanismos etiopatogénicos adicionales: un aumento del punto de regulación para la secreción de PTH debido a cambios en los receptores sensores de calcio de las glándulas paratiroides restantes y una reducción de la sensibilidad periférica a la PTH1,2,4,7–9,10-13,16–21.
El objetivo de este trabajo es conocer, en nuestro entorno, la prevalencia del HPPTNCPP en los primeros 6 meses después de una paratiroidectomía exitosa por un adenoma único, evaluar los posibles factores etiológicos y marcadores predictivos asociados, el tratamiento administrado y la evolución después de más de 12 meses de seguimiento.
Material y métodosEstudio retrospectivo observacional basado en la práctica clínica habitual en un centro hospitalario. Se incluyeron 42 pacientes sometidos a paratiroidectomía entre mayo de 2017 y mayo de 2022, con resultado anatomopatológico de adenoma paratiroideo único, para comparar aquellos con HPPTNCPP con los que tuvieron PTH y calcemia normales posparatiroidectomía. Todos tuvieron un seguimiento postoperatorio superior a 6 meses, y aquellos con HPPTNCPP superior a 12 meses. Se excluyeron quienes tuvieron un descenso de la PTH en las primeras 24horas posparatirodectomía menor del 60% por considerar que la intervención pudo no haber sido exitosa10, y los que recibieron tratamiento con cinacalcet preoperatorio, que pudo modificar los valores de PTH y el punto de regulación de la secreción de PTH mediado por la calcemia. El estudio ha sido aprobado por el Comité Ético de Investigación Clínica de la Fundació Assistencial Mútua de Terrassa.
Las variables recogidas de la historia clínica fueron: datos personales (sexo, edad y peso en el momento de la paratiroidectomía), resultado de la radiografía ósea de columna dorsolumbar y de la densitometría ósea preoperatoria; evolución de los parámetros analíticos preoperatorios y postoperatorios en las primeras 8 y 24horas, primera semana, primer mes, sexto mes y seguimiento posterior de la PTH, CCA, calcidiol, calciuria de 24horas, creatinina plasmática y filtrado glomerular estimado según CKD-EPI creatinina de 2009, y fosfato y magnesio plasmáticos en los casos de síndrome del hueso hambriento; tratamiento preoperatorio y postoperatorio con sales de calcio, suplementos de vitamina D y antirresortivos óseos y tiempo de seguimiento del paciente.
Las variables de evaluación principal fueron:
- -
Prevalencia del HPPTNCPP objetivado en una determinación analítica a los 6 meses después de la paratiroidectomía.
- -
Los posibles factores etiológicos asociados al HPPTNCPP2:
- ∘
Síndrome de remineralización ósea: definido en función de la aparición de síndrome del hueso hambriento (CCA menor de 8mg/dl en las primeras 24horas del postoperatorio prolongada más de 4 días con hipofosfatemia e hipomagnesemia) y/o fracturas patológicas en la columna dorsal o lumbar y/o densitometría ósea previa a la intervención quirúrgica con valores de osteoporosis en la columna lumbar y/o fémur21,22.
- ∘
Déficit de calcidiol a los 6 meses de la paratiroidectomía: calcidiol plasmático inferior a 30 ng/ml.
- ∘
Insuficiencia renal a los 6 meses de la paratiroidectomía: filtrado glomerular estimado menor de 60ml/min.
- ∘
Hipercalciuria en los primeros 6 meses tras la paratiroidectomía: calcio en orina de 24horas superior a 4mg/kg/día23.
- ∘
- -
Los posibles mecanismos etiopatogénicos asociados al HPPTNCPP:
- ∘
Cambio en el punto de regulación de la secreción de PTH mediada por la calcemia, evaluada mediante el porcentaje de descenso de la PTH y de la CCA en las primeras 24horas del postoperatorio6.
- ∘
Disminución de la sensibilidad periférica a la PTH evaluado como la ratio PTH/CCA preoperatoria.
- ∘
- -
Los posibles marcadores predictivos del HPPTNCPP2:
- ∘
Edad del paciente.
- ∘
Concentraciones de PTH, CCA y calcidiol preoperatorios y durante los primeros 6 meses postoperatorios.
- ∘
Ratios evolutivas de la PTH:
- •
Ratio PTH intraoperatoria postexéresis/PTH intraoperatoria preexéresis.
- •
Ratio PTH 8h postexéresis/PTH prequirúrgica.
- •
Ratio PTH 24h postexéresis/PTH prequirúrgica.
- •
Ratio PTH 24h postexéresis/PTH 8h postexéresis.
- •
- ∘
Ratio PTH/CCA pre y postoperatoria.
- ∘
Las variables de evaluación secundaria fueron la evolución después de 6 o más meses de seguimiento del HPPTNCPP valorado como normalización de la PTH (al menos las 2 últimas PTH son normales), persistencia de elevación de la PTH o recurrencia del HPPT y el efecto del tratamiento con sales de calcio, suplementos de vitamina D y/o antirresortivos óseos.
La calcemia se determinó mediante el método 5-nitro-5’-methyl-BAPTA, el calcio en orina con la complexona de orto-cresolftaleína, la albúmina plasmática mediante el verde de bromocresol y la PTH intacta y el calcidiol mediante un inmunoanálisis electroquimioluminiscente. Los valores de referencia para la calcemia fueron 8,6-10,0mg/dl, con un coeficiente de variación del 0,61%, y para la PTH intacta 15,0-65,7pg/ml con un coeficiente de variación del 3,05% y una sensibilidad del ensayo de 5,5pg/ml. El resto de parámetros bioquímicos fueron realizados por procedimientos estándar. En las radiografías de columna dorsal y lumbar se valoró la presencia de fracturas vertebrales por una disminución mayor o igual al 20% de la altura anterior, media o posterior del cuerpo vertebral. La densidad mineral ósea en la columna lumbar (L2-L4) y en el fémur proximal se valoró mediante absorciometría dual de rayos X (equipo Lunar PRODIGY).
Se realizó un análisis descriptivo de las variables recogidas. El análisis univariante de las diferencias entre variables continuas y categóricas se analizó con la prueba «t» de Student, y la relación entre variables categóricas con la prueba de Chi cuadrado o F de Fisher. Se realizó un análisis de regresión logística binaria para investigar la independencia de las variables predictoras del HPPTNCPP. Se generaron curvas COR para conocer la sensibilidad y especificidad en la predicción del HPPTNCPP. La significación estadística se estableció en p<0,05 (2 colas). El análisis estadístico se realizó con el software Epidat, versión 3.1 (Servizo Galego de Saúde, Galicia, España).
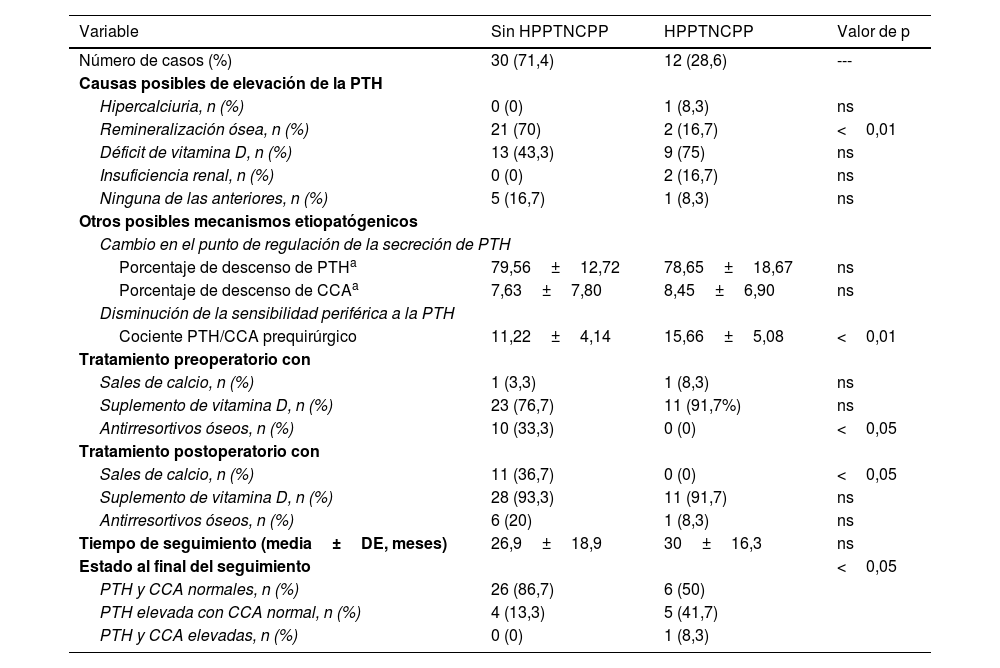
ResultadosSe han incluido 42 pacientes, 39 mujeres (92,9%) y 3 hombres (7,1%), con una edad media de 58,6±11 años. La prevalencia de pacientes con HPPTNCPP fue de 12 casos (28,6%). Las causas relacionadas, el tratamiento recibido y la evolución se detallan en la tabla 1.
Prevalencia, posibles causas, tratamiento recibido y evolución de los pacientes con HPPTNCPP comparado con los pacientes sin HPPTNCPP después de la paratiroidectomía
| Variable | Sin HPPTNCPP | HPPTNCPP | Valor de p |
|---|---|---|---|
| Número de casos (%) | 30 (71,4) | 12 (28,6) | --- |
| Causas posibles de elevación de la PTH | |||
| Hipercalciuria, n (%) | 0 (0) | 1 (8,3) | ns |
| Remineralización ósea, n (%) | 21 (70) | 2 (16,7) | <0,01 |
| Déficit de vitamina D, n (%) | 13 (43,3) | 9 (75) | ns |
| Insuficiencia renal, n (%) | 0 (0) | 2 (16,7) | ns |
| Ninguna de las anteriores, n (%) | 5 (16,7) | 1 (8,3) | ns |
| Otros posibles mecanismos etiopatógenicos | |||
| Cambio en el punto de regulación de la secreción de PTH | |||
| Porcentaje de descenso de PTHa | 79,56±12,72 | 78,65±18,67 | ns |
| Porcentaje de descenso de CCAa | 7,63±7,80 | 8,45±6,90 | ns |
| Disminución de la sensibilidad periférica a la PTH | |||
| Cociente PTH/CCA prequirúrgico | 11,22±4,14 | 15,66±5,08 | <0,01 |
| Tratamiento preoperatorio con | |||
| Sales de calcio, n (%) | 1 (3,3) | 1 (8,3) | ns |
| Suplemento de vitamina D, n (%) | 23 (76,7) | 11 (91,7%) | ns |
| Antirresortivos óseos, n (%) | 10 (33,3) | 0 (0) | <0,05 |
| Tratamiento postoperatorio con | |||
| Sales de calcio, n (%) | 11 (36,7) | 0 (0) | <0,05 |
| Suplemento de vitamina D, n (%) | 28 (93,3) | 11 (91,7) | ns |
| Antirresortivos óseos, n (%) | 6 (20) | 1 (8,3) | ns |
| Tiempo de seguimiento (media±DE, meses) | 26,9±18,9 | 30±16,3 | ns |
| Estado al final del seguimiento | <0,05 | ||
| PTH y CCA normales, n (%) | 26 (86,7) | 6 (50) | |
| PTH elevada con CCA normal, n (%) | 4 (13,3) | 5 (41,7) | |
| PTH y CCA elevadas, n (%) | 0 (0) | 1 (8,3) | |
Entre los casos de síndrome de remineralización no hubo ninguno con síndrome del hueso hambriento postoperatorio. En algunos pacientes se pudo reconocer más de una causa: en el grupo de pacientes con HPPTNCPP hubo un caso de hipercalciuria y déficit de vitamina D y otro de remineralización y déficit de vitamina D, y en el grupo de pacientes sin HPPTNCPP hubo 9 casos de déficit de vitamina D y remineralización. Todos los fármacos antirresortivos óseos administrados fueron bifosfonatos.
En cuanto al estado al final del seguimiento, en el grupo sin HPPTNCPP 4 casos tuvieron HPPT normocalcémico como consecuencia del déficit de vitamina D. En el grupo HPPTNCPP solo hubo una recurrencia del HPPT en un paciente con insuficiencia renal crónica, y en los 5 casos que persistieron con PTH elevada y calcemia normal al final del seguimiento las causas reconocidas fueron remineralización en un caso, déficit de vitamina D en 2 casos, hipercalciuria y déficit de vitamina D en un caso y déficit de vitamina D y remineralización en un caso; ninguno recibió tratamiento preoperatorio con sales de calcio ni bifosfonatos, pero sí en todos los casos suplementos de vitamina D, y en el postoperatorio ninguno había recibido tratamiento con sales de calcio, 4 recibieron suplementos de vitamina D y uno bifosfonatos.
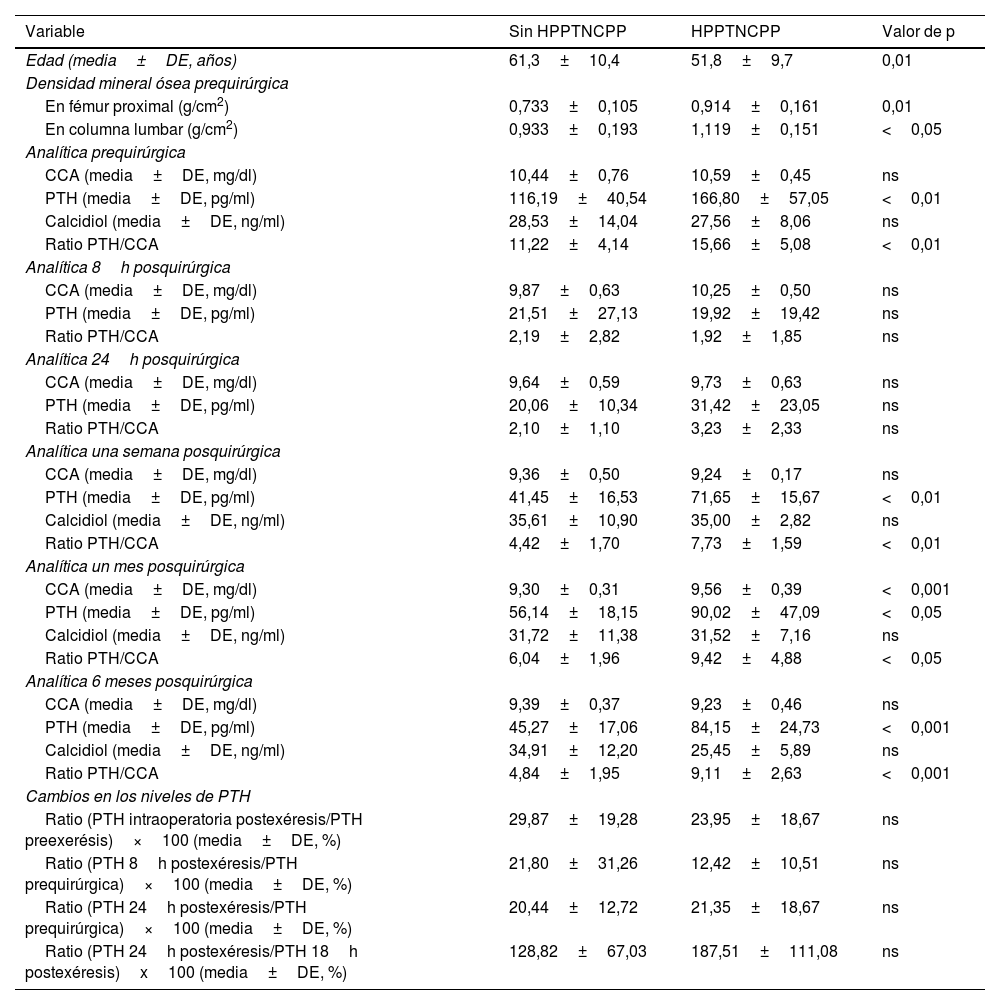
En la tabla 2 se detallan los posibles marcadores predictivos del HPPTNCPP. En el análisis de regresión logística solo la variable ratio PTH/CCA una semana posquirúrgica estuvo asociada independientemente al HPPTNCPP (odds ratio 3,929, IC 95%: 1,054-14,647; p<0,05). Cuando se extrajo dicha variable del modelo la variable PTH 1 semana posquirúrgica fue la única independientemente asociada al HPPTNCPP (odds ratio 1,130, IC 95%: 1,002-1,275; p<0,05).
Posibles factores predictivos del HPPTNCPP
| Variable | Sin HPPTNCPP | HPPTNCPP | Valor de p |
|---|---|---|---|
| Edad (media±DE, años) | 61,3±10,4 | 51,8±9,7 | 0,01 |
| Densidad mineral ósea prequirúrgica | |||
| En fémur proximal (g/cm2) | 0,733±0,105 | 0,914±0,161 | 0,01 |
| En columna lumbar (g/cm2) | 0,933±0,193 | 1,119±0,151 | <0,05 |
| Analítica prequirúrgica | |||
| CCA (media±DE, mg/dl) | 10,44±0,76 | 10,59±0,45 | ns |
| PTH (media±DE, pg/ml) | 116,19±40,54 | 166,80±57,05 | <0,01 |
| Calcidiol (media±DE, ng/ml) | 28,53±14,04 | 27,56±8,06 | ns |
| Ratio PTH/CCA | 11,22±4,14 | 15,66±5,08 | <0,01 |
| Analítica 8h posquirúrgica | |||
| CCA (media±DE, mg/dl) | 9,87±0,63 | 10,25±0,50 | ns |
| PTH (media±DE, pg/ml) | 21,51±27,13 | 19,92±19,42 | ns |
| Ratio PTH/CCA | 2,19±2,82 | 1,92±1,85 | ns |
| Analítica 24h posquirúrgica | |||
| CCA (media±DE, mg/dl) | 9,64±0,59 | 9,73±0,63 | ns |
| PTH (media±DE, pg/ml) | 20,06±10,34 | 31,42±23,05 | ns |
| Ratio PTH/CCA | 2,10±1,10 | 3,23±2,33 | ns |
| Analítica una semana posquirúrgica | |||
| CCA (media±DE, mg/dl) | 9,36±0,50 | 9,24±0,17 | ns |
| PTH (media±DE, pg/ml) | 41,45±16,53 | 71,65±15,67 | <0,01 |
| Calcidiol (media±DE, ng/ml) | 35,61±10,90 | 35,00±2,82 | ns |
| Ratio PTH/CCA | 4,42±1,70 | 7,73±1,59 | <0,01 |
| Analítica un mes posquirúrgica | |||
| CCA (media±DE, mg/dl) | 9,30±0,31 | 9,56±0,39 | <0,001 |
| PTH (media±DE, pg/ml) | 56,14±18,15 | 90,02±47,09 | <0,05 |
| Calcidiol (media±DE, ng/ml) | 31,72±11,38 | 31,52±7,16 | ns |
| Ratio PTH/CCA | 6,04±1,96 | 9,42±4,88 | <0,05 |
| Analítica 6 meses posquirúrgica | |||
| CCA (media±DE, mg/dl) | 9,39±0,37 | 9,23±0,46 | ns |
| PTH (media±DE, pg/ml) | 45,27±17,06 | 84,15±24,73 | <0,001 |
| Calcidiol (media±DE, ng/ml) | 34,91±12,20 | 25,45±5,89 | ns |
| Ratio PTH/CCA | 4,84±1,95 | 9,11±2,63 | <0,001 |
| Cambios en los niveles de PTH | |||
| Ratio (PTH intraoperatoria postexéresis/PTH preexerésis)×100 (media±DE, %) | 29,87±19,28 | 23,95±18,67 | ns |
| Ratio (PTH 8h postexéresis/PTH prequirúrgica)×100 (media±DE, %) | 21,80±31,26 | 12,42±10,51 | ns |
| Ratio (PTH 24h postexéresis/PTH prequirúrgica)×100 (media±DE, %) | 20,44±12,72 | 21,35±18,67 | ns |
| Ratio (PTH 24h postexéresis/PTH 18h postexéresis)x100 (media±DE, %) | 128,82±67,03 | 187,51±111,08 | ns |
En las curvas COR para diferenciar pacientes con y sin HPPTNCPP las variables que obtuvieron una mayor área bajo la curva, de magnitud similar, fueron el cociente PTH/CCA y la PTH, ambas a la semana de la intervención quirúrgica (tabla 3).
Variables con poder predictivo para diferenciar entre pacientes con y sin HPPTNCPP
| Variable | Área bajo la curva (IC 95%) | Punto de corte | Sensibilidad (IC 95%) | Especificidad (IC 95%) |
|---|---|---|---|---|
| PTH/CCA una semana postoperatoria | 0,947(0,839-1) | 5,47 | 100%(100%) | 78,9% (64,3-93,5%) |
| PTH una semana postoperatoria | 0,914(0,780-1) | 49,5 | 100%(100%) | 73,7%(58-89,4%) |
Hasta donde alcanza nuestro conocimiento, esta es la primera serie de pacientes de nuestro país donde se analiza el HPPTNCPP. La prevalencia encontrada del 28,6% resulta intermedia entre las series previamente documentadas, si bien cabe resaltar que el rango de referencia de esta prevalencia es muy amplio, del 8% al 44%1,2,5–15,19,24. La razón de esta disparidad no se conoce, pero podría tener que ver con la causa del HPPTNCPP, no siempre fácil de detectar ni de valorar, que en nuestro caso ha resultado ser predominantemente el déficit de vitamina D.
La mayoría de estudios previos evalúan solo alguna de las etiologías responsables del HPPTNCPP, con lo cual no hay datos sobre la incidencia real de cada una y no se pueden establecer comparaciones. El déficit de vitamina D es común y ocurre con mayor frecuencia en los pacientes con HPPT debido al mayor catabolismo de la vitamina D, y este a su vez puede ocasionar un HPPT secundario1,6,11,12,15. En nuestra serie resultó ser el factor etiológico más frecuente relacionado con el HPPTNCPP y estuvo menos presente, aunque sin significación estadística, quizás por el pequeño número de casos en los pacientes sin HPPTNCPP. La gran mayoría de los pacientes de cada grupo recibió tratamiento pre y postoperatorio con suplementos de vitamina D, y normalizaron los niveles durante el primer mes, pero en el grupo de pacientes con HPPTNCPP descendieron al llegar al sexto mes posparatiroidectomía, lo cual se pudo reflejar en un ascenso supranormal de la PTH.
La remineralización ósea puede ser un factor muy influyente en el HPPTNCP y su efecto puede durar entre uno y 4 años8,10,11,21. Se justifica por el depósito de sales cálcicas en el hueso, que produce una disminución del calcio sérico, lo cual provoca la elevación de la PTH para mantener el nivel normal de calcio extracelular2. La mejora significativa densitométrica de la osteoporosis al año de la paratiroidectomía de pacientes con HPPT primario constituye una prueba valiosa sobre la remineralización ósea que acontece en estos casos25. El clásico síndrome del hueso hambriento, máximo exponente de la remineralización ósea, de presentación aguda posquirúrgica, es una rareza que no suele documentarse en las series de las últimas décadas de pacientes con HPPT primario debido a su diagnóstico precoz11,21. La definición del síndrome de remineralización ósea es poco precisa, pues está basada en algunas características asociadas a una situación de desmineralización ósea, como son la presencia de fracturas patológicas, la menor densidad mineral ósea, los niveles elevados de fosfatasa alcalina o de osteocalcina, una menor calcemia y mayor PTH postoperatorias, la mejora del perfil bioquímico de la PTH y de la calcemia con el tratamiento a base de sales de calcio con o sin suplementos de vitamina D, y su tendencia a la extinción evolutiva posparatiroidectomía. En la práctica asistencial de pacientes con HPPT disponemos de datos densitométricos y datos radiológicos y clínicos sobre fracturas patológicas para poder justificar un fenómeno de remineralización ósea. Sin embargo, no existe una forma validada, precisa y estratificada de reconocerla, por lo que pueden pasar desapercibidas formas «menos intensas» de remineralización. En nuestra serie, la remineralización ósea basada en criterios densitométricos de osteoporosis con o sin fracturas patológicas se reconoció en una pequeña proporción de pacientes con HPPTNCPP, y sorprendentemente fue más frecuente en el grupo de los pacientes sin HPPTNCPP, probablemente influido por su mayor edad; la mayor frecuencia de tratamiento preoperatorio con antirresortivos óseos y postoperatorio con sales de calcio pudo colaborar a evitar la elevación supranormal de la PTH.
La insuficiencia renal es claramente un factor que contribuye al HPPTNCPP. Con filtrados glomerulares por debajo de 70ml/min ya se incrementan los valores de PTH, y por debajo de 60ml/min se consiguen niveles supranormales de PTH, aunque sin un efecto sustancial sobre la calcemia hasta que el filtrado glomerular es inferior a 20ml/min4,6,12,13. No ocurre lo mismo con la hipercalciuria, pues su efecto sobre el HPPTNCPP es controvertido. En la década de 1970 y 1980 se comunicaron los primeros casos aislados, donde se relacionó la hipercalciuria con la recurrencia de un HPPT16. En el año 2005 Farooki et al.20 insistieron en que la hipercalciuria debía considerarse como causa del HPPTNCPP. La hipercalciuria idiopática es una anomalía metabólica que se puede acompañar de cálculos urinarios y disminución de la densidad mineral ósea, pero característicamente los pacientes no tienen valores supranormales de PTH, a diferencia de aquellos con hipercalciuria secundaria al HPPT23,26–28. Ello es discordante con otros estudios donde se atribuyó a algunos pacientes con hipercalciuria idiopática unos valores elevados de PTH28,29, y han dado lugar a que en revisiones actuales se siga considerando la hipercalciuria idiopática una causa de PTH supranormal1–3. En los pacientes con HPPTNCPP e hipercalciuria habría que considerar que la hipercalciuria es secundaria al HPPTNCPP, o bien que se trata de 2 enfermedades concomitantes, una hipercalciuria idiopática y otro factor que conduce a la elevación de la PTH. En nuestra serie hubo un caso reconocido de hipercalciuria entre los pacientes con HPPTNCPP, asociado a un déficit de vitamina D, tratado con suplementos de vitamina D en el preoperatorio, pero no en el postoperatorio, por lo cual no llegó a normalizar los niveles de calcidiol y permaneció con PTH supranormal durante el seguimiento. En este caso no pudimos establecer cuál fue el papel de la hipercalciuria en la elevación de la PTH.
Un cambio en el punto de regulación de la calcemia sobre la secreción de PTH ha sido desestimado en 2 estudios con metodologías diferentes tras evaluar esta posible etiopatogenia del HPPTNCPP6,10. Un menor porcentaje de descenso de la PTH en el postoperatorio precoz de los pacientes con HPPTNCPP sugiere un aumento en el punto de regulación de la secreción de PTH mediada por la calcemia6, pero esto tampoco ocurrió en nuestros pacientes, con lo cual parece razonable descartar este fenómeno como causa del HPPTNCPP.
La resistencia periférica a la acción de la PTH también ha sido considerada un posible mecanismo etiopatogénico del HPPTNCPP1,2. Inicialmente se comunicó una resistencia al efecto renal de la PTH en pacientes con HPPT secundario al déficit de vitamina D, por una respuesta disminuida en la generación de adenosín monofosfato cíclico tras la administración exógena de PTH, que se normalizó tras un tratamiento con vitamina D17. En otro estudio, a las 6 semanas de la paratiroidectomía, se apreció que tras una infusión de PTH el ascenso de la calcemia y la disminución de la fosfatemia eran menores en los pacientes con HPPTNCPP que en aquellos que mantenían la PTH normal, lo cual se interpretó como una disminución en la sensibilidad periférica a la PTH18. Este fenómeno de resistencia periférica a la PTH podía estar ocasionado por unos niveles inferiores de vitamina D y/o por un HPPT preoperatorio más grave, que produciría una regulación a la baja en el número de receptores de PTH10,18. En el estudio de Dhillon et al.19 la menor ratio de 1,25dihidroxivitamina D/PTH encontrada en los pacientes con HPPTNCPP se valoró como una resistencia renal a la PTH, lo cual fue refrendado por el grupo de Yamashita et al.12 por una mayor ratio preoperatoria PTH/adenosín monofosfato cíclica renal, especificando que esta resistencia a la PTH era mayor en los casos con insuficiencia renal y con déficit de vitamina D. Los estudios sobre la resistencia periférica a la acción de la PTH son escasos, y de ellos no se desprende una fórmula uniforme y validada para poder aplicarla rutinariamente en la práctica clínica. Se fundamentan en la respuesta a la administración de PTH o en la ratio de la PTH con algún metabolito producido como consecuencia de su acción. En nuestro caso hemos evaluado la ratio PTH/CCA preoperatoria, habida cuenta que la CCA es un metabolito directamente relacionado con la acción de la PTH, y que en el período preoperatorio no está influida por los cambios dinámicos del postoperatorio. Esta ratio PTH/CCA, aquí descrita por primera vez, resultó significativamente superior en los pacientes con HPPTNCPP, indicando que un mayor nivel de PTH no resulta en una mayor calcemia de forma proporcionada, lo cual podría ser compatible con una resistencia periférica a la acción de la PTH. Ello se podría relacionar con un HPPT más grave dados los mayores niveles de PTH preoperatorios, con el déficit de vitamina D y con la mayor presencia de pacientes con insuficiencia renal crónica en este grupo de pacientes con HPPTNCPP.
Sobre los marcadores predictivos del HPPTNCPP, la mayoría de autores describen una mayor concentración de PTH preoperatoria5,6,10–15,19 y un mayor tamaño del adenoma resecado10,13,18. La elevación de la osteocalcina10, un menor contenido mineral óseo, niveles menores de vitamina D y una menor calcemia postoperatoria5,6,11–13,15 también han sido descritos como marcadores predictivos del HPPTNCPP. La mayor edad de los pacientes ha resultado un predictor del HPPTNCPP en relación con un mayor déficit asociado de vitamina D6,10,13–15,21. En nuestro estudio la edad de los casos con HPPTNCPP resultó significativamente inferior, al revés de lo esperado, posiblemente porque otros factores como el mayor nivel de PTH preoperatoria incidieron en este grupo. Asimismo, los valores mayores de densidad mineral ósea en estos pacientes pudieron estar en relación con su menor edad. Por otra parte, los valores de PTH y especialmente el cociente PTH/CCA en el período postoperatorio temprano, a la semana de la intervención, han permitido obtener puntos de corte con elevada sensibilidad y especificidad para la predicción del HPPTNCPP, que no han sido descritos previamente. La ligera elevación de la CCA encontrada al mes de la intervención pudo ser debida al gran incremento de la PTH en las semanas previas.
Una gran proporción de pacientes con HPPTNCPP consiguen normalizar la PTH durante el seguimiento, como ha ocurrido en el 50% de nuestros pacientes. En otras series entre el 30% y el 60% normalizan la PTH en un tiempo de seguimiento de 1-1,5 años1,2,6–11,13,19,30. Esta normalización de la PTH podría responder a la corrección postoperatoria espontánea o inducida por un tratamiento del déficit de vitamina D y del déficit en la ingesta o absorción intestinal de calcio, y también a la resolución de la remineralización ósea8,10,11,25. Nuestra serie adolece de un bajo porcentaje de pacientes tratados con sales de calcio, lo cual podría haber empeorado su evolución. Ocasionalmente los pacientes con HPPTNCPP progresan a HPPT recurrente al desarrollar hipercalcemia, lo cual ocurre entre el 0% y 4,8% a 10 años de seguimiento7,8,11,13,15,19, y hasta el 5,4% si se incluyen pacientes con enfermedad multiglandular14,24. Los pacientes con recurrencia del HPPT han sido relacionados con una mayor afectación preoperatoria del HPPT, una mayor calcemia y deterioro de la función renal preoperatorias13 y una mayor calcemia postoperatoria14. Las tasas de recurrencia descritas no han sido uniformemente superiores a las encontradas en los pacientes sin HPPTNCPP, como ha ocurrido en nuestro estudio2,3,15.
Actualmente no hay consenso acerca del manejo de los pacientes con HPPTNCPP. En cualquier caso, parece recomendable asegurar que tengan un nivel correcto de vitamina D y suficiente ingesta alimentaria de calcio3. El tratamiento a base de sales de calcio con o sin suplementos de vitamina D ha producido aumento de la densidad mineral ósea y descensos significativos y normalizaciones de la PTH postoperatoria7,12,21. En algunos centros ha sido rutinariamente recomendado a todos los pacientes sometidos a paratiroidectomía por HPPT1, mientras que en otros solo a los pacientes con HPPTNCPP2. El tratamiento con vitamina D en el postoperatorio también ha demostrado reducir la incidencia del HPPTNCPP9 y ha sido recomendado a pacientes con HPPTNCPP basándose en la resistencia renal a la acción de la PTH en los casos con déficit de vitamina D12. En nuestra serie casi todos los pacientes habían recibido tratamiento con suplementos de vitamina D, pero en el grupo del HPPTNCPP fueron insuficientes para mantener unos niveles adecuados de calcidiol durante los 6 meses posparatiroidectomía. Por otra parte, han sido pocos, y de forma significativamente menor en el grupo del HPPTNCPP, los casos que han recibido sales de calcio. El tratamiento preoperatorio con bifosfonatos en los pacientes con osteoporosis e HPPT tiene un claro efecto beneficioso, mejorando la densidad mineral ósea al disminuir o normalizar significativamente el recambio óseo22. Este efecto también pudo haber acontecido de forma importante en el grupo de pacientes sin HPPTNCPP, pues habían recibido bifosfonatos con mayor frecuencia. La demostración de la utilidad de los bifosfonatos para casos menos expresivos de remineralización ósea, sin osteoporosis, está aún por estudiar.
El estudio tiene limitaciones. El carácter retrospectivo ha comportado la falta de algunos datos en el registro de variables, lo cual se ha tenido en cuenta en cada análisis estadístico efectuado. El tamaño de la muestra es relativamente pequeño, intermedio respecto al de otros estudios6,8,9,10,12,18,19,25, y ha podido comportar un menor poder estadístico para detectar diferencias significativas. El período de seguimiento medio postoperatorio de los casos con HPPTNCPP se limitó a unos 2,5 años; un tiempo más prolongado podría haber modificado la evolución. La definición del síndrome de remineralización ósea resulta poco precisa, pues no existen criterios diagnósticos en función de su gravedad, de manera que formas menos intensas de las aquí registradas pudieron pasar desapercibidas. No hemos podido evaluar la inadecuada ingesta o absorción de calcio como causa del HPPTNCPP, como ha ocurrido en otros estudios de carácter retrospectivo. El tratamiento con bifosfonatos en el grupo de pacientes sin HPPTNCPP pudo haber incrementado ligeramente el valor de la PTH y reducido el valor de la calcemia, pero este efecto no impidió reconocer los valores superiores de la PTH y del cociente PTH/CCA del grupo con HPPTNCPP.
En conclusión, el HPPTNCPP representa una situación clínica compleja y frecuente. Este es el primer estudio realizado en nuestro país que pone de manifiesto una prevalencia media de pacientes con HPPTNCPP, y reconoce que en la mayoría de los casos está relacionada con un déficit de vitamina D y una posible resistencia periférica a la acción de la PTH, teniendo en cuenta que no se dispone de una definición y estratificación precisas y operativas de la remineralización ósea posparatiroidectomía. Asimismo, resulta cuestionable seguir considerando como causas del HPPTNCPP la hipercalciuria y el cambio en el punto de regulación de la secreción de PTH mediada por la calcemia. Describimos el cociente PTH/CCA y la PTH a la semana del postoperatorio como marcadores predictivos precisos del HPPTNCPP. La mitad de los casos con HPPTNCPP evolucionan normalizando la PTH y la tasa de recurrencias del HPPT no ha resultado superior en este grupo de pacientes. El tratamiento preoperatorio con bifosfonatos en los casos de osteoporosis y el tratamiento con suplementos de vitamina D en el postoperatorio pueden minimizar la frecuencia de HPPTNC, si bien llamamos la atención sobre el escaso uso del tratamiento postoperatorio con sales de calcio.
AutoríaCada autor ha contribuido materialmente en la investigación y preparación del artículo. En concreto:
- -
Luis García Pascual: concepción y diseño del estudio, adquisición y análisis de datos, interpretación de resultados, escritura del borrador y aprobación de la versión final.
- -
Andreu Simó-Servat, Carlos Puig-Jové, Lluís García-González: concepción y diseño del estudio, interpretación de resultados, revisión crítica y aprobación de la versión final.
- -
Protección de personas y animales. Los autores declaran que en esta investigación no se han llevado a cabo experimentos con humanos ni animales.
- -
Confidencialidad de los datos. Los autores declaran que han cumplido los protocolos de su centro de trabajo para la publicación de datos de pacientes.
La presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de interesesNinguno.