Serratia marcescens es un microorganismo ubicuo, de gran importancia por su frecuente implicación en infecciones nosocomiales. Su habilidad para sobrevivir en ambientes húmedos con escasos nutrientes contribuye a su persistencia en soluciones antisépticas y desinfectantes1, habiéndose descrito numerosos brotes asociados al uso de soluciones contaminadas de clorhexidina2-4.
El 19 de diciembre de 2014 la Agencia Española de Medicamentos y Productos Sanitarios emitió la primera alerta sanitaria (ref. COS 2/2014) informando de la retirada del mercado de los lotes I-33, I-34 e I-35 del producto antiséptico Bohmclorh® solución acuosa al 2% de clorhexidina, envase de 250ml, por estar contaminados con S. marcescens5. El día 23 de diciembre se emitió una nueva alerta (ref. COS 3/2014) en la que se ampliaba la retirada a los lotes I-36 e I-37 y se confirmaba la inmovilización del resto de los lotes y presentaciones del producto6. Posteriormente, el 30 de diciembre se emitió una nota (ref. COS 4/2014) indicando la retirada de todos los lotes fabricados a partir del 8 de octubre de 20147 y, finalmente, el 9 de enero de 2015 (ref. COS 01/2015) se retiraron también las fórmulas magistrales de clorhexidina elaboradas por el laboratorio con la misma materia prima8. Por otro lado, el 18 de diciembre de 2014 se informó, desde el servicio de Microbiología a Medicina Preventiva de nuestro hospital, de la detección simultánea de varios casos de infección por S. marcescens en la sección de Neonatología. Posteriormente, se constató el uso en dicha sección de la solución acuosa al 2% de clorhexidina Bohmclorh® de 60ml (lote sin especificar). Ante la coincidencia temporal de los casos y las alertas sanitarias emitidas, se planteó la necesidad de realizar un estudio de epidemiología molecular para establecer la posible relación del brote con el uso de la solución de clorhexidina.
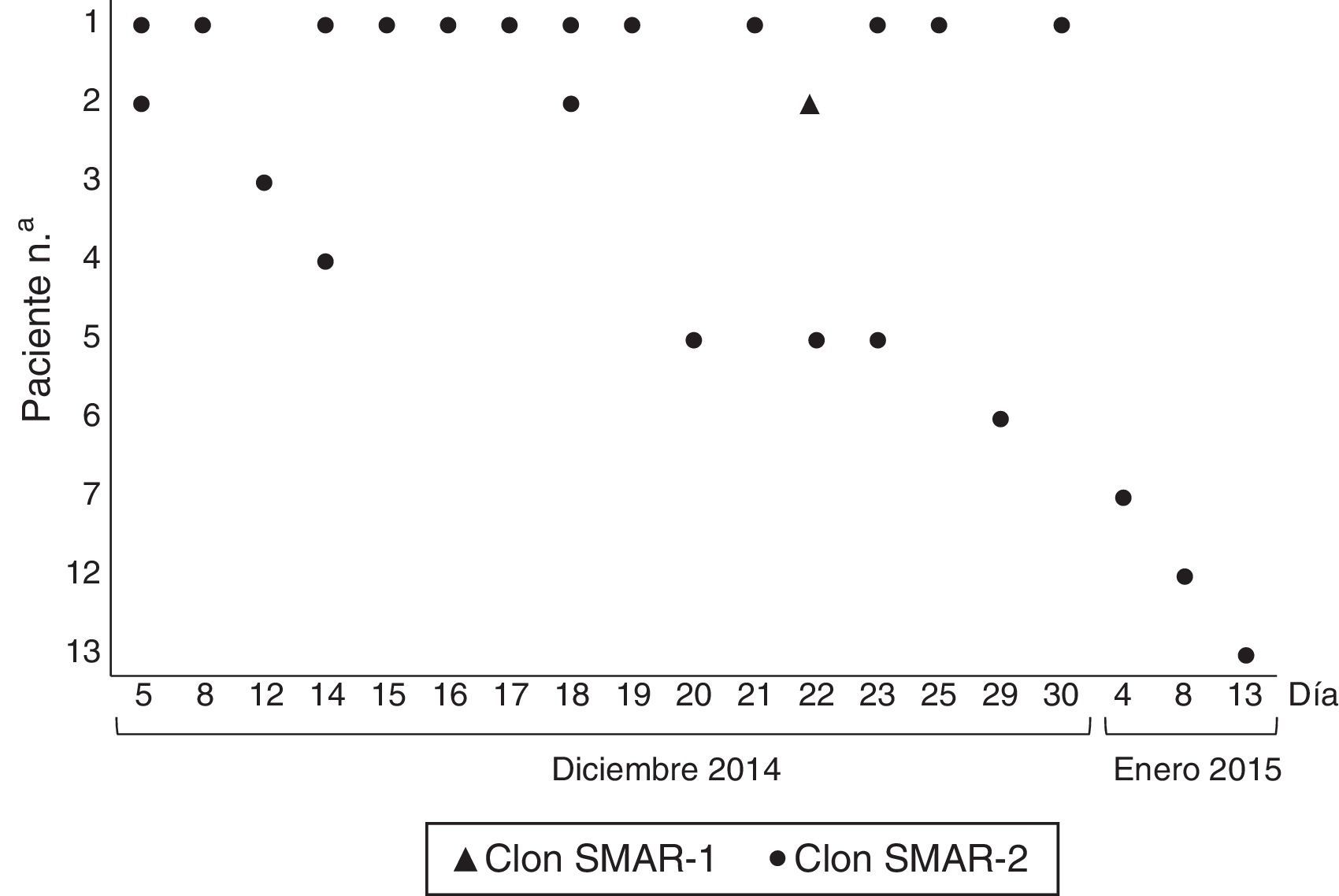
En primer lugar, se realizó un análisis retrospectivo de todos los cultivos positivos para S. marcescens detectados por el servicio de Microbiología desde el día 1 de diciembre de 2014 al 22 de enero de 2015. La identificación bacteriana se realizó mediante espectrometría de masas MALDI-TOF (MALDI Biotyper). En el período de estudio se detectaron 29cultivos positivos para S. marcescens correspondientes a 13pacientes: 9pacientes de Neonatología, 3pacientes de la UCI de adultos y un paciente de Nefrología-Diálisis. El análisis retrospectivo de los casos de Neonatología evidenció la existencia de un brote (fig. 1).
También se analizaron un total de 28muestras procedentes de las soluciones de clorhexidina Bohmclorh® 2% que habían sido abiertas y empleadas en la sección de Neonatología durante el brote, aislándose S. marcescens en 18 de ellas. Dichas muestras se remitieron al servicio de Microbiología identificadas por número de box de procedencia, por lo que no fue posible asignarlas retrospectivamente a un lote de fabricación concreto. Del mismo modo, se analizaron alícuotas de clorhexidina Bohmclorh® 2% de 8 frascos que no habían sido abiertos previamente (I-1, I-2, I-4, I-5, I-6, I-7, I-9 e I-11), y únicamente se detectó este microorganismo en uno de los lotes analizados (I-11). Todos las muestras fueron manipuladas en estrictas condiciones de esterilidad y cultivadas, sin concentración previa, mediante siembra de una alícuota de manera cuantitativa en agar sangre e inoculación directa en caldo tioglicolato.
La clonalidad de todos los aislados de S. marcescens se estableció mediante la técnica de electroforesis de campo pulsado con la enzima de restricción XbaI. Los pulsotipos obtenidos se analizaron y compararon aplicando los criterios de Tenover et al9. El análisis del tipado molecular reveló la existencia de 8clones distintos. Todos los aislados de las soluciones de clorhexidina se identificaron como el mismo clon, designado como SMAR-1. Únicamente uno de los aislados clínicos, procedente de un paciente de Neonatología, fue identificado como SMAR-1 (fig. 1). Por el contrario, otra muestra del mismo paciente y todos los aislados de los otros 8pacientes de Neonatología pertenecieron a un clon diferente pero igual en todos ellos, designado como SMAR-2 (fig. 1). El resto de aislados analizados de los 4 pacientes adultos de otras unidades hospitalarias pertenecieron a un clon diferente, ninguno de ellos relacionado con los anteriores (SMAR-3 a SMAR-8).
Cabe destacar que, a pesar de lo esperado por su coincidencia temporal, el brote acontecido en la sección de Neonatología de nuestro hospital no estuvo relacionado con el uso de la solución contaminada de clorhexidina. El único aislado clínico identificado como clon SMAR-1 correspondía a una muestra de líquido cefalorraquídeo extraída a través de un catéter intraventricular que recibía lavados diarios de clorhexidina, por lo que fue considerado como una posible contaminación.
En conclusión, y a la vista de los resultados obtenidos, este trabajo ilustra la necesidad de llevar a cabo estudios de epidemiología molecular en la filiación de brotes de infección nosocomial.
A la Dra. Olga Delgado del servicio de Farmacia y a los Dres. Xavier Mulet, Enrique Ruiz de Gopegui, Cristina Taboada y Carla López-Causapé, del servicio de Microbiología del Hospital Unversitario Son Espases, por su inestimable colaboración.