El Procedimiento Microbiológico número 61 de la Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica (SEIMC) titulado «Métodos microbiológicos para la monitorización de la limpieza, desinfección y esterilización de dispositivos médicos» se centra en los dispositivos médicos reutilizables calificados de semicríticos o de riesgo medio; aquellos que entran en contacto con las mucosas sin penetrar en tejidos estériles y que precisan de, al menos, una desinfección de alto nivel. En este sentido, nos gustaría mostrar un estudio relativo a la contaminación microbiana de aparatos de nebulización de anfotericina B liposomal en trasplantados pulmonares.
Los nebulizadores son dispositivos para la administración de un fármaco a través de la vía respiratoria mediante aerosoles. En el contexto del trasplante pulmonar, la profilaxis con anfotericina B nebulizada, de administración domiciliaria, es eficazmente utilizada para la prevención de la infección por Aspergillus spp.1. Estos equipos son una fuente potencial de infecciones en caso de contaminación microbiana2. Existen pocos estudios que evalúen la incidencia de contaminación microbiana en nebulizadores y su repercusión clínica3, especialmente en el trasplante pulmonar4. También, falta consenso en la estandarización de los procedimientos de limpieza y desinfección; así como de los controles microbiológicos de estos dispositivos5. El objetivo del estudio es estimar la prevalencia de contaminación microbiana en sistemas de nebulización de anfotericina B utilizados por trasplantados pulmonares, y evaluar su impacto en la microbiología del paciente.
Todos los pacientes al inicio de la profilaxis eran instruidos en una apropiada limpieza y desinfección del nebulizador (lavado con cepillo, agua y jabón e inmersión en solución de hipoclorito sódico al 1%). Tras el trasplante, los pacientes se visitaban cada mes durante el primer año, cada 2 meses el segundo y cada 3-4 meses posteriormente. En estas visitas se les realizaba cultivo de esputo si el paciente expectoraba y, además, ocasionalmente, fibrobroncoscopia.
Durante los años 2012, 2013 y 2014 se muestrearon los equipos de nebulización de una cohorte de trasplantados pulmonares. Se estudiaron 75 cultivos de 71 pacientes; 42 varones, con una edad media de 49 años (rango: 5-64 años), y 29 mujeres, con una edad media de 51 años (22-66 años). Se recogieron muestras de la pipeta, el reservorio y la tubuladura del dispositivo. La mediana del tiempo entre el trasplante y la recogida de la muestra es de 666 días (rango: 68-1.470 días). Adicionalmente, se revisaron los resultados de los cultivos de muestras respiratorias recogidas los 3 meses anteriores y posteriores al muestreo del nebulizador.
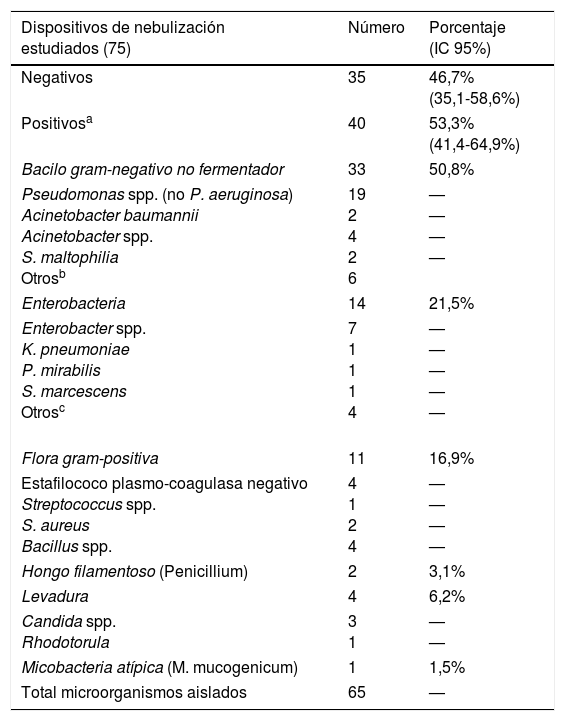
Se detectó contaminación microbiana en el 53,3% de los nebulizadores (tabla 1). La tasa de contaminación fue significativamente mayor en la pipeta y el reservorio (50,7%) en comparación con la tubuladura del dispositivo (11,5%) (p<0,005). No se aisló Pseudomonas aeruginosa en ningún nebulizador.
Microorganismos aislados en los nebulizadores
| Dispositivos de nebulización estudiados (75) | Número | Porcentaje (IC 95%) |
|---|---|---|
| Negativos | 35 | 46,7% (35,1-58,6%) |
| Positivosa | 40 | 53,3% (41,4-64,9%) |
| Bacilo gram-negativo no fermentador | 33 | 50,8% |
| Pseudomonas spp. (no P. aeruginosa) Acinetobacter baumannii Acinetobacter spp. S. maltophilia Otrosb | 19 2 4 2 6 | — — — — |
| Enterobacteria | 14 | 21,5% |
| Enterobacter spp. K. pneumoniae P. mirabilis S. marcescens Otrosc | 7 1 1 1 4 | — — — — — |
| Flora gram-positiva | 11 | 16,9% |
| Estafilococo plasmo-coagulasa negativo Streptococcus spp. S. aureus Bacillus spp. | 4 1 2 4 | — — — — |
| Hongo filamentoso (Penicillium) | 2 | 3,1% |
| Levadura | 4 | 6,2% |
| Candida spp. Rhodotorula | 3 1 | — — |
| Micobacteria atípica (M. mucogenicum) | 1 | 1,5% |
| Total microorganismos aislados | 65 | — |
A pesar de los hallazgos microbianos, solo en uno de los 71 pacientes a estudio (1,4%) existió correspondencia entre el microorganismo aislado en el nebulizador y el aislado en muestras respiratorias. En este caso, Proteus mirabilis se aisló en 2 esputos 14 y 24 días después de su correspondiente hallazgo en el nebulizador.
Existen pocos trabajos similares al que presentamos aquí, donde estimamos la prevalencia de contaminación microbiana en sistemas de nebulización de anfotericina B utilizados por trasplantados pulmonares. En un estudio previo de 20054, la adhesión de los pacientes al protocolo de limpieza y desinfección fue bajo, del 39%. Tras estos hallazgos se intensificó la educación del paciente en relación al cuidado del dispositivo de nebulización.
El Procedimiento Microbiológico mencionado, destaca la magnitud del problema de la infección nosocomial asociada a dispositivos semicríticos y la insuficiente vigilancia a la que están sometidos. También, recomienda encarecidamente la realización de cultivos microbiológicos periódicos como parte del control de calidad del proceso de limpieza y desinfección. No obstante, este documento no revisa los dispositivos de terapia nebulizada, de administración domiciliaria en algunos contextos clínicos como la fibrosis quística o el trasplante pulmonar, que requieren también las mismas consideraciones.
A pesar de las limitaciones de nuestro estudio, creemos que este trabajo evidencia la necesidad de estandarizar unos mecanismos apropiados para la desinfección de los aparatos de nebulización. En esta línea, consideramos también necesario la protocolización de controles microbiológicos exhaustivos en estos dispositivos para evaluar este proceso; especialmente en trasplantados pulmonares y otros pacientes inmunológicamente comprometidos.