La criptococosis es una micosis oportunista que suele afectar a inmunodeprimidos. Aunque es característica del sida, puede aparecer en otras formas de inmunosupresión como terapia con esteroides o trasplante de órgano sólido (TOS). Las formas clínicas más comunes son la neumonía y la meningitis aunque puede afectar a múltiples órganos en el contexto de una infección diseminada. Se describe un caso de criptococosis diseminada (CD) en una paciente con trasplante cardiaco (TC) que representa la primera comunicación en España de esta entidad y se revisan sus principales características clínicas.
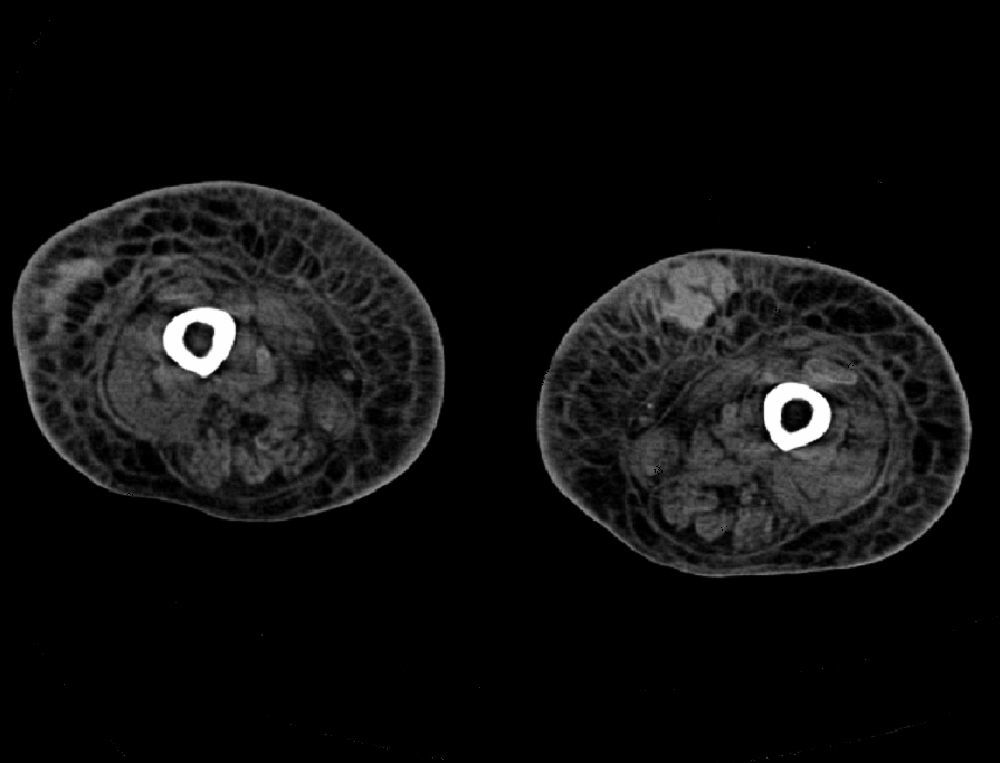
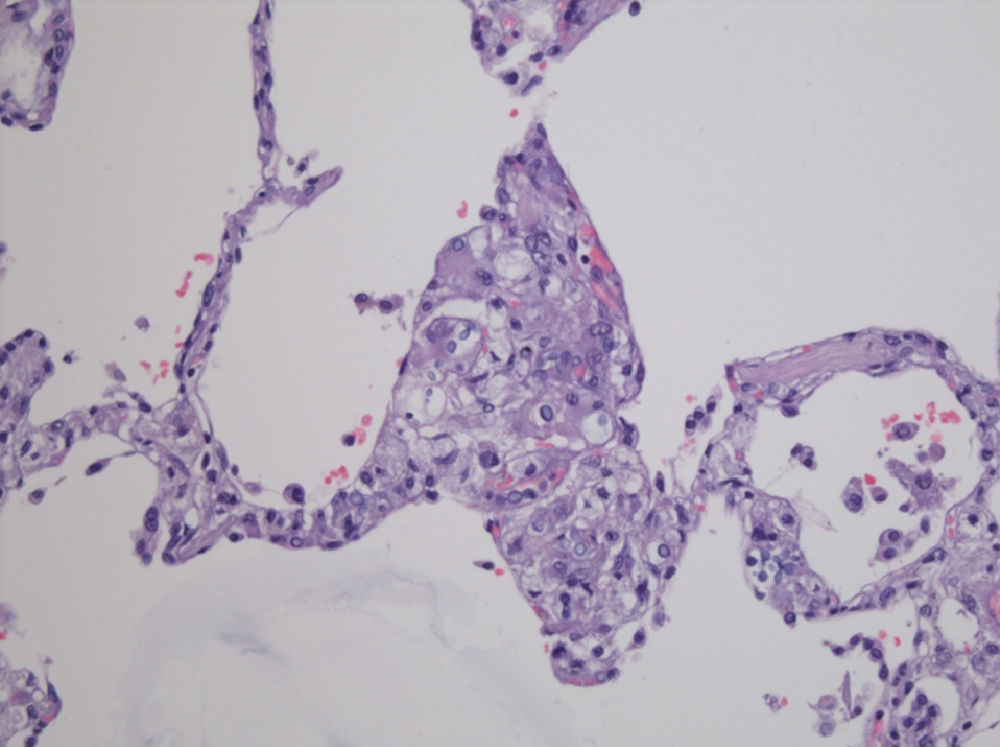
Mujer de 57 años con antecedente de miocardiopatía dilatada idiopática que ingresa en UCI tras la realización de TC, recibiendo inmunosupresión con metilprednisolona y tacrolimus. En la segunda semana postrasplante presentó fracaso renal e insuficiencia cardiaca secundaria a taponamiento de causa no filiada (líquido pericárdico con cultivo negativo y biopsia endomiocárdica sin signos de rechazo), que precisó ventana pericárdica y que mejoró con tratamiento sintomático. Posteriormente presentó neumonía por Klebsiella pneumoniae y Pseudomonas aeruginosa y bacteriemia asociada a catéter por S. epidermidis, que prolongaron su estancia en UCI con ventilación mecánica y terapia renal sustitutiva. En la séptima semana presentó de forma brusca hipotermia (34°C), hipotensión y desaturación que precisaron drogas vasoactivas y aumento de soporte respiratorio (FiO2 80%). En la analítica destacaba leucocitosis con neutrofilia (leucocitos 15,2 × 109/l, neutrófilos 82%), anemia (hemoglobina 7,4g/dl), trombopenia (plaquetas 38 × 109/l) y acidosis láctica (ácido láctico 11mmol/l). En los días siguientes aparecieron lesiones nodulares hemorrágicas en miembros inferiores con posterior extensión a tronco y miembros superiores. En las técnicas de imagen se observaron los siguientes hallazgos: radiografía de tórax con infiltrados alveolares basales y derrame pleural, tomografía computarizada de miembros inferiores con múltiples hematomas subcutáneos (fig. 1) y ecocardiograma transtorácico con reaparición de derrame pericárdico. Se tomaron cultivos de sangre, aspirado traqueal, líquido pericárdico y lesiones cutáneas y se pautó terapia empírica con piperacilina/tazobactam y linezolid. En cultivos de sangre y líquido pericárdico se aisló 5 días más tarde Cryptococcus neoformans var. grubii por lo que se pautó tratamiento con anfotericina B liposomal (5mg/kg/día); el cultivo del aspirado traqueal fue negativo. La evolución clínica fue desfavorable con persistencia de shock refractario y fracaso multiorgánico, falleciendo 10 días después. En la necropsia se documentó la presencia de criptococosis diseminada angioinvasiva que afectaba a pulmón (fig. 2), vasos periganglionares de hilio pulmonar y tejido celular subcutáneo de miembros inferiores; no se autorizó el estudio de tejido cerebral o meníngeo.
Aunque la criptococosis se ha asociado clásicamente al sida es también una complicación habitual de otras situaciones de inmunodepresión. Si se excluyen los casos asociados al sida, entre el 20% y el 60% de las criptococosis aparecen en pacientes con TOS, siendo la tercera causa de micosis invasiva en estos pacientes tras candidiasis y aspergilosis1. Su incidencia global en el TOS oscila entre 0,3 y 5%2, que varía según el órgano trasplantado: 1-7% en hepático, 0,8-2% en pulmonar, 0,4-19% en renal, y 2,5-3,5% en TC3,4. Aunque los factores de riesgo en el TC son poco conocidos, parece ser más frecuente en pacientes con insuficiencia renal como en el caso presentado, así como en diabéticos o infectados por VHB5. La criptococosis es una complicación tardía del TOS que suele aparecer en el segundo año postrasplante1,2. Respecto al TC los datos varían según las publicaciones. Aunque puede aparecer como en nuestra paciente entre el segundo y el sexto mes6, su presentación suele ser más tardía tras un tiempo mediano y medio de 25 y 32 meses, respectivamente3,7. De forma ocasional, la criptococosis asociada a TOS puede presentarse de forma incluso más precoz en el primer mes postrasplante, cuando la inmunosupresión es más intensa, y se ha sugerido que en estos casos la criptococosis puede ser secundaria a reactivación de una infección latente del receptor o a su adquisición a través del órgano trasplantado8. En el caso presentado no existía evidencia clínica ni microbiológica de ninguna de estas dos situaciones. Las formas clínicas más frecuentes son la pulmonar y la meníngea, pero se han descrito otras (renal, osteoarticular o cutánea) así como formas diseminadas, definidas por la presencia de funguemia, afectación de sistema nervioso central o de dos órganos no contiguos9. Nuestra enferma presentaba una CD que cursó con afectación cutánea, pulmonar y funguemia, pero no se pudo realizar punción lumbar para descartar meningitis a causa de la trombopenia. El aislamiento de criptococo en líquido pericárdico se interpretó como secundario a funguemia pues en la necropsia no había evidencia de afectación cardiaca. La detección de antígeno criptocócico en suero es una técnica útil para el diagnóstico de la criptococosis, cuya sensibilidad en el TOS oscila entre 33-100% en la neumonía3,9 y 8-91% en la meningitis1,3.
No existen estudios específicos sobre el tratamiento de la CD en pacientes con TOS por lo que suele emplearse la misma terapia que en otros inmunodeprimidos. El tratamiento de las formas graves de criptococosis en el TOS, como la CD o meníngea, se basa en la combinación de anfotericina B en formulación lipídica (AnBL) y flucitosina durante dos semanas (periodo de inducción), seguida de terapia de mantenimiento con fluconazol durante 12 meses. Si no se emplea flucitosina, se debe prolongar la inducción con AnBL durante 4-6 semanas aunque esta pauta presenta mayor riesgo de fracaso10. En nuestra paciente no se utilizó flucitosina debido a la presencia de trombopenia grave.
El pronóstico de la criptococosis depende de su forma clínica y el grado de inmunodepresión, siendo su mortalidad elevada en pacientes con TOS (15-42%), especialmente en el TC (60%) o cuando existe afectación meníngea (50%)7,9. Es importante destacar que la insuficiencia renal se ha revelado como el único factor de riesgo independiente de mortalidad de esta infección en el TOS7. A pesar de terapia con AnBL, nuestra paciente falleció debido a la extrema gravedad de la infección (diseminada y complicada con insuficiencia renal) y a la grave inmunodepresión subyacente.
En conclusión, se debe considerar a la criptococosis en el diagnóstico diferencial de las infecciones sistémicas de pacientes con TOS, especialmente si existe afectación cutánea. La combinación de AnBL y flucitosina es el tratamiento de elección pero su pronóstico es habitualmente desfavorable, sobre todo cuando existe enfermedad diseminada e insuficiencia renal asociada.