La infección primaria aguda por el virus de la hepatitis C (VHC) es muy frecuentemente asintomática y pocas veces origina demanda de diagnóstico etiológico. En una revisión publicada recientemente en esta revista1, los autores afirman que no existe ningún marcador serológico específico que sea útil para su diagnóstico, lo que dificulta obtener datos sobre la incidencia real de la hepatitis C aguda.
En 1997, nuestro grupo comunicó en esta misma revista algunos resultados que demostraban la utilidad de la estimación de la avidez de la IgG específica en el diagnóstico de la infección primaria aguda por el VHC2. Previamente se había demostrado dicha utilidad durante el estudio de un brote de hepatitis C en receptores habituales de inmunoglobulina humana endovenosa, en el que cinco de los 21 pacientes inmunodeficientes afectados que lograron responder con anticuerpos sólo pudieron ser diagnosticados correctamente mediante este marcador3.
Entre los años 1998 y 2009 se estudiaron en nuestro laboratorio muestras de suero de pacientes involucrados en nueve brotes nosocomiales de infección por VHC, enviadas desde nueve centros sanitarios diferentes de las provincias de Alicante, Barcelona, Ciudad Real, Granada y Madrid. Cuatro de ellos afectaron a pacientes hemodializados, dos a pacientes quirúrgicos y uno a pacientes hematológicos, faltando datos al respecto en los dos restantes. Siete brotes respondieron a la transmisión de cepas de VHC del genotipo 1b, uno de ellos mixto con una cepa del genotipo 4c/4d. Los dos restantes fueron causados por cepas de los genotipos 3a y 4d. Sólo se han publicado hasta la fecha resultados de uno de ellos4.
Las investigaciones de laboratorio realizadas involucraron un total de 152 pacientes. En 107 de ellos se llegó a detectar la presencia del genoma viral en suero (tabla 1). Pudo documentarse seroconversión para anti-VHC en 25 casos. En los 82 restantes (77%), la primera muestra disponible para estudio era ya positiva para ARN viral y para anti-VHC, un resultado que no permitía discriminar entre infección aguda reciente e infección crónica y que dificultaba la identificación de los pacientes realmente afectados por el brote.
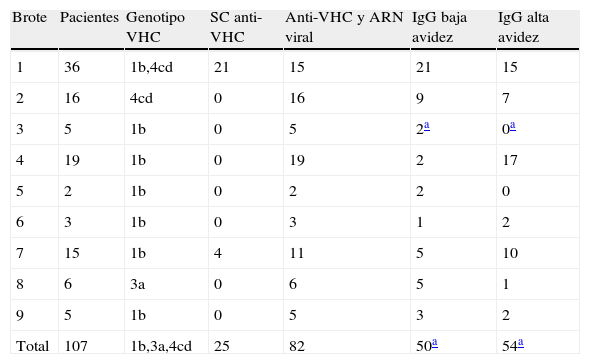
Resultados obtenidos mediante la prueba de avidez de la IgG específica en las muestras de 107 pacientes positivos para ARN viral e involucrados en nueve brotes nosocomiales de infección por el VHC estudiados entre los años 1998 y 2009
Se pudieron realizar pruebas de evaluación de la avidez de la IgG específica en los 25 casos con seroconversión y en 79 de los 82 pacientes restantes. Se obtuvieron resultados indicativos de presencia de anticuerpos IgG anti-VHC de baja avidez en todos los primeros y en 25 de los segundos (32%). En los 54 restantes, los resultados indicaron la presencia de anticuerpos de alta avidez. En conjunto, los ensayos de avidez de IgG identificaron, por tanto, 50 pacientes con infección primaria aguda reciente que se consideraron como afectados, duplicando el rendimiento de los estudios de laboratorio respecto de la detección de seroconversión. Los 54 restantes se juzgaron infectados con anterioridad y se investigaron como posibles fuentes para los brotes en los que se hallaban involucrados.
Los ensayos de evaluación de la avidez de la IgG específica ayudan, por consiguiente, a identificar la infección primaria aguda por VHC cuando la toma de la muestra más temprana se ha realizado después de la aparición de los anticuerpos específicos en el suero del paciente, y son útiles para diferenciar entre afectados y fuentes potenciales de virus durante la investigación de los brotes epidémicos. La utilidad de este marcador serológico específico para el diagnóstico de la hepatitis C aguda ha sido, por lo demás, documentada también por otros grupos5–7.