El tratamiento de la hepatitis C se basa en la combinación de peginterferón (PEG-INF) alfa (2a o 2b) más ribavirina, sin establecerse qué peginterferón es más eficaz. El objetivo principal de este trabajo es comparar la efectividad del tratamiento de la hepatitis C en función del tipo de peginterferón.
Material y métodosEstudio de cohortes, prospectivo, de noviembre 2002 a mayo 2004 con seguimiento de hasta 12 meses tras finalizar el tratamiento a todos los pacientes. Se incluyeron pacientes naïve monoinfectados. Grupo A: peginterferón alfa-2a más ribavirina; grupo B: peginterferón alfa-2b más ribavirina. Variables principales: Respuesta bioquímica, respuesta viral sostenida y efectividad del tratamiento (respuesta bioquímica y virológica).
ResultadosSe incluyeron 202 pacientes (grupo A: 87; grupo B: 115), sin diferencias significativas en las características basales de ambos grupos de pacientes. Respuesta viral sostenida: el 71,3 frente al 64,3% (p = 0,293); respuesta bioquímica sostenida: el 75,2 frente al 75,7% (p = 0,934); efectividad: el 64,2 frente al 60,87% (p = 0,628).
ConclusiónNo hay diferencias en la obtención de respuesta viral sostenida, bioquímica sostenida y efectividad del tratamiento entre ambos grupos de pacientes, por lo que se pueden considerar ambos peginterferones igual de efectivos para el tratamiento de la hepatitis C en pacientes monoinfectados.
Treatment of hepatitis C is based on the combination of peginterferon alfa-2a or -2b plus ribavirin; the more effective peginterferon for this purpose has not been established. The aim of this study is to compare the effectiveness of hepatitis C treatment according to the type of peginterferon used.
MethodsA prospective cohort study was performed from November 2002 to May 2004, with up to 12 months of follow-up in all patients after completion of treatment. The study included naïve monoinfected patients, divided into two groups: Group A: peginterferon alfa-2a plus ribavirin and Group B: peginterferon alfa-2b plus ribavirin. The main variables studied were plasma glutamate pyruvate transferase levels (biochemical response), viral load (virologic response), and treatment effectiveness (biochemical and virologic response).
ResultsA total of 202 patients were studied (Group A: 87; Group B: 115), there were no significant differences in baseline characteristics between the two groups. Sustained biochemical response: 75.8% vs. 76.2% (P = .908); Sustained virological response: 71.3% vs. 64.3% (P = .293); Effectiveness of treatment: 64.2% vs. 60.87% (P = .628).
ConclusionNo differences in the sustained virological or biochemical response were found between groups receiving peginterferon alfa-2a or peginterferon alfa-2b plus ribavirin, suggesting that the two types of peginterferon alfa are similarly effective for treating hepatitis C in monoinfected patients.
La hepatitis C es una enfermedad de etiología vírica que supone un importante problema de salud pública. Según la Organización Mundial de la Salud (OMS) existen más de 170 millones de portadores del virus de la hepatitis C (VHC) en todo el mundo, con más de 5 millones de infectados en Europa1.
El objetivo final del tratamiento de la infección por el VHC es evitar el desarrollo a largo plazo de complicaciones como cirrosis y/o hepatocarcinoma celular. La efectividad del tratamiento ha aumentado en estos últimos años gracias a la introducción de nuevos fármacos. La monoterapia con interferón alfa obtenía respuestas al tratamiento bajas2, y fue con la introducción de la ribavirina cuando se produjo un aumento importante de la efectividad del tratamiento3,4. La pegilación del interferón alfa permite obtener concentraciones plasmáticas más elevadas y durante más tiempo con una sola administración a la semana, consiguiendo una supresión de la replicación viral constante y aumentando la probabilidad de obtener una respuesta al tratamiento. Tanto el peginterferón alfa-2a como el 2b han demostrado tener mayor efectividad y mejor perfil de seguridad que sus respectivos interferones convencionales5,6, y la terapia combinada con ribavirina es el tratamiento de elección para la hepatitis C en pacientes naïve y en pacientes que no han respondido a la terapia con interferón convencional7-9. Sin embargo, aún no se ha podido establecer qué peginterferón alfa es más eficaz y/o seguro.
El objetivo principal de este trabajo es comparar, en la práctica clínica habitual, la efectividad del tratamiento de la hepatitis C en función del tipo de peginterferón que reciben los pacientes.
El objetivo secundario es identificar factores predictores para la obtención de respuesta viral sostenida y efectividad del tratamiento antiviral.
MétodosSe realizó un estudio de cohortes (observacional, analítico, longitudinal y prospectivo), de 42 meses de duración (de noviembre de 2002 a abril de 2006) con recogida prospectiva y consecutiva de datos. El período de inclusión de pacientes fue de noviembre de 2002 a abril de 2004. Se realizó un seguimiento de 12 meses a todos los pacientes incluidos en el estudio tras finalizar el tratamiento.
Criterios de inclusiónSe incluyeron en el estudio todos los pacientes monoinfectados por el VHC, con confirmación del diagnóstico por reacción en cadena de la polimerasa (PCR) a tiempo real (Amplicor® HCV Test v2.0, límite de sensibilidad de 50 UI/ml), que aceptaron participar en el estudio, no tratados anteriormente (pacientes naïve) y que iniciaban tratamiento con peginterferón alfa (2a o 2b) más ribavirina.
Criterios de exclusiónSe excluyeron del estudio los pacientes menores de 18 años, infectados por el virus de la inmunodeficiencia humana (VIH), con infección activa por el virus de la hepatitis B, con alteraciones psiquiátricas, signos o síntomas de hepatocarcinoma celular o cirrosis descompensada, consumo activo de drogas o alcohol, recuento de plaquetas inferior a 90.000 células/μl, recuento de neutrófilos inferior a 1.500 células/μl, hemoglobina inferior a 12 g/dl en mujeres e inferior a 13 g/dl en hombres.
MetodologíaLos pacientes se dividieron en dos grupos en función del peginterferón que se les prescribió, sin realizarse ninguna actuación sobre la prescripción de los fármacos y dejando libertad al médico para que prescribiera un peginterferón u otro según su experiencia o preferencia personal, de forma que no se modificara la práctica clínica habitual. En el grupo A se incluyeron los pacientes tratados con peginterferón alfa-2a más ribavirina, y en el grupo B se incluyeron los pacientes con peginterferón alfa-2b más ribavirina. Se han incluido pacientes de diversos servicios clínicos y de varios médicos para reducir al máximo un posible sesgo en la selección de pacientes.
La recogida de la información se realizó en el momento de la dispensación de los medicamentos desde la Unidad de Atención Farmacéutica a Pacientes Externos (UFPE) del Servicio de Farmacia, durante la entrevista del farmacéutico especialista con el paciente (con una periodicidad de 2 meses). Esta información se completó de forma indirecta a través de los datos obtenidos durante las visitas médicas y presentes en la historia clínica.
Las variables que considerar en cada grupo de pacientes fueron:
- –
Datos del paciente: sexo, edad, índice de masa corporal.
- –
Estado de la enfermedad: grado de fibrosis hepática (escala METAVIR10), bilirrubina total, glutamato-piruvato transaminasa (GPT), genotipo (test Inno LiPA® HCV II) y carga viral al inicio del tratamiento (determinada con el Amplicor® HCV Monitor v2.0 con límite de sensibilidad de 600 UI/ml) clasificando a los pacientes como con baja carga viral cuando ésta estaba por debajo de 800.000 UI/ml11.
- –
Tratamiento: tipo y dosis de peginterferón alfa, dosis de ribavirina, siguiendo las indicaciones de las fichas técnicas de los productos12,13.
- –
Modificaciones del tratamiento, siguiendo las indicaciones de la ficha técnica de los productos.
- –
Respuesta viral: carga viral plasmática durante el tratamiento (1, 3, 6 meses), y a los 6 meses de finalizar el tratamiento (respuesta viral sostenida).
- –
Respuesta bioquímica: valores de GPT durante el tratamiento (1, 3, 6 meses) y a los 6 meses de finalizar el tratamiento (respuesta bioquímica sostenida).
- –
Finalización del tratamiento, pudiendo completarse el mismo o interrumpirse por reacciones adversas a medicamentos (gradación de la gravedad según CTCEA v3.014) o por fracaso terapéutico.
- –
Grado de permanencia en el tratamiento: relación porcentual entre el tiempo en semanas teórico y el tiempo real de tratamiento.
- –
Adherencia a las dosis teóricas de cada fármaco: relación porcentual entre la dosis total teórica que debería recibir el paciente durante el tratamiento y la dosis total real recibida.
Para los pacientes infectados con genotipo 1 y 4 se realizó una prueba de predictibilidad de la respuesta, de forma que si a los tres meses de tratamiento la carga viral del VHC era negativa o había disminuido dos logaritmos con respecto al valor basal se consideró la obtención de respuesta viral temprana (RVT). En caso contrario, se finalizó el tratamiento debido a la baja probabilidad de alcanzar la respuesta viral sostenida, considerándose fallo de tratamiento12,15.
La respuesta viral sostenida (RVS)16 suele ser la principal variable para definir la efectividad del tratamiento, ya que se suele asociar a una respuesta bioquímica e histológica. Sin embargo, esto no siempre sucede, pues hay pacientes que a pesar de tener una RVS continúan con valores elevados de GPT que evidencian que la inflamación hepática persiste y, con ello, el riesgo de complicaciones a largo plazo. Según este dato, en este trabajo se ha definido la efectividad como "la obtención de una RVS junto con una normalización de los valores de GPT a los seis meses de haber finalizado el tratamiento (respuesta bioquímica sostenida)", siendo la situación de máximo beneficio para el paciente.
Análisis estadísticoEl análisis de los datos se realizó con la intención de instaurar un tratamiento. Las variables cuantitativas se estudiaron en función de las medidas de distribución y dispersión (media, desviación estándar, mediana, moda, máximo y mínimo), y las cualitativas mediante su frecuencia absoluta y relativa. Las variables cuantitativas y cualitativas se compararon aplicando una prueba de homogeneidad utilizando el estadístico z de contraste. En todos los casos, los intervalos de confianza calculados fueron del 95% (IC 95%), y para variables cualitativas con celdas n < 5 se aplicó una prueba exacta por métodos condicionados (Fisher). Finalmente, se realizó una regresión logística para identificar factores independientes predictores de RVS y efectividad del tratamiento, considerando la RVS y efectividad del tratamiento como variable dependiente. En el análisis multivariante se incluyeron las variables que mostraron ser significativas en la obtención de RVS o efectividad en un análisis univariante previo. Para conocer la evolución de la negativización de la carga viral plasmática en ambos grupos de pacientes se utilizó el método de Kaplan-Meier, comparándose ambos grupos con el test log-Rank. En todos los casos se estableció un nivel de significación alfa de 0,05 bilateral.
ResultadosDurante la primera fase del estudio un total de 462 pacientes iniciaron el tratamiento de la hepatitis C, de los que sólo 202 cumplieron los criterios de inclusión. La coinfección con el VIH fue la principal causa de exclusión de los pacientes.
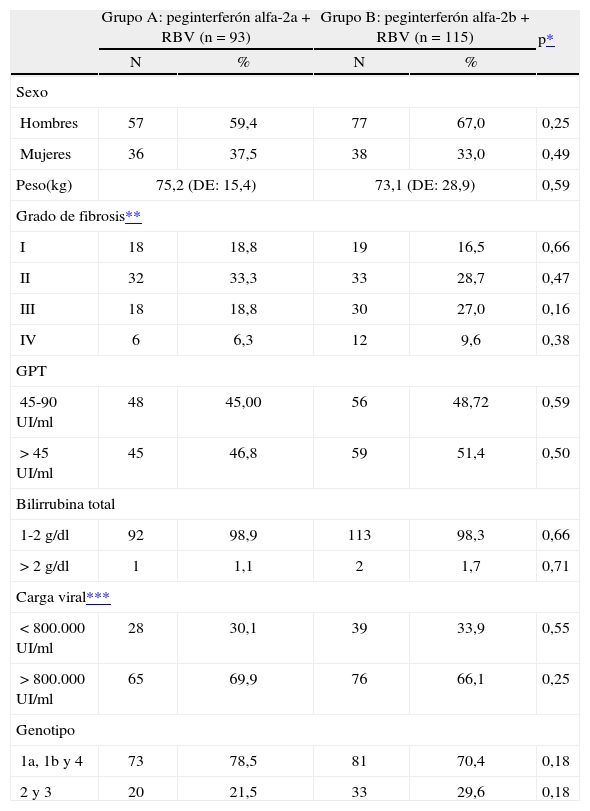
Las características basales de los pacientes incluidos en el estudio se muestra en la tabla 1; no se encuentran diferencias significativas entre ambos grupos de pacientes. Hay que destacar que cerca del 65% del total de los pacientes estaban infectados por el genotipo 1 (20% genotipo 1a y 45% genotipo 1b). En el grupo tratado con peginterferón alfa-2a, 83 pacientes iniciaron el tratamiento con dosis de 180 μg a la semana, y 4 con dosis de 135 μg/semana debido a su bajo peso (< 50 kg). En el grupo tratado con peginterferón alfa-2b todos los pacientes iniciaron con dosis de 1,5 μg/kg/semana.
Características basales de la población incluida en el estudio
| Grupo A: peginterferón alfa-2a + RBV (n = 93) | Grupo B: peginterferón alfa-2b + RBV (n = 115) | p* | |||
| N | % | N | % | ||
| Sexo | |||||
| Hombres | 57 | 59,4 | 77 | 67,0 | 0,25 |
| Mujeres | 36 | 37,5 | 38 | 33,0 | 0,49 |
| Peso(kg) | 75,2 (DE: 15,4) | 73,1 (DE: 28,9) | 0,59 | ||
| Grado de fibrosis** | |||||
| I | 18 | 18,8 | 19 | 16,5 | 0,66 |
| II | 32 | 33,3 | 33 | 28,7 | 0,47 |
| III | 18 | 18,8 | 30 | 27,0 | 0,16 |
| IV | 6 | 6,3 | 12 | 9,6 | 0,38 |
| GPT | |||||
| 45-90 UI/ml | 48 | 45,00 | 56 | 48,72 | 0,59 |
| > 45 UI/ml | 45 | 46,8 | 59 | 51,4 | 0,50 |
| Bilirrubina total | |||||
| 1-2 g/dl | 92 | 98,9 | 113 | 98,3 | 0,66 |
| > 2 g/dl | 1 | 1,1 | 2 | 1,7 | 0,71 |
| Carga viral*** | |||||
| < 800.000 UI/ml | 28 | 30,1 | 39 | 33,9 | 0,55 |
| > 800.000 UI/ml | 65 | 69,9 | 76 | 66,1 | 0,25 |
| Genotipo | |||||
| 1a, 1b y 4 | 73 | 78,5 | 81 | 70,4 | 0,18 |
| 2 y 3 | 20 | 21,5 | 33 | 29,6 | 0,18 |
DE: desviación estándar; GPT: glutamato-piruvato transaminasa;
RBV: ribavirina.
El 76% de los pacientes completaron el tratamiento (el 80,65% del grupo A frente al 72,17% del grupo B; p > 0,05), con el 12% de los pacientes que lo interrumpieron por reacciones adversas y otro 12% que también lo interrumpieron por fallo de tratamiento al no conseguir la erradicación viral. Estas situaciones se produjeron con mayor frecuencia en el grupo de pacientes tratados con peginterferón alfa-2b (p > 0,05).
Las principales reacciones adversas identificadas fueron la aparición de anemia (grado I-II), neutropenia (grado III-IV), fiebre (grado I-II) y fatiga, sin encontrarse diferencias significativas entre ambos grupos de pacientes. El nadir de neutrófilos se alcanzó en ambos grupos de pacientes al tercer mes de tratamiento, y el valor mínimo de hemoglobina, entre el tercer y el sexto mes de tratamiento. Estas situaciones coinciden en el tiempo con el momento en el que se produce la mayor parte de las reducciones de dosis de peginterferón alfa y de ribavirina.
En el grupo tratado con peginterferón alfa-2a, el 18,27% de los pacientes tuvo un grado de permanencia en el tratamiento inferior al 80% del establecido inicialmente, frente al 9,50% de los pacientes tratados con peginterferón alfa-2b (p = 0,0651).
La adherencia a las dosis de ribavirina fue alta, de forma que en ambos grupos de pacientes sólo el 5,30% recibió una dosis total de ribavirina inferior al 80% de la teórica. En cuanto a la adherencia a las dosis acumuladas de peginterferón alfa, el 13,97% de los pacientes tratados con peginterferón alfa-2a recibió dosis inferiores al 80% de las teóricas, frente al 11,30% de los pacientes tratados con peginterferón alfa-2b (p = 0,524).
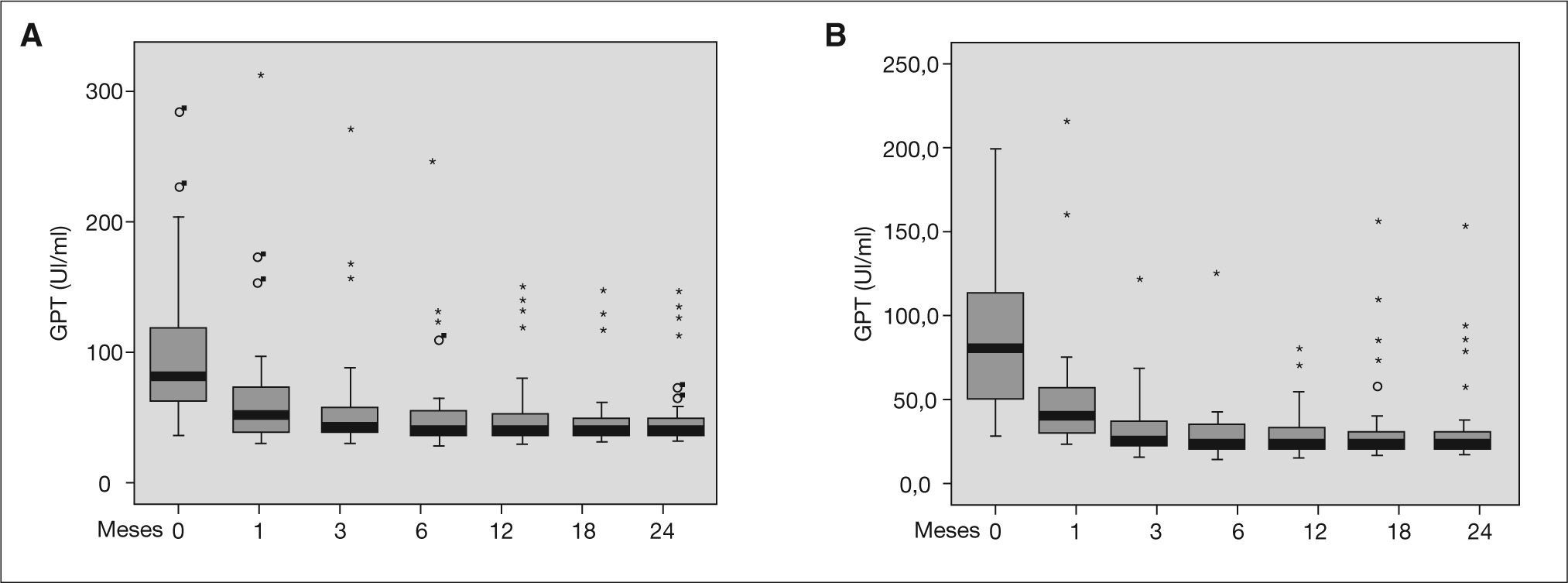
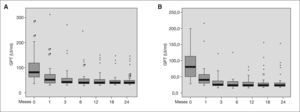
La normalización de los valores de GPT a los 6 meses de haber finalizado el tratamiento (respuesta bioquímica sostenida) fue mayor en el grupo tratado con peginterferón alfa-2b, con el 76,5% (IC 95%: 68,8-84,2%) frente al 75,8% (IC 95%: 66,9-84,7%) del grupo tratado con peginterferón alfa-2a, aunque sin encontrarse diferencias significativas (p = 0,908). En la figura 1 se muestran los valores de GPT durante el tratamiento y seguimiento en ambos grupos de pacientes, observándose en ambos grupos una disminución importante en los valores de GPT ya en el primer mes de tratamiento.
Diagrama de cajas en el que se muestra la evolución de los valores medios de glutamato-piruvato transaminasa (GPT) durante el tratamiento de la hepatitis C y su seguimiento (hasta 12 meses tras fin de tratamiento). A) Valores de GPT en pacientes tratados con peginterferón alfa-2a más ribavirina, B) Valores de GPT en pacientes tratados con peginterferón alfa-2b más ribavirina.
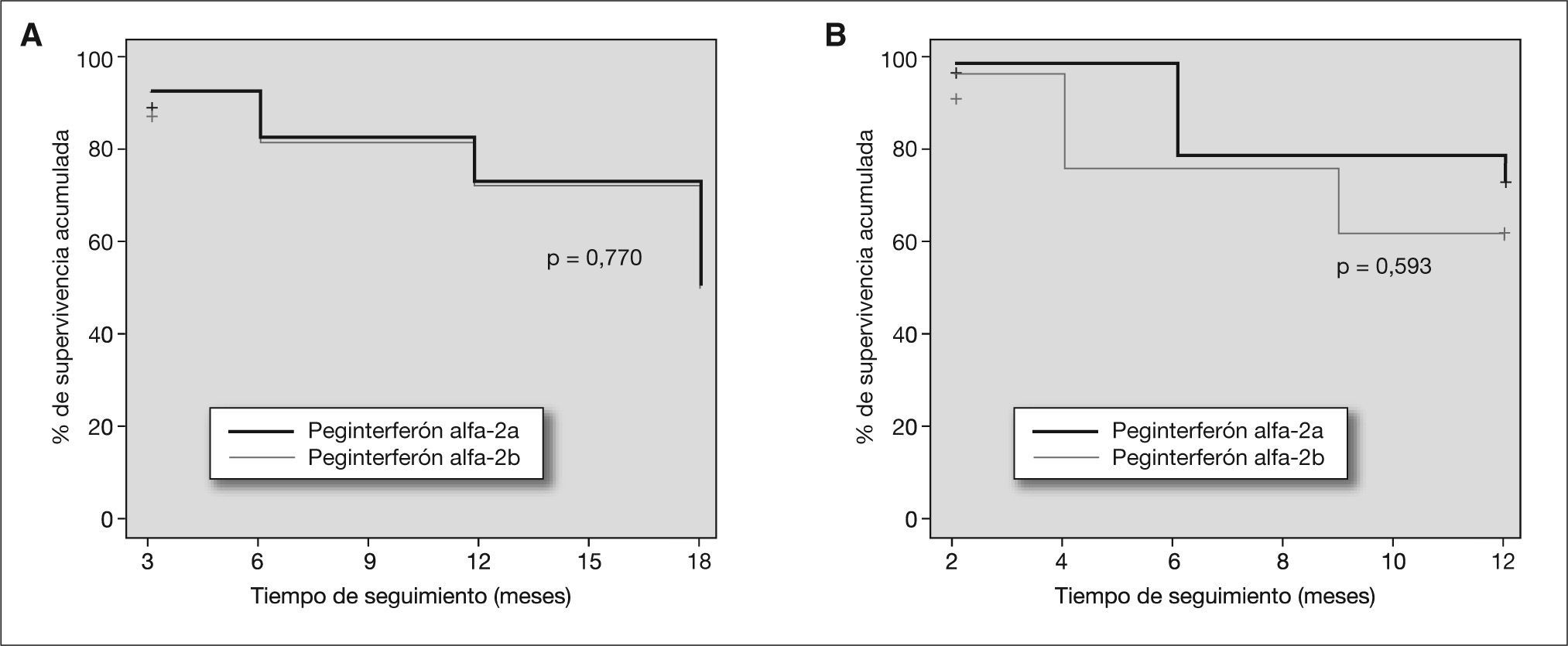
Con respecto a la erradicación viral (respuesta virológica), el 71,3% (IC 95%: 61,8-80,8%) de los pacientes tratados con peginterferón alfa-2a consiguió una RVS frente al 64,3% (IC 95%: 55,7-72,9%) de los pacientes tratados con peginterferón alfa-2b más ribavirina (p = 0,284). De los pacientes que erradicaron el virus, el 3,2% del grupo tratado con peginterferón alfa-2a y el 8,1% en el grupo tratado con peginterferón alfa-2b tenían una carga viral plasmática alta antes de iniciar el tratamiento (p = 0,229). De los pacientes infectados con los genotipos 1-4, el 76,6% del grupo tratado con peginterferón alfa-2a y el 71,8% del grupo tratado con peginterferón alfa-2b (p = 0,522) que obtuvieron una respuesta viral sostenida habían conseguido ya la erradicación del virus a los 3 meses de iniciar el tratamiento, obteniendo, por tanto, una respuesta virológica temprana. En la curva de supervivencia de negativización de la carga viral plasmática (fig. 2), se observa que no hay diferencias significativas en cuanto a erradicación viral a lo largo del tratamiento y seguimiento de los pacientes entre ambos tipos de peginterferón alfa, independientemente del genotipo viral que produce la infección.
Curvas de supervivencia de negativización de la carga viral plasmática para ambos tipos de peginterferón alfa en función del genotipo viral (genotipo 1-4 [A]; genotipo 2-3 [B]) que produce la infección (sobrevivir = no negativización de carga viral plasmática; se utilizó el test log-Rank para encontrar diferencias significativas entre ambos tratamientos).
Considerando la definición de efectividad realizada anteriormente, el tratamiento con peginterferón alfa-2a fue efectivo en el 64,2% de los pacientes, y en el grupo tratado con peginterferón alfa-2b lo fue en el 60,87% de los pacientes, sin encontrarse diferencias significativas o clínicas entre ambos tratamientos (p = 0,338).
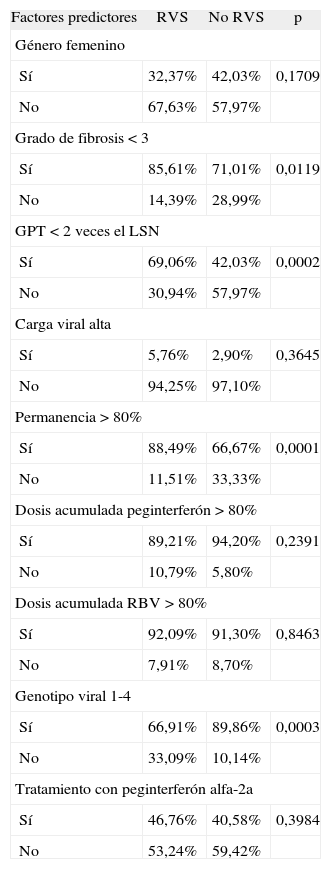
En las tablas 2 y 3 se muestran los resultados del análisis univariante realizado para evaluar la obtención de RVS y para la efectividad del tratamiento, respectivamente. Las variables seleccionadas para el análisis univariante son aquéllas potencialmente implicadas en la respuesta al tratamiento en los ensayos clínicos realizados. En las tablas 4 y 5 se muestran los resultados del análisis multivariante realizado sobre las variables que mostraron diferencias significativas en el análisis univariante: grado de fibrosis < 3, GPT < 2 veces el límite superior de normalidad, grado de permanencia en el tratamiento > 80%, adherencia a las dosis de ribavirina > 80%, genotipo viral 1-4. Tras el estudio del factor de incremento de varianza se decidió eliminar la variable grado de fibrosis < 3, ya que se encontró posible colinealidad con la variable GPT < 2 veces el límite superior de normalidad.
Resultados del análisis univariante para respuesta viral sostenida
| Factores predictores | RVS | No RVS | p |
| Género femenino | |||
| Sí | 32,37% | 42,03% | 0,1709 |
| No | 67,63% | 57,97% | |
| Grado de fibrosis < 3 | |||
| Sí | 85,61% | 71,01% | 0,0119 |
| No | 14,39% | 28,99% | |
| GPT < 2 veces el LSN | |||
| Sí | 69,06% | 42,03% | 0,0002 |
| No | 30,94% | 57,97% | |
| Carga viral alta | |||
| Sí | 5,76% | 2,90% | 0,3645 |
| No | 94,25% | 97,10% | |
| Permanencia > 80% | |||
| Sí | 88,49% | 66,67% | 0,0001 |
| No | 11,51% | 33,33% | |
| Dosis acumulada peginterferón > 80% | |||
| Sí | 89,21% | 94,20% | 0,2391 |
| No | 10,79% | 5,80% | |
| Dosis acumulada RBV > 80% | |||
| Sí | 92,09% | 91,30% | 0,8463 |
| No | 7,91% | 8,70% | |
| Genotipo viral 1-4 | |||
| Sí | 66,91% | 89,86% | 0,0003 |
| No | 33,09% | 10,14% | |
| Tratamiento con peginterferón alfa-2a | |||
| Sí | 46,76% | 40,58% | 0,3984 |
| No | 53,24% | 59,42% | |
GPT: glutamato-piruvato transaminasa; LSN: límite superior de normalidad; RBV: ribavirina; RVS: respuesta viral sostenida.
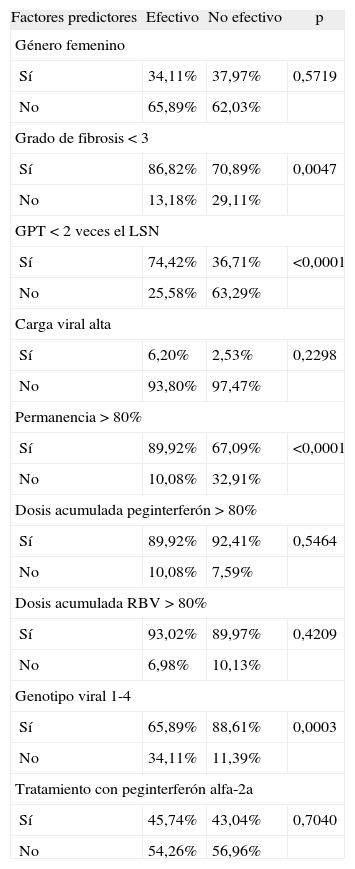
Resultados del análisis univariante para efectividad del tratamiento
| Factores predictores | Efectivo | No efectivo | p |
| Género femenino | |||
| Sí | 34,11% | 37,97% | 0,5719 |
| No | 65,89% | 62,03% | |
| Grado de fibrosis < 3 | |||
| Sí | 86,82% | 70,89% | 0,0047 |
| No | 13,18% | 29,11% | |
| GPT < 2 veces el LSN | |||
| Sí | 74,42% | 36,71% | <0,0001 |
| No | 25,58% | 63,29% | |
| Carga viral alta | |||
| Sí | 6,20% | 2,53% | 0,2298 |
| No | 93,80% | 97,47% | |
| Permanencia > 80% | |||
| Sí | 89,92% | 67,09% | <0,0001 |
| No | 10,08% | 32,91% | |
| Dosis acumulada peginterferón > 80% | |||
| Sí | 89,92% | 92,41% | 0,5464 |
| No | 10,08% | 7,59% | |
| Dosis acumulada RBV > 80% | |||
| Sí | 93,02% | 89,97% | 0,4209 |
| No | 6,98% | 10,13% | |
| Genotipo viral 1-4 | |||
| Sí | 65,89% | 88,61% | 0,0003 |
| No | 34,11% | 11,39% | |
| Tratamiento con peginterferón alfa-2a | |||
| Sí | 45,74% | 43,04% | 0,7040 |
| No | 54,26% | 56,96% | |
GPT: glutamato-piruvato transaminasa; LSN: límite superior de normalidad; RBV: ribavirina.
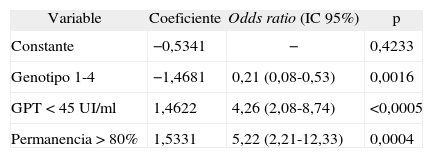
Resultados de la regresión logística para respuesta viral sostenida
| Variable | Coeficiente | Odds ratio (IC 95%) | p |
| Constante | −0,5341 | − | 0,4233 |
| Genotipo 1-4 | −1,4681 | 0,21 (0,08-0,53) | 0,0016 |
| GPT < 45 UI/ml | 1,4622 | 4,26 (2,08-8,74) | <0,0005 |
| Permanencia > 80% | 1,5331 | 5,22 (2,21-12,33) | 0,0004 |
GPT: glutamato-piruvato transaminasa; IC: intervalo de confianza.
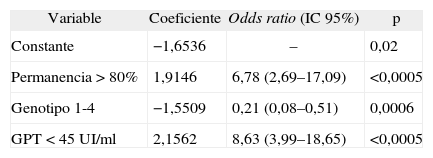
Resultados de la regresión logística para efectividad de la respuesta
| Variable | Coeficiente | Odds ratio (IC 95%) | p |
| Constante | −1,6536 | – | 0,02 |
| Permanencia > 80% | 1,9146 | 6,78 (2,69–17,09) | <0,0005 |
| Genotipo 1-4 | −1,5509 | 0,21 (0,08–0,51) | 0,0006 |
| GPT < 45 UI/ml | 2,1562 | 8,63 (3,99–18,65) | <0,0005 |
GPT: glutamato-piruvato transaminasa; IC: intervalo de confianza.
Ambas poblaciones de pacientes son comparables en cuanto a distribución por sexos, edad, peso inicial, valores analíticos, estado de la enfermedad antes del tratamiento, distribución por genotipo viral y carga viral basal. Hay que destacar que cerca del 65% de los pacientes estaba infectado por el genotipo 1 del VHC, que se asocia con una peor respuesta al tratamiento y mayor agresividad sobre el hígado.
El porcentaje de pacientes que obtienen una respuesta viral sostenida es similar en ambos grupos, sin encontrarse diferencias clínicamente significativas, incluido el análisis realizado en función del genotipo viral que produce la infección y la carga viral plasmática antes de iniciar el tratamiento. Estos resultados difieren de los obtenidos en el metaanálisis realizado por Almasio et al17, en el que la obtención de respuesta viral sostenida era significativamente mayor en el grupo tratado con peginterferón alfa-2b para pacientes con genotipo 1 (p = 0,017). En el grupo tratado con peginterferón alfa-2a, la frecuencia relativa de obtención de RVS es significativamente mayor que la obtenida por Fried et al6 (71,3% frente al 56%; p = 0,0134). En los pacientes tratados con peginterferón alfa-2b se produce una situación similar, con frecuencias relativas de RVS mayores que la obtenida por Manns et al5, aunque sin diferencias significativas (64,3% frente al 54%; p = 0,063) y acordes a los descritos en la ficha técnica del peginterferón alfa-2b12.
Esta falta de concordancia con nuestros resultados puede explicarse por diferencias en las características de nuestros pacientes como, por ejemplo, el peso corporal y la carga viral plasmática inicial. Además, los resultados obtenidos en ensayos clínicos no siempre se reproducen en la práctica clínica habitual, ya que en esta situación los fármacos se administran a pacientes de todo tipo y con situaciones fisiopatológicas muy variadas. En nuestro trabajo se han introducido unos criterios de inclusión y exclusión para intentar controlar factores externos con influencia potencial en los resultados, teniendo en cuenta que este control no ha sido tan estricto como en un ensayo clínico, y que nuestro trabajo pretende reflejar los resultados de la práctica clínica diaria que se obtienen en una población real de pacientes.
Como se ha comentado, la respuesta virológica se suele asociar a una respuesta bioquímica, aunque en ocasiones existe discrepancia entre ambas, debido a la persistencia de bajo grado de replicación del virus no detectable con los tests disponibles (límites de sensibilidad de la PCR), a un efecto directo del peginterferón, o a otras causas de daño hepático, etc. Así, al analizar la efectividad del tratamiento, tampoco se han encontrado diferencias significativas entre el grupo tratado con peginterferón alfa-2a y el tratado con peginterferón alfa-2b, y puede considerarse que ambos fármacos son igual de efectivos. El análisis multivariante realizado confirma los resultados obtenidos, ya que el tipo de peginterferón con el que se trata al paciente no es un factor predictor de obtención de respuesta viral sostenida ni de efectividad.
De los factores predictores de respuesta viral sostenida y efectividad del tratamiento que se han encontrado en el análisis multivariante, hay que destacar la importancia de la permanencia al tratamiento, ya que sobre el resto de factores predictores no podemos actuar al depender del genotipo que produce la infección o daño hepático producido por el virus, y el genotipo viral es el principal factor relacionado con la respuesta al tratamiento18. La relación entre la permanencia en el tratamiento y la respuesta a éste se ha evidenciado en varias patologías, incluyendo la terapia antiviral frente a la infección del VHC18,19. El porcentaje de pacientes con un grado de permanencia superior al 80% es similar en ambos grupos, y también en ambos grupos se encuentra una relación significativa entre una permanencia superior al 80% y la obtención de respuesta viral sostenida y efectividad del tratamiento. En este sentido, es importante destacar la necesidad de aplicar medidas preventivas para evitar o reducir la gravedad de los posibles efectos adversos derivados del tratamiento antiviral (administrar factores de crecimiento hematopoyético, etc.). Aunque los pacientes tratados con peginterferón alfa-2b tienen mayor permanencia en el tratamiento, esto no se traduce en mayor efectividad que el grupo tratado con peginterferón alfa-2a. Como se observa en la figura 2, la probabilidad de eliminación del virus en el aspecto plasmático es similar en ambos tratamientos, y como se ha indicado en el análisis multivariante, esta probabilidad aumenta con mayor permanencia en el tratamiento. En este sentido, los resultados de Zeuzem et al20 que apoyan una reducción de la duración del tratamiento en determinados subgrupos de pacientes deben tomarse con precaución, de forma que esta medida no puede generalizarse a todos los pacientes.
Las principales limitaciones de este trabajo son la falta de aleatorización de los pacientes y su tamaño muestral, que no permite obtener una potencia estadística del 80% para detectar diferencias en la prueba de contraste. Con respecto a la falta de aleatorización y para evitar el sesgo de selección, no se modificó el hábito de prescripción del médico, de forma que se reflejara la realidad terapéutica de nuestra población de pacientes. Además, se implantaron otras medidas ya comentadas como la inclusión de pacientes de diferentes facultativos y servicios clínicos (medicina interna, digestivo, unidad de enfermedades infecciosas, etc.).
En conclusión, teniendo en cuenta las limitaciones comentadas y los posibles sesgos que no se hayan podido controlar en este estudio, podemos considerar que en el marco de la práctica clínica diaria, tanto la terapia con peginterferón alfa-2a más ribavirina como con peginterferón alfa-2b más ribavirina son igual de efectivas en el tratamiento de la hepatitis C en pacientes naïve monoinfectados, con una tasa de respuesta viral sostenida similar entre ambos fármacos. En este sentido, es necesario realizar estudios de minimización de costes o de impacto presupuestario para poder establecer qué peginterferón debe ser considerado de primera elección. Se ha encontrado que un grado de permanencia en el tratamiento superior al 80% es un factor predictor de respuesta a la terapia antiviral.






![Curvas de supervivencia de negativización de la carga viral plasmática para ambos tipos de peginterferón alfa en función del genotipo viral (genotipo 1-4 [A]; genotipo 2-3 [B]) que produce la infección (sobrevivir = no negativización de carga viral plasmática; se utilizó el test log-Rank para encontrar diferencias significativas entre ambos tratamientos). Curvas de supervivencia de negativización de la carga viral plasmática para ambos tipos de peginterferón alfa en función del genotipo viral (genotipo 1-4 [A]; genotipo 2-3 [B]) que produce la infección (sobrevivir = no negativización de carga viral plasmática; se utilizó el test log-Rank para encontrar diferencias significativas entre ambos tratamientos).](https://static.elsevier.es/multimedia/0213005X/0000002600000003/v1_201305090034/S0213005X08726764/v1_201305090034/es/main.assets/thumbnail/gr2.jpeg?xkr=ue/ImdikoIMrsJoerZ+w96p5LBcBpyJTqfwgorxm+Ow=)

