A pesar de la disminución de la prevalencia de la infección de la hepatitis C en las prisiones españolas en los últimos años, sigue existiendo un reservorio de la infección. El objetivo de este trabajo es analizar las características de estos pacientes y la respuesta al tratamiento antiviral a lo largo de los últimos 18 años.
MétodosEstudio observacional retrospectivo en internos diagnosticados de infección por VHC entre los años 2002 y 2020 y que llevan más de 6 meses institucionalizados en el centro penitenciario Araba.
Se realiza un análisis descriptivo de las características de los pacientes y de la respuesta a las 3 modalidades de tratamientos antivirales: peg-interferón y ribavirina, peg-interferón, ribavirina y un inhibidor de la proteasa de primera generación y diferentes combinaciones de antivirales de acción directa.
ResultadosSe prescribieron en total 248 tratamientos antivirales. Hasta 2015 el 65% de los sujetos estudiados respondieron al tratamiento, y después de 2015 alcanzó el 93,7%. Los pacientes no respondedores fueron la causa principal de no respuesta al tratamiento en los períodos 1 y 2 (40-50%), mientras que en el período 3 el motivo mayoritario fue viral breakthrough (67%).
ConclusiónDespués de 18 años de experiencia tratando a todos los pacientes que ingresan en prisión con VHC según criterio clínico, se ha logrado remitir la infección activa de hepatitis C. Por tanto, la estancia en prisión en sí misma y conjuntamente con la atención sanitaria continuada de aquellos sujetos que son liberados de la prisión puede constituir una oportunidad para disminuir el reservorio de la enfermedad también en la comunidad.
Despite the decrease of hepatitis C in Spanish prisons in the last years, it still remains a reservoir for infection. The aim of this work is to analyze the characteristics of these patients and the response to antiviral treatment over the last 18 years.
MethodsRetrospective observational study in inmates of Araba penitentiary center diagnosed with HCV infection between 2002 and 2020.
A descriptive analysis of patient characteristics and the response to the 3 antiviral treatment modalities was performed: peg-interferon and ribavirin, peg-interferon, ribavirin and a first-generation protease inhibitor and different combinations of direct-acting antivirals.
ResultsA total of 248 antiviral treatments were prescribed. Treatment response rate up to 2015 was 65% and 93,7% after that year. Interferon non-responders were the main cause of non-response to treatment in periods 1 and 2 (40-50%). Conversely, in period 3 viral breakthrough (67%) was the main culprit.
ConclusionAfter 18 years, active hepatitis C infection in prison inmates has resolved with treatment according to clinical criteria. Therefore, the stay in prison may represent an opportunity to reduce the reservoir of the disease in the community, together with continued health care for those released from prison.
La Organización Mundial de la Salud estima el número de personas que padecen infección crónica por el virus de la hepatitis C (VHC) en 71 millones, con una prevalencia del 0,5-2,3%1. Según estudios epidemiológicos realizados en España entre 2017 y 2018, la prevalencia de personas con anticuerpos frente al VHC en población general de 20 a 80 años fue de 0,85% y de infección activa de 0,22%2.
Se estima que la prevalencia de infección por VHC en las personas institucionalizadas en prisión es hasta 10 veces mayor que en la población general3. Estas cifras varían dependiendo de la ubicación geográfica del centro penitenciario, el país de origen de los reclusos, la estancia previa en prisión o el número de usuarios de drogas por vía parenteralUDVP4. También ha variado a lo largo de los últimos 18 años, produciéndose una reducción del 39% en 2002 al 10,6% en 20185. En el centro penitenciario Araba los valores alcanzados durante este período de tiempo oscilan entre un 44,7% en 2002 hasta un 16,6% en 20176.
La principal causa de esta disminución de la prevalencia de la infección activa por VHC es el aumento en la eficacia de los tratamientos antivirales7. Otras causas son el cambio de la vía de administración de sustancias de abuso y la implementación de los programas de intercambio de jeringuillas y de deshabituación a opiáceos que se realiza en las prisiones.
A pesar de ello, la prevalencia de infección activa entre los pacientes institucionalizados en prisión continúa siendo elevada y constituye un importante reservorio de la infección5,8. Por este motivo, los centros penitenciarios se convierten en elementos clave en los programas de tratamiento del VHC en la lucha para eliminar el virus9.
Los largos períodos en prisión posibilitan que los servicios sanitarios penitenciarios implementen programas de prevención para controlar enfermedades crónicas como las infecciones por VHC y por VIH, con beneficios para la salud pública de la comunidad9,10. Sin embargo, y a pesar de que deben aplicarse los principios de equidad en el acceso a los recursos sanitarios11, todavía existen muchos países sin planes específicos de prevención y con diferentes niveles de cobertura de intervenciones en reducción de daños, pruebas y tratamiento del VHC en pacientes de los centros penitenciarios11.
La Organización Mundial de la Salud, en sintonía con otras instituciones sanitarias y gobiernos, estableció en el año 2016 una estrategia global en el sector sanitario en hepatitis virales, con el objetivo de conseguir su eliminación para el año 2030. Dicha estrategia define la eliminación como una reducción del 80% en las nuevas infecciones por VHC y una reducción del 65% en la mortalidad por VHC12. Además, en 2017 se propuso la estrategia de microeliminación dirigida a poblaciones de riesgo como las personas institucionalizadas en prisión13. En esta línea se han desarrollado planes estratégicos a nivel nacional y autonómico14.
La escasa tasa de tratamiento de estos pacientes y la variada tasa de respuesta antes de la introducción de los antivirales de acción directa han motivado este estudio, cuyo objetivo es analizar las características de los pacientes con infección por VHC del centro penitenciario Araba y la respuesta al tratamiento antiviral a lo largo de los últimos 18 años.
MétodosEstudio observacional retrospectivo de todos los tratamientos prescritos en el centro penitenciario Araba en el período comprendido entre noviembre de 2002 y octubre 2020. Este centro alberga una media de 650 internos, siendo el 10% mujeres.
El estudio fue aprobado por el Comité Ético de Investigación Clínica del Hospital Universitario de Araba (HUA) (Expte.2020-088).
Los tratamientos administrados a lo largo del período del estudio han ido variando conforme a lo establecido en las guías de práctica clínica. Se delimitaron 3 períodos de estudio según el tratamiento antiviral empleado:
- -
Período 1: noviembre 2002-septiembre 2012, pacientes tratados con peg-interferón y ribavirina.
- -
Período 2: octubre 2012-diciembre 2014, pacientes tratados con peg-interferón, ribavirina y un inhibidor de la proteasa de primera generación (telaprevir).
- -
Período 3: enero 2015-octubre 2020, se incluyeron diferentes combinaciones de antivirales de acción directa.
Aquellos pacientes que cumplían los siguientes criterios eran incluidos en el programa de tratamiento: carga viral de VHC detectable (ARN-VHC), cualquier genotipo VHC (salvo en el segundo período que solo se incluía el genotipo 1), estabilidad de enfermedad mental con control coordinado con psiquiatría e infección por VIH con control virológico e inmunológico (carga viral indetectable durante al menos 6 meses y linfocitos T CD4+ mayores de 500 células/mm3). Se excluyeron pacientes con enfermedad psiquiátrica grave no controlada y estancia estimada en prisión inferior al tiempo de tratamiento. En el primer período, se excluyeron, además, pacientes con hepatopatía crónica, otras hepatopatías (hemocromatosis, hepatitis autoinmune, enfermedad de Wilson) y epilepsia no controlada.
Desde 2002 hasta 2011 la primera consulta se realizaba presencialmente en el hospital, continuando posteriormente un seguimiento telefónico a través de su médico de prisión. A partir de 2011 los pacientes eran atendidos en una sala ubicada en la prisión, equipada para realizar una consulta de telemedicina con el médico de enfermedades infecciosas del hospital. A esa consulta asistían presencialmente, junto al paciente, el equipo médico de atención primaria y de farmacia hospitalaria. La prescripción del tratamiento, supervisión, seguimiento de tolerabilidad y adherencia y realización de los controles analíticos era responsabilidad del equipo sanitario penitenciario. El seguimiento de los pacientes se realizaba según los protocolos de tratamiento establecidos en cada caso.
Mediante la revisión de las historias clínicas se recogieron todas las variables que afectaban a la respuesta al tratamiento: edad de inicio de tratamiento, sexo, genotipo del VHC, número de copias de ARN-VHC, grado de fibrosis previo al tratamiento (medido por elastografía transitoria, FibroScan®) y coinfección con VIH junto con parámetros clínicos, inmunológicos y virológicos (clasificación CDC15). También se recogieron los tratamientos en los que se trataba una reinfección, el lugar en el que había ocurrido esa reinfección del VHC (fuera o dentro de la prisión) y la respuesta obtenida a esa terapia. Como reinfección se establece aquellos casos de pacientes que habiendo sido tratados previamente y con respuesta viral sostenida (RVS), presentan de nuevo ARN-VHC detectable.
La carga viral de VHC se analizó con los equipos Cobas Amplicor y Cobas Taqman 48 (Roche). El genotipo del VHC se determinó utilizando la prueba de PCR en tiempo real para la identificación cualitativa de los genotipos 1 a 6 y los subtipos A y B del genotipo 1 del VHC en plasma o suero.
La RVS fue definida como ARN-VHC indetectable a las 12 o 24 semanas tras finalizar el tratamiento, dependiendo de la terapia recibida.
El motivo de falta de respuesta al tratamiento se clasificó como: no respuesta al tratamiento, recaída, viral breakthrough, suspensión por efectos adversos y abandono de la terapia. La recaída se definió como ARN-VHC indetectable al final del tratamiento, pero detectable durante el seguimiento posterior. Viral breakthrough se definió como la reaparición de la carga viral de VHC después de la negativización viral durante el tratamiento.
La salida del centro (por libertad o traslado a otra prisión) y fallecimiento por otras causas no relacionadas con la hepatopatía se consideraron pérdidas en el seguimiento a efectos de respuesta al tratamiento.
Plan estadísticoLa descripción general de la muestra de pacientes se realiza mediante la media y desviación estándar para las variables continuas, y la frecuencia y proporción para las categóricas.
Se describen las características de los pacientes y para cada uno de los 3 períodos de tiempo establecidos (2002-2012, 2012-2014 y 2015-2020). Y se realiza un análisis descriptivo de los tratamientos antivirales y la respuesta correspondiente a los tratamientos a lo largo de todo el período de tiempo por intención de tratar y por protocolo.
Análogamente se lleva a cabo un análisis descriptivo para el grupo de reinfectados.
El análisis estadístico se realiza con el programa IBM SPSS versión 23 para Windows.
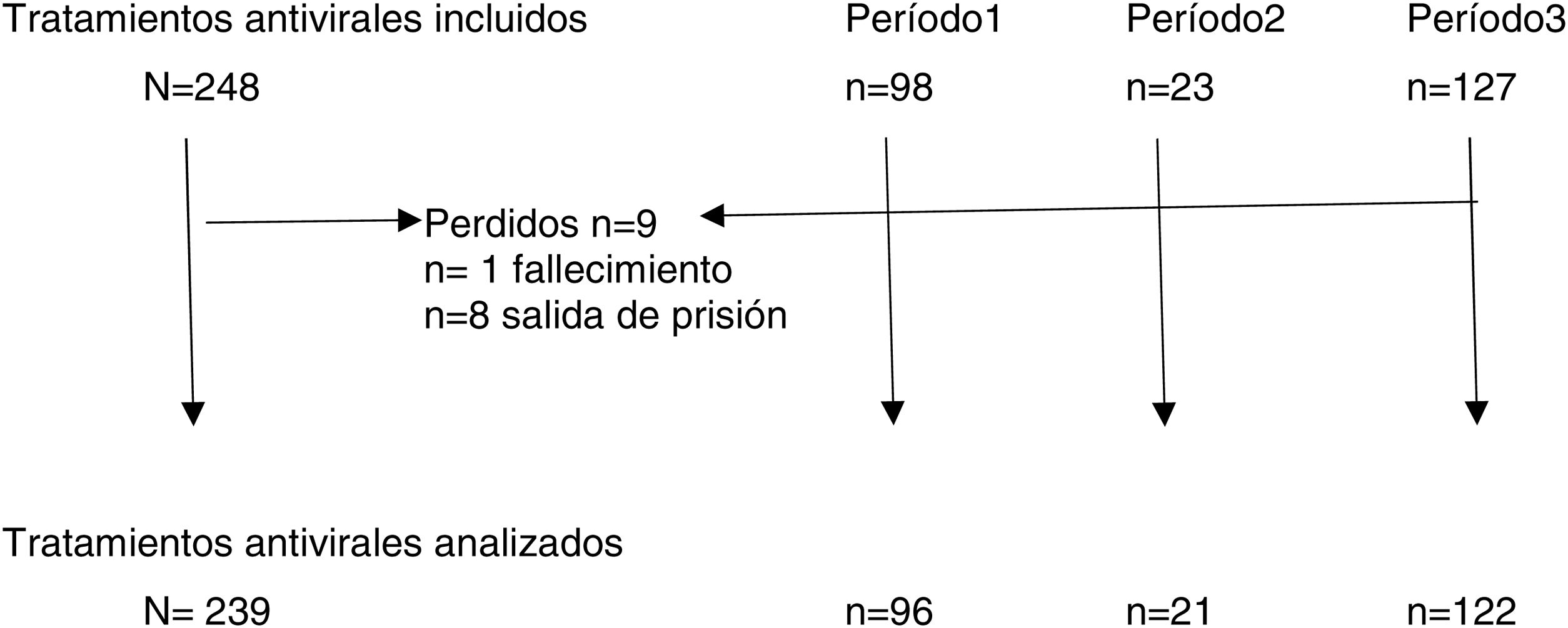
ResultadosEntre enero del 2002 y octubre de 2020 se prescribieron un total de 248 tratamientos antivirales en esta prisión. No se pudo completar el seguimiento en 9 pacientes, en uno de ellos por fallecimiento y en el resto por salida de la prisión (3 de ellos por traslado a otro centro penitenciario y 5 por alta de la prisión o salida en libertad) (fig. 1).
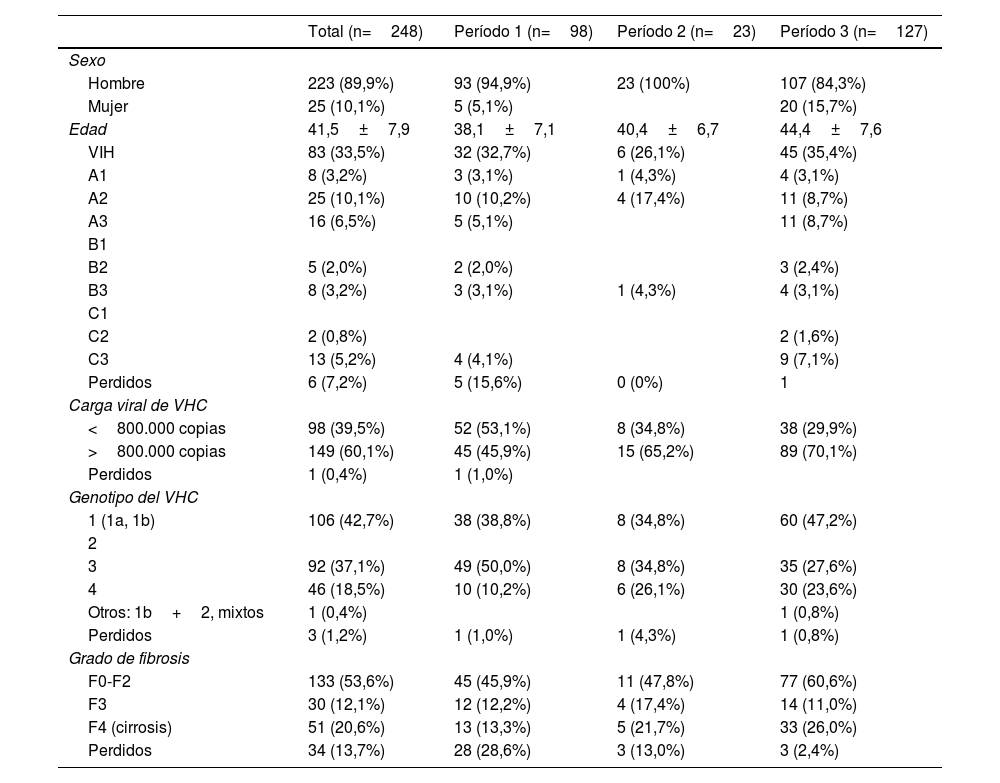
En la tabla 1 se presentan las características de los pacientes que reciben tratamiento antiviral. El 90% eran hombres, con una edad media de 41 años, el 33% presentaba coinfección por VIH, el 60% una carga viral de VHC superior a 800.000 copias y el 53% un grado de fibrosis F0-F2.
Descripción de la población a estudio
| Total (n=248) | Período 1 (n=98) | Período 2 (n=23) | Período 3 (n=127) | |
|---|---|---|---|---|
| Sexo | ||||
| Hombre | 223 (89,9%) | 93 (94,9%) | 23 (100%) | 107 (84,3%) |
| Mujer | 25 (10,1%) | 5 (5,1%) | 20 (15,7%) | |
| Edad | 41,5±7,9 | 38,1±7,1 | 40,4±6,7 | 44,4±7,6 |
| VIH | 83 (33,5%) | 32 (32,7%) | 6 (26,1%) | 45 (35,4%) |
| A1 | 8 (3,2%) | 3 (3,1%) | 1 (4,3%) | 4 (3,1%) |
| A2 | 25 (10,1%) | 10 (10,2%) | 4 (17,4%) | 11 (8,7%) |
| A3 | 16 (6,5%) | 5 (5,1%) | 11 (8,7%) | |
| B1 | ||||
| B2 | 5 (2,0%) | 2 (2,0%) | 3 (2,4%) | |
| B3 | 8 (3,2%) | 3 (3,1%) | 1 (4,3%) | 4 (3,1%) |
| C1 | ||||
| C2 | 2 (0,8%) | 2 (1,6%) | ||
| C3 | 13 (5,2%) | 4 (4,1%) | 9 (7,1%) | |
| Perdidos | 6 (7,2%) | 5 (15,6%) | 0 (0%) | 1 |
| Carga viral de VHC | ||||
| <800.000 copias | 98 (39,5%) | 52 (53,1%) | 8 (34,8%) | 38 (29,9%) |
| >800.000 copias | 149 (60,1%) | 45 (45,9%) | 15 (65,2%) | 89 (70,1%) |
| Perdidos | 1 (0,4%) | 1 (1,0%) | ||
| Genotipo del VHC | ||||
| 1 (1a, 1b) | 106 (42,7%) | 38 (38,8%) | 8 (34,8%) | 60 (47,2%) |
| 2 | ||||
| 3 | 92 (37,1%) | 49 (50,0%) | 8 (34,8%) | 35 (27,6%) |
| 4 | 46 (18,5%) | 10 (10,2%) | 6 (26,1%) | 30 (23,6%) |
| Otros: 1b+2, mixtos | 1 (0,4%) | 1 (0,8%) | ||
| Perdidos | 3 (1,2%) | 1 (1,0%) | 1 (4,3%) | 1 (0,8%) |
| Grado de fibrosis | ||||
| F0-F2 | 133 (53,6%) | 45 (45,9%) | 11 (47,8%) | 77 (60,6%) |
| F3 | 30 (12,1%) | 12 (12,2%) | 4 (17,4%) | 14 (11,0%) |
| F4 (cirrosis) | 51 (20,6%) | 13 (13,3%) | 5 (21,7%) | 33 (26,0%) |
| Perdidos | 34 (13,7%) | 28 (28,6%) | 3 (13,0%) | 3 (2,4%) |
Período 1: entre enero del 2002 y septiembre de 2012, pacientes que se trataron con peg-interferón y ribavirina.
Período 2: entre octubre de 2012 y diciembre de 2014, pacientes que se trataron con peg-interferón, ribavirina y un inhibidor de la proteasa de primera generación.
Período 3: entre enero de 2015 y octubre de 2020, se incluyeron diferentes combinaciones de antivirales de acción directa.
El 51,2% de los pacientes fueron tratados entre 2015 y 2020, el 39,5% entre 2012-2014 y el 9,3% de 2002-2012. Se observa un incremento de la edad en cada uno de los períodos analizados, así como de la carga viral y el grado de fibrosis F0-F2 y F4. El genotipo 3 es el más frecuente en primer período mientras que en el último lo es el genotipo 1.
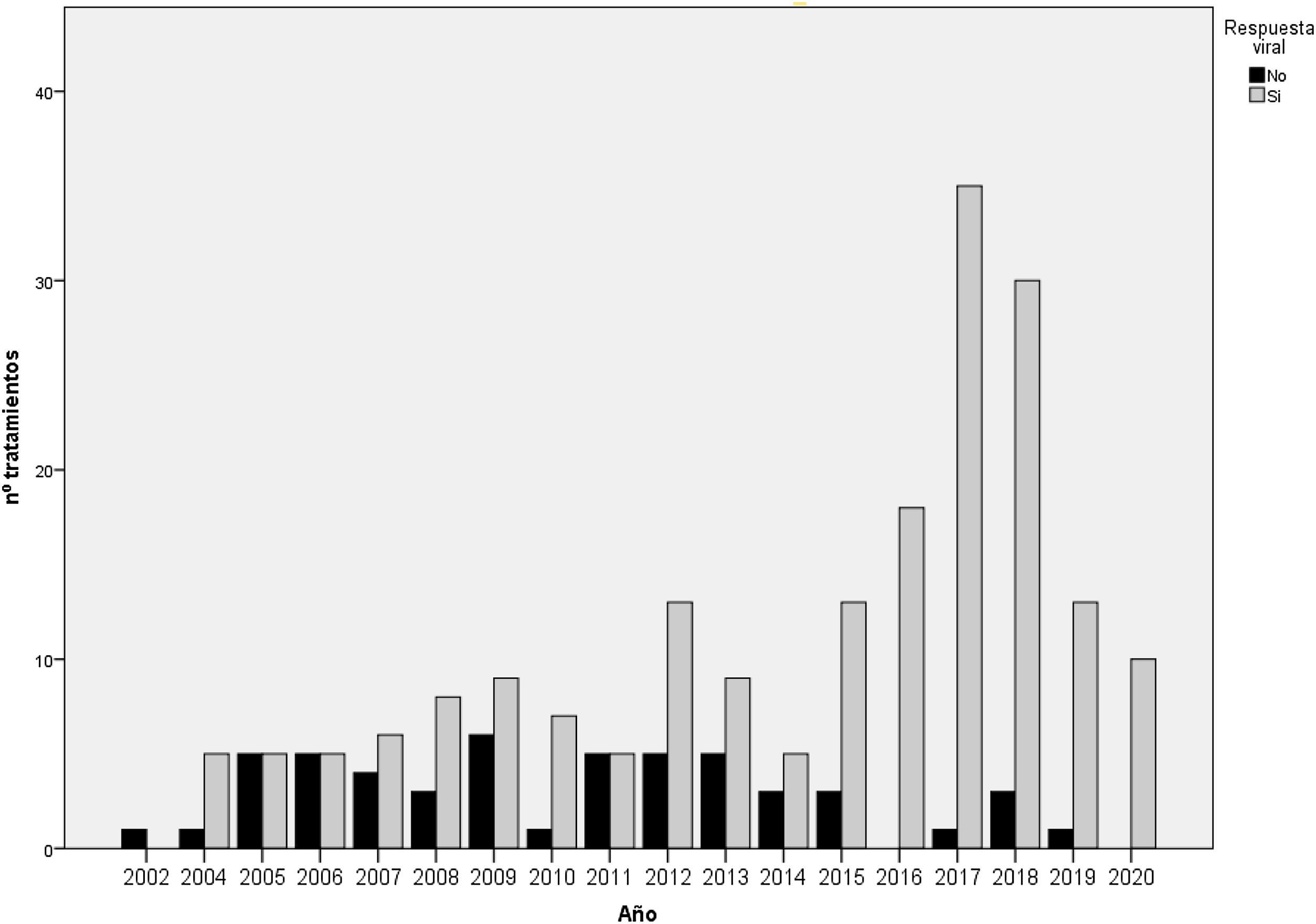
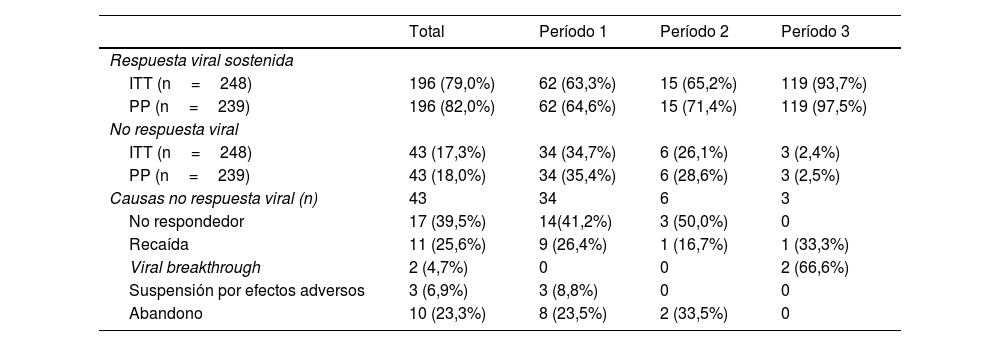
Los resultados de los tratamientos se presentan en la tabla 2 y en la figura 2. Hasta 2015 el 63-65% de los sujetos estudiados respondieron al tratamiento, mientras que después de 2015 la RVS fue del 93,7%. Analizando los datos por protocolo y excluyendo a los pacientes con pérdida de seguimiento, el porcentaje de RVS es del 64-71% y del 97,5%, respectivamente. Al final del período del estudio, el número de pacientes con carga viral de VHC indetectable que llevaban más de 6 meses institucionalizados fue del 100%.
Resultados de los tratamientos antivirales en los 3 períodos analizados
| Total | Período 1 | Período 2 | Período 3 | |
|---|---|---|---|---|
| Respuesta viral sostenida | ||||
| ITT (n=248) | 196 (79,0%) | 62 (63,3%) | 15 (65,2%) | 119 (93,7%) |
| PP (n=239) | 196 (82,0%) | 62 (64,6%) | 15 (71,4%) | 119 (97,5%) |
| No respuesta viral | ||||
| ITT (n=248) | 43 (17,3%) | 34 (34,7%) | 6 (26,1%) | 3 (2,4%) |
| PP (n=239) | 43 (18,0%) | 34 (35,4%) | 6 (28,6%) | 3 (2,5%) |
| Causas no respuesta viral (n) | 43 | 34 | 6 | 3 |
| No respondedor | 17 (39,5%) | 14(41,2%) | 3 (50,0%) | 0 |
| Recaída | 11 (25,6%) | 9 (26,4%) | 1 (16,7%) | 1 (33,3%) |
| Viral breakthrough | 2 (4,7%) | 0 | 0 | 2 (66,6%) |
| Suspensión por efectos adversos | 3 (6,9%) | 3 (8,8%) | 0 | 0 |
| Abandono | 10 (23,3%) | 8 (23,5%) | 2 (33,5%) | 0 |
ITT: intención de tratar (con pérdidas); PP: por protocolo (sin pérdidas).
Período 1: entre enero del 2002 y septiembre de 2012, pacientes que se trataron con peg-interferón y ribavirina.
Período 2: entre octubre de 2012 y diciembre de 2014, pacientes que se trataron con peg-interferón, ribavirina y un inhibidor de la proteasa de primera generación.
Período 3: entre enero de 2015 y octubre de 2020, se incluyeron diferentes combinaciones de antivirales de acción directa.
El principal motivo de no respuesta en los 2 primeros períodos fue la falta de respuesta al tratamiento (41% en 2002-2011 y 50% en 2012-2014), mientras que en el último período fue viral breakthrough (67%).
Durante los 18 años del estudio se trataron 12 reinfecciones dentro de prisión, de las cuales 11 fueron con regímenes libres de interferón. El 83,3% correspondieron a hombres, con una edad media de 41,1 años y el 41,4% presentaban coinfección por VIH. En 10 de los 12 casos se obtuvo una RVS al tratamiento y en los 2 casos restantes se desconoce la respuesta final; uno falleció por causas ajenas a su hepatitis y el otro salió de prisión (alta o salida en libertad).
DiscusiónHasta el año 2012, el tratamiento de elección para el VHC era la combinación de interferón pegilado y ribavirina durante 24-48 semanas. Con esta combinación se lograban tasas de RVS de alrededor del 50% en pacientes con genotipo 116,17. Sin embargo, había una alta tasa de efectos secundarios y estaba contraindicado en muchos pacientes incluyendo aquellos con cirrosis avanzada18. En la prisión de Araba, la tasa de RVS fue del 63,3%, similar a los ensayos clínicos pivotales.
Con la llegada de los inhibidores de la proteasa de primera generación (boceprevir y telaprevir) en el año 2012, se logró una tasa de RVS en pacientes naïve entre un 63-75%19,20 y entre un 29-88% en pacientes con VHC genotipo 1 sin respuesta al tratamiento con doble terapia21,22. En el caso de la cárcel de Araba se obtuvo una RVS del 65,2%.
Con la comercialización de los antivirales de acción directa a partir de 2015 se comenzaron a mostrar tasas de RVS superiores y próximas al 100%23,24. En caso del centro penitenciario Araba, la tasa de RVS alcanzada fue del 93,7%. Si excluimos a los pacientes perdidos por falta de seguimiento al salir de la prisión, esa tasa se elevaría al 97,5%, similar a la observada en los estudios pivotales de los diferentes fármacos antivirales de acción directa.
Por tanto, teniendo en cuenta que todos los pacientes que llevaban más de 6 meses institucionalizados con VHC son tratados según criterio clínico y que, tras 18 años, cerca del 100% presenta carga viral indetectable, la estancia en prisión se presenta como un momento idóneo para tratar a estos pacientes. Ejerce, además, una gran contribución comunitaria en el control de la infección25.
En consecuencia, las tasas de no respuesta al tratamiento han disminuido a lo largo del tiempo, partiendo del 26-34% con los regímenes de tratamiento iniciales basados en interferón hasta alcanzar el 2,4% con los regímenes libres de interferón. El principal motivo de no respuesta en los primeros fue la falta de respuesta al tratamiento (41-50%), mientras que con los tratamientos sin interferón fue por viral breakthrough (66%). Además, en los tratamientos sin interferón no encontramos ningún caso de falta de respuesta por abandono ni de efectos adversos.
En la evidencia científica publicada hasta el momento encontramos resultados similares a los nuestros en el caso de los tratamientos sin interferón, con tasas de no respuesta por abandono y efectos adversos del 0,47 y 0,48%26,27. Para los tratamientos con interferón se observan tasas de no respuesta del 22%28, aunque los principales motivos son la salida de prisión (36%) y los efectos adversos (15,5%). Finalmente, una revisión sistemática reciente29,30 señala la existencia de una gran variabilidad en los motivos de no respuesta al tratamiento de los diferentes estudios incluidos tanto en los regímenes con interferón como sin interferón.
Por otra parte, la pérdida de seguimiento por salida del centro penitenciario afecta al 3,2%. La discontinuación del tratamiento por la salida del centro plantea así un desafío que podría resolverse con la continuación de la atención terapéutica de los reclusos puestos en libertad mediante una adecuada coordinación entre los sistemas de salud penitenciarios y comunitarios13,28. Además, serían necesarias estrategias y protocolos dirigidos sobre todo hacia la prevención de las reinfecciones y a aquellos con cirrosis que requieran de un control posterior en la comunidad.
Una de las limitaciones del estudio es que el manejo de los pacientes de la prisión se realizó bajo un régimen supervisado y no se contabilizaron aquellos que continuaron el tratamiento en otro centro, aunque en la mayoría de los casos se conoció la respuesta final al mismo. En los casos de excarcelación, se les derivó a su hospital de referencia y en los traslados a otros centros penitenciarios se contactó con el servicio sanitario correspondiente para conocer el resultado final. Para minimizar el posible sesgo de información asociado, se ha realizado el análisis por intención de tratar y por protocolo.
Por otra parte, no se determinó el número de pacientes que rechazaban el tratamiento ni los motivos para ello.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de interesesNo existe ningún conflicto de intereses.
A Javier Marijuan García, por su colaboración en la adquisición de los datos desde el inicio del trabajo en 2002 hasta su jubilación en 2018.
María Isabel Santamaría Mas, por su colaboración en la adquisición de los datos de grado de fibrosis hepática desde el inicio del trabajo en 2002 hasta su jubilación en 2018.