Introducción
Los particulares cambios morfológicos y funcionales que se producen en el tracto urinario de la gestante hacen que la infección del tracto urinario (ITU) sea la segunda patología médica más frecuente del embarazo, por detrás de la anemia. Las 3 entidades de mayor repercusión son:
Bacteriuria asintomática (BA) (2-11%), cuya detección y tratamiento son fundamentales durante la gestación, pues se asocia a prematuridad, bajo peso y elevado riesgo de progresión a pielonefritis aguda (PA) y sepsis.
Cistitis aguda (CA) (1,5%).
Pielonefritis aguda (1-2%), principal causa de ingreso no obstétrico en la gestante, que en el 10 al 20% de los casos supone alguna complicación grave que pone en riesgo la vida materna y la fetal.
Definiciones
La ITU se define como la existencia de bacterias en el tracto urinario capaces de producir alteraciones funcionales y/o morfológicas. Mediante el análisis de orina, debemos probar la presencia de bacteriuria significativa (> 100.000 unidades formadoras de colonias (UFC)/ml de un único uropatógeno recogida por micción espontánea en 2 muestras consecutivas, > 1.000 UFC/ml si se recoge por sondaje vesical, o cualquier cantidad si la muestra se obtiene por punción suprapúbica) 1.
Bacteriuria asintomática: bacteriuria significativa no asociada a síntomas clínicos. Únicamente se trata en situaciones especiales, como el embarazo.
Infección del tracto urinario y embarazo
Su frecuencia se sitúa entre el 5 y el 10% 2. Además, se relaciona con importantes problemas para el feto, como parto prematuro, bajo peso, infección y mortalidad perinatal 3,4, y para la madre, como anemia e hipertensión.
Fisiopatología
En la gestante se añaden unas modificaciones fisiológicas y anatómicas que elevan el riesgo de ITU. La más importante es la dilatación pielocalicial, a la que contribuyen factores mecánicos y hormonales, dando lugar al hidrouréter/hidronefrosis. Esta ectasia ureterorrenal puede albergar hasta 200 ml de orina. La compresión mecánica del útero y de la vena ovárica sobre el uréter derecho se inicia al final del primer trimestre. La dextrorrotación uterina, la interposición del colon sigmoide y el tránsito en paralelo del uréter y de los vasos ováricos en el lado izquierdo también favorecen el predominio derecho de la compresión ureteral. Por ello, 9 de cada 10 PA asientan sobre el lado derecho.
La influencia hormonal, tanto de progesterona como de algunas prostaglandinas, disminuye el tono y la contractilidad del uréter y favorece el reflujo vesicoureteral. El vaciado vesical incompleto también facilita el reflujo y la migración bacteriana ascendente. Los estrógenos pueden inducir una hiperemia en el trígono e indirectamente favorecen la adherencia de los gérmenes sobre el epitelio.
El incremento del 50% del volumen circulante provoca un aumento del filtrado glomerular, que favorece la estasis urinaria. La alcalinización de la orina (incremento en la excreción de bicarbonato) y el aumento en la concentración urinaria de azúcares, de aminoácidos y de estrógenos facilitan asimismo el crecimiento bacteriano.
Durante el embarazo la médula renal es particularmente sensible a la infección. En ella el ambiente hipertónico inhibe la migración leucocitaria, la fagocitosis y la actividad del complemento. Las alteraciones del sistema inmunitario también parecen favorecer las ITU. Se ha demostrado que la producción de interleucina (IL)-6 y la respuesta antigénica específica para Escherichia coli es menor en gestantes 5,6.
Factores de riesgo
El principal factor de riesgo es el antecedente de ITU previo al embarazo. Del 24 al 38% de las mujeres que presentan BA en la gestación tienen antecedentes de ITU sintomática. En segundo lugar, las pacientes con malas condiciones socioeconómicas presentan una incidencia 5 veces mayor de BA durante la gestación. La drepanocitemia es un factor de riesgo que debe tenerse en cuenta fundamentalmente en la raza negra, pues duplica el riesgo de adquirir BA 7. La diabetes mellitus, incluida la diabetes gestacional, favorece la frecuencia de ITU y la aparición de formas más graves. Otras patologías predisponentes incluyen a trasplantadas renales, alteraciones en el tracto urinario, pacientes con lesiones medulares (vejiga neurógena) y gestantes portadoras de reservorios ileales.
Etiología
Como en la no gestante, predominan los bacilos gramnegativos de la familia Enterobacteriaceae. E. coli es responsable del 75-90% de las infecciones. Klebsiella spp., Proteus mirabilis (ambas suponen el 10-13% de los casos), Enterobacter spp. (3%), Citrobacter spp., Serratia spp. y Pseudomonas spp. (1-2%) son otros bacilos gramnegativos responsables de ITU que se aíslan con mayor frecuencia en ITU complicadas y pacientes hospitalizadas. Entre los grampositivos el más frecuentemente aislado es Streptococcus agalactiae, que es el segundo en frecuencia en algunas poblaciones 8. Si se detecta ITU por este estreptococo del grupo B en cualquier momento del embarazo, es obligatoria la profilaxis antibiótica durante el parto para prevenir la sepsis neonatal, independientemente de que la infección haya sido tratada adecuadamente. Staphylococcus saprophyticus causa un pequeño porcentaje de infecciones (< 1%). Enterococcus spp. se aísla ocasionalmente y en relación con el empleo previo de antibióticos (cefalosporinas).
Tratamiento antibiótico en la embarazada
Comentaremos alguna de las características de los antibióticos indicados para el tratamiento de la ITU en la embarazada, según los protocolos de la Sociedad Española de Ginecología y Obstetricia (SEGO) 2 (tabla 1).
El tratamiento inicialmente será empírico, modificándose de acuerdo con los resultados del urocultivo y el antibiograma. Éste se establece de acuerdo con la prevalencia de los gérmenes más frecuentes, sus resistencias y la gravedad del cuadro clínico. El uso de betalactámicos, de fosfomicina-trometamol y de nitrofurantoína cumple con los criterios de seguridad y eficacia requeridos en la mayoría de los casos. El empleo en monodosis para el tratamiento de la BA sólo es aceptado por la Food and Drug Administration (FDA) estadounidense para la fosfomicina-trometamol, ya que su larga vida media (4,5 h) y su prolongada eliminación urinaria (48-72 h) permiten que su efecto en monodosis de 3 g sea similar al de la pauta larga de 7 días, con un 85% de erradicación. La amoxicilina-ácido clavulánico, las cefalosporinas y la nitrofurantoína no han demostrado la misma eficacia en monodosis a causa de su rápida eliminación urinaria 9-12. En unas recomendaciones recientes de la Sociedad Americana de Enfermedades Infecciosas se recomienda que la BA se trate de 3-7 días con una evidencia A-III 11.
En circunstancias como alergias o infecciones graves puede considerarse el empleo de aztreonam o de aminoglucósidos.
La mayoría de los fármacos empleados en el tratamiento de las ITU son eficaces porque se eliminan a través del riñón, sin una metabolización previa importante 8. El aclaramiento renal incrementado es otro factor favorable.
También hay que valorar el paso de la barrera placentaria, que tiene lugar con pesos moleculares inferiores a 500 daltons 13.
El potencial tóxico o teratogénico de los antimicrobianos queda recogido en la clasificación de la FDA de Estados Unidos 14:
Categoría B (sin riesgo fetal en estudios animales pero sin datos en humanos): penicilinas, inhibidores de las betalactamasas, cefalosporinas, aztreonam, nitrofurantoína, macrólidos, clindamicina, metronidazol y fosfomicina-trometamol.
Categoría C (efectos adversos sobre el feto en animales y sin estudios comparativos en humanos): sulfamidas (altera la captación de bilirrubina, con riesgo de ictericia, anemia hemolítica y querníctero en el recién nacido si se emplean cerca del término); trimetroprim (anemia megaloblástica materna y embriotoxicidad; debe evitarse en el primer trimestre; en caso de administración, suplementar con ácido fólico); imipenem (convulsiones y efectos secundarios digestivos); quinolonas (malformaciones osteoarticulares): su efecto nocivo osteoarticular es dudoso 15,16; en un estudio reciente 16 las quinolonas sólo aumentaron ligeramente el riesgo de malformaciones óseas administradas un mes antes de la concepción o en el primer trimestre del embarazo, por lo que podrían utilizarse en el 2.º-3.er trimestre en casos seleccionados en los cuales no se dispusiera de otras opciones terapéuticas seguras.
Categoría D (evidencias de riesgo en humanos, pero sus beneficios en gestantes son tan importantes que se admite su empleo, si no existen otras alternativas): tetraciclinas (toxicidad dental en el niño y riesgo de hígado graso materno). Los aminoglucósidos están incluidos en las categorías C-D por su riesgo de ototoxicidad y nefrotoxicidad (estrecha vigilancia de la concentración plasmática).
Bacteriuria asintomática
La incidencia de BA alcanza el 2-11% de las gestantes. Esta variabilidad en la incidencia depende principalmente del nivel socioeconómico de la población elegida. Si se incluyen otros gérmenes, como Ureaplasma y Gardnerella vaginalis, puede alcanzar el 25% 17. Diversos factores se han asociado con la presencia de BA: nivel socioeconómico bajo 18, diabetes, antecedentes de ITU en embarazos previos, paridad, actividad sexual, anomalías del tracto urinario y anemia falciforme. No se ha podido demostrar asociación ni con la raza ni con el grupo étnico. La relación con la edad y la paridad está poco aclarada.
Efectos del embarazo sobre la bacteriuria
La BA es detectable al principio de la gestación, y menos del 1% de las gestantes con urocultivo negativo la adquirirán a lo largo de la misma 19. La mayoría de las mujeres con BA lo es de forma previa al embarazo. No obstante, el riesgo de aparición aumenta conforme lo hace el embarazo: desde el 0,8% en la 12.ª semana hasta el 1,93% al final.
La patogenia implica una infección ascendente como resultado de las modificaciones gravídicas, junto con alguno o varios de los factores ya indicados.
Efectos de la bacteriuria sobre el embarazo
A diferencia de la mujer no gestante, en la embarazada la BA representa un significativo riesgo para su salud. La BA predispone a la pielonefritis aguda (PA): hasta dos tercios de los casos aparecen en gestantes con BA, y el 30% desarrollará esta complicación si no se trata. El tratamiento reduce la incidencia de progresión a PA al 3-4% 19. Los programas de cribado y tratamiento han conseguido reducir la progresión de BA a PA del 2-4% al 1% o menos 18,21.
Otros efectos adversos incluyen: anemia materna, hipertensión arterial, amenaza de parto pretérmino y aumento de la tasa de recién nacidos de bajo peso 22,23. El metaanálisis de Romero 24 demuestra que las gestantes con BA tratada tienen la mitad de riesgo de parto pretérmino (5,28% frente al 9,02%) y dos terceras partes del riesgo de tener un recién nacido de bajo peso (7,8% frente al 13,3%) que las embarazadas en las que ésta no se trata.
Investigación de la presencia de BA en el embarazo
Las complicaciones expuestas justifican que tanto los Servicios de Prevención de Estados Unidos como la SEGO aconsejen el establecimiento de programas de cribado universal de la BA en el embarazo. Estos programas detectan del 40 al 70% de las gestantes que van a desarrollar alguna complicación derivada de la BA 25. La etapa ideal para establecer la presencia de BA es la 16.ª semana de gestación, cuando mayor es la prevalencia de BA.
Sin embargo, aún no se han establecido las estrategias para la detección precoz por métodos baratos y eficaces.
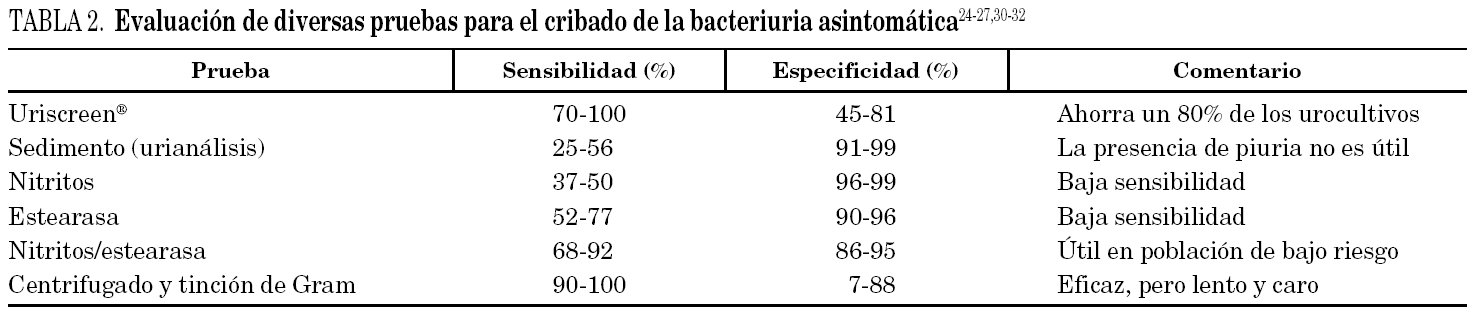
La prueba de elección es el urocultivo, ya que el diagnóstico se establece cuando éste es positivo. Pero es un procedimiento caro, por lo que se están investigando otros métodos más baratos y fáciles de aplicar, con una eficacia que sea aceptable. Hagay 26 concluye que el Uriscreen® (test urinario enzimático rápido de cribado) es una alternativa de alta sensibilidad y baja especificidad, y aconseja su uso para reducir el empleo del urocultivo a las pacientes con una prueba positiva, ahorrando un 80% de los urocultivos. Para otros autores, su eficacia es limitada 11,27,28.
Las tiras reactivas para detección de nitritos (urine dipstick test) y estearasas leucocitarias revelan alrededor de la mitad de las BA, pero son muy limitadas para detectar grampositivos 29.
El análisis urinario microscópico para detectar piuria es muy específico, pero su sensibilidad no supera a la de otras pruebas. Keeler 30 da más valor a la tinción Gram del centrifugado de orina porque es muy sensible, barata, rápida y puede realizarse en la consulta ambulatoria, pero otros autores no la consideran aceptable por su baja especificidad.
La IL-8 urinaria, según Shelton 31, tiene una sensibilidad del 70% y una especificidad del 95%. En conclusión, ninguna de estas pruebas es óptima para ser usada en el cribado de la BA (tabla 2). La SEGO recomienda la realización de un cultivo de orina a todas las gestantes en la primera consulta prenatal.
Manejo de la BA en el embarazo
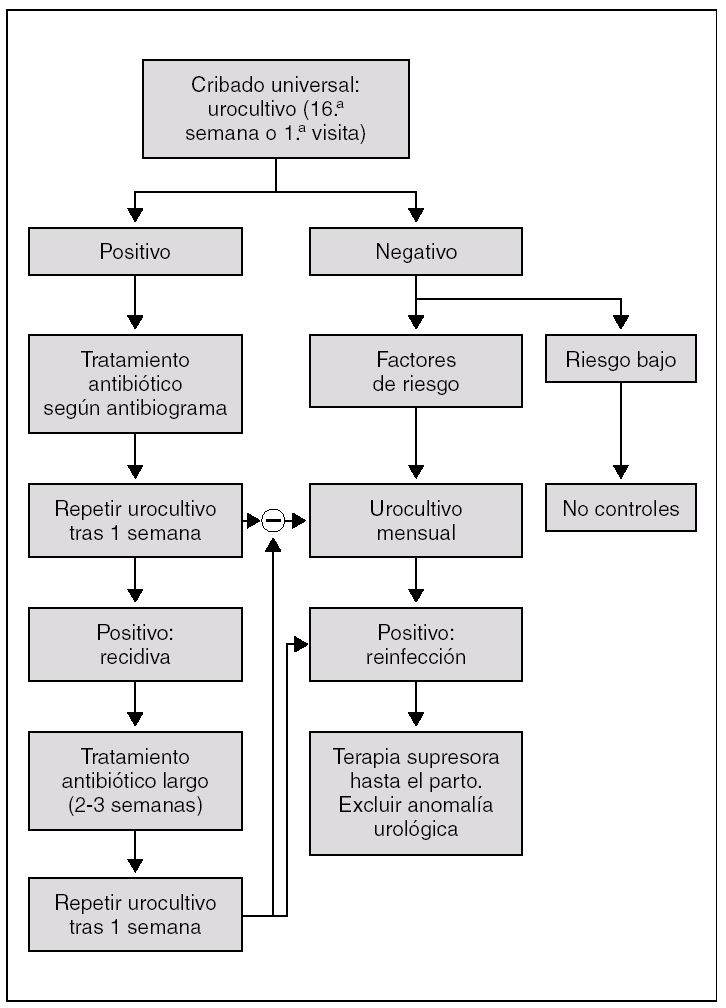
Se trata de un aspecto complejo. Por un lado, la erradicación de la BA reduce la incidencia de infección del tracto urinario sintomática en un 80-90% de los casos 11,35. Por otro lado, la posibilidad de recidiva tras recibir tratamiento es elevada, alcanzando cifras del 30%, debido a que en la embarazada con gran frecuencia existirá una infección parenquimatosa renal asintomática, responsable de la recolonización de la orina. Por ello es necesario efectuar un seguimiento de las gestantes con BA, repitiendo el urocultivo a la semana postratamiento y, en caso de recurrencia, usar pautas largas y considerar la supresión continua con antibióticos (fig. 1). En el capítulo sobre IU recurrentes se especifica con más detalle la actuación.
Figura 1. Protocolo de manejo de la BA en el embarazo.
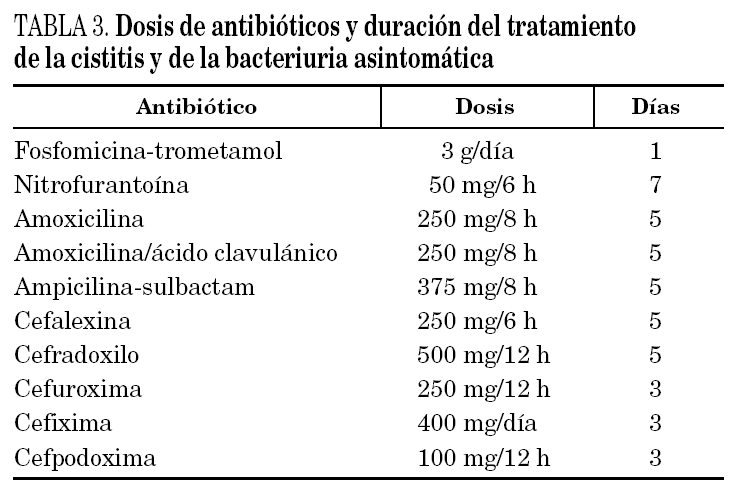
Los antibióticos más empleados en el tratamiento de la BA son los betalactámicos y la nitrofurantoína 12, aunque se va imponiendo cada vez más el empleo de fosfomicina-trometamol en pauta corta, pues su eficacia es similar (tasa de erradicación del 77-94%), con escasos efectos secundarios 10,36-38. Se aconsejan 2 dosis de 3 g/día separadas por 3 días, preferiblemente lejos de las comidas y después de orinar. El uso empírico de la ampicilina y del cotrimoxazol se desaconseja actualmente por el creciente número de resistencias de E. coli a estos antibióticos (tabla 3).
La revisión sistemática de Villar 39, publicada por la Cochrane Library, concluye que no existe evidencia para evaluar la equivalencia entre las pautas cortas y largas, aunque probablemente esta evidencia se obtenga cuando, a finales de 2005, concluya el ensayo actualmente auspiciado por la Organización Mundial de la Salud (OMS). No obstante, existen muchos ensayos bien diseñados que demuestran una eficacia similar para las pautas cortas con fosfomicina-trometamol en comparación con un régimen de 7-10 días con nitrofurantoína o cotrimoxazol. Además, las pautas cortas resultan especialmente interesantes por su menor coste, mejor cumplimiento, menor dosis empleada, menor riesgo de selección de cepas resistentes, menor alteración de la flora intestinal y menor incidencia de candidiasis vaginal 10.
Cistitis aguda
La CA es una ITU que afecta a la pared vesical y cursa con síndrome miccional, sin alteración del estado general. La CA del embarazo debe considerarse como una ITU primaria independiente de las otras formas de ITU, puesto que, al contrario que la PA, no depende de la existencia previa de BA 40,41.
Su incidencia es del 1,3-1,5%, mucho más baja que la de la BA, y se mantiene invariable a pesar del cribado y del tratamiento. En casi el 90% de los casos la ITU queda confinada a la vejiga, sin que exista bacteriuria renal, por lo que las tasas de recurrencia (15-17%) son menores que en la BA, pero lo suficientemente elevadas como para justificar un seguimiento similar al propuesto para la BA 42.
No suele progresar a PA, pero puede suceder que una pielonefritis debute con síntomas similares a una CA e inicialmente sea diagnosticada como tal.
La etiología y los factores de riesgo son superponibles a los ya expuestos para las ITU. En el 95% de los casos la infección es monobacteriana.
Suele presentarse en el segundo trimestre. Se caracteriza por la existencia de un síndrome miccional: disuria, polaquiuria, tenesmo y urgencia miccional. Suelen existir molestias suprapúbicas que aumentan a la presión, orina turbia y, en ocasiones, hematúrica. No hay fiebre, dolor lumbar ni afectación general. Estos síntomas pueden ser fácilmente confundidos con los producidos por las vulvovaginitis (sobre todo la candidiásica).
El diagnóstico se confirma mediante el urocultivo positivo, aunque puede ser negativo hasta en el 50% de los casos. Ello se debe a 3 razones. En primer lugar, como demostró Stamm, la CA puede presentarse con cifras inferiores a 100.000 UFC/ml; en presencia de síntomas urinarios, un urocultivo con más de 100 UFC/ml se considera positivo. En segundo lugar, el cuadro de cistitis puede estar provocado por Chlamydia trachomatis, que no crece en los cultivos habituales. Estos casos se engloban en el denominado síndrome ureteral agudo o cistitis abacteriúrica, y en realidad corresponden a uretritis no gonocócicas. En tercer lugar, puede deberse a que exista obstrucción del tracto urinario 41-43.
El sedimento de orina demuestra piuria (> 10 leucocitos/mm 3).
El tratamiento de la CA también es similar al de la BA (tabla 3), y en la actualidad entre las opciones se admite la utilización de fosfomicina-trometamol en monodosis de 3 g o en pauta corta de 2 días (separada cada una de ellas por 3 días) 44. Debe iniciarse de forma empírica tras recoger una muestra para urocultivo y antibiograma. Antes de usar una pauta corta debe descartarse que se trate de una PA incipiente, en cuyo caso el tratamiento deberá ser más prolongado.
El síndrome ureteral agudo por Chlamydia responde al tratamiento con macrólidos; las tetraciclinas están desaconsejadas por sus conocidos efectos secundarios.
Pielonefritis aguda
La PA es una ITU acompañada de manifestaciones clínicas que sugieren afectación renal. Es frecuente en el embarazo, y ocupa el primer lugar entre las causas no obstétricas de hospitalización en la gestante. Debe considerarse una complicación seria, puesto que es la principal causa de shock séptico y puede asociarse a trabajo de parto pretérmino y a retraso del crecimiento intrauterino.
La incidencia se sitúa entre el 1-2% pero varía según la población, dependiendo fundamentalmente de la prevalencia de BA y de la existencia de programas para su detección y tratamiento.
Es más común en el segundo (45-50%) y tercer trimestre (40-45%) que en el primero (10%) 45. El riesgo de recurrencia durante la misma gestación es del 15%. Casi un tercio de las embarazadas que padecen PA tendrán infecciones recurrentes y/o alteraciones renales estructurales en el futuro. Por ello es necesario efectuar un seguimiento con urocultivos similar al propuesto para la BA. En la PA recidivante o con complicaciones urológicas, las pacientes deben ser reevaluadas en el posparto.
El lado derecho está afectado en el 90% de los casos, y la afectación puede ser bilateral en un 25%. No se observan diferencias significativas entre las diversas etnias, pero se asocia con más frecuencia a nuliparidad y a menor edad 7.
La etiología y los factores de riesgo son los que se comentan en la introducción. E. coli es responsable de alrededor del 80% de los casos. En las PA, E. coli pertenece al serotipo 0 y las cepas presentan factores de virulencia en mayor porcentaje que en la BA. Por ejemplo, la expresión de citotoxinas que favorecen la lesión tisular y de fimbrias tipo 1, P y S que facilitan la adherencia al tracto urinario es más frecuente entre E. coli causante de PA que en las cepas de BA. El ambiente favorecedor que se da en el embarazo para la colonización bacteriana del tracto urinario facilita la supervivencia de cepas con escasa expresión de factores de virulencia, lo que les permite eludir la respuesta inmune responsable de la piuria. Estas cepas son frecuentes en la BA, pero en un tercio de los casos se trata de cepas virulentas que pueden desembocar en PA 46. Este hallazgo puede ser interesante en el futuro para conocer qué cepas de E. coli causantes de BA son las que presentan un mayor riesgo de causar una PA.
La clínica suele establecerse en horas, y es fundamental para el diagnóstico. Al síndrome miccional se une la fiebre alta (39-40 °C) que cursa en picos (debido a la liberación de toxinas y pirógenos), el malestar general y el dolor lumbar intenso y constante, unilateral o bilateral (se debe recordar el predominio del lado derecho), que se irradia siguiendo el trayecto ureteral hasta las fosas ilíacas. Son frecuentes la sudoración y los escalofríos (que sugieren bacteriemia) así como las náuseas, los vómitos y la consecuente deshidratación. La orina suele estar concentrada.
La puñopercusión renal es positiva (hipersensibilidad del ángulo costovertebral) en el lado afectado, y también pueden ser dolorosas la palpación de la fosa ilíaca y el fondo vaginal de ese mismo lado.
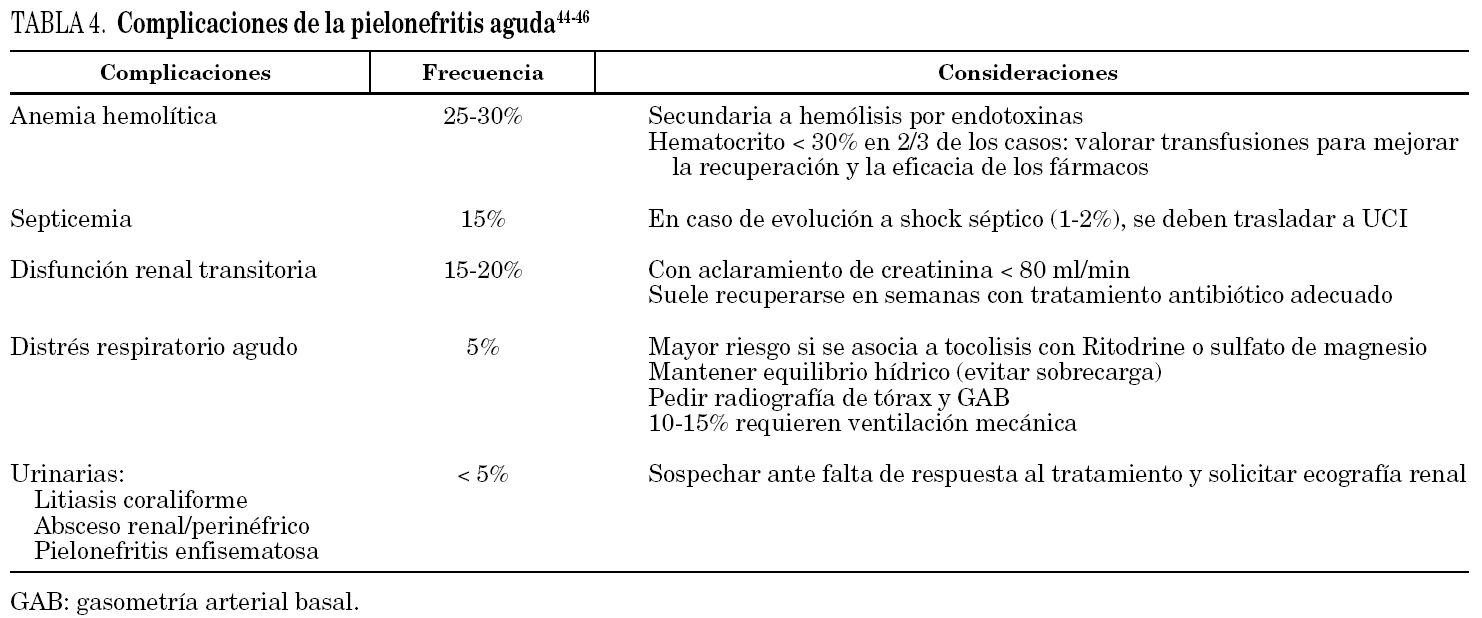
La aparición de hipotensión arterial, taquipnea, taquicardia y fiebre persistente o la no desaparición de la clínica tras 48 h de adecuado tratamiento antibiótico deben sugerir posibles complicaciones (tabla 4).
La sospecha diagnóstica de la PA es clínica y se confirma por el urocultivo positivo. En el sedimento de orina suele detectarse piuria y cilindros leucocitarios.
Las pruebas complementarias son:
Analítica completa: hemograma (existe leucocitosis con neutrofilia), función renal, electrolitos (al ingreso y a las 48 h de evolución).
Urocultivos: pueden ser negativos si la paciente se autoadministró antibioterapia.
Hemocultivos: positivos en el 15% de los casos. El microorganismo debe coincidir con el aislado en el urocultivo. Desde un punto de vista de coste-eficacia se ha cuestionado la necesidad de obtener urocultivo y hemocultivo al ingreso, debido a que en más del 95% de los casos las bacterias aisladas son sensibles al tratamiento empírico. Solamente el 3% de los urocultivos y el 2% de los hemocultivos pedidos al ingreso influyen en un cambio de antibióticos. Según esto, su obtención podría reservarse a los casos en que persista la clínica tras 48 h de tratamiento empírico 50. Sin embargo, la mayoría de los autores y la SEGO indican que deben realizarse.
Ecografía renal: se puede observar pelvis dilatada, cálculos renales y alteraciones anatómicas como duplicación ureteral. Aunque la SEGO recomienda su realización tras el ingreso, su beneficio es muy limitado, ya que no suele modificar el manejo ni el pronóstico. Está claramente indicada si persiste la fiebre tras 48-72 h de tratamiento, para descartar obstrucción de la vía urinaria o absceso renal/perinefrítico. Como la sensibilidad de la ecografía es inferior al 80% para la detección de litiasis 51, si se sigue sospechando obstrucción puede ser útil realizar una resonancia magnética 52, si está disponible, para evitar la exposición a las radiaciones que supondría la práctica de una pielografía.
Radiografía de tórax y gasometría arterial: si aparecen síntomas respiratorios.
El diagnóstico diferencial debe realizarse con la corioamnionitis, con la colecistitis, con el desprendimiento de placenta, con el mioma infartado, con la rotura de quiste ovárico, con el trabajo de parto y, fundamentalmente, con la apendicitis.
El tratamiento requiere una correcta reposición hídrica y el inicio inmediato de antibioterapia de forma empírica, en ambos casos por vía intravenosa. En la actualidad no se recomienda, en nuestro medio, utilizar empíricamente la ampicilina ni las cefalosporinas de primera generación por las elevadas tasas de resistencia. Las principales opciones terapéuticas se exponen en la tabla 5. Se recomienda la hospitalización de la paciente, al menos durante las primeras 48 h, hasta poder cambiar a la vía oral y excluir la presencia de complicaciones, ya que tras este tiempo las pacientes suelen encontrarse asintomáticas y apiréticas. De no ser así, debe sospecharse resistencia a los antibióticos o complicaciones urinarias (nefrolitiasis, absceso renal, obstrucción).
Varios estudios actuales defienden el tratamiento ambulatorio de las PA en embarazadas en casos seleccionados, mediante la administración intramuscular de ceftriaxona (1-2 g) y la observación de la paciente durante unas horas 53,54. Consideramos que esta actitud puede ser correcta si se seleccionan bien los casos 7 (tabla 6) y se dispone de infraestructura para el control domiciliario o en hospital de día.
Correspondencia:
Dr. M.A. Herráiz-Martínez.
Departamento de Obstetricia y Ginecología. Hospital Clínico San Carlos.
Prof. Martín Lagos, s/n. 28040 Madrid. España.
Correo electrónico: maherraizm@meditex.es