La simplificación del tratamiento antirretroviral es una estrategia útil para mejorar la adherencia, la calidad de vida, y prevenir o revertir efectos secundarios en los pacientes con infección por el virus de la inmunodeficiencia humana. La disponibilidad de nuevos fármacos con alta eficacia y mejor tolerados, en presentaciones 1 vez al día o en combinación a dosis fija, puede ofrecer una mejor opción para un tratamiento prolongado. Rilpivirina, un nuevo no análogo de nucleósido, ha demostrado alta eficacia antiviral en ensayos clínicos en pacientes naïve, con menor incidencia de efectos adversos y buena tolerancia del paciente. Su uso en simplificación ha sido evaluado tras el cambio desde efavirenz, demostrando que no precisa ajuste de dosis, y en un amplio estudio aleatorizado en pacientes que recibían inhibidores de la proteasa, con mantenimiento de la eficacia virológica, menor incidencia de efectos adversos, y mejoría en los parámetros lipídicos y en el cálculo de riesgo cardiovascular. Dada la comodidad de uso y la tolerancia, recientes comunicaciones a congresos demuestran la rápida aplicabilidad de los resultados de estudios en la clínica diaria en este escenario.
Antiretroviral simplification is a useful strategy to improve adherence and quality of life and prevent or reverse adverse effects in patients with HIV infection. The availability of new drugs with high efficacy and better tolerability in once-daily formulations or in fixed-dose combinations may be a better option for prolonged treatment. Rilpivirine, a new nonnucleoside reverse transcriptase inhibitor (NNRTI), has shown high antiviral efficacy in clinical trials with treatment-naïve patients, with a lower incidence of adverse effects and good tolerability. Its use in simplification regimens has been evaluated after the switch from efavirenz, demonstrating that dose adjustment is not required. In a large randomized study in patients who were receiving protease inhibitors, virological efficacy was maintained, with a lower incidence of adverse effects and improved lipid parameters and cardiovascular risk score. Given the ease of administration and good tolerability of this drug, recent communications at congresses have shown the rapid applicability of the results of studies in daily clinical practice in this scenario.
El tratamiento antirretroviral de gran actividad (TARGA) ha producido una impresionante disminución de la morbilidad y mortalidad en pacientes con infección por el virus de la inmunodeficiencia humana (VIH)1. Sin embargo se ha mostrado incapaz de erradicar la infección2–4, y el TAR debe utilizarse de forma indefinida para conseguir una supresión mantenida de la replicación viral. Por ello, el desarrollo de efectos adversos, la intolerancia y las dificultades para cumplir correctamente con la medicación son las causas más frecuentes de fracaso del TAR5–7. Este último aspecto, la adherencia al TARGA, es indispensable para alcanzar una buena eficacia terapéutica a largo plazo. El problema del cumplimiento terapéutico es multifactorial, y resultan fundamentales la simplicidad y la ausencia de toxicidad del tratamiento6,8, aspectos que se relacionan directamente con la calidad de vida del paciente. Una característica favorable de los fármacos es la vida media prolongada, que permite reducir el número de tomas de medicación y confiere un margen de “perdón” en el caso de olvido o retraso en la toma9. Una importante estrategia adicional, para facilitar el cumplimiento de la medicación, es la formulación de varios principios activos en un solo comprimido en las llamadas combinaciones a dosis fijas (CDF, o en inglés STR, single tablet regimen)10. Todos estos factores, tratamiento de por vida, necesidad de adherencia casi perfecta, mejoría de la calidad de vida y evitar efectos adversos, y disponibilidad de nuevos fármacos con ventajas en número de tomas, pastillas o tolerancia, han hecho que la estrategia de simplificación del tratamiento continúe siendo una relevante estrategia terapéutica.
Concepto y objetivos de la simplificaciónDe acuerdo con las recomendaciones nacionales formuladas por el grupo de expertos españoles de GeSIDA (Grupo de Estudio de SIDA)11, se entiende por simplificación del TARGA el cambio de un esquema terapéutico que ha conseguido una adecuada respuesta virológica e inmunológica por otro más sencillo que mantiene la supresión de la replicación viral y, al mismo tiempo, facilita la adherencia y mejora la calidad de vida del paciente. La importancia de conseguir un régimen sencillo ha sido recogida incluso en los puntos de ONUSIDA en su informe “Tratamiento 2.0”12.
Un tratamiento más sencillo implica un menor número de fármacos, de pastillas, de tomas al día y/o de restricciones alimentarias.
Algunos autores incluyen en simplificación el concepto de prevenir la aparición o revertir la presencia de toxicidad de laboratorio (p. ej., hiperlipidemia), o efectos leves/moderados que afectan la calidad de vida del paciente y pueden empeorar la adherencia y la eficacia a medio o largo plazo, así como aumentar los riesgos asociados a la edad. De hecho, la mayoría de los estudios de simplificación incluyen el cambio ante efectos adversos que pueden beneficiar al paciente, como los lípidos y el riesgo cardiovascular, la función renal, ósea, o los beneficios sobre efectos adversos del sistema nervioso central.
Estrategias de simplificaciónEn varios estudios se ha demostrado que la adherencia al TARGA se relaciona claramente con el número de comprimidos y con el número de tomas al día13. Pero hay que tener en cuenta que las características individuales y las preferencias de cada paciente pueden ser muy diferentes. En general, cuanto más simple es el tratamiento más fácilmente podrá adaptarse a las necesidades del paciente; sin embargo, para algunos será más importante reducir el número de comprimidos y para otros el número de tomas al día. En este sentido es de primordial importancia explicar detalladamente las características de las diferentes posibilidades terapéuticas para poder elegir conjuntamente, médico y paciente, el tratamiento de simplificación más conveniente.
La reducción del número de fármacos se ha explorado recientemente en la simplificación a monoterapia con un inhibidor de la proteasa potenciado con ritonavir (IP/r), tras un período de inducción con triple terapia con pautas que incluyen análogos de nucleósidos, o el mantenimiento con triple terapia con 2 análogos y un IP no potenciado (atazanavir [ATV]), con retirada de ritonavir después de un período de inducción con IP/r (ATV/r)14,15. La reducción del número de tomas, pasando a una terapia 1 vez al día (QD), se ha demostrado en otras enfermedades crónicas, donde la adherencia media de los tratamientos 1, 2, 3 y 4 veces al día es del 79, 69, 65 y 51%, respectivamente16. Una sola dosis diaria también facilita la regularidad horaria en la ingesta del tratamiento, evita errores de prescripción o confusiones del paciente. Múltiples estudios demuestran que las pautas QD mejoran la adherencia de forma significativa en pacientes VIH+, incluso en comparación con regímenes administrados 2 veces al día13,17.
Es de destacar que la simplificación a terapias en comprimido único, QD, reúne todas las ventajas que buscamos en reducción de fármacos (menos cajas), número de pastillas y de tomas. Por ello, todos los estudios de simplificación a dicho regimen han demostrado un beneficio añadido, que llega a incluir menor hospitalización, incluso cuando se compara con recibir los mismos fármacos de forma separada y, por tanto, no se podía esperar cambios en los efectos adversos18. Hasta el momento, solo se disponía de una presentación en pastilla única (tenofovir [TDF]/emtricitabina [FTC]/efavirenz [EFV]), y estudios de simplificación aleatorizados han demostrado no inferioridad, con mejoría de calidad de vida, adherencia y satisfacción del tratamiento, con mayor preferencia del paciente10.
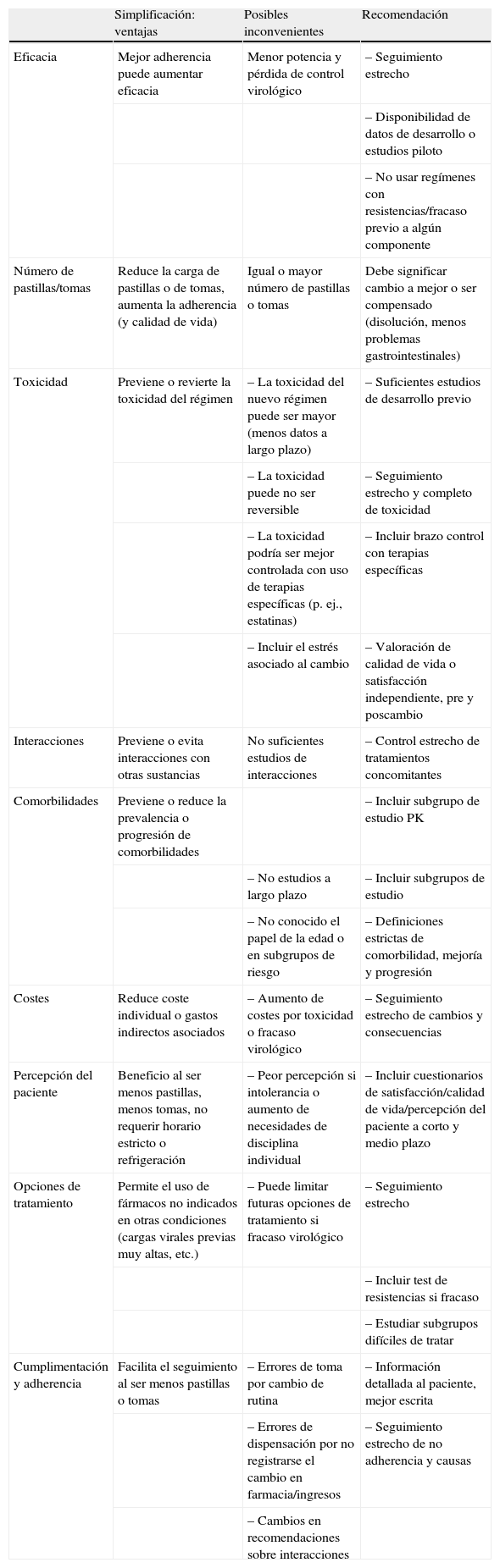
Consideraciones sobre simplificaciónEn los últimos años, y ante la llegada de nuevos fármacos, varios autores han remarcado las limitaciones que tienen los estudios de simplificación19. Dado que los pacientes candidatos a simplificación ya están recibiendo un tratamiento adecuado, que por definición mantiene la supresión virológica, los diseños de no inferioridad de dichos estudios, con su intervalo de confianza (IC) estadístico, pueden reflejar un riesgo para el paciente, que se somete a un estudio donde no se conoce si tendrá igual eficacia el nuevo fármaco, posibles efectos secundarios y fracaso. Por ello se recomienda que los pacientes sean informados adecuadamente sobre el potencial perjuicio, y no solo sobre falta de beneficio si todo continúa igual. Todos los estudios deberían incluir no solo la variable de eficacia “no-inferioridad” como end-point primario, sino objetivos secundarios serios y bien definidos para demostrar que la simplificación a ese régimen puede aportar beneficios adicionales y no solo el cambio de número de tomas o número de pastillas. Ejemplos que se han dado como estudios de simplificación fallidos son conocidos, como el estudio Switchmrk, donde el cambio a raltegravir se asoció a mayor tasa de fracaso virológico frente a continuar con el mismo IP, o los estudios donde se utilizó abacavir como tercer fármaco, con mayor tasa de fracaso virológico por resistencias a los análogos acompañantes. Con esta idea en mente, en la tabla 1 se muestran los beneficios y riesgos potenciales, y las recomendaciones sobre variables a ser incluidas en estudios de simplificación. Es lógico pensar, con lo expuesto, que los estudios de simplificación serían más útiles y deberían realizarse especialmente con los fármacos o regímenes con potencial para producir un beneficio significativo en varios aspectos como adherencia, calidad de vida, efectos adversos y tolerancia, sin menoscabar la eficacia del régimen que el paciente está recibiendo. Todas estas características se han descrito con rilpivirina (RPV).
Potenciales ventajas, inconvenientes y recomendaciones de los estudios de simplificación o cambio por toxicidad
| Simplificación: ventajas | Posibles inconvenientes | Recomendación | |
| Eficacia | Mejor adherencia puede aumentar eficacia | Menor potencia y pérdida de control virológico | – Seguimiento estrecho |
| – Disponibilidad de datos de desarrollo o estudios piloto | |||
| – No usar regímenes con resistencias/fracaso previo a algún componente | |||
| Número de pastillas/tomas | Reduce la carga de pastillas o de tomas, aumenta la adherencia (y calidad de vida) | Igual o mayor número de pastillas o tomas | Debe significar cambio a mejor o ser compensado (disolución, menos problemas gastrointestinales) |
| Toxicidad | Previene o revierte la toxicidad del régimen | – La toxicidad del nuevo régimen puede ser mayor (menos datos a largo plazo) | – Suficientes estudios de desarrollo previo |
| – La toxicidad puede no ser reversible | – Seguimiento estrecho y completo de toxicidad | ||
| – La toxicidad podría ser mejor controlada con uso de terapias específicas (p. ej., estatinas) | – Incluir brazo control con terapias específicas | ||
| – Incluir el estrés asociado al cambio | – Valoración de calidad de vida o satisfacción independiente, pre y poscambio | ||
| Interacciones | Previene o evita interacciones con otras sustancias | No suficientes estudios de interacciones | – Control estrecho de tratamientos concomitantes |
| Comorbilidades | Previene o reduce la prevalencia o progresión de comorbilidades | – Incluir subgrupo de estudio PK | |
| – No estudios a largo plazo | – Incluir subgrupos de estudio | ||
| – No conocido el papel de la edad o en subgrupos de riesgo | – Definiciones estrictas de comorbilidad, mejoría y progresión | ||
| Costes | Reduce coste individual o gastos indirectos asociados | – Aumento de costes por toxicidad o fracaso virológico | – Seguimiento estrecho de cambios y consecuencias |
| Percepción del paciente | Beneficio al ser menos pastillas, menos tomas, no requerir horario estricto o refrigeración | – Peor percepción si intolerancia o aumento de necesidades de disciplina individual | – Incluir cuestionarios de satisfacción/calidad de vida/percepción del paciente a corto y medio plazo |
| Opciones de tratamiento | Permite el uso de fármacos no indicados en otras condiciones (cargas virales previas muy altas, etc.) | – Puede limitar futuras opciones de tratamiento si fracaso virológico | – Seguimiento estrecho |
| – Incluir test de resistencias si fracaso | |||
| – Estudiar subgrupos difíciles de tratar | |||
| Cumplimentación y adherencia | Facilita el seguimiento al ser menos pastillas o tomas | – Errores de toma por cambio de rutina | – Información detallada al paciente, mejor escrita |
| – Errores de dispensación por no registrarse el cambio en farmacia/ingresos | – Seguimiento estrecho de no adherencia y causas | ||
| – Cambios en recomendaciones sobre interacciones |
RPV es un nuevo fármaco no análogo de nucleósido recientemente introducido en el arsenal terapéutico. Su larga vida media permite su administración QD, y se ha desarrollado una CDF para comercialización junto con TDF y FTC. En los estudios en fase IIb de búsqueda de dosis se demostró que 25mg al día producían igual eficacia clínica sin más efectos adversos que dosis mayores, y esta fue la dosis elegida para estudios en fase III, que han demostrado una alta eficacia antiviral. Ha demostrado una toxicidad significativamente menor que EFV a nivel neuropsiquiátrico y lipídico, menor frecuencia de exantema que otros no análogos, y no se ha descrito la aparición de efectos adversos específicos. Como limitaciones, además de la mayor tasa de fracaso virológico en pacientes naïve con cargas virales muy elevadas, se ha demostrado un descenso de los valores plasmáticos de alrededor del 40% cuando se administra junto con inhibidores de la bomba de protones, y una menor absorción si se ingiere en ayunas. Aunque ambos son estudios farmacocinéticos, parece recomendable tenerlos en consideración para asegurar la eficacia virológica. RPV es un inhibidor leve de la secreción tubular de creatinina a nivel de las células del túbulo renal, por lo que puede haber ligeros cambios en la creatinina sérica o en el filtrado glomerular sin significación clínica. Dada su principal característica, su excelente tolerancia y baja toxicidad, era de esperar que se desarrollaran estudios sobre su papel en simplificación20.
Estudios de simplificación con rilpivirinaRPV cumple muchas de las premisas formuladas en las consideraciones sobre fármacos para simplificación: adecuada eficacia virológica, menor tasa de efectos adversos, buena tolerancia, interacciones conocidas, vida media prolongada y posibilidad de administración en CDF. Hasta el momento se han comunicado 2 estudios sobre cambio de tratamiento a este fármaco, desde EFV y desde IP, que nos ayudan a situar en su justo alcance esta estrategia.
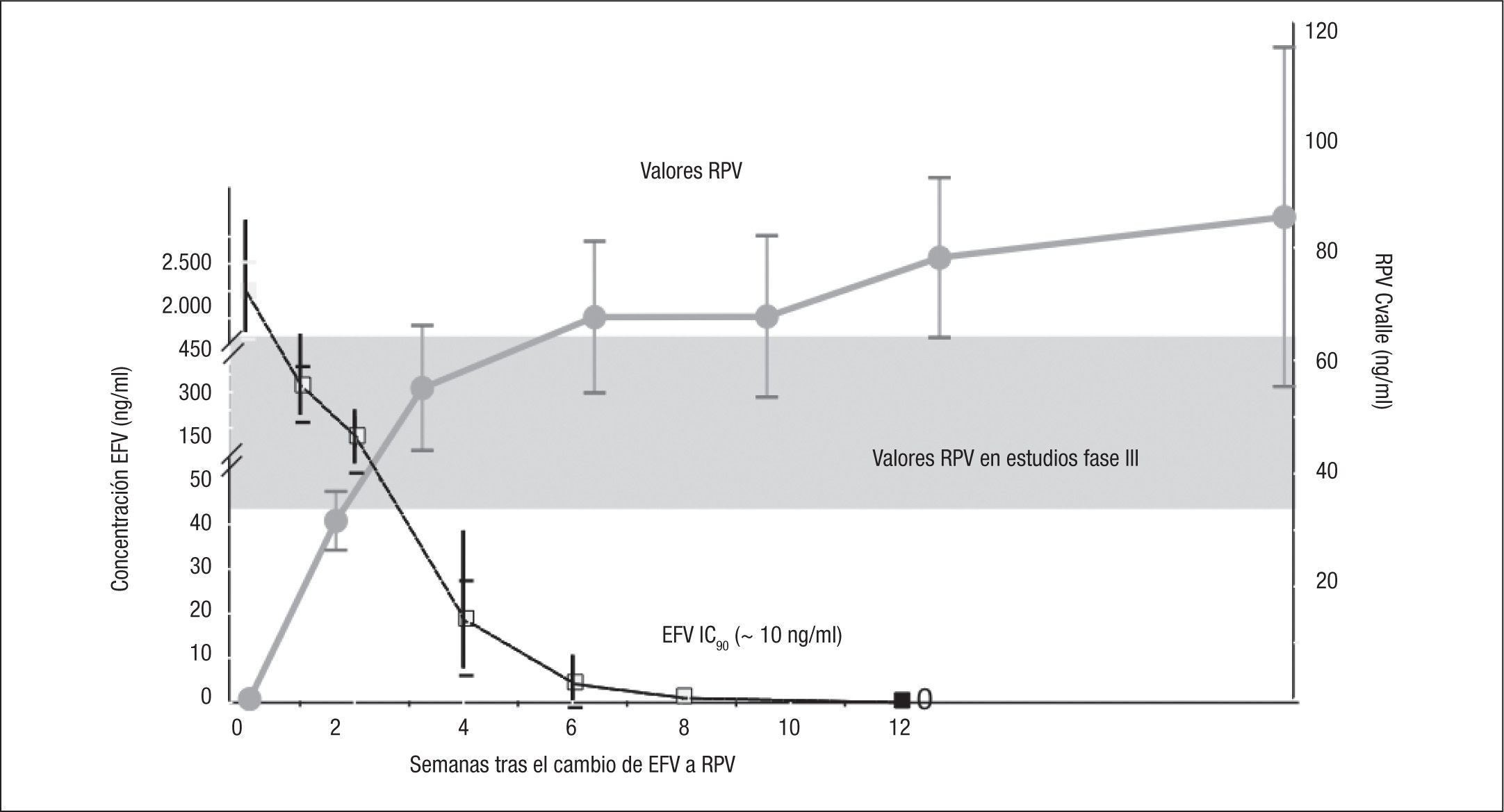
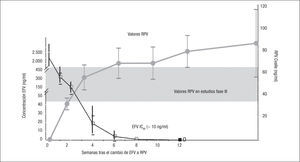
El estudio GS 264-111 fue un estudio fase IIb abierto, no aleatorizado, incluyendo parámetros farmacocinéticos, de cambio de EFV a RPV, ambos en CDF junto con TDF/FTC21. El objetivo fue evaluar el efecto que podía tener sobre los valores plasmáticos de RPV la persistencia del efecto inductor de EFV tras su retirada, tras haberse demostrado en voluntarios sanos un descenso del 10–25% de la concentración valle (Cvalle) durante 4 semanas tras el cambio. En este estudio, pacientes que recibían EFV al menos 3 meses, con más de 8 semanas de carga viral indetectable, sin resistencias genotípicas y con un filtrado glomerular > 50ml/min, se cambiaron a RPV con evaluación a las 12, 24 y 48 semanas. El objetivo primario fue el porcentaje de pacientes con carga viral < 50 copias/ml a las 12 semanas del cambio, mientras que los secundarios fueron la seguridad, la persistencia de indetectabilidad a las 24 y 48 semanas, y las modificaciones de los valores plasmáticos. Se incluyeron 50 pacientes, pero 1 abandonó antes de recibir RPV. A las 12 semanas, el 100% de los pacientes continuaban indetectables, cifra que se mantenía a las 24 semanas. El estudio farmacocinético demostró que los valores medianos de la Cvalle de RPV a las 2 semanas del cambio fue 52ng/ml, y a las 4 semanas osciló entre 66 y 84ng/ml, ambos puntos de corte dentro del rango observado en los estudios en pacientes naïve (fig. 1). No hubo efectos adversos grados 3–4, ningún paciente tuvo que interrumpir el tratamiento y las cifras de creatinina no cambiaron de forma significativa (aumento medio de 0,11mg/dl en la semana 12). Como conclusión, este estudio demuestra que no es necesario el ajuste de dosis de RPV cuando se utiliza como simplificación a EFV, con buena tolerancia y mantenimiento de la eficacia, aunque no existía un grupo control.
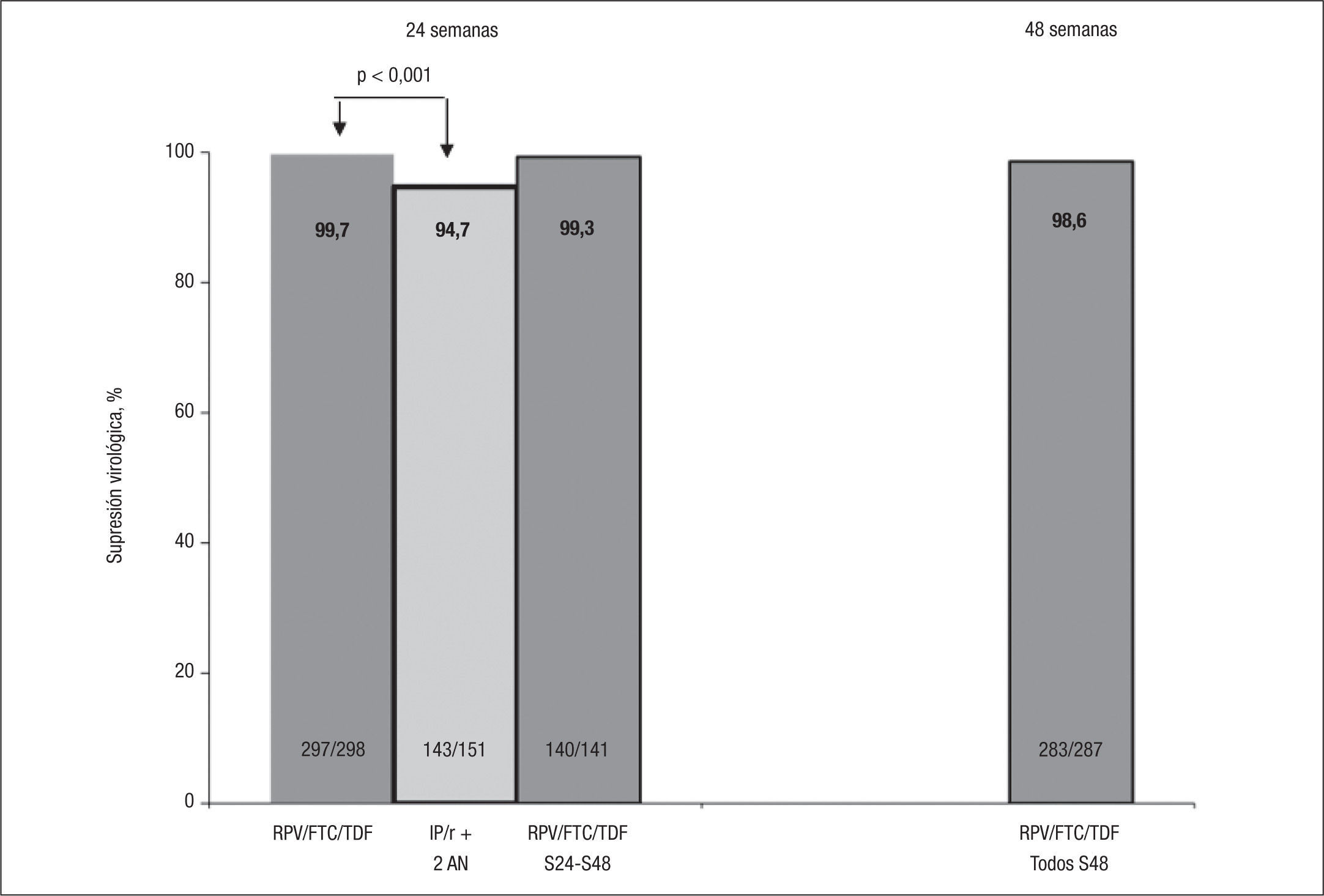
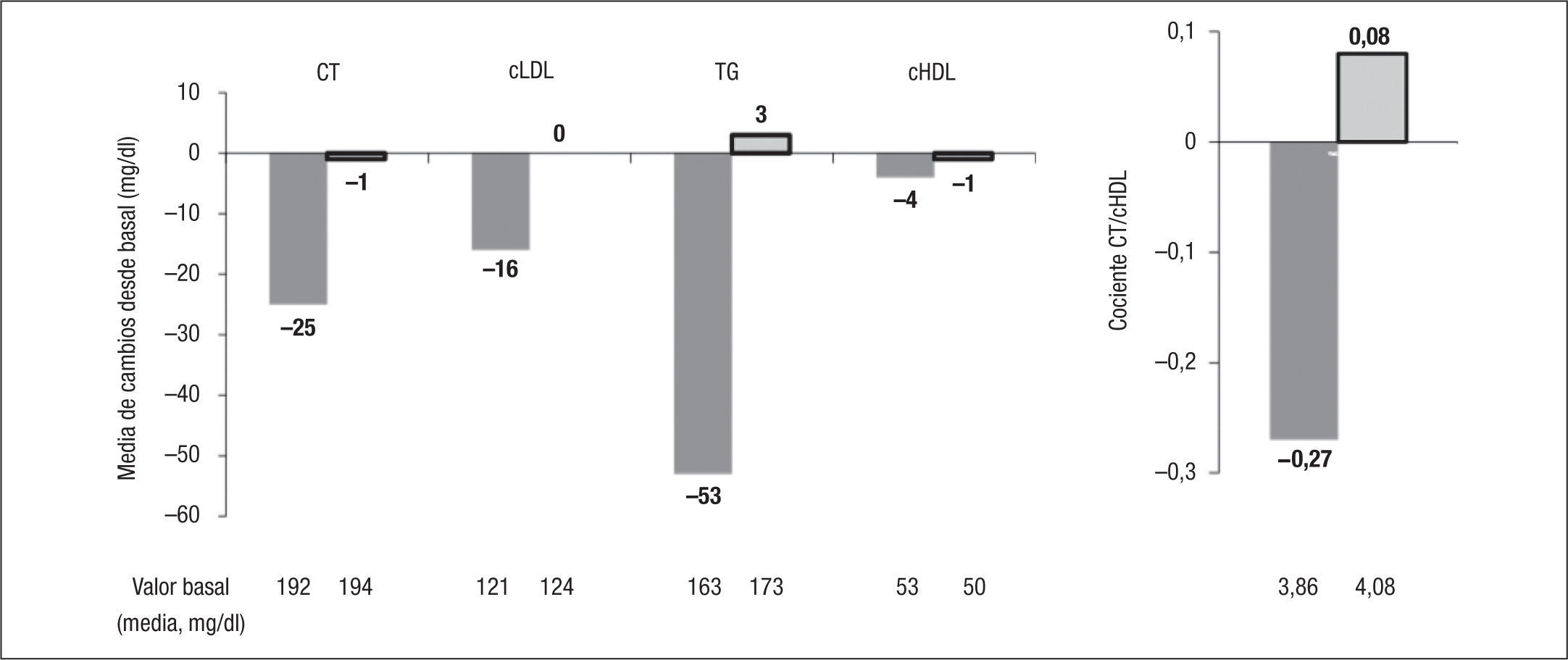
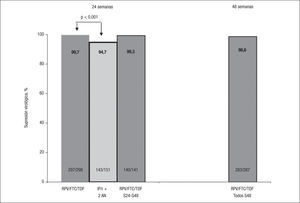
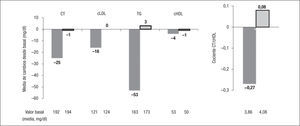
Para estudiar la simplificación a una pauta con una coformulación a dosis fijas de RPV/TDF/FTC desde un régimen basado en IP se ha llevado a cabo el estudio SPIRIT (Switching boosted PI to Rilpivirine In Combination with Truvada as a Single Tablet Regimen). Se trata de un ensayo clínico abierto, aleatorizado, en pacientes con supresión de la replicación viral durante al menos 6 meses, con un régimen de un IP/r + 2 análogos de nucleósidos18. No se incluyeron en él pacientes que hubiesen recibido previamente fármacos no análogos de nucleósidos o tuviesen resistencia genotípica conocida frente a estos fármacos, ni que hubiesen sido tratados previamente con más de 2 pautas distintas de antirretrovirales. Los 476 pacientes incluidos fueron aleatorizados a razón 2:1 a recibir RPV/TDF/FTC o a continuar con la pauta previa. El 37% de los pacientes estaba recibiendo ATV/r, el 33% lopinavir (LPV/r) y el 20% darunavir (DRV/r), y desde el punto de vista de análogos de nucleósidos, el 81% ya recibía TDF/FTC. El objetivo principal del estudio fue demostrar la no inferioridad (± 12%) de la simplificación a RPV/TDF/FTC en la semana 24 (por análisis snapshot de la FDA). Como objetivos secundarios se contemplaron la seguridad y tolerancia, los cambios en los parámetros lipídicos y el cambio en CD4, todo ello a las 24 y 48 semanas. En el análisis a la semana 24, el 94% de pacientes en el grupo de RPV y el 90% en el grupo de IP mantenían carga vira indetectable (IC del 95%, −2,0% a +8,9%), con un 0,9 y un 5% presentando fracaso virológico, respectivamente (fig. 2). Esta diferencia fue significativa entre ambos grupos (el 99,7 frente al 94,7%; p<0,01) cuando se excluía a los pacientes en tratamiento y sin datos a la semana 24. De forma llamativa, no hubo diferencias cuando se consideró el efecto de la carga viral elevada (mayor o menor de 100.000 copias/ml) pretratamiento, y todos los pacientes con la mutación K103N previa (17 pacientes) mantuvieron carga viral indetectable. Los efectos adversos grados 3–4 fueron poco frecuentes en ambos grupos (el 5 frente al 6,4%), al igual que las anomalías de laboratorio (el 6,3 frente al 11,3%) y, en todo caso, favorables al nuevo régimen. Uno de los objetivos secundarios, el cambio en los valores de lípidos en ayunas, demostró beneficio significativo en el grupo que pasó a RPV en las cifras de colesterol total (media, −25mg/dl), colesterol unido a lipoproteínas de baja densidad (cLDL) (−16mg/dl) y triglicéridos (−53mg/dl) (fig. 3). De este modo, durante el estudio, el cociente colesterol total/colesterol unido a lipoproteínas de alta densidad (cHDL) descendió 0,27 en el grupo de RPV y se elevó 0,08 en el grupo que continuaba con IP. Estos cambios se tradujeron en un beneficio en el cálculo de riesgo cardiovascular a 10 años por la escala de Framingham (fig. 3). Los pacientes que recibían RPV tuvieron un descenso leve (−4ml/min), aunque significativo, en el cálculo del filtrado glomerular. En el grupo de RPV/TDF/FTC se registraron menos acontecimientos adversos gastrointestinales. Igualmente se incluyeron subestudios sobre satisfacción con el tratamiento y síntomas relacionados con el VIH o con el tratamiento, con mejorías significativas tras el cambio a RPV. En la continuación del estudio a la semana 48, con todos los pacientes ya recibiendo RPV en CDF, la eficacia fue similar a la observada en el grupo de RPV a la semana 24 (fig. 2).
Respuesta virológica (porcentaje de supresión virológica por “snapshot”) a las semanas 24 y 48 tras el cambio de inhibidores de la proteasa (IP) potenciados a la combinación en dosis fija de rilpivirina (RPV) (TDF/FTC/RPV) en el estudio SPIRIT. FTC: emtricitabina; r: ritonavir; TDF: tenofovir.
Cambios medios en lípidos tras el cambio de inhibidor de la proteasa potenciado a rilpivirina (RPV). Datos a 24 semanas. cHDL: colesterol unido a lipoproteínas de alta densidad; cLDL: colesterol unido a lipoproteínas de baja densidad; CT: colesterol total; TG: triglicéridos. p<0,001 en todas las comparaciones.
Dada su tolerancia, y su comercialización hace más de 1 año en distintos países, RPV ha sido incorporada a estrategias de simplificación en la práctica clínica. En el reciente congreso de Glasgow, autores americanos comentaban su experiencia con 111 pacientes simplificados a RPV en CDF desde EFV o IP22. Como era de esperar, la tolerancia fue muy buena, solo un paciente tuvo fracaso virológico, y a las 24 semanas ningún paciente había discontinuado por efectos adversos. Es de destacar que se utilizó en pacientes con cargas virales pretratamiento > 100.000 copias/ml e incluso con fracaso previo a no análogos y presencia de la mutación K103N (5 pacientes), en los que no hubo casos de fracaso. Similares resultados han sido reportados por otros autores. Cevik et al23 refieren su uso en 65 pacientes, en 56 casos en simplificación, de los que 54 continuaban indetectables a las 12 semanas. En ambos estudios hubo mejoría de las cifras de lípidos y, llamativamente, la mayor parte de los pacientes estaba recibiendo una terapia basada en EFV antes del cambio.
Potenciales usosPor todo lo referido, el uso de RPV podría ser una opción para la simplificación del régimen antirretroviral en muchos supuestos, que sin ánimo de ser exhaustivos se recogen en la tabla 2. Uno de los inconvenientes encontrados en los estudios en pacientes naïve, la mayor tasa de fracaso virológico en aquellos con carga viral alta, no debería ser un problema en pacientes que ya presentan supresión virológica, como se observa en los estudios arriba mencionados, y por tanto el cambio ofrece la posibilidad de recibir un régimen eficaz, cómodo y con buen perfil de tolerancia.
Potenciales indicaciones de rilpivirina como estrategia de simplificación
| Pacientes en tratamiento, con supresión virológica, y: |
| 1. Problemas de toma o número de pastillas |
| – Pacientes con problemas de toma por horario laboral o con cambios frecuentes |
| – Quejas sobre el número de pastillas o el número de tomas que complique la adherencia o disminuya la calidad de vida |
| 2. Efectos adversos/tolerancia |
| – Efectos adversos del SNC que dificulten la adherencia o disminuyan la calidad de vida |
| – Hiperlipidemia o riesgo cardiovascular elevado, con difícil control |
| – Intolerancia gastrointestinal |
| – Problemas de tolerancia subjetiva (malestar, diarrea ocasional, etc.) |
SNC: sistema nervioso central.
La simplificación continúa siendo una estrategia útil para mejorar la adherencia, la calidad de vida y prevenir o revertir efectos secundarios o intolerancia a las terapias actuales. A pesar de los avances en el TAR, disponer de fármacos mejor tolerados en dosis QD o coformulados puede conseguir disminuir los cambios y fracasos del tratamiento que se observan actualmente. En este sentido, RPV, tanto en CDF como fármaco independiente, ha demostrado similar eficacia virológica en comparación con EFV, con una mejor tolerancia. Su única limitación en pacientes naïve, su mayor tasa de fracaso virológico en aquellos con cargas virales muy elevadas, no se aplicaría en el caso de simplificación, donde los pacientes se encuentran con carga viral suprimida, y refuerza esta estrategia como una potencial indicación de este fármaco.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.