Comisión de Expertos* del Grupo de Trabajo de Enfermedades Infecciosas de la Sociedad Española de Medicina Intensiva, Crítica y Unidades Coronarias (GTEI-SEMICYUC), Área de Trabajo de Tuberculosis e Infecciones Respiratorias de la Sociedad Española de Patología del Aparato Respiratorio (TIR-SEPAR) y Grupo de Estudio de Infección Hospitalaria de la Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica (GEIH-SEIMC)*
*La relación de participantes en la comisión de expertos se expone al final del artículo. El grupo de expertos ha contado con la colaboración de los laboratorios Wyeth Farma, España, para la realización de las reuniones de trabajo.
Introducción
El retraso en la instauración de un tratamiento antibiótico adecuado para la neumonía intrahospitalaria grave (NIG) se acompaña de un peor pronóstico1-6, además de una prolongación de la estancia hospitalaria y, por tanto, de un incremento de los costes. Por otra parte, en el ámbito de las neumonías asociadas a la ventilación mecánica (NAVM), la modificación de una terapia antibiótica empírica inadecuada una vez se ha aislado el microorganismo causante de la infección no mejora significativamente la mala evolución inicial1,2. Parece pues evidente que la adecuada elección de la antibioticoterapia empírica es uno de los pocos factores pronósticos de mortalidad de la NIG que pueden ser modificados. Por contra, hay que tener en cuenta que el uso indiscriminado de antibióticos y la excesiva duración de los tratamientos pueden acompañarse de aparición de flora emergente multirresistente con la consiguiente repercusión en las políticas antibióticas de los hospitales.
Metodología
Se constituyó un equipo de trabajo (task force) formado por expertos en enfermedad infecciosa del paciente crítico pertenecientes a las 3 sociedades científicas promotoras del proyecto. Se incluyeron los siguientes temas relacionados con el tratamiento de las NIG:
1. Revisión crítica de las guías existentes y definición de los grupos de riesgo.
2. Criterios de ingreso en la unidad de cuidados intensivos (UCI de las NIG).
3. Tratamiento de la NIG en función de los grupos de riesgo.
4. Situaciones especiales en el tratamiento de las NIG.
5. Controles durante el tratamiento.
A partir de una propuesta inicial, basada en una revisión de la bibliografía, se elaboraron diversos borradores que fueron mejorados tras su debate por los miembros de la task force hasta llegar al documento final. El criterio general fue la elaboración de unas guías para el uso racional de los antibióticos de forma rutinaria, tanto en su forma empírica como orientada por antibiograma, dirigidas a todos los profesionales que atienden a pacientes con riesgo de sufrir una neumonía dentro del hospital, al margen del nivel asistencial del hospital en que realizan su trabajo. Este documento incluye el grado de acuerdo de los participantes en la reunión final en cada una de las recomendaciones, aunque en algunas de ellas se abstuvieron los que carecían de experiencia personal.
Las recomendaciones, que se proponen a continuación, se han clasificado, atendiendo a criterios de calidad de la evidencia7, en los siguientes niveles:
1. Recomendaciones basadas de forma directa en evidencias científicas.
2. Recomendaciones basadas en evidencias científicas complementadas con opiniones de expertos.
3. Recomendaciones sólo basadas en opiniones de expertos.
4. Recomendaciones sin evidencias científicas ni opinión de expertos.
Estas recomendaciones no hacen referencia a niños, ya que las características propias de dicha población requieren un tratamiento específico.
Protocolos terapéuticos de neumonía nosocomial de sociedades científicas. Definición de los grupos de riesgo
En la última década, la investigación clínica de la neumonía intrahospitalaria (NIH) ha aportado una gran información en aspectos de su patogénesis, diagnóstico, terapéutica y prevención. La necesidad de agrupar de forma sistematizada todos los conceptos aprendidos dio paso a la publicación de 2 normativas: la primera, en 1996, fue el resultado de una reunión de expertos de la American Thoracic Society (ATS)8 y la segunda, publicada un año más tarde, estuvo patrocinada por la Sociedad Española de Neumología y Cirugía Torácica (SEPAR)9.
En la primera de ellas se afirmaba que el manejo adecuado de la NIH requiere de una colaboración estrecha entre neumólogos, intensivistas y especialistas en enfermedades infecciosas, lo que refleja el espíritu del presente documento. Ambas normativas sentaron las bases de la estratificación de los pacientes de acuerdo con las principales variables que condicionan la etiología de la NIH y, consecuentemente, su tratamiento adecuado. En este apartado se efectúa un resumen de las recomendaciones para el tratamiento empírico de las NIH de las 2 normativas anteriores8,9.
Recomendaciones de la American Thoracic Society8
El espectro de los microorganismos patógenos en la NIH está condicionado por una variedad de factores que incluyen la gravedad de la neumonía, la presencia de factores de riesgo relacionados con una posible causalidad de microorganismos específicos y el período de la estancia hospitalaria previo a la aparición de la neumonía. Se ha confirmado que estas 3 variables determinan de forma bastante adecuada los microorganismos causales de NIH.
La gravedad de la neumonía se definió con la presencia de alguno de los siguientes signos o síntomas: ingreso en UCI; insuficiencia respiratoria grave (necesidad de ventilación mecánica y necesidad de una fracción de oxígeno inspirado (FiO2) > 35% para mantener una saturación arterial de oxígeno (SaO2) > 90%); progresión radiográfica o cavitación o afección multilobular; y evidencia de sepsis grave con hipotensión o disfunción orgánica (presión arterial [PA] sistólica < 90 mmHg o PA diastólica < 60 mmHg, necesidad de drogas vasopresoras > 4 h, volumen urinario < 20 ml/h u 80 ml/4 h, fallo renal agudo con necesidad de hemodiálisis). Estas variables definitorias de gravedad se extrapolaron de las normativas de la ATS para la neumonía adquirida en la comunidad publicadas en 199310 y no han sido validadas específicamente para la NIH.
La segunda variable considerada fue la presencia de factores de riesgo específico para determinados microorganismos que se detallan a continuación: a) microorganismos anaerobios: cirugía abdominal reciente o aspiración a las vías aéreas; b) S. aureus: presencia de coma o traumatismo craneal, diabetes mellitus o fracaso renal; c) Legionella spp.: dosis altas de glucocorticoides, y d) P. aeruginosa: estancia en UCI prolongada, utilización de glucocorticoides o antibióticos de amplio espectro, o enfermedad pulmonar estructural.
Finalmente, la última variable a tener en cuenta fue la estancia hospitalaria previa. El punto de corte escogido fue de 5 días para clasificar a las neumonías en precoces (< 5 días) o tardías (≥ 5 días) ya que se ha demostrado que la colonización anómala por flora intrahospitalaria de la orofaringe se inicia a partir de los 5 días de ingreso.
Con estas 3 variables puede establecerse una clasificación de los pacientes en 3 grupos, a efectos de los microorganismos potencialmente causales y, en consecuencia, del tratamiento empírico a aplicar:
Grupo I: pacientes con NIH no grave y sin factores de riesgo, independientemente del período de inicio, o bien pacientes con NIH de inicio temprano, cuyos microorganismos potencialmente causales corresponderían a Streptococcus pneumoniae; Haemophilus influenzae; S. aureus sensible a meticilina (SASM) o a bacilos gramnegativos (BGN) entéricos tipo Escherichia coli, Klebsiella pneumoniae, Proteus spp. o Enterobacter spp. Este conjunto de microorganismos se considera potencialmente infectante en cualquiera de los grupos, por lo que se los define como microorganismos principales ("core").
Grupo II: pacientes con NIH no grave con factores de riesgo, independientemente del período de inicio. Se incluyen en este grupo, junto a los microorganismos principales, microorganismos anaerobios en el caso de pacientes postoperados, S. aureus en pacientes con trastornos de la conciencia y Legionella spp. o P. aeruginosa en enfermos en tratamiento con corticoides.
Grupo III: pacientes con NIG con factores de riesgo e inicio temprano o bien con NIG de inicio tardío. La posible etiología debe incluir, además de los microorganismos principales, una serie de microorganismos multirresistentes como P. aeruginosa, Acinetobacter spp. o Staphylococcus aureus resistente a meticilina (SARM).
En las normativas de la ATS se abordaron otros aspectos, como la penetración tisular de los antibióticos, su mecanismo de acción (bactericida o bacteriostático); el efecto postantibiótico de algunos antimicrobianos; la administración de los aminoglucósidos en dosis única; las indicaciones de monoterapia y de terapia combinada; la duración de la terapia antibiótica; la evaluación de la respuesta al tratamiento empírico (patrón de resolución, causas de falta de respuesta y su evaluación). Por la extensión que supondría desarrollar estos apartados referimos al lector a la publicación correspondiente8.
Recomendaciones de la Sociedad Española de Neumología y Cirugía Torácica9
Las recomendaciones de la SEPAR, publicadas un año más tarde que las de la ATS, fueron bastante similares, sin diferencias respecto a los grupos de riesgo y únicamente se realizaron modificaciones en el tratamiento antibiótico a elegir. Por este motivo no volveremos a exponerlas en este apartado.
Conclusiones
1. Las normativas descritas han representado el primer intento de sistematización para el tratamiento empírico de la NIH. Desde su publicación hasta la actualidad han surgido nuevas evidencias científicas que obligan a su puesta al día, aunque los criterios de estratificación de los pacientes no variarían sustancialmente.
2. En estudios recientes11 se ha demostrado que los factores más significativos relacionados con la presencia de microorganismos potencialmente resistentes a los antibióticos son el período de ventilación mecánica y el tipo y la duración de la antibioticoterapia previa.
Recomendaciones
No existen normativas específicas para el tratamiento de la NAVM, como se ha reflejado recientemente en las recomendaciones del Task Force de varias sociedades europeas12. El punto de partida de las recomendaciones para el tratamiento de la NAVM debe ser la estratificación de los pacientes para su tratamiento empírico. Grado de evidencia II. Acuerdo entre expertos 17/17 (100%).
El factor más importante en la etiología de la NAVM es la hospitalización previa. La gravedad de la NAVM no es un factor a considerar en la estratificación, ya que estar intubado y ventilado mecánicamente es en sí mismo un hecho de gravedad. Está claramente demostrado que a partir de los 5 días de hospitalización puede haber un cambio en la flora orofaríngea de los pacientes, y aparecer microorganismos propios de la flora hospitalaria13. Asimismo, otros factores también contribuyen a modificar esta flora colonizante y deben tenerse en cuenta, como la antibioticoterapia en los 15 días previos11 y los factores relacionados con el propio huésped8. Finalmente, es crucial conocer las peculiaridades de la flora de cada unidad14. Grado de evidencia II. Acuerdo entre expertos 17/17 (100%).
De acuerdo con las consideraciones efectuadas en el párrafo anterior se propone la clasificación expuesta en la tabla 1. Cuando los microorganismos potencialmente multirresistentes sean endémicos en una unidad u hospital determinado, ello debe valorarse como un factor de riesgo para aquéllos. Grado de evidencia II. Acuerdo de expertos 16/17 (94%).
Indicaciones de ingreso en la UCI de las neumonías intrahospitalarias
Consideraciones generales
La mayoría de las series de pacientes con NIG presenta un espectro variado de agentes etiológicos. La inestabilidad hemodinámica y la hipoxemia son las 2 causas principales de mortalidad. La identificación temprana de los pacientes con riesgo elevado, basada en los estudios que han identificado factores de mal pronóstico8,15-18, permite la instauración temprana de medidas de soporte y tratamiento específico y la posible reducción de la mortalidad19. Por el contrario, la demora en el inicio de estas medidas se asocia a un peor pronóstico, especialmente una vez se ha instaurado el síndrome del distrés respiratorio agudo (SDRA) o el fallo multiorgánico.
La indicación de cuidados intensivos debe plantearse en los pacientes que puedan beneficiarse de cuidados especiales de carácter médico o de enfermería. Esta indicación no debe demorarse hasta que el paciente tenga criterios de intubación, ya que hoy la instauración de presión positiva de la vía aérea mediante mascarilla de forma temprana puede evitar este procedimiento en pacientes, que por otra parte, requieren de una vigilancia intensiva.
La valoración inicial debe hacerse en base a la frecuencia respiratoria (FR) y una gasometría arterial tras la administración de oxígeno con mascarilla facial a concentraciones adecuadas. La realización de una radiografía de tórax permitirá evaluar la extensión y progresión radiológica.
Indicaciones específicas de ingreso en la UCI
La presencia de cualquiera de las siguientes condiciones, evaluadas recientemente en nuestro país20, justifica la clasificación como neumonía grave y establece la indicación de ingreso en la UCI8,10:
1. Insuficiencia respiratoria grave definida como cualquiera de las siguientes: a) FR mayor de 30 latidos/min; b) imposibilidad de mantener una SaO2 superior al 90% con mascarilla y concentración de oxígeno superior al 35% (excepto pacientes con hipoxemia crónica), o c) necesidad de soporte ventilatorio, por cualquier motivo.
2. Presencia de sepsis grave con hipotensión o disfunción multiorgánica, que se manifiesta por cualquiera de las siguientes: a) presencia de shock (sepsis con hipotensión a pesar de un adecuado aporte de volumen junto con la presencia de hipoperfusión que puede incluir, pero no limitarse, a acidosis láctica, oliguria o una alteración aguda del estado mental); b) necesidad de administrar vasopresores durante más de 4 h (los pacientes que reciben fármacos inotrópicos o vasopresores pueden no tener hipotensión en el momento en que se detectan signos de hipoperfusión periférica), y c) insuficiencia renal aguda que requiere diálisis o diuresis inferior a 0,5 ml/kg/h, una vez descartadas otras causas.
La afección radiológica grave, definida por afección multilobular y progresión de los infiltrados pulmonares superior a un 50% en menos de 48 h, ha sido incluida como indicación de ingreso en la UCI por algunos autores20. Su presencia es un signo de mal pronóstico que obliga al ingreso en la UCI cuando se asocia con alguno de los criterios incluidos en los apartados que acabamos de mencionar21.
Conclusiones
La NIG es una entidad que, por su complejidad y elevada mortalidad, requiere ingreso en la UCI para su control y tratamiento. La definición de NIG viene dada tanto por signos directamente relacionados con la afección del parénquima pulmonar como por la repercusión generada por la situación de sepsis. Su detección y tratamiento temprano se han acompañado de una reducción de la mortalidad. No obstante, la mayoría de las NIG se presentan en las unidades de medicina intensiva y están asociadas al uso de ventilación mecánica.
Recomendaciones
Se recomienda el ingreso temprano en la UCI de las NIG. El retraso en el ingreso aumenta la mortalidad. Grado de evidencia II. Acuerdo entre los expertos 17/17 (100%).
Se considera NIG la que cumple alguno de los siguientes supuestos: FR ≥ 30; SaO2 ≤ 90% con FiO2 > 35%; extensión radiológica en 48 h o afección multilobular; necesidad de ventilación mecánica (invasiva o no invasiva); presencia de sepsis grave o shock séptico o disfunción orgánica distinta de la pulmonar. Grado de evidencia I. Acuerdo entre los expertos 17/17 (100%).
Tratamiento de la neumonía intrahospitalaria grave asociada a ventilación mecánica
Neumonía asociada a ventilación mecánica precoz sin factores de riesgo (grupo I)
Diferentes estudios han mostrado que entre las 48 h y el 5.º día de ingreso, la neumonía es producida mayoritariamente por flora endógena primaria, es decir, S. pneumoniae, H. influenzae y SASM, y enterobacterias tipo E. coli, K. pneumoniae o Enterobacter spp. Probablemente el grupo de pacientes con mayor riesgo para la infección por flora endógena primaria corresponde a los que presentan lesiones neurológicas agudas (traumatismo craneoencefálico y accidente cerebrovascular)22,23, y hay una especial relación entre los pacientes con traumatismo craneoencefálico y la infección/colonización por S. aureus24. La presencia de SARM en las neumonías precoces es excepcional y habrá que tenerla en cuenta únicamente en pacientes seleccionados, con ingresos hospitalarios recientes o procedentes de centros de crónicos.
La mortalidad en la NAVM precoz se sitúa alrededor del 24%25, además de prolongar el tiempo de ventilación mecánica y la estancia en la UCI y, por tanto, los costes26.
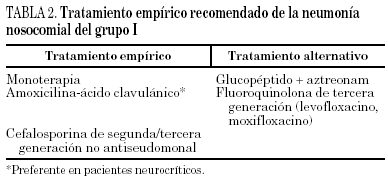
No se dispone de estudios especialmente diseñados para evaluar la eficacia de los diferentes antibióticos en el tratamiento de la neumonía precoz. Las diferentes opciones que se plantean en el tratamiento vienen dadas por opiniones de expertos a través de las diferentes guías terapéuticas editadas por las sociedades científicas27. En este grupo de pacientes, definidos en todos los casos como grupo I de bajo riesgo, se recomienda la administración de monoterapia con amoxicilina-ácido clavulánico o cefuroxima o una cefalosporina de tercera generación sin actividad frente a P. aeruginosa. La terapia combinada no parece necesaria en este grupo de pacientes28. La decisión del régimen antibiótico de elección debe tener en cuenta la progresiva aparición de resistencias a diferentes fármacos en nuestro entorno, sobre todo respecto a S. pneumoniae, H. influenzae y E. coli. En un reciente estudio se pudo observar que el 25% de las cepas de H. influenzae eran productoras de β-lactamasas que en algunas zonas se situaba en el 47,9% de los casos y con resistencias a claritromicina hasta el 22% de las cepas29. Respecto a S. pneumoniae es sobradamente conocido el incremento de resistencia a la penicilina y por extensión a los otros β-lactámicos, aunque suelen tener poca relevancia en la práctica clínica habitual cuando se utilizan estos antibióticos.
En la actualidad está teniendo un importante auge el uso de fluoroquinolonas en el tratamiento de la neumonía grave30, por su actividad in vitro, características farmacocinéticas y penetración en el tejido pulmonar. Sin embargo, su utilización indiscriminada se ha acompañado de la aparición progresiva de resistencias. En un estudio31, 750 mg/12 h de levofloxacino ha demostrado la misma eficacia que imipenem en el tratamiento de la neumonía nosocomial. No obstante, dada la poca homogeneidad de los casos (no son únicamente pacientes ventilados, no diferencia por grupos de riesgo, se precisa añadir nuevos antibióticos frente a gérmenes multirresistentes), es preciso un mayor número de ensayos para su evaluación. Se recomienda su uso en los pacientes con reacciones adversas a los β-lactámicos. La asociación de aztreonam y glucopéptidos ofrece también una adecuada cobertura empírica frente a los microorganismos infectantes y es la recomendación alternativa en este grupo de pacientes.
El tratamiento empírico recomendado para la neumonía precoz se refleja en la tabla 2.
Conclusiones
La neumonía precoz sin factores de riesgo asociados está ocasionada preferentemente por flora endógena primaria, con ausencia de microorganismos multirresistentes. Su presentación ocurre dentro de los primeros 5 días de ingreso y el factor más determinante para la variación de la flora esperada es el uso previo de antibióticos. El progresivo incremento en las resistencias a cefalosporinas y macrólidos de S. pneumoniae y H. influenzae aconseja una cierta precaución en el empleo de estos antibióticos en la terapia empírica de la neumonía precoz. Las quinolonas de tercera generación se presentan como una opción de tratamiento.
Recomendaciones
La neumonía precoz puede tratarse con monoterapia mediante amoxicilina-ácido clavulánico o cefalosporinas, en cuyo caso es preferible el uso de cefalosporinas de tercera generación, a no ser que se tenga conocimiento exacto de las sensibilidades de los microorganismos a las cefalosporinas de segunda generación. Grado de evidencia I. Acuerdo entre los expertos 17/17 (100%).
La utilización de fluoroquinolonas de tercera generación debe contemplarse por el momento como un tratamiento alternativo hasta la aparición de más ensayos que valoren su eficacia. No obstante, y dada la utilidad mostrada en otro tipo de infecciones, puede plantearse como tratamiento alternativo. La asociación de glucopéptidos y aztreonam es recomendada como tratamiento alternativo en caso de reacciones adversas a β -lactámicos. Grado de evidencia III. Acuerdo de expertos 16/17 (93%).
Neumonía asociada a ventilación mecánica precoz con factores de riesgo o tardía (grupo II)
Pauta antibiótica recomendada
La pauta recomendada con más frecuencia es la asociación de un β -lactámico y un aminoglucósido32. El uso de una monoterapia empírica es en principio planteable, en base al amplio espectro antibacteriano que proporcionan las modernas quinolonas y los β -lactámicos, que incluye la mayoría de BGN y P. aeruginosa. Estos antibióticos tienen moderada/buena penetración en el tejido pulmonar y buenos perfiles de seguridad y en algunos estudios se ha demostrado su eficacia33. Sin embargo, la aparición de cepas resistentes durante el tratamiento, sobre todo si está implicada P. aeruginosa, a menudo asociada a fracaso terapéutico28, es una observación frecuente. Así, es una opinión generalizada que no debe utilizarse monoterapia en los pacientes con NAVM y factores de riesgo predisponentes para tener P. aeruginosa.
La terapia combinada extiende el espectro de actividad, lo que tiene particular importancia teniendo en cuenta que hasta un 55% de las NAVM son polimicrobianas, para reducir al máximo la posibilidad de un tratamiento empírico inapropiado. Además, puede disminuir la aparición de resistencias durante el tratamiento34 y proporcionar mejores resultados debido al efecto sinérgico de la combinación, como ha sido demostrado en algún trabajo al disminuir la mortalidad en infecciones graves bacteriémicas por P. aeruginosa o Klebsiella spp.35,36. Por el contrario, la terapia combinada comporta un mayor riesgo de toxicidad, especialmente en regímenes que incluyen aminoglucósidos y un posible aumento de los costes37.
Parece, pues, razonable que durante los primeros días y a la espera de resultados microbiológicos, la terapia empírica en pacientes con NIG con factores de riesgo, especialmente aquéllos con fracaso multiorgánico y sepsis severa, incluya un β -lactámico con actividad frente a P. aeruginosa, ya sea una cefalosporina, ureidopenicilina asociada o no a inhibidores de β-lactamasas, monobactam o carbapenem combinado con un aminoglucósido con una dosificación óptima.
La asociación de 2 β -lactámicos ofrece pocas ventajas y presenta potenciales problemas secundarios como la inducción de β -lactamasas cromosómicas que inactiven a ambos38 o efectos secundarios hematológicos.
La asociación de un β-lactámico y una quinolona resulta atrayente, pero su eficacia no está actualmente contrastada y existe alguna referencia a una posible resistencia cruzada entre ciprofloxacino e imipenem39.
Los aminoglucósidos alcanzan su máxima eficacia cuando se administran a dosis altas y en una sola dosis diaria40. Para obtener una respuesta clínica adecuada, la concentración pico tiene que ser 8-10 veces la concentración mínima inhibitoria (CMI). La utilización de una dosis única diaria comporta una mayor eficacia y reduce la aparición de efectos secundarios, sobre todo nefro y ototoxicidad41.
Los b -lactámicos, por su parte, parecen alcanzar su máxima capacidad bactericida administrados de forma continua42,43. La administración tópica de antibióticos tales como colistina, aminoglucósido o ceftazidima se ha utilizado tanto de forma profiláctica como terapéutica, sobre todo en pacientes con fibrosis quística44. Su eficacia en el tratamiento de la NAVM no está bien evaluada45,46.
Como norma generalizada, las sociedades científicas recomiendan cubrir lo que denominan microorganismos "core" de las neumonías tempranas y los específicos relacionados con determinados factores de riesgo, generalmente multirresistentes.
En las unidades con una elevada prevalencia de SARM, y sobre todo si han recibido b -lactámicos previamente, debería incluirse un glucopéptido. Recientemente se han publicado datos sobre la eficacia de linezolid en el tratamiento empírico de la NAVM, que muestran una mayor supervivencia del 80 frente al 63,5% de los pacientes tratados con vancomicina47. Sin embargo, el hecho de que el estudio sea el resultado de la fusión de 2 estudios que por separado no apreciaron esta eficacia, que no se observe la misma eficacia en el grupo completo de S. aureus, y que se tenga que administrar a todos los pacientes para cubrir el 14% de las infecciones, con el coste añadido que ello representa, hacen recomendable la espera de nuevos estudios que confirmen estas buenas expectativas.
Duración del tratamiento antibiótico
El tiempo de tratamiento de la NAVM ha sido motivo de controversia, recomendándose hasta la fecha una duración entre 14 y 21 días, sobre todo si los microorganismos aislados son multirresistentes. Recientemente Chastre et al48 han observado la misma mortalidad en los pacientes tratados durante 8 días y los tratados 15 días. En ambos grupos el 30% de los gérmenes eran potencialmente conflictivos (P. aeruginosa, Acinetobacter spp., Stenotrophomonas spp. o SARM) y un 11% polimicrobianos. Sin embargo, en los pacientes con terapia corta se apreció un número significativo de sobreinfecciones y recurrencias por BGN no fermentadores, no así en SARM.
Así, si la evolución clínica es buena y el agente etiológico pertenece a la flora endógena primaria, una pauta de 8 días es suficiente. Aunque según el estudio de Chastre, las infecciones por SARM parecen tener este mismo comportamiento, aunque dada la elevada morbimortalidad reportada es de esperar estudios específicos para poder estar seguros de esta respuesta. Frente a los microorganismos multirresistentes, sobre todo BGN no fermentadores, sería por tanto recomendable una pauta más prolongada, no menor de 14 días. En cualquiera de las situaciones, debe existir mejoría clínica y un período mínimo de apirexia de 48 h.
Conclusiones
La terapia antibiótica debe iniciarse de forma temprana.
El tratamiento empírico debe ser combinado e incluir antibióticos no utilizados previamente
La antibioticoterapia debe ajustarse o modificarse de acuerdo con los resultados microbiológicos.
Los protocolos terapéuticos deben adaptarse a la realidad local.
Si se realiza un cambio antibiótico, los nuevos antibióticos deben pertenecer a un grupo distinto.
Debido a que los agentes etiológicos y su sensibilidad pueden variar dependiendo de la zona geográfica, del hospital, del tipo de unidad y con el tiempo, las guías de las diferentes sociedades científicas para el tratamiento antibiótico de las NAVM deben modificarse teniendo en cuenta los modelos locales de etiología y sensibilidades.
Recomendaciones
El tratamiento debe ser instaurado de forma temprana. Grado de evidencia I. Acuerdo entre expertos 17/17 100%).
S. aureus y P. aeruginosa son, por su prevalencia, de cobertura empírica obligatoria. Grado de evidencia I. Acuerdo entre expertos 17/17 (100%).
El tratamiento empírico será con terapia combinada buscando la ampliación del espectro, la disminución de las resistencias y el sinergismo. Grado de evidencia II. Acuerdo entre expertos 17/17 (100%).
Debe incluir un antibiótico β -lactámico activo frente a P. aeruginosa y SASM junto a un aminoglucósido. En la tabla 3 se expone el tratamiento recomendado. Grado de evidencia II. Acuerdo entre expertos 17/17 (100%).
El aminoglucósido debe emplearse a dosis altas y dosis única diaria. Grado de evidencia II. Acuerdo entre expertos 17/17 (100%).
Es recomendable que en pacientes con exposición previa a antibióticos se priorice los de familias diferentes de los anteriores. Grado de evidencia III. Acuerdo entre expertos 17/17 (100%).
La eficacia de la asociación de un b -lactámico y una quinolona no está suficientemente contrastada por lo que debería utilizarse preferentemente como antibioticoterapia alternativa. Grado de evidencia III. Acuerdo entre expertos 16/17 (93%).
Las quinolonas son la alternativa al β-lactámico en alérgicos a penicilinas. Grado de evidencia III. Acuerdo entre expertos 17/17 (100%).
Hay que tener presente la situación de endemia de SARM o BGN multirresistentes, en cuyo caso su cobertura es obligatoria. Grado de evidencia II. Acuerdo entre expertos 17/17 (100%).
Situaciones especiales
Neumonía asociada a ventilación mecánica por Acinetobacter baumannii
La neumonía por A. baumannii se observa preferentemente en el paciente sometido a ventilación mecánica. En España la frecuencia de la NAVM se ha mantenido bastante estable en los últimos 5 años, cifrada en 16,6 episodios/1.000 días de ventilación mecánica en el año 2002 según datos del estudio ENVIN. Las máximas frecuencias registradas para A. baumannii fueron de 18% en 1994 y 13% en 1996. Estos episodios representaron cerca del 10% de las neumonías tardías en esta población49.
En los últimos años estos microorganismos han desarrollado resistencia a todas las familias de antibióticos conocidas, especialmente los modernos β -lactámicos, aminoglucósidos, fluoroquinolonas y recientemente carbapenémicos. El patrón del antibiograma, no obstante, puede ser variable según las cepas y los hospitales considerados. La resistencia a los carbapenémicos que ha aparecido en los últimos años comporta una especial preocupación, ya que imipenem ha sido el tratamiento de referencia para las infecciones graves por A. baumannii, incluidas las NAVM50. El porcentaje de resistencia a carbapenémicos entre las neumonías por A. baumannii según datos del ENVIN fue de 31,2% en 1998, 57,5% en 1999 y 28% en 200049. En un estudio multicéntrico reciente efectuado por el GEIH-SEIMC en pacientes hospitalizados en UCI y salas convencionales de más de 40 hospitales españoles, el porcentaje de resistencia de A. baumannii a imipenem fue de alrededor del 40%. En muchos de estos casos la colistina es el único antibiótico que mantiene su actividad in vitro y se plantea la disyuntiva de utilizar este antibiótico como monoterapia para el tratamiento de los pacientes con este tipo de neumonía. La utilización de colistina por vía sistémica ha sido casi excepcional durante las 3 últimas décadas, por su nefrotoxicidad y considerarse un antibiótico con menor actividad en comparación con los β -lactámicos, aminoglucósidos y fluoroquinolonas. Aunque la información clínica disponible hasta la fecha sobre su utilización en el tratamiento de esta infección es escasa, algunos estudios muestran la eficacia y poca toxicidad de la colistina endovenosa51.
Dadas las dificultades terapéuticas que plantean estas infecciones y la mortalidad atribuible, es razonable considerar la posible aportación de un tratamiento tópico con aerosoles de colistina. Aunque no hay una información contrastada al respecto, las altas concentraciones de antibiótico que pueden alcanzarse con los aerosoles en los bronquios y las peculiaridades que comporta el tratamiento sistémico con colistina hacen recomendable este empleo por vía tópica en los casos producidos por cepas resistentes a los carbapenémicos. Para el cálculo de la dosis administrada hay que tener en cuenta que un vial de colistina contiene 1.000.000 U u 80 mg de colimicina sulfometato (equivalentes a 33,3 mg de colistina base); los aerosoles se administran a dosis de 500.000-1.000.000 U (16,6-33,3 mg de colistina base)/6 h diluidos en 5 ml de suero fisiológico.
En un reciente estudio de infección experimental se ha estudiado la eficacia de colistina respecto a la de los b -lactámicos, aminoglucósidos y rifampicina en un modelo de neumonía por A. baumannii en el ratón52. Se pudo comprobar que la colistina era comparativamente el antibiótico menos eficaz frente a la infección producida por cepas sensibles a los diversos antibióticos, e incluso frente a cepas con sensibilidad disminuida a b -lactámicos, aminoglucósidos y rifampicina. Ello sugeriría que estos antibióticos podrían ser más activos que la colistina, aun teniendo un grado de actividad in vitro menor. Fue destacable la eficacia de la rifampicina en este modelo, a pesar de que las cepas estudiadas mostraron una resistencia moderada (CMI 8-16 μg/ml). Dentro del grupo de aminoglucósidos, tobramicina es el que presenta mayor eficacia, tanto sola como en combinación.
Conclusiones
La neumonía por A. baumannii es una entidad que predomina especialmente en las UCI. Su repercusión clínica parece claramente menor que la de otros BGN, ya que en situaciones de endemia, su aislamiento puede tener únicamente el significado de un marcador de la situación epidemiológica. No obstante, hay datos que muestran una elevada mortalidad por esta infección, por lo que se debe ser cauto en su infravaloración. El tratamiento empírico de los pacientes con sospecha de neumonía por A. baumannii dependerá del grado de sospecha y de la epidemiología de la UCI correspondiente.
Recomendaciones
El uso empírico de la combinación de imipenem con aminoglucósidos o con colistina, según los casos, parece el más apropiado. Deberá considerarse la indicación de iniciar o no empíricamente la administración de aerosoles de colistina según el grado de resistencia de la cepa que predomine en cada UCI. Grado de evidencia III. Acuerdo entre expertos 17/17 (100%).
Frente a cepas sensibles el tratamiento con b -lactámicos o fluoroquinolonas puede hacerse como monoterapia. Si la cepa es sensible a alguno de los b -lactámicos habitualmente más activos (ticarcilina, piperacilina, ceftazidima, cefepima e imipenem), éstos podrían considerarse la primera opción. Grado de evidencia III. Acuerdo entre expertos 17/17 (100%).
En los casos con sensibilidad disminuida a los β-lactámicos (sensibilidad intermedia o resistencia moderada) y resistencia a fluoroquinolonas, la asociación de β-lactámicos y aminoglucósidos es probablemente la mejor alternativa; en estos casos puede ser recomendable utilizar adicionalmente aerosoles de colistina (tabla 4). Grado de evidencia III. Acuerdo entre expertos 17/17 (100%).
Para el tratamiento de la neumonía ocasionada por cepas con alta resistencia a β-lactámicos, incluidos imipenem y sulbactam, fluoroquinolonas y aminoglucósidos, debe considerarse la indicación de colistina administrada por vía sistémica y en aerosol; sin embargo, en estos casos es recomendable asociar rifampicina si las cepas son sensibles o muestran una resistencia sólo moderada (CMI 8-16 μg/ml). La posibilidad de utilizar otras combinaciones con rifampicina, así como otros tipos de antibióticos como cotrimoxazol, tetraciclinas o macrólidos, debe tenerse en cuenta en función del antibiograma. Grado de evidencia III. Acuerdo entre expertos 17/17 (100%).
Neumonía asociada a ventilación mecánica por Pseudomonas aeruginosa
La NIG por P. aeruginosa supone el 15-20% de las neumonías hospitalarias en EE.UU.53 y entre el 20 y 45% de las NAVM54,55. En nuestro país, según el estudio ENVIN de 2001, su incidencia fue del 15,9% de las NAVM en nuestras UCI49. Cuando se presenta asociada a la ventilación mecánica (NAVM-P) comporta una especial gravedad, con una alta mortalidad relacionada: 27-70%, debido a la virulencia del microorganismo y al estado inmunitario de los pacientes en los que incide56,57. Su evolución es a menudo tórpida, con frecuentes recidivas, persistencia de la colonización e infecciones recurrentes debidas al daño provocado en el parénquima pulmonar7. Asimismo, es destacable la capacidad de P. aeruginosa para desarrollar resistencias, inclusive en el curso de una antibioticoterapia apropiada28. Ello ocurre con mayor frecuencia si se utiliza monoterapia, tanto con b -lactámicos, aminoglucósidos o fluoroquinolonas.
Otro aspecto a considerar en el tratamiento de las NAVM-P es la cuestionable eficacia de los aminoglucósidos en los tejidos pulmonares infectados, por lo que deben ser utilizados siempre en combinación con otros antibióticos y se ha planteado su posible administración por inhalación12,58. Sin embargo, los aminoglucósidos siguen teniendo un papel importante en el tratamiento de estas infecciones, ya que tienen mayor actividad intrínseca frente a Pseudomonas spp. que los β-lactámicos, tienen una capacidad altamente bactericida dependiente de su concentración lo que permite su prescripción diaria, y un notable efecto postantibiótico. Entre ellos tobramicina y amikacina son los más activos frente a P. aeruginosa58.
Entre las cefalosporinas, ceftazidima y cefepima son las que tienen mayor actividad bactericida frente a P. aeruginosa, del tipo tiempo-dependiente. Este hecho y las dificultades terapéuticas habituales en esta clase de infecciones han llegado a postular la conveniencia de su utilización en perfusión continua59, aunque ello debería ser confirmado en más estudios. Meropenem tiene mayor actividad intrínseca frente P. aeruginosa que imipenem, con un mejor perfil de toxicidad, lo que permite la administración de dosis más elevadas60. La piperacilina asociada con tazobactam presenta una efectividad similar que las cefalosporinas mencionadas y los carbapenémicos en el tratamiento de las NAVM-P57,61. La asociación de b -lactámicos y aminoglucósidos es a menudo sinérgica, incluso frente a cepas resistentes a uno de ellos; en algún estudio se ha observado esta sinergia más a menudo con piperacilina-tazobactam que con ceftazidima62. El monobactámico aztreonam ha recibido considerable atención tras un metaanálisis de Boucher63 que mostraba excelentes perfiles de actividad y seguridad en la NAVM por BGN.
Entre las quinolonas, el ciprofloxacino es el que tiene mayor actividad frente a P. aeruginosa, si bien se requieren dosis más elevadas que las utilizadas en otras infecciones (400 mg/8 h), que deben ser administradas siempre en combinación con otros antibióticos28.
En resumen, se ha recomendado la utilización de una combinación de antibióticos con efecto sinérgico64, preferentemente de un β -lactámico anti-Pseudomonas de amplio espectro (cefepime, ceftazidima, piperacilina-tazobactam, meropenem, imipenem) con un aminoglucósido, o en su defecto con ciprofloxacino17. La combinación de 2 β -lactámicos no es recomendable, por la potenciación de la inducción de β -lactamasas y de efectos secundarios38. La utilización de las diversas combinaciones vendrá condicionada por el antibiograma y las características ecológicas de cada servicio.
En la tabla 5 se expone la dosificación antibiótica recomendada para el tratamiento de la NAVM por P. aeruginosa.
Se ha empleado la instilación directa de los antibióticos, sobre todo aminoglucósidos, en el tubo endotraqueal o cánula de traqueotomía, para intentar aumentar la concentración de los antibióticos en las secreciones bronquiales y el tejido pulmonar, evitando en lo posible su toxicidad sistémica58. La utilización de esta ruta inhalada ha hecho posible el rescate de antibióticos abandonados hace tiempo por la toxicidad inherente a su empleo por vía parenteral, pese a ser eficaces ante P. aeruginosa multirresistente. Así, Hamer65 empleó de forma satisfactoria colistina en aerosol en 2 pacientes con NAVM-P y otro con traqueobronquitis por P. aeruginosa multirresistente sometido a ventilación mecánica. Asimismo, la utilización con buenos resultados de la solución nebulizada de tobramicina para el tratamiento de la infección bronquial crónica por P. aeruginosa en la fibrosis quística ha permitido sugerir que podría ser efectiva en la NAVM-P66.
Conclusiones
El tratamiento de la neumonía por P. aeruginosa continúa siendo controvertido por la gran capacidad de adquisición de resistencias del microorganismo y su elevada mortalidad relacionada. Diferentes combinaciones antibióticas se han mostrado efectivas in vitro; sin embargo, el fracaso terapéutico en casi todas las series se sitúa en el 20%. El ensayo de otras opciones, como la perfusión continua de b -lactámicos o la administración de aminoglucósidos en aerosoles, para implementar sus ventajas farmacodinámicas, no se ha acompañado hasta la actualidad de mejoras significativas en el pronóstico.
Recomendaciones
El tratamiento se realizará siempre con terapia combinada de un b -lactámico con un aminoglucósido o, en su defecto y sobre todo en presencia de fracaso renal, con una quinolona de tercera generación. Grado de evidencia I. Aceptación de expertos 17/17 (100%).
Entre los β-lactámicos se recomienda el uso preferente de ceftazidima, cefepime o piperacilina/tazobactam. Los carbapenémicos deberían reservarse para situaciones especiales o de alta resistencia y el ciprofloxacino para los casos de reacciones adversas a β-lactámicos. Grado de evidencia III. Aceptación de expertos 17/17 (100%).
Se recomienda mantener el tratamiento con b -lactámicos durante 15 días. Grado evidencia II. Aceptación de expertos 17/17 (100%).
Probablemente es suficiente administrar el aminoglucósido únicamente durante los primeros 5-7 días, si la respuesta clínica es correcta. Grado de evidencia III. Aceptación de expertos 17/17 (100%).
Neumonía asociada a ventilación mecánica por Staphylococcus aureusresistente a meticilina
Los glucopéptidos han sido el tratamiento estándar de la mayoría de las infecciones por SARM en nuestro país. Por este motivo, este grupo de antibióticos se incluye a menudo en la terapéutica empírica utilizada en aquellas zonas hospitalarias con una tasa elevada de pacientes con SARM. Ello ha determinado su amplio consumo, con el consiguiente riesgo de acarrear el desarrollo de resistencias entre los cocos grampositivos.
Al analizar el patrón de antibiograma de SARM, es bien conocido que la resistencia a meticilina implica resistencia a todos los β-lactámicos. Hasta hace pocos años, la mayoría de las infecciones de SARM en España se debían a un clon muy predominante llamado "clon ibérico", sensible exclusivamente a glucopéptidos, cotrimoxazol, cloranfenicol y fosfomicina. Sin embargo, recientemente se ha apreciado una diversificación en la epidemiología del SARM, en España y también en otros países europeos, con la aparición y el progresivo predominio de otros clones más sensibles; las cepas aisladas en nuestro país son sensibles en un 40% de los casos a clindamicina y alrededor del 80% a rifampicina, además de a los antibióticos previamente mencionados. Por este motivo, asumir que cualquier infección grave por SARM requiere la administración de glucopéptidos podría ser reconsiderado a la luz de los datos actuales y en función del tipo de infección.
Por otra parte, la eficacia de los glucopéptidos en el tratamiento de la NAVM por SARM ha sido cuestionada. Su capacidad de letalidad frente a S. aureus es inferior a la de los β-lactámicos; así necesitan concentraciones máximas muy por encima de la CMI para asegurar su eficacia, las cuales son difíciles de conseguir, dados su potencial toxicidad y estrecho rango terapéutico. Además, estas consideraciones podrían ser particularmente importantes en el caso del tratamiento de la neumonía, por la deficiente difusión pulmonar de estos antibióticos67. La dosis recomendada de vancomicina es 1 g/12 h y la de teicoplanina de 400 mg/12 h. Sin embargo, se ha contemplado la posibilidad de utilizar la perfusión continua para aumentar estas dosis y también el empleo de la vía inhalatoria. Por lo que respecta a la administración en perfusión, en un estudio su farmacocinética y efectividad (500 mg de carga, seguidos de 2 g/24 h) fueron similares a las observadas con las dosis convencionales de 1 g/12 h, siempre que los niveles pico y valle fueran adecuados68. Respecto a la administración inhalatoria de glucopéptidos en aerosol, la información es escasa69 y no carece de riesgos70.
La experiencia en el tratamiento de la NAVM con otros antibióticos como fosfomicina y cotrimoxazol es muy limitada71,72. Un estudio prospectivo y aleatorizado en grandes quemados mostró que los pacientes tratados de forma profiláctica con trimetoprima-sulfametoxazol tuvieron una incidencia de NAVM por SARM significativamente inferior que los que recibieron placebo (4,8 frente a 36,8%; p = 0,017)73. En los últimos años se han incorporado 2 nuevas moléculas, quimupristina/dalfopristina (QD) y linezolid como posibles tratamientos de las infecciones por SARM, incluidas las cepas con resistencia a los glucopéptidos. Ambos son productos que comportan un gran dispendio económico, con precios medios de tratamiento de 2.700 y 1.260 €, respectivamente74. En el caso de QD su efecto bactericida no está bien documentado para las cepas de S. aureus resistentes a clindamicina75 y hasta la fecha la Food and Drug Administration (FDA) ha aprobado su utilización únicamente para bacteriemia por Enterococcus faecalis resistente a vancomicina. Ambos han mostrado un eficacia clínica similar a la de la vancomicina en diversos estudios clínicos comparativos76-79; sin embargo, la experiencia con linezolid para el tratamiento de la NAVM por SARM se considera todavía insuficiente. El reciente estudio de Wunderink et al47, que no correspondió a tratamientos dirigidos, abre nuevas expectativas al tratamiento de la NAVM por SARM. Una importante ventaja adicional de estos fármacos sería que no necesitan ajustarse si hay disfunción renal.
Dadas las dificultades terapéuticas observadas con cualquiera de las monoterapias mencionadas y la gravedad de la NAVM por SARM, se ha considerado el posible beneficio obtenido utilizando una combinación antibiótica con efecto sinérgico. La presencia de sinergismo entre vancomicina y diversos β -lactámicos como cloxacilina80,81 o imipenem82,83 se ha demostrado en cepas de S. aureus con cierto grado de resistencia a glucopéptidos. También se ha descrito sinergia entre QD y vancomicina, cefepima, ceftazidima e imipenem75. El problema del sinergismo es que se trata de un fenómeno in vitro, difícilmente extrapolable a la clínica y que el beneficio clínico del uso de una terapia combinada no está contrastado. Con todo, en los casos de NAVM grave por SARM la combinación de vancomicina con rifampicina, clindamicina o inclusive con QD o linezolid puede ser considerada.
Recomendaciones
Hasta el momento el tratamiento con glucopéptidos es el de referencia en el tratamiento de la NAV por SARM. Grado de evidencia III. Aceptación de expertos 17/17 (100%).
No obstante, en la valoración actual de este tratamiento, debe contemplarse también la posibilidad de utilizar otros antibióticos como la rifampicina, clindamicina o fosfomicina, según el antibiograma de la cepa causante. Grado de evidencia II. Aceptación de expertos 17/17 (100%).
La actividad de la vancomicina es similar a la de la teicoplanina si se aumentan las dosis de esta última, aunque se igualan los efectos tóxicos. El uso preferencial de vancomicina viene avalado por el hecho de que la mayoría de los estudios se ha hecho con este antibiótico, cuyo empleo puede además ser monitorizado mediante el control de los valores séricos. Grado de evidencia II. Aceptación de expertos 17/17 (100%).
La recomendación de incrementar la dosis de vancomicina no puede sustentarse en ningún nivel de evidencia, mientras que su administración en perfusión continua podría reducir la toxicidad con similar eficacia. Grado de evidencia IV. Aceptación de expertos 17/17 (100%).
Se desaconseja la administración de glucopéptidos en aerosol. Grado de evidencia II. Aceptación de expertos 17/17 (100%).
La monitorización sistemática de valores séricos en el curso del tratamiento de la NAVM con vancomicina es recomendable para garantizar la eficacia necesaria y reducir la posible toxicidad renal, teniendo en cuenta el perfil de paciente de UCI con múltiples factores de riesgo. Grado de evidencia II. Aceptación de expertos 17/17 (100%).
El uso de una terapia combinada de glucopéptidos con rifampicina, clindamicina, fosfomicina, β -lactámicos (para los casos de S. aureus resistentes a glucopéptidos) o inclusive QD o linezolid en casos graves o de mala evolución clínica parece razonable, a pesar de que no hay una evidencia contrastada. Grado de evidencia III. Aceptación de expertos 17/17 (100%).
Los nuevos antibióticos activos frente a SARM (QD y linezolid) parecen tener una eficacia igual (QD) o superior (linezolid) a la vancomicina. En el momento actual el tratamiento con linezolid podría ser considerado, pero la experiencia es todavía escasa, por lo que su uso en monoterapia debería limitarse a las infecciones por cepas resistentes a glucopéptidos o a pacientes con función renal alterada. Grado de evidencia II. Aceptación de expertos 17/17 (100%).
En relación con sus características farmacocinéticas y penetración pulmonar, antibióticos como la clindamicina o el linezolid podrían ser superiores a los glucopéptidos. Grado de evidencia III. Aceptación de expertos 17/17 (100%).
Neumonía asociada a ventilación mecánica sin diagnóstico microbiológico
El 10-20% de las técnicas utilizadas para el diagnóstico de la NAVM no consiguen un aislamiento bacteriano84. En nuestro entorno hasta el 10,6% de las neumonías no tuvo diagnóstico etiológico, cifra que puede variar en relación con el tiempo de aparición de la infección; así mientras que en el primer episodio de NAVM el cultivo fue negativo en el 13,5% de los casos, en el segundo episodio únicamente lo fue en el 2,3% y en el tercero en ningún caso49.
Este hecho responde en ocasiones a la presencia de un proceso no infeccioso (atelectasia, insuficiencia cardíaca, SDRA)85 y traduce un uso inadecuado de antibióticos. En otros casos se debe a la administración de antibióticos previa o simultáneamente a la toma de muestras respiratorias, lo que conlleva una reducción mayor del 40% en su rendimiento86. Raramente la etiología no es bacteriana y se requieren otro tipo de pruebas diagnósticas.
Shing et al87 han propuesto un modelo de diferenciación de la neumonía de un proceso no infeccioso. Para ello utilizaron como base de actuación la puntuación clínica de infección pulmonar (PCIP), desarrollada por Pugin et al88, modificada (PCIPm). A los pacientes que mantenían la PCIP ≤ 6 transcurridos 3 días de tratamiento con ciprofloxacino, se les suspendió el tratamiento antibiótico. No hubo diferencias con respecto a la mortalidad, ni otros parámetros clínicos o radiológicos, y se obtuvo un menor consumo de antibióticos, y una menor emergencia de cepas multirresistentes, sobre todo P. aeruginosa, SARM y enterococo, y un descenso en los costes.
Recientemente Luna et al89 evaluaron de forma prospectiva la correlación entre la puntuación de la PCIPm y la evolución de la NAVM, y observaron que en los pacientes en los que la PCIPm descendía, la evolución era adecuada en contraposición a los que mantenían la PCIPm > 6.
Recomendaciones
En los casos de sospecha de NAVM sin diagnóstico microbiológico, se debe hacer una evaluación clínica del paciente al inicio y posteriormente al tercer día, mediante la PCIPm o PCIP. Si su valor es ≤ 6 se recomienda retirar la terapia antibiótica. Grado de evidencia II. Aceptación grupo de expertos 16/17 (93%).
Si la PCIP > 6 se recomiendan nuevas pruebas diagnósticas mediante métodos invasivos y aumentar el escalón terapéutico cubriendo los microorganismos no englobados previamente. Grado de evidencia III. Aceptación de expertos 17/17 (100%).
Neumonía asociada a ventilación mecánica con mala evolución
La resolución de la NAVM no está claramente definida y se sustenta en aspectos clínicos y microbiológicos. Desde el punto de vista clínico, la resolución o mejoría de la NAVM correspondería a la disminución o desaparición progresiva de los signos y síntomas que determinaron su diagnóstico (fiebre, secreciones purulentas) y de los datos de las exploraciones complementarias (cifra de leucocitos, PaO2/FiO2 y radiología)90. El factor más importante en esta definición es el tiempo en el que debe considerarse que la respuesta al tratamiento es inadecuada. El punto tomado habitualmente para valorar la respuesta es el de 72 h tras el inicio del tratamiento, asumiendo las definiciones extraídas de la neumonía nosocomial en general91, si bien no hay estudios específicos en el ámbito de la NAVM. Se contemplan hasta 3 términos que pueden definir la mala respuesta en la NAVM. Por un lado, la NAVM progresiva: rápido deterioro (≤ 72 h) de los signos y síntomas a pesar del tratamiento antibiótico. En segundo lugar, la NAVM persistente: neumonía que no presenta mejoría de los signos y síntomas a pesar de > 72 h de tratamiento antibiótico. Y, por último, la NAVM de lenta resolución: mejoría de los signos y síntomas, pero con resolución radiográfica de < 50% en una semana92. Las causas de mala respuesta engloban aspectos relacionados con el huésped, con los microorganismos infectantes y con patologías no infecciosas. En el caso de la neumonía progresiva, las causas más frecuentes de ausencia de respuesta al tratamiento son la patología no infecciosa, la presencia de microorganismos con resistencia primaria al tratamiento antibiótico empírico, de microorganismos con gran virulencia y una respuesta sistémica grave (sepsis grave o shock séptico). Con respecto a la neumonía persistente o de lenta resolución, las causas más comunes corresponden a enfermedad no infecciosa, persistencia de la infección (ya sea por resistencia primaria del microorganismo infectante, no cubierto por la terapia empírica, o por resistencia emergente o dosificación antibiótica inadecuada o complicaciones anatómicas [empiema, absceso]), por una sobreinfección de un microorganismo diferente del inicial o por una infección extrapulmonar concomitante93,94.
Recomendaciones
En la neumonía progresiva (deterioro en las primeras 72 h) y pendientes de resultado definitivo se debe descartar una causa no infecciosa pulmonar o un foco infeccioso extrapulmonar (tomografía computarizada, nuevos cultivos extrapulmonares, isótopos), modificar la terapéutica empírica inicial cambiando los antibióticos o aumentando su cobertura. Grado de evidencia III. Aceptación de expertos 17/17 (100%).
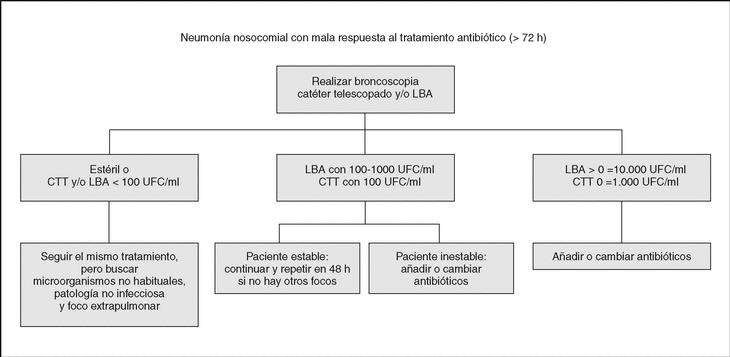
Realizar nueva toma de muestras pulmonares mediante fibrobroncoscopia, y buscar patógenos no habituales (Legionella, Mycobacterium tuberculosis, Aspergillus, Nocardia), actuando según se indica en la figura 1 cuando hayamos obtenido el resultado etiológico. Grado de evidencia III. Aceptación de expertos 17/17 (100%).
Figura 1. Neumonía de mala evolución con persistencia de los signos locales y sistémicos de infección pulmonar. LBA: lavado broncoalveolar; CTT: catéter telescopado; UFC: unidades formadoras de colonias.
Neumonía asociada a ventilación mecánica recurrente o recidivante
La neumonía se define como recurrente cuando aparece un nuevo episodio de NAVM en la que se aísla el mismo microorganismo que en el episodio anterior, después de haber suspendido el tratamiento antibiótico correcto en cuanto espectro, dosis y duración, durante más de 72 h95.
Aproximadamente entre el 18 y el 22% de las NAVM pueden presentar esta evolución95-98; los microorganismos habitualmente implicados son P. aeruginosa, E. coli y S. aureus resistente o no a la meticilina. Rello et al96, mediante técnicas de replicación genética, demostraron que el 93% de las cepas de P. aeruginosa aisladas en 9 episodios de recurrencia correspondían al mismo microorganismo inicial.
Los factores predisponentes más significativos identificados en el análisis multivariante fueron el SDRA y la enfermedad pulmonar obstructiva crónica96,97. Otros factores destacados fueron la falta de drenaje bronquial, la inmunosupresión o la presencia de reservorios (intubación orotraqueal, empiema o neumonía abscesificada)57,98. Como factor añadido microbiológico se observó que más del 50% de los aislados presentó resistencia a los antibióticos administrados durante el episodio inicial.
Recomendaciones
Se ha de tener una alta sospecha de NAVMR en los pacientes con NAVM previa por P. aeruginosa, S. aureus o E. coli. Grado de evidencia II. Aceptación de expertos 17/17 (100%).
Dado que los factores del huésped y microbiológicos no son modificables, ha de descartarse de forma activa la presencia de reservorios por lo que se recomienda la práctica de una tomografía computarizada torácica. Grado de evidencia III. Aceptación de expertos 17/17 (100%).
Siempre se iniciará la cobertura antibiótica con antibióticos no administrados previamente. Grado de evidencia III. Aceptación de expertos 17/17 (100%).
Controles durante el tratamiento de la neumonía nosocomial
El empleo de los antibióticos en los pacientes con NAVM no debe ser un acto rutinario. Su administración debe seguirse de una atenta vigilancia de la evolución clínica, que es un indicador de eficacia, así como de la posible aparición de efectos secundarios y la selección de nuevos patógenos multirresistentes durante o al final del tratamiento99.
Valoración de la evolución clínica
La primera valoración de la respuesta terapéutica tiene que hacerse a las 72 horas de iniciado el tratamiento empírico. La aparición de nuevos signos de infección o el empeoramiento de los signos iniciales debe hacer sospechar que los antibióticos que se administran no son adecuados para tratar los agentes patógenos causantes de la neumonía. En este caso se debe repetir la obtención de muestras pulmonares (con métodos invasivos, si es posible) y de sangre, y proceder al cambio de los antibióticos iniciales, aumentando el escalón terapéutico con antimicrobianos más potentes, de mayor espectro y con cobertura para patógenos menos frecuentes. En el caso contrario, en el que se observa una disminución de los signos iniciales, se continuará el tratamiento hasta la identificación de los patógenos y su sensibilidad, en cuyo caso se procede a su readaptación, utilizando los antibióticos activos de primera elección para cada uno de los microorganismos.
En los casos en los que el tratamiento sea adecuado en base a la sensibilidad antibiótica, pero la evolución desfavorable, es necesario tener en cuenta las caracter&isticas farmacocinéticas de los antibióticos administrados en lo que se refiere a su penetración en los tejidos infectados, a las dosis y a los intervalos utilizados, para garantizar las concentraciones apropiadas en el foco.
Determinación de valores plasmáticos
En los pacientes críticos, la frecuente presencia de alteraciones hemodinámicas, insuficiencia renal y hepática, edemas generalizados, y otras complicaciones que interfieren el metabolismo, distribución o eliminación de los antibióticos, determina una amplia variabilidad interindividual en los niveles séricos cuando se administran las mismas dosis. Por ello, es necesario la optimización de las dosis de antibióticos, en especial de aquéllos con un margen terapéutico estrecho (diferencia entre concentraciones tóxicas y concentraciones terapéuticas) como los aminoglucósidos y la vancomicina. La determinación de los valores plasmáticos debe realizarse el segundo día de la administración del antibiótico, cuando se supone que se ha alcanzado el equilibrio con el resto de los compartimentos de distribución. La incorporación de programas de farmacocinética diseñados específicamente para la monitorización de antibióticos permite ajustar su dosificación para obtener la máxima eficacia clínica con la mínima incidencia de afectos adversos100.
Vigilancia microbiológica para detectar la aparición de cepas multirresistentes o de nuevos patógenos resistentes a los antibióticos administrados
La utilización de antibióticos en los pacientes con NAVM favorece la aparición de agentes patógenos multirresistentes, cuya presencia puede asociarse a fracaso de la terapia administrada en un paciente concreto, pero que tiene además una importancia epidemiológica. La selección de la flora que forma el ecosistema de cada unidad condicionará en un futuro la política de antibióticos de esa UCI101-103.
La obtención de nuevas muestras debe realizarse siempre que se detecte una mala evolución clínica. El estudio microbiológico al finalizar el tratamiento en los pacientes que continúan con ventilación mecánica no se recomienda como práctica rutinaria habitual, fuera del contexto de estudios epidemiológicos.
Recomendaciones
Evaluar a las 72 h (± 24 h) la respuesta clínica al tratamiento. En el caso de mala evolución se procederá a la toma de nuevas muestras, preferentemente con métodos invasivos, y se indicarán nuevos antibióticos empíricos, con mayor cobertura para los agentes habituales y con cobertura para otros menos frecuentes. En caso de buena evolución y conocimiento del patógeno y de su sensibilidad se procederá al ajuste del tratamiento. Grado de evidencia II. Aceptación de expertos 17/17 (100%).
Realizar, siempre que sea posible, la determinación de niveles plasmáticos de aminoglucósidos y glucopéptidos. Valorar su repetición en función de las condiciones del enfermo y los resultados de las determinaciones previas. Grado de evidencia I. Aceptación de expertos 17/17 (100%).
Realizar controles de muestras respiratorias siempre que se observe una mala evolución clínica. Grado de evidencia II. Aceptación de expertos 17/17 (100%).
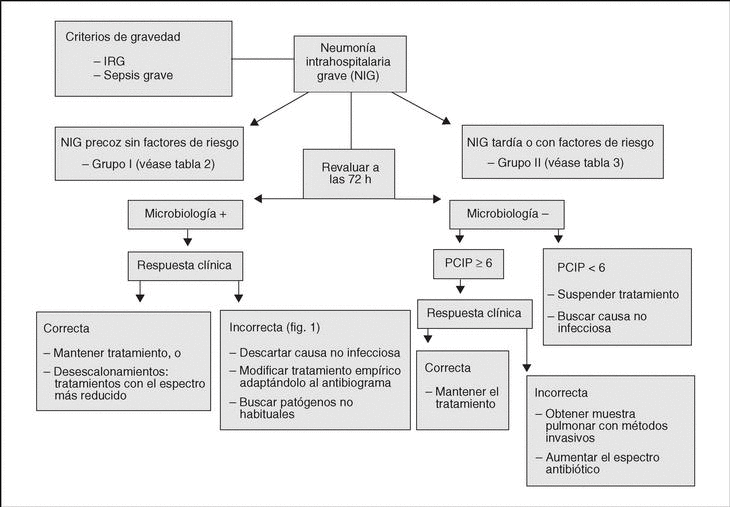
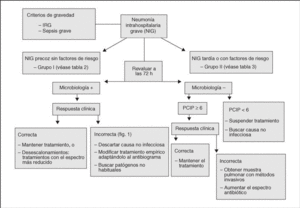
Algoritmo de actuación en el tratamiento de la neumonía intrahospitalaria grave (fig. 2)
Figura 2. Algoritmo de actuación en el tratamiento de la neumonía intrahospitalaria grave. IRG: insuficiencia respiratoria grave; PCIP: puntuación clínica de infección pulmonar.
Iniciar tratamiento empírico en base al tiempo de presentación y la presencia de factores de riesgo, sobre todo la administración previa de antibióticos. En el caso de NIG del grupo I iniciar monoterapia con β -lactámicos. Si la NIG pertenece al grupo II es recomendable la asociación de un β -lactámico anti-Pseudomonas y un aminoglucósido. El uso empírico de glucopéptidos depende de la situación endémica de cada unidad.
Revaluar la evolución clínica a las 72 h, y siempre que se obtenga resultado microbiológico.
Ante un microorganismo identificado y con buena evolución clínica, adaptar el tratamiento al espectro más específico, incluida la monoterapia si no se trata de bacterias multirresistentes.
Si la evolución es inadecuada, hay que descartar causas que mantengan la NIG, y revaluar el tratamiento según el microorganismo aislado, adaptándolo al antibiograma. En caso de bacterias multirresistentes es recomendable el uso de asociaciones sinérgicas.
En ausencia de aislamiento, y mala evolución, es obligado recoger nuevas muestras para cultivo con técnicas fibrobroncoscópicas, que incluirán estudio de microorganismos no habituales, y modificar el tratamiento en relación al espectro y los antibióticos usados.
Relación de los participantes en la comisión e expertos
GTEI-SEMICYUC: F. Álvarez Lermaa (Hospital del Mar, Barcelona), L. Álvarez Rochaa (Hospital Juan Canalejo, A Coruña), F. Barcenilla Gaitea (Hospital Arnau de Vilanova, Lleida), R. Jordà Marcosa (Clínica Rotger, Palma de Mallorca), J. Insausti Ordeñanaa (Hospital de Navarra, Pamplona), M.J. López Pueyoa (Hospital General Yagüe, Burgos), A. Martínez Pellúsa (Hospital de la Arrixaca, Murcia), P. Olaechea Astigarragaa (Hospital de Galdakano, Vizcaya), M. Palomar Martíneza (Hospital Vall d'Hebron, Barcelona), J. Relloa,b (Hospital Joan XXIII, Tarragona), J. Valles Daunisa (Hospital Parc Taulí, Sabadell).
ÁREA TIR-SEPAR: J. Blanquer Olivasc (Hospital Clínico, Valencia), R. Menéndez (Hospital La Fe, Valencia), F. Rodríguez de Castro (Hospital Universitario Dr. Negrín, Las Palmas de Gran Canaria), A. Torres Martíc (Hospital Clínic, Barcelona).
GEIH-SEIMC: X. Ariza Cardenal (Hospital de Bellvitge, Barcelona), M. Lizasoain (Hospital 12 de Octubre, Madrid).
aTambién son miembros del GEIH-SEIMC.
bTambién son miembros del Área TIR-SEPAR.
cTambién son miembros del GTEI-SEMICYUC.
Este artículo también se ha publicado íntegramente en Medicina Intensiva [Med Intensiva 2004;25(5):262-78] y Archivos de Bronconeumología [Arch Bronconeumol 2004;40(11):515-30].