*Al final del manuscrito se ofrece la relación de Red de Laboratorios de Vigilancia de Parálisis Flácida Aguda.
Introducción
La poliomielitis es una infección causada por los poliovirus tipos 1, 2 y 3 (Picornaviridae, enterovirus humanos), que puede afectar de forma grave al sistema nervioso central, con destrucción de las neuronas motoras de la médula espinal, y dar lugar a una parálisis flácida aguda (PFA). En mayo de 1988, en la reunión anual de la Organización Mundial de la Salud (OMS) en Ginebra, se elaboró un plan de actuaciones para conseguir la erradicación de la poliomielitis en el mundo. Dichas actuaciones fueron las siguientes: a) implantar un sistema de vigilancia eficaz de la PFA en menores de 15 años para demostrar la interrupción de la circulación de poliovirus salvaje; b) alcanzar y mantener coberturas de vacunación elevadas; c) organizar un sistema de vigilancia ambiental de enterovirus, d) realizar estudios seroepidemiológicos que analizaran el estado inmunitario de la población frente al virus de la poliomielitis y, por último, e) la búsqueda y control de poliovirus salvajes almacenados en los laboratorios. Estas cinco actuaciones se están llevando a cabo en España desde 1997 1-6.
Los progresos en la erradicación de la poliomielitis han ido en aumento en todo el mundo. El número de casos de polio se ha reducido el 99%, pasando de 350.000 casos estimados en 1988 a 918 casos en noviembre de 2004. El número de países endémicos ha disminuido de 125 en 1988 a 6 en enero de 2004: India, Nigeria, Pakistán, Egipto, Afganistán y Níger. En la actualidad, hay tres regiones de las establecidas por la OMS certificadas ya como libres de la circulación de poliovirus salvaje (América, en 1994; Pacífico Occidental, en 2000, y Europa, en 2002).
El propósito de este trabajo es presentar los resultados de los 6 años de funcionamiento de la vigilancia de poliovirus en España, para demostrar que no existe circulación de poliovirus salvaje en nuestro país.
Métodos
1. Vigilancia del Plan de Erradicación de la Poliomielitis en España. Anualmente desde 1997, el Laboratorio de Enterovirus del Centro Nacional de Microbiología (CNM) ha sido acreditado por la OMS mediante controles de calidad, revisión de procedimientos y uso de indicadores estándares, como Laboratorio Nacional de Poliovirus en España (LNP). En 1998 se constituyó en España la Red de Laboratorios para el Plan de Erradicación de la Poliomielitis en la Vigilancia de PFA (RLPEP). Dicha red está constituida por 9 laboratorios distribuidos por todo el territorio nacional 7 y es coordinada por el LNP. La RLPEP adoptó los protocolos y técnicas recomendados por la OMS 5 y es evaluada anualmente por el LNP mediante controles de calidad. El funcionamiento de la red es apoyado por los epidemiólogos responsables del Plan de Erradicación en cada comunidad autónoma, que supervisan el estudio de todos los casos de PFA declarados en su comunidad. El estudio virológico primario se realiza en el laboratorio designado por su comunidad o en caso de no tener laboratorio designado, se realiza en el laboratorio de microbiología diagnóstica del CNM que actúa como laboratorio primario de esas comunidades.
Desde 1999 hasta la actualidad, los sistemas de vigilancia se han visto reforzados por los datos de aislamientos y detección de enterovirus en otros síndromes respiratorios o neurológicos, principalmente los aislamientos procedentes de brotes de meningitis aséptica aportados por la red al LNP.
2. La RLPEP realiza el estudio virológico de pacientes menores de 15 años que ingresan en el hospital con síndrome de PFA, según el protocolo establecido 5. Dicho protocolo recomienda el estudio virológico de dos muestras de heces separadas de 24 a 48 h, dentro de los 14 días siguientes al desarrollo del cuadro clínico. Además, incluye la posibilidad del estudio de entre tres y cinco contactos por cada caso de PFA. Las muestras se inoculan en cultivos celulares (líneas celulares recomendadas Hep 2, RD y L20B) observando la aparición de efecto citopático durante un mínimo de 15 días. Todo efecto debe ser confirmado mediante técnicas de inmunofluorescencia, que permitan además identificar los aislados como poliovirus o enterovirus no polio.
Adicionalmente, los laboratorios recogen y envían cada mes al LNP los datos de todos los enterovirus aislados, tanto de los casos de PFA y sus contactos como de otros síndromes.
3. Entre las responsabilidades del LNP se encuentran las de analizar todos los datos enviados y caracterizar los aislados mediante las siguientes técnicas:
a) Serotipado de los enterovirus no polio, mediante técnicas de microneutralización usando las mezclas de antisueros de Melnick 8 y/o tipificación molecular mediante la amplificación, secuenciación y estudio del extremo 3' del gen VPI 9.
b) Serotipado de los poliovirus mediante dos metodologías diferentes: a) inmunofluorescencia con un panel de cinco anticuerpos anti poliovirus 1, anti poliovirus 2, anti poliovirus 3, anti-EV71 y enterovirus genérico) (Chemicon, EE.UU. y Dako, Glostrup, Dinamarca); b) neutralización con antisueros policlonales combinados en 4 grupos para identificar las mezclas de poliovirus (RIVM pools, National Institute of Public Health and the Environment, Países Bajos).
c) Caracterización intratípica de poliovirus para diferenciar las cepas vacunales de las salvajes mediante reacción en cadena de la polimerasa (RT-PCR) específica para poliovirus vacunal (recomendada por la OMS) 10 y Nested-PCR seguida del análisis con enzimas de restricción (RFLP) usando las técnicas descritas por Balanant et al 11.
d) Técnicas complementarias en caso de poliovirus vacunales asociados a casos de parálisis: a) identificación de poliovirus derivados de vacuna, con una homología en el gen VP1 menor del 99%, mediante amplificación de dicho gen, secuenciación y estudio de la secuencia; b) identificación de mutaciones en la región 5' no codificante asociadas con reversión a neurovirulencia 12.
Resultados
Actividad de los sistemas de vigilancia
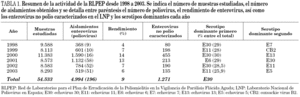
El total de muestras estudiadas por la RLPEP durante los 6 años ha sido de 54.533 (13% heces y 87% de líquido cefalorraquídeo [LCR] y exudados faríngeos). Los síndromes estudiados se dividen en PFA (3%) y otros (97%). Entre estos últimos el síndrome dominante fue meningitis aséptica. El 9% del total de muestras estudiadas presentaron aislamiento de enterovirus. Los datos detallados por año se presentan en la tabla 1.
Casos de PFA
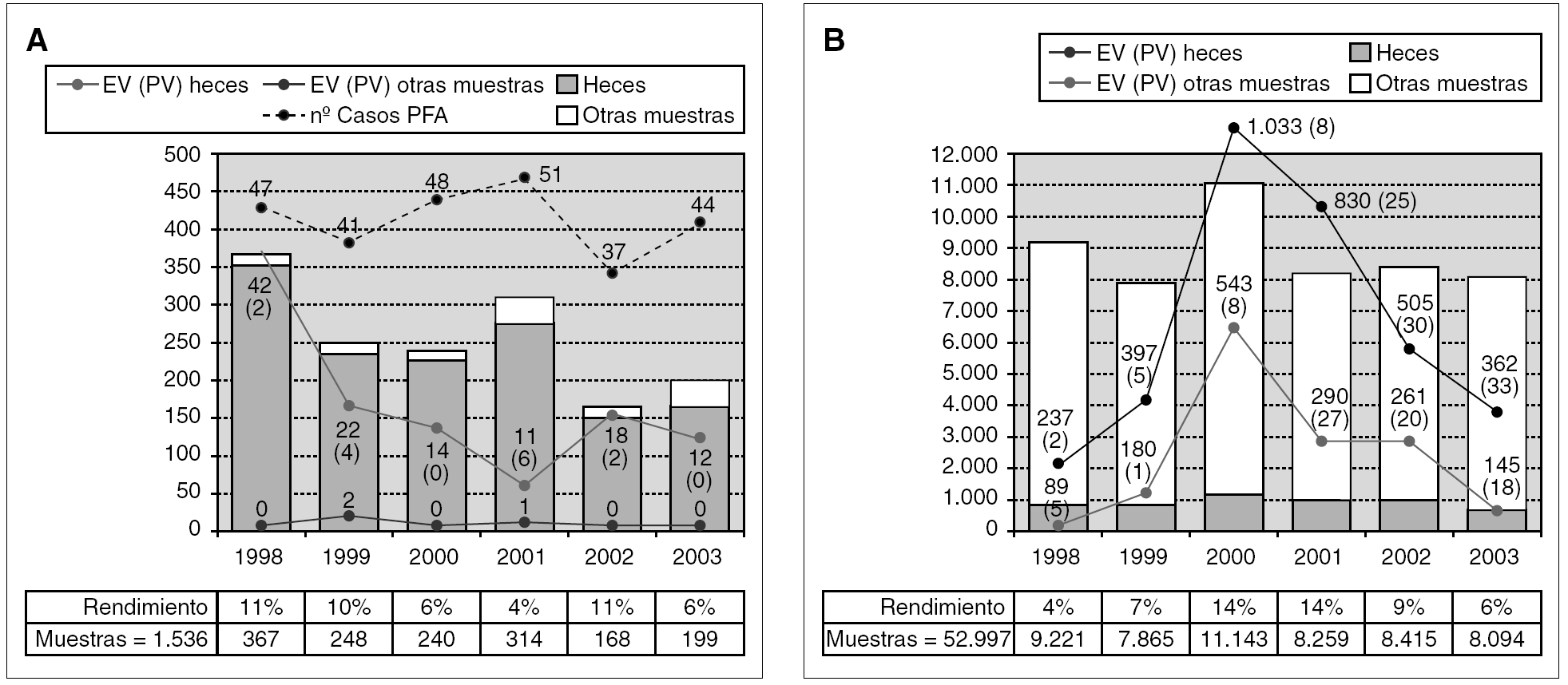
En el estudio de los 268 casos de PFA declarados, el total de muestras de casos y contactos estudiados fue de 1.536 (el 92%, heces). La distribución de los casos de PFA a lo largo de los 6 años ha sido: 47 (1998), 41 (1999), 48 (2000), 51 (2001), 37 (2002) y 44 (2003). En la figura 1A se indica la distribución del número de muestras estudiadas, el número de positivos obtenido cada año y el rendimiento anual obtenido. En el primer año es cuando más muestras se estudiaron, debido a un mayor número de contactos por cada caso de PFA, con un total del 11% de aislamientos de enterovirus. Por el contrario, el año 2002 fue en el que menos muestras se estudiaron coincidiendo con el menor número de casos declarados (n = 37). El rendimiento medio de enterovirus aislados de las muestras de PFA durante los 6 años ha sido del 8%.
Figura 1. Resumen de la actividad de la Red de Laboratorios para el Plan de Erradicación de la Poliomielitis en la Vigilancia de Parálisis Flácida Aguda (A) y otros síndromes (B). Las líneas discontinuas indican el número de casos de PFA por año. El gráfico de barras representa el número y tipo de muestras estudiadas. Las líneas continuas indican los enterovirus obtenidos en heces (gris claro) y en otras muestras (gris oscuro) apareciendo el número total de enterovirus aislados así como el de poliovirus entre paréntesis. En la parte inferior se detalla el número total de muestras estudiadas y el rendimiento anual en el aislamiento de enterovirus.
Otros síndromes
Se han estudiado un total de 52.997 muestras procedentes de otros síndromes. El 90% han sido de LCR, por ser la muestra adecuada para establecer una relación directa con los síndromes neurológicos (fig. 1B). En este tipo de síndromes los enterovirus obtenidos representaron una media del 9%.
Tipificación de enterovirus no polio
El resumen de esta actividad se presenta en la tabla 1. El año 2000 es el de mayor número de aislamientos caracterizados en el LNP con 455 enterovirus no polio, seguido del año 2001 con 213. Los serotipos más frecuentes varían según los años. El Echovirus 30 es en los años 1998, 2000 y 2002, Echovirus 11 en 1999 y 2003 y Echovirus 6 en 2001. Destaca el comportamiento del Echovirus 13, segundo más frecuente en 2000 y nunca antes detectado en nuestro país 13-15.
Tipificación y caracterización intratípica de poliovirus
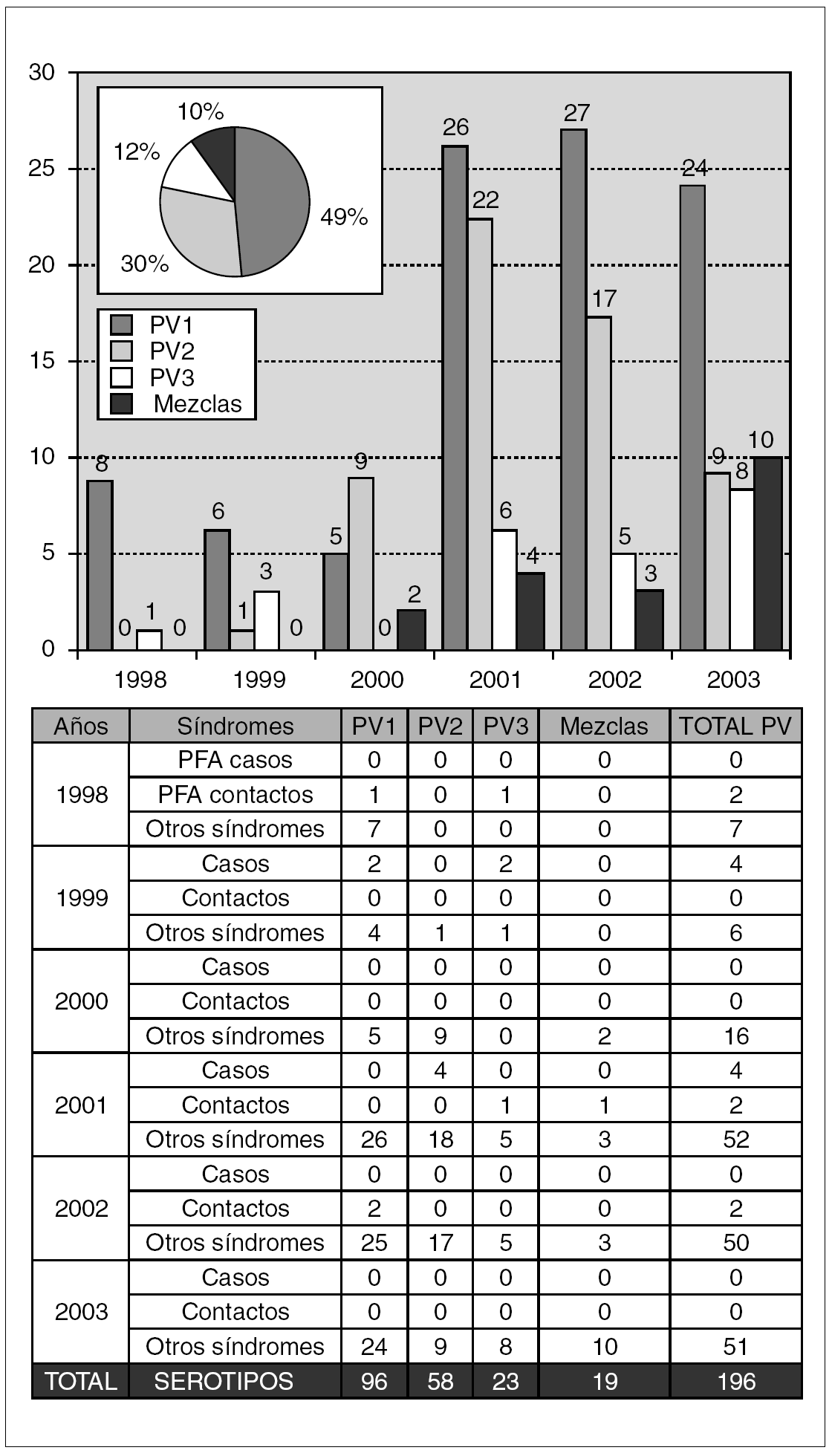
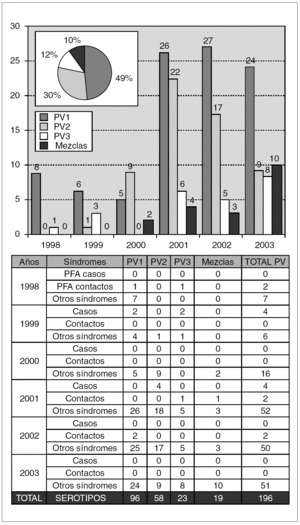
En la figura 2 se indican todos los aislamientos de poliovirus en cada año del estudio. El total de poliovirus aislados durante los 6 años fue de 196, de los cuales el 56% procedía de muestras de exudados faríngeos obtenidas de niños con patología respiratoria y el 44% restante de heces. El 87% de los casos se aislaron en niños menores de un año. Todos los poliovirus se caracterizaron como Sabin-like (SL) y fueron confirmados como tales por el Laboratorio Regional Europeo (Robert Koch Institut, Berlín). El serotipo mayoritario fue poliovirus 1 SL (49%), seguido de poliovirus 2 SL (29%) y poliovirus 3 SL (12%), aunque también se aislaron mezclas. En el año 1998, los nueve aislamientos se obtuvieron en niños menores de 3 meses. Es de destacar un poliovirus 1 y un poliovirus 2 aislados en contactos sanos de casos de PFA. En 1999, todos los poliovirus se aislaron en niños menores de 6 meses excepto un poliovirus 1 aislado de un paciente de 70 años con diarrea. En ese año se aislaron cuatro poliovirus de las heces de dos casos de PFA, aunque finalmente uno de ellos se descartó como tal. En el año 2000, todos los poliovirus (n = 16) procedían de otros síndromes distintos de PFA, y de nuevo correspondían a niños menores de 6 meses. Estos primeros 3 años de seguimiento destacan por el bajo número de poliovirus aislados en comparación con los 3 años siguientes.
Figura 2. Caracterización de los distintos tipos de poliovirus vacunales en cada año del estudio (gráfico de barras) y en total (gráfico de sectores). La tabla inferior detalla la distribución de los aislamientos por año y síndrome clínico, diferenciando entre las muestras de casos y contactos de parálisis flácida aguda (PFA).
En el año 2001 se aislaron cuatro poliovirus 2 a partir de cuatro heces consecutivas de un mismo caso de PFA. El paciente fue diagnosticado de inmunodeficiencia combinada severa después de recibir las primeras 2 dosis de la vacuna oral. En el año 2002, el 83% de los aislados se obtuvieron en niños menores de 6 meses. Se aislaron dos poliovirus 1 de las heces de un contacto de una paciente adulta diagnosticada de PFA. En el año 2003 el 92% de los poliovirus se obtuvieron en menores de 6 meses. De entre éstos la edad mayoritaria era de 2 meses, con el 47%. Todos los aislados procedían de otros síndromes distintos de PFA.
Discusión
La actividad de la RLPEP ha sido satisfactoria, ya que durante estos años se ha estudiado un elevado número de muestras, se ha obtenido un alto porcentaje de aislamientos y, por tanto, se puede concluir que según la clasificación virológica de la OMS no ha habido casos de poliomielitis causados por poliovirus salvaje en España en los años estudiados y el territorio puede considerarse libre de la circulación de poliovirus salvaje. De hecho, España, junto con el resto de la región europea fue certificada como libre de poliovirus salvaje en 2002.
El rendimiento en cuanto al número de enterovirus aislados, está en consonancia con las epidemias de meningitis por enterovirus. El año 2000 destaca como el de mayor circulación y el de mayor actividad 16. Las actividades del Plan de Erradicación de la Poliomielitis han permitido estudiar sistemáticamente las infecciones por enterovirus, permitiendo mejorar los datos sobre su circulación. En este sentido se han confirmado como los enterovirus más frecuentemente caracterizados Echovirus 30, 6 y 11 y se ha comprobado su patrón de circulación de periodicidad trianual en los brotes de meningitis, con aislamientos esporádicos en los años intermedios para la mayoría de ellos. Además, parece existir un desplazamiento cada año de unos serotipos por otros, describiéndose además la aparición brusca de alguno de ellos, como el Echovirus 13 13-15,17. Los 9 laboratorios de la RLPEP participan en los controles anuales de calidad y analizan las muestras de casos de PFA de su área. Sin embargo, su actividad en el estudio de infecciones por enterovirus en otros síndromes es heterogénea. Los laboratorios con mayor número de muestras estudiadas y aislamientos son Madrid (CNM), Barcelona, Granada, Las Palmas de Gran Canaria y Bilbao.
Por otra parte, respecto al aislamiento de poliovirus, se ha producido un incremento en los últimos 3 años consecuencia de una mayor vigilancia y concienciación por parte de los laboratorios integrantes de la red. La mayoría de los poliovirus analizados en este estudio han sido aislamientos casuales en niños acabados de vacunar que presentaban síntomas respiratorios o febriles. Sólo en 2 casos los aislamientos se relacionaban directamente con la patología de parálisis flácida aguda, concretamente un caso del año 1999 (PFA 3003) y otro en el año 2001 (PFA 4809) se han considerado poliomielitis posvacunal.
Es preciso consolidar los esfuerzos alcanzados en el programa de erradicación, y en esa línea el 15 de enero de 2004, se produjo la declaración de Ginebra para la erradicación de la poliomielitis, mediante la que los ministros de Sanidad de los Gobiernos de Afganistán, Pakistán, Níger, Nigeria, Egipto y la India, los 6 países prioritarios para interrumpir la transmisión de los poliovirus en el mundo, se comprometieron a intensificar todas las actividades de inmunización y de vigilancia de la polio con el fin de lograr interrumpir la transmisión del poliovirus salvaje.
Todos los procedimientos establecidos deben continuar en todos los países hasta que se consiga la interrupción en el mundo de la circulación del poliovirus salvaje, y así evitar la introducción de dichos poliovirus en zonas libres de ellos. Precisamente, en algunos países declarados libres de polio como Benin, Burkina Faso, Camerún, República Central de África, Chad, Costa de Marfil, Ghana y Togo se han detectado recientemente casos de poliovirus salvaje, relacionados genéticamente con los aislados en el norte de Nigeria. Estas importaciones parecen relacionadas con un importante rebrote de la enfermedad en Nigeria, a consecuencia de la suspensión, en agosto de 2003, de las campañas de inmunización en algunos estados del norte. En febrero de 2004 se detectó un caso de poliovirus tipo I en Botswana, país que llevaba libre de polio desde 1991, y que se relacionó con el brote de Nigeria 18. Dicho país ha reanudado las campañas de inmunización en febrero-marzo de 2004. De enero de 2004 hasta el 10 de noviembre del mismo año, se confirmaron 98 casos de polio salvaje ocurridos en 10 países previamente declarados como libres de polio; se restablecía en cinco de ellos la transmisión endémica de los poliovirus importados. En los 6 países endémicos se confirmaron 820 casos 19. Los objetivos propuestos por la OMS en los años próximos (2004-2008) son: a) interrumpir la transmisión de poliovirus salvaje mediante la intensificación de todas las actividades de inmunización (2004-2005); b) alcanzar la certificación mundial continuando con la vigilancia PFA y con el plan de contención de los poliovirus salvaje en los laboratorios (2006-2008); c) desarrollar políticas para la era de la poscertificación, ya que el cese de la vacuna oral está previsto para el año 2009, y d) mantener la infraestructura creada en el plan de la erradicación de la poliomielitis y continuar con la vigilancia e inmunización.
España, por su situación geográfica, puede ser puerta de entrada de poliovirus salvaje y dar lugar a casos importados de poliomielitis, con lo que el proceso de vigilancia debe mantenerse y potenciarse consolidando los laboratorios actuales y aumentando si es posible la participación de laboratorios de otras comunidades. Está previsto un cambio en el número de aislamientos de poliovirus vacunal debido a la sustitución desde enero de 2004 de la vacuna oral por la inactivada en España. Por tanto, a partir de ahora cualquier aislamiento de poliovirus debe ser considerado como extremadamente sospechoso de ser un poliovirus salvaje o un poliovirus derivado de vacuna. Además es muy importante que siga en activo el programa de la contención de los poliovirus salvajes en los laboratorios para prevenir la reintroducción accidental desde los laboratorios de poliovirus salvajes 6,20,21.
La era posterior a la erradicación planteará nuevos desafíos, incluido un esfuerzo masivo para garantizar el confinamiento seguro de las reservas de laboratorio de poliovirus salvajes y quizá lo más difícil de todo, la aplicación de una estrategia coordinada a escala mundial para suspender definitivamente la vacunación con la vacuna oral (OPV). Dado el riesgo poco frecuente pero real de poliomielitis paralítica asociada a la vacuna, puede que sea necesario dejar de utilizar las cepas actuales de OPV poco después de certificar la erradicación. Las investigaciones en curso determinarán si se necesitará alguna vacuna en la era posterior a la erradicación 19,22.
Agradecimientos
Los autores quieren agradecer a Isidoro Bustillo, Hortensia del Pozo y Purificación Higueras la asistencia técnica prestada. También a María Paz Sánchez-Seco su colaboración en los primeros años del estudio y a Inmaculada Casas por los estudios de tipificación molecular.
Relación de Red de Laboratorios de Vigilancia de Parálisis Flácida Aguda
Andalucía (Granada): José M. Navarro; Canarias (Las Palmas de Gran Canaria): Carmen Pérez; Castilla y León (Valladolid): Raúl Ortiz de Lejarazu; Cataluña (Barcelona): Nuria Rabella; Comunidad de Madrid (Madrid): Antonio Tenorio; Comunidad Valenciana (Valencia): Beatriz Acosta; Galicia (Vigo, Pontevedra): Isabel López Miragaya; Galicia (Santiago, A Coruña): Eduardo Varela; País Vasco (Bilbao): Gurutze Rubio.
Correspondencia: Dra. G. Trallero.
Laboratorio Nacional de Poliovirus. Servicio de Virología.
Centro Nacional de Microbiología. Instituto de Salud Carlos III.
Ctra. de Majadahonda a Pozuelo, km 2. 28220 Majadahonda. Madrid. España.
Correo electrónico: gtralle@isciii.es
Manuscrito recibido el 3-2-2005; aceptado el 16-6-2005.