La información existente sobre el riesgo cardiovascular (RCV) de los pacientes con infección por el virus de la inmunodeficiencia humana (VIH) en España en el momento actual es limitada.
MétodoAnálisis de una cohorte prospectiva multicéntrica nacional de pacientes con infección por el VIH (CoRIS) entre enero de 2010 y junio de 2011. El RCV de los pacientes se evaluó con las escalas de Framingham, REGICOR y SCORE.
ResultadosSe incluyeron 1.019 pacientes (76% varones, edad media 40 años) procedentes de 13 centros que representaban a 10 comunidades autónomas. El 65,4% estaba recibiendo tratamiento antirretroviral, el 36,7% con no análogos de nucleósidos, el 24% con inhibidores de proteasa (IP) (52% con atazanavir/r o darunavir/r) y el 4,6% con raltegravir. El 56,2% tenía una carga viral del VIH <50 copias/ml. La prevalencia de factores de riesgo cardiovascular era: tabaquismo 46%, colesterol HDL (C-HDL) < 40 mg/dl 36,1%, colesterol total (C-total) > 200 mg/dl 27,8%, edad > 45 años 27,2%, síndrome metabólico 11,5%, hipertensión 9,4%, consumo de cocaína 7% y diabetes 2,9%. El tratamiento antirretroviral se asoció con concentraciones más elevadas de C-total y C-LDL, aunque también mayor C-HDL y menor cociente C-total/C-HDL; los pacientes tratados con IP potenciados con dosis altas de ritonavir tuvieron los niveles más altos de C-total y del cociente C-total/C-HDL. Según Framingham cardiovascular, coronario, REGICOR y SCORE, el 15,2, el 6,4, el 4,2 y el 3,9% de los pacientes, respectivamente, se clasificaron en el grupo de «riesgo moderado-alto».
ConclusiónEn los pacientes con infección por VIH de CoRIS, la prevalencia de factores de riesgo modificables es todavía elevada. Las escalas habituales identifican un número relativamente reducido de personas con RCV elevado.
Current information on cardiovascular risk (CVR) in HIV-infected patients in Spain is limited.
MethodsAn analysis was made of a prospective multicentre cohort of Spanish HIV-infected patients (CoRIS) between January-2010 and July-2011. CVR was evaluated using Framingham, REGICOR and SCORE equations.
ResultsThe study included 1019 patients (76% males, mean age 40 years) recruited from 13 hospitals belonging to 10 autonomous communities in Spain. Almost two-thirds (65.4%) of patients were on antiretroviral therapy (ART), 36.7% with non-nucleoside analogs, 24% with protease inhibitors (PIs) (52% with atazanavir/r or darunavir/r) and 4,6% with raltegravir. More than half (56.2%) of the patients had an HIV viral load <50 copies/ml. Smoking prevalence was 46%, HDL cholesterol (HDL-C) <40mg/dl 36.1%, total cholesterol (total-C) >200mg/dl 27.8%, age >45years 27.2%, metabolic syndrome 11.5%, hypertension 9.4%, cocaine use 7%, and diabetes 2.9%. ART was associated with higher total-C and LDL-C concentrations, although also higher HDL-C and lower total-C/HDL-C ratio; patients receiving PIs boosted with a high ritonavir dose showed higher total-C levels and higher total-C/HDL-C ratio. According to Framingham cardiovascular, and coronary, REGICOR, and SCORE equations, 15.2%, 6.4%, 4.2% and 3.9% of patients, respectively, were classified as having moderate or high CVR.
ConclusionIn HIV-infected patients from CoRIS, prevalence of modifiable CVR factors is still high. Commonly used scores identify a relatively low number of patients with high CVR.
La disminución de la mortalidad asociada al sida con la introducción del tratamiento antirretroviral (TAR) de gran eficacia1,2 y el consecuente envejecimiento paulatino de las personas infectadas por el virus de la inmunodeficiencia humana (VIH) han conducido a un aumento en la prevalencia y en la mortalidad por enfermedades cardiovasculares (ECV) en este colectivo3. Existen varios estudios que demuestran que el riesgo de desarrollo de ECV es mayor, hasta del doble, en estos pacientes que en la población general4-6. La mayor prevalencia de factores de riesgo cardiovascular (RCV), el propio virus y otros copatógenos, y el TAR y sus complicaciones, se han implicado entre los principales responsables del incremento del riesgo7-10. Por todo ello, el diagnóstico precoz, el tratamiento y la prevención de la ECV se han convertido en una de las prioridades en la atención de estos pacientes.
En la población general, las medidas de prevención han demostrado ser eficaces en la reducción del riesgo de desarrollo de ECV en individuos asintomáticos11 y, aunque hasta ahora no existen datos sobre reducción del número de episodios con la intervención en personas infectadas por el VIH, es esperable que este beneficio sea también extrapolable a este colectivo12. La estimación del RCV absoluto o global permite tomar decisiones sobre las prioridades de prevención cardiovascular en personas asintomáticas de modo más eficiente que mediante el abordaje de cada uno de los factores de riesgo por separado13. En las últimas décadas, el cálculo del riesgo absoluto de presentar un episodio coronario se ha basado en la ecuación de Framingham14. Sin embargo, esta ecuación sobreestima el riesgo en los países europeos, donde la incidencia de enfermedad coronaria es más baja que en Norteamérica15. Por este motivo, en nuestro país se han incorporado otras herramientas para el cálculo del riesgo, como las basadas en el estudio REGICOR (Registre Gironí del Cor)16, en que se recalibró la ecuación de Framingham para adaptarla a la población española, o la ecuación del proyecto SCORE (Systematic Coronary Risk Evaluation), que estima el riesgo de ECV mortal a 10 años en países de Europa17.
Hasta el momento, la información sobre el RCV de los pacientes con infección por el VIH en España es muy escasa. Los datos disponibles se limitan a zonas geográficas concretas y son anteriores a 200618-20. La prescripción preferente en los últimos años de nuevos inhibidores de la proteasa (IP) potenciados con dosis bajas (100mg) de ritonavir, con menores efectos metabólicos que los IP previos, la incorporación de nuevos fármacos con un perfil cardiovascular más favorable, los cambios producidos en las características demográficas de la población debido a los continuos flujos migratorios y al envejecimiento progresivo de los pacientes, y las modificaciones en el estilo de vida, como la reciente prohibición del tabaco en nuestro país, podrían haber contribuido a modificar el RCV de los pacientes con infección por el VIH. Sería deseable disponer de información actualizada y representativa desde el punto de vista geográfico sobre el RCV de los pacientes con infección por el VIH en España, con el fin de planificar estrategias de actuación a nivel general.
La cohorte de la Red Española de Investigación en Sida (CoRIS) es una cohorte nacional multicéntrica de pacientes con infección por el VIH. El objetivo del presente estudio fue evaluar el RCV en el momento actual en personas integrantes de CoRIS, conocer su relación con las características sociodemográficas, inmunovirológicas y el TAR de los pacientes e identificar los principales factores implicados en el riesgo más elevado.
MétodosPoblación de estudio y recogida de datosEl estudio se realizó con participantes de CoRIS, una cohorte abierta, prospectiva y multicéntrica de pacientes con infección por el VIH confirmada, naïve al TAR al inicio del estudio, en la que participan centros públicos de 13 comunidades autónomas en España desde 200421,22. Anualmente se realiza una actualización de los datos inmunológicos, virológicos, cambios en el tratamiento y desarrollo de episodios al centro coordinador ubicado en el Centro Nacional de Epidemiología en Madrid. Esta cohorte está, además, asociada a un repositorio de muestras biológicas. En el presente proyecto participaron 13 centros de CoRIS que representaban a 10 comunidades autónomas distribuidas por diversas áreas geográficas, que incluyen Andalucía, Canarias, Cataluña, Comunidad Valenciana, Islas Baleares, La Rioja, Madrid, Murcia, Navarra y País Vasco. Todos los pacientes adultos con infección por el VIH que acudían regularmente a las unidades de los hospitales participantes y que pertenecían a la cohorte eran candidatos para ser incluidos. La recogida de la información se efectuó entre enero de 2010 y junio de 2011, a medida que los pacientes de CoRIS acudían a las consultas de los centros participantes, a través de una aplicación informática común (Excel, Microsoft Office 2003) que incluía una calculadora con la que se obtuvo la puntuación de las escalas. Se recogieron los siguientes datos: edad, sexo, hábito tabáquico, antecedentes de diabetes, medida de la presión arterial (PA) y concentraciones plasmáticas de colesterol total (C-total), colesterol HDL (C-HDL) y colesterol LDL (C-LDL). De forma opcional se recogió también información sobre el antecedente de hipertensión arterial diagnosticada o tratada, consumo de cocaína, enfermedad cardiovascular previa, antecedentes familiares de enfermedad cardiovascular precoz (en pariente de primer grado —padres o hermanos— antes de los 55 años si es hombre o antes de los 65 años si es mujer), existencia de lipodistrofia, peso, talla, índice de masa corporal, perímetro de cintura, niveles de glucemia y triglicéridos. Con esta información, la aplicación determinaba de forma automática si existía síndrome metabólico. La hipertensión se definió por unas cifras >140/90mmHg en 2 mediciones separadas al menos 2 semanas o un diagnóstico previo en un paciente en tratamiento antihipertensivo. La diabetes se definió por una cifra de glucemia en ayunas >126mg/dl o un diagnóstico previo en un paciente en tratamiento antidiabético, y el síndrome metabólico se definió por un perímetro de cintura >102cm en hombres o >88cm en mujeres, más al menos 2 de los siguientes criterios: triglicéridos >150mg/dl, C-HDL <40mg/dl en hombres o <50mg/dl en mujeres, PA ≥130/85mmHg, o glucosa en ayunas ≥100mg/dl o diagnóstico de diabetes tipo 214. Se clasificaron como fumadores los pacientes que habían fumado al menos un cigarrillo en el último mes, y como consumidores de cocaína los que la habían consumido alguna vez en el último año. La presencia de lipodistrofia se definió por alteraciones en la distribución de la grasa corporal evidentes para el paciente y para el médico.
Las variables relacionadas con las características sociodemográficas y todos los datos relativos a la infección por el VIH —vía de transmisión, categoría del CDC, nadir de CD4, recuento de CD4, carga viral del VIH y TAR— se obtuvieron cruzando los anteriores con los datos de la cohorte CoRIS. Para evaluar el TAR solo se incluyeron los pacientes cuya pauta no se había modificado al menos en los últimos 3meses. Lopinavir/ritonavir, fosamprenavir/ritonavir y saquinavir/ritonavir se clasificaron como IP potenciados con dosis altas (200mg) de ritonavir, y atazanavir/ritonavir y darunavir/ritonavir como IP potenciados con dosis bajas (100mg). El recuento de linfocitos CD4 y la carga viral se obtuvieron con un período ventana de ±8 meses con respecto a la recogida de la información relativa al RCV. Todos los participantes de CoRIS firman un consentimiento informado a la entrada en la cohorte21, y puesto que toda la información recogida para el estudio forma parte de la que se obtiene de forma rutinaria en la atención ambulatoria de personas infectadas por el VIH, o que sería deseable obtener según el documento de calidad asistencial de GESIDA23, no se solicitó un nuevo consentimiento informado.
Determinación del riesgo cardiovascularLa probabilidad individual de desarrollar a los 10 años enfermedad coronaria (infarto agudo de miocardio, angina o muerte de causa coronaria) y cardiovascular (incluye además ictus, insuficiencia cardiaca congestiva y enfermedad arterial periférica) se calcularon con la ecuación de Framingham24. Se estimó también el riesgo coronario global a 10 años con las tablas REGICOR y la probabilidad de muerte de causa cardiovascular a los 10 años con las tablas SCORE. Se clasificó a los individuos en 3 categorías de riesgo: bajo, moderado y alto, equivalente a <10, 10-19 y ≥20% con las ecuaciones de Framingham; <5, 5-9,9 y ≥10% con REGICOR, y <3, 3-4 y ≥5% con SCORE. A los pacientes diabéticos se les asignó directamente una puntuación de 20% en las escalas de Framingham de acuerdo a los criterios del ATP III del NCEP14.
Análisis estadísticoPara comparar la prevalencia de los factores de RCV clásicos en diferentes subgrupos de pacientes en relación con sus características sociodemográficas y clínicas se utilizó la prueba de chi-cuadrado o el test exacto de Fisher, y el test de Mann-Whitney para comparar las medianas de los valores obtenidos en las escalas de riesgo. Se evaluó por regresión logística el peso de cada uno de los factores de RCV tradicionales en la asociación de una mayor puntuación en la escala de Framingham con diferentes características sociodemográficas y clínicas de los pacientes. Se utilizó como variable dependiente una probabilidad de episodio coronario mayor del 5% a los 10 años según las tablas de Framingham. Los análisis estadísticos se realizaron con el paquete SPSS versión 12.0 (SPSS). Se consideró significativa una p<0,05.
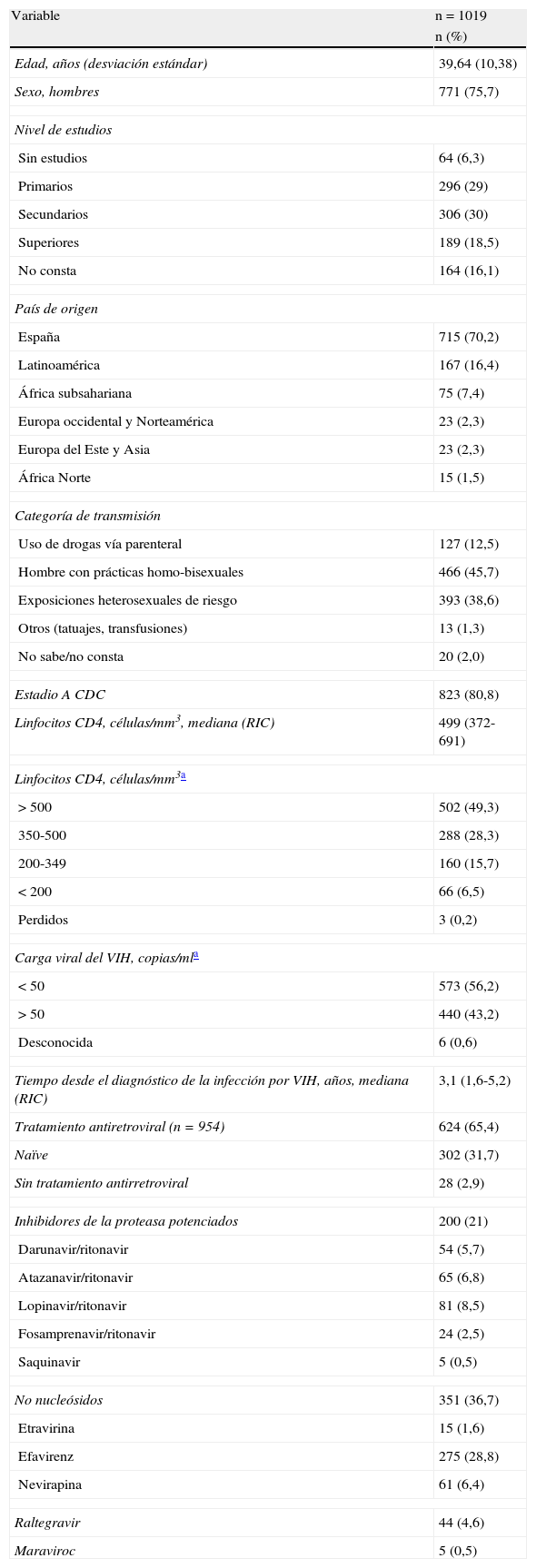
ResultadosDe 1.421 personas evaluadas se excluyeron 402, en las que faltaba información sobre alguna de las variables necesarias para el cálculo del riesgo por las escalas, por lo que se analizaron finalmente 1.019 pacientes (tabla 1). Las características sociodemográficas y las referentes a la infección por el VIH (edad, procedencia española, nivel de estudios, categoría de transmisión de la infección, tiempo desde el diagnóstico y recuento de linfocitos CD4 a la entrada) en el grupo excluido fueron similares a las del conjunto de la cohorte, con excepción del sexo, ya que el número de mujeres fue mayor en el grupo de estudio del RCV (24,1 vs. 19,3%, p<0,001). Para el análisis de los datos relativos al TAR se excluyeron 65 pacientes en los que se había modificado la pauta de tratamiento en los últimos 3 meses. Las características sociodemográficas se detallan en la tabla 1. La categoría de transmisión predominante eran las prácticas homo/bisexuales en varones (45,7%), seguida de transmisión heterosexual (38,6%). El 80,8% de los pacientes estaba asintomático y el 10,9% pertenecía a la categoría C del CDC. El 56,2% tenía una carga viral plasmática del VIH <50copias/ml. Seiscientos veinticuatro (65,4%) pacientes estaban recibiendo TAR: el 36,7% con inhibidores de la transcriptasa inversa no análogos de nucleósidos (ITINAN), el 24% con inhibidores de la proteasa (IP) (52% de ellos con atazanavir con/sin ritonavir o con darunavir/ritonavir), y el 4,6% con raltegravir. Trescientos dos (31,7%) eran naïve al TAR y 28 (2,9%) habían interrumpido el tratamiento.
Características de los pacientes
| Variable | n=1019 |
| n (%) | |
| Edad, años (desviación estándar) | 39,64 (10,38) |
| Sexo, hombres | 771 (75,7) |
| Nivel de estudios | |
| Sin estudios | 64 (6,3) |
| Primarios | 296 (29) |
| Secundarios | 306 (30) |
| Superiores | 189 (18,5) |
| No consta | 164 (16,1) |
| País de origen | |
| España | 715 (70,2) |
| Latinoamérica | 167 (16,4) |
| África subsahariana | 75 (7,4) |
| Europa occidental y Norteamérica | 23 (2,3) |
| Europa del Este y Asia | 23 (2,3) |
| África Norte | 15 (1,5) |
| Categoría de transmisión | |
| Uso de drogas vía parenteral | 127 (12,5) |
| Hombre con prácticas homo-bisexuales | 466 (45,7) |
| Exposiciones heterosexuales de riesgo | 393 (38,6) |
| Otros (tatuajes, transfusiones) | 13 (1,3) |
| No sabe/no consta | 20 (2,0) |
| Estadio A CDC | 823 (80,8) |
| Linfocitos CD4, células/mm3, mediana (RIC) | 499 (372-691) |
| Linfocitos CD4, células/mm3a | |
| >500 | 502 (49,3) |
| 350-500 | 288 (28,3) |
| 200-349 | 160 (15,7) |
| <200 | 66 (6,5) |
| Perdidos | 3 (0,2) |
| Carga viral del VIH, copias/mla | |
| <50 | 573 (56,2) |
| >50 | 440 (43,2) |
| Desconocida | 6 (0,6) |
| Tiempo desde el diagnóstico de la infección por VIH, años, mediana (RIC) | 3,1 (1,6-5,2) |
| Tratamiento antiretroviral (n=954) | 624 (65,4) |
| Naïve | 302 (31,7) |
| Sin tratamiento antirretroviral | 28 (2,9) |
| Inhibidores de la proteasa potenciados | 200 (21) |
| Darunavir/ritonavir | 54 (5,7) |
| Atazanavir/ritonavir | 65 (6,8) |
| Lopinavir/ritonavir | 81 (8,5) |
| Fosamprenavir/ritonavir | 24 (2,5) |
| Saquinavir | 5 (0,5) |
| No nucleósidos | 351 (36,7) |
| Etravirina | 15 (1,6) |
| Efavirenz | 275 (28,8) |
| Nevirapina | 61 (6,4) |
| Raltegravir | 44 (4,6) |
| Maraviroc | 5 (0,5) |
RIC: rango intercuartílico.
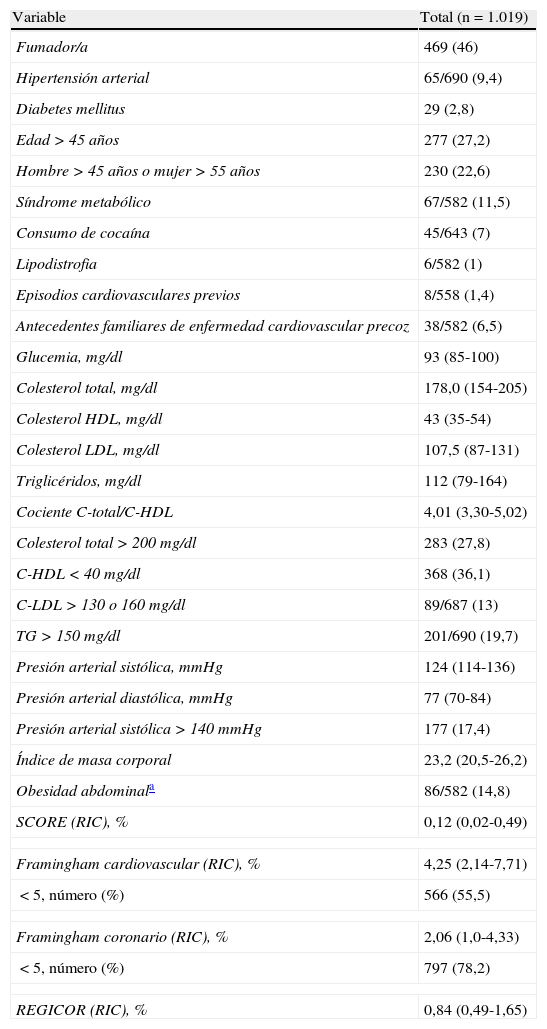
La prevalencia de tabaquismo era del 46%; la de hipertensión, del 9,4%; la de diabetes, del 2,8%; la de C-total >200mg/dl, del 27,8%; la de C-HDL <40mg/dl, del 36,1%; la de triglicéridos >150mg/dl, del 19,7%; la de edad >45 años, del 27,2%; la de síndrome metabólico, del 11,5%, y la de consumo de cocaína, del 7% (tabla 2). Solo un 1% de los pacientes tenía lipodistrofia. Hubo una mayor prevalencia de factores de RCV en los hombres, que eran con más frecuencia hipertensos (10,9 vs. 5,7%), tenían un C-HDL más bajo (41 vs. 53mg/dl), los triglicéridos más altos (120 vs. 101mg/dl), mayores cifras de tensión sistólica (126 vs. 117mmHg) y diastólica (78 vs. 75mmHg), y mayor consumo de cocaína (8,2 vs. 3,9%), aunque también menores cifras de C-total (176 vs. 184mg/dl) y menor frecuencia de obesidad abdominal (10,3 vs. 25,3%) que las mujeres (p<0,05 en todos los casos). La tabla 3 muestra la prevalencia de los factores de RCV en relación con diferentes características sociodemográficas, inmunológicas y virológicas de los pacientes. Los españoles y los procedentes de países occidentales eran con más frecuencia varones, tenían mayor edad y fumaban más que los pacientes de otras nacionalidades. Entre estos últimos, la mayor proporción de mujeres se encontró en las originarias de África subsahariana (69,3% mujeres vs. 30,7% varones) y la mayor proporción de no fumadores en los africanos (88,9%) y latinoamericanos (70,5%). En las personas con menor nivel de estudios la edad era superior, había una mayor proporción de mujeres y una tendencia a un mayor consumo de tabaco que en los que tenían estudios medios o superiores.
Prevalencia de factores de riesgo cardiovascular y puntuación de las escalas de riesgo (SCORE, Framingham y REGICOR)
| Variable | Total (n=1.019) |
| Fumador/a | 469 (46) |
| Hipertensión arterial | 65/690 (9,4) |
| Diabetes mellitus | 29 (2,8) |
| Edad >45 años | 277 (27,2) |
| Hombre >45 años o mujer >55 años | 230 (22,6) |
| Síndrome metabólico | 67/582 (11,5) |
| Consumo de cocaína | 45/643 (7) |
| Lipodistrofia | 6/582 (1) |
| Episodios cardiovasculares previos | 8/558 (1,4) |
| Antecedentes familiares de enfermedad cardiovascular precoz | 38/582 (6,5) |
| Glucemia, mg/dl | 93 (85-100) |
| Colesterol total, mg/dl | 178,0 (154-205) |
| Colesterol HDL, mg/dl | 43 (35-54) |
| Colesterol LDL, mg/dl | 107,5 (87-131) |
| Triglicéridos, mg/dl | 112 (79-164) |
| Cociente C-total/C-HDL | 4,01 (3,30-5,02) |
| Colesterol total >200mg/dl | 283 (27,8) |
| C-HDL <40mg/dl | 368 (36,1) |
| C-LDL >130 o 160mg/dl | 89/687 (13) |
| TG >150mg/dl | 201/690 (19,7) |
| Presión arterial sistólica, mmHg | 124 (114-136) |
| Presión arterial diastólica, mmHg | 77 (70-84) |
| Presión arterial sistólica >140mmHg | 177 (17,4) |
| Índice de masa corporal | 23,2 (20,5-26,2) |
| Obesidad abdominala | 86/582 (14,8) |
| SCORE (RIC), % | 0,12 (0,02-0,49) |
| Framingham cardiovascular (RIC), % | 4,25 (2,14-7,71) |
| <5, número (%) | 566 (55,5) |
| Framingham coronario (RIC), % | 2,06 (1,0-4,33) |
| <5, número (%) | 797 (78,2) |
| REGICOR (RIC), % | 0,84 (0,49-1,65) |
C-total: colesterol total; C-HDL: colesterol HDL; C-LDL: colesterol LDL; TG: triglicéridos; RIC: rango intercuartílico.
Las variables categóricas se expresan en números (%). Las variables continuas como medianas y rangos intercuartílicos.
Prevalencia de los factores de riesgo cardiovascular tradicionales en relación con diferentes características de los pacientes
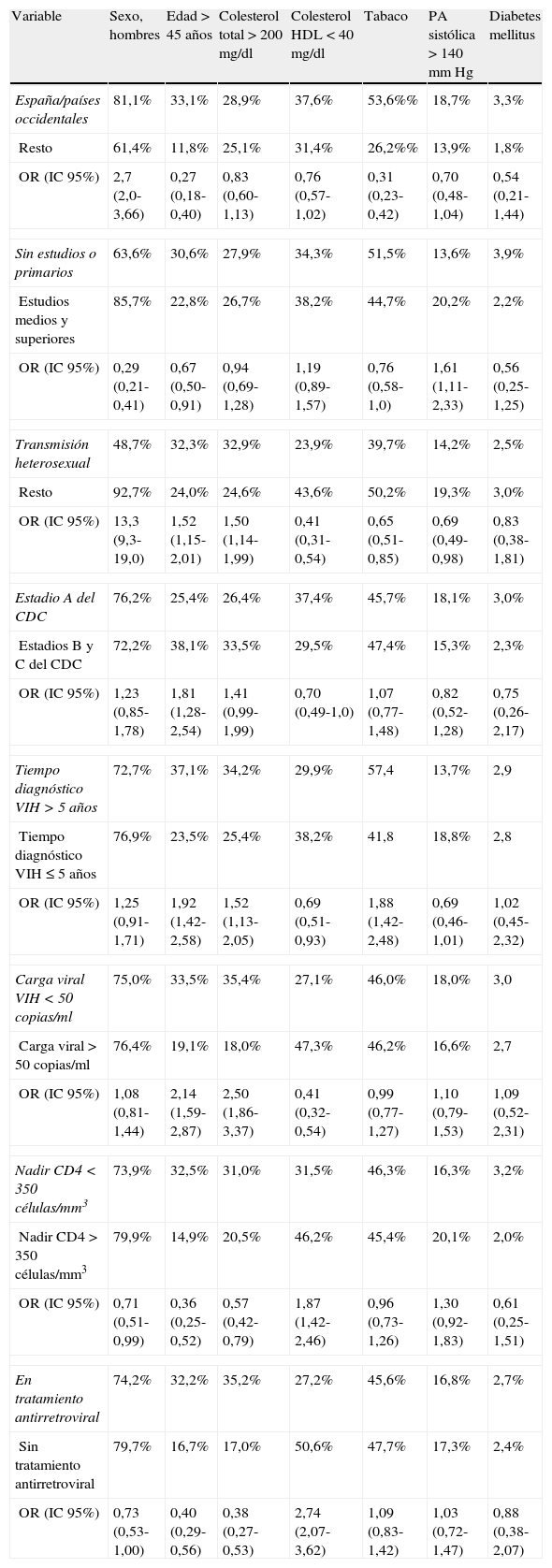
| Variable | Sexo, hombres | Edad >45 años | Colesterol total >200mg/dl | Colesterol HDL <40mg/dl | Tabaco | PA sistólica >140mm Hg | Diabetes mellitus |
| España/países occidentales | 81,1% | 33,1% | 28,9% | 37,6% | 53,6%% | 18,7% | 3,3% |
| Resto | 61,4% | 11,8% | 25,1% | 31,4% | 26,2%% | 13,9% | 1,8% |
| OR (IC 95%) | 2,7 (2,0-3,66) | 0,27 (0,18-0,40) | 0,83 (0,60-1,13) | 0,76 (0,57-1,02) | 0,31 (0,23-0,42) | 0,70 (0,48-1,04) | 0,54 (0,21-1,44) |
| Sin estudios o primarios | 63,6% | 30,6% | 27,9% | 34,3% | 51,5% | 13,6% | 3,9% |
| Estudios medios y superiores | 85,7% | 22,8% | 26,7% | 38,2% | 44,7% | 20,2% | 2,2% |
| OR (IC 95%) | 0,29 (0,21-0,41) | 0,67 (0,50-0,91) | 0,94 (0,69-1,28) | 1,19 (0,89-1,57) | 0,76 (0,58-1,0) | 1,61 (1,11-2,33) | 0,56 (0,25-1,25) |
| Transmisión heterosexual | 48,7% | 32,3% | 32,9% | 23,9% | 39,7% | 14,2% | 2,5% |
| Resto | 92,7% | 24,0% | 24,6% | 43,6% | 50,2% | 19,3% | 3,0% |
| OR (IC 95%) | 13,3 (9,3-19,0) | 1,52 (1,15-2,01) | 1,50 (1,14-1,99) | 0,41 (0,31-0,54) | 0,65 (0,51-0,85) | 0,69 (0,49-0,98) | 0,83 (0,38-1,81) |
| Estadio A del CDC | 76,2% | 25,4% | 26,4% | 37,4% | 45,7% | 18,1% | 3,0% |
| Estadios B y C del CDC | 72,2% | 38,1% | 33,5% | 29,5% | 47,4% | 15,3% | 2,3% |
| OR (IC 95%) | 1,23 (0,85-1,78) | 1,81 (1,28-2,54) | 1,41 (0,99-1,99) | 0,70 (0,49-1,0) | 1,07 (0,77-1,48) | 0,82 (0,52-1,28) | 0,75 (0,26-2,17) |
| Tiempo diagnóstico VIH >5años | 72,7% | 37,1% | 34,2% | 29,9% | 57,4 | 13,7% | 2,9 |
| Tiempo diagnóstico VIH ≤5años | 76,9% | 23,5% | 25,4% | 38,2% | 41,8 | 18,8% | 2,8 |
| OR (IC 95%) | 1,25 (0,91-1,71) | 1,92 (1,42-2,58) | 1,52 (1,13-2,05) | 0,69 (0,51-0,93) | 1,88 (1,42-2,48) | 0,69 (0,46-1,01) | 1,02 (0,45-2,32) |
| Carga viral VIH <50copias/ml | 75,0% | 33,5% | 35,4% | 27,1% | 46,0% | 18,0% | 3,0 |
| Carga viral >50copias/ml | 76,4% | 19,1% | 18,0% | 47,3% | 46,2% | 16,6% | 2,7 |
| OR (IC 95%) | 1,08 (0,81-1,44) | 2,14 (1,59-2,87) | 2,50 (1,86-3,37) | 0,41 (0,32-0,54) | 0,99 (0,77-1,27) | 1,10 (0,79-1,53) | 1,09 (0,52-2,31) |
| Nadir CD4 <350células/mm3 | 73,9% | 32,5% | 31,0% | 31,5% | 46,3% | 16,3% | 3,2% |
| Nadir CD4 >350células/mm3 | 79,9% | 14,9% | 20,5% | 46,2% | 45,4% | 20,1% | 2,0% |
| OR (IC 95%) | 0,71 (0,51-0,99) | 0,36 (0,25-0,52) | 0,57 (0,42-0,79) | 1,87 (1,42-2,46) | 0,96 (0,73-1,26) | 1,30 (0,92-1,83) | 0,61 (0,25-1,51) |
| En tratamiento antirretroviral | 74,2% | 32,2% | 35,2% | 27,2% | 45,6% | 16,8% | 2,7% |
| Sin tratamiento antirretroviral | 79,7% | 16,7% | 17,0% | 50,6% | 47,7% | 17,3% | 2,4% |
| OR (IC 95%) | 0,73 (0,53-1,00) | 0,40 (0,29-0,56) | 0,38 (0,27-0,53) | 2,74 (2,07-3,62) | 1,09 (0,83-1,42) | 1,03 (0,72-1,47) | 0,88 (0,38-2,07) |
OR: odds ratio; IC: intervalo de confianza; PA: presión arterial.
Con respecto a los pacientes sin TAR, los tratados eran mayores y tenían concentraciones más elevadas de C-total y C-LDL, aunque también mayores concentraciones de C-HDL, menor cociente C-total/C-HDL y eran con mayor frecuencia mujeres (tabla 4). Cuando se compararon los pacientes que recibían cualquier IP potenciado con el resto de los que tomaban TAR, no hubo diferencias en el C-total o sus fracciones, pero el cociente C-total/C-HDL fue más alto en los primeros. Los pacientes que tomaban IP potenciados con dosis altas de ritonavir tuvieron un C-total y un cociente C-total/C-HDL más elevado que el resto de los que recibían TAR, algo que no se encontró en los que recibían IP potenciados con 100mg de ritonavir. Estos hallazgos se reprodujeron cuando se compararon los pacientes con lopinavir/ritonavir (n=89) con el resto de los pacientes en TAR (p=0,009 y p=0,01, respectivamente). Por el contrario, los pacientes en tratamiento con ITINAN tuvieron un C-HDL más elevado y un cociente C-total/C-HDL más bajo. Todos estos resultados se mantuvieron cuando se ajustó por edad y sexo. Las cifras de triglicéridos fueron significativamente más altas en pacientes tratados con cualquier IP potenciado (137 vs. 104mg/dl, p<0,001), con IP potenciados con dosis altas de ritonavir (170 vs. 104mg/dl, p<0,001) y con lopinavir/ritonavir (176.5 vs. 104mg/dl, p<0,001), mientras que las diferencias fueron menores entre los tratados con IP potenciados con 100mg de ritonavir y los tratados con cualquier pauta ARV sin IP potenciados (120 vs. 104mg/dl, p=0,045) (n=652 pacientes con cifras de triglicéridos disponibles).
Distribución de los factores de riesgo cardiovascular en relación con el tratamiento antirretroviral
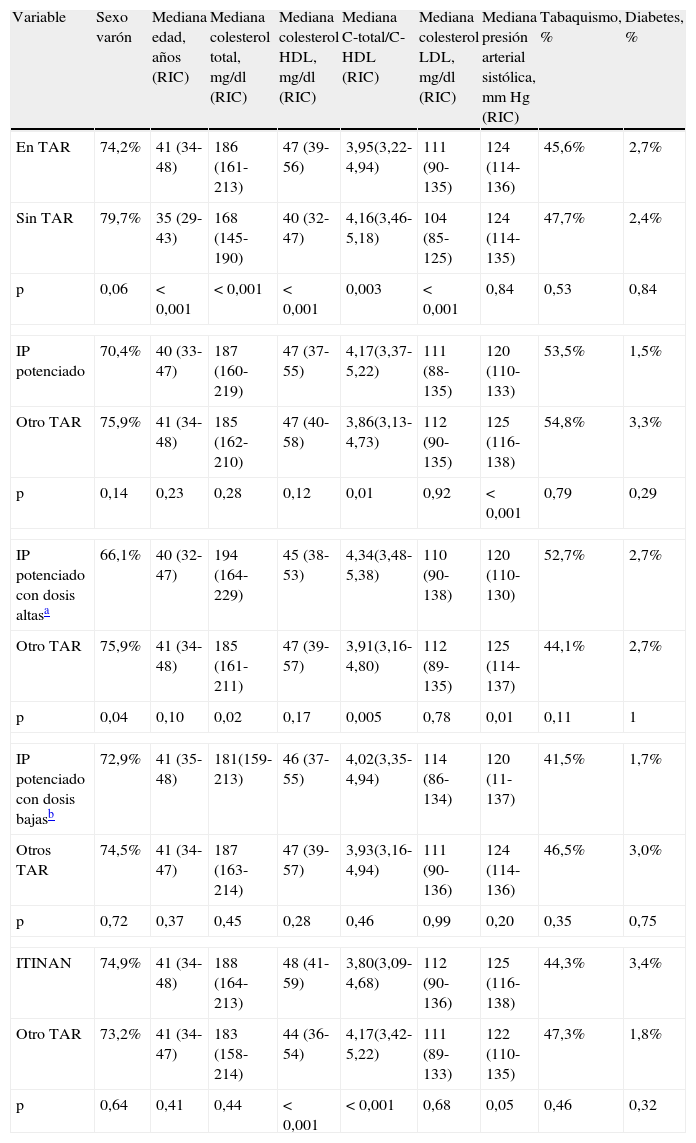
| Variable | Sexo varón | Mediana edad, años (RIC) | Mediana colesterol total, mg/dl (RIC) | Mediana colesterol HDL, mg/dl (RIC) | Mediana C-total/C-HDL (RIC) | Mediana colesterol LDL, mg/dl (RIC) | Mediana presión arterial sistólica, mm Hg (RIC) | Tabaquismo, % | Diabetes, % |
| En TAR | 74,2% | 41 (34-48) | 186 (161-213) | 47 (39-56) | 3,95(3,22-4,94) | 111 (90-135) | 124 (114-136) | 45,6% | 2,7% |
| Sin TAR | 79,7% | 35 (29-43) | 168 (145-190) | 40 (32-47) | 4,16(3,46-5,18) | 104 (85-125) | 124 (114-135) | 47,7% | 2,4% |
| p | 0,06 | <0,001 | <0,001 | <0,001 | 0,003 | <0,001 | 0,84 | 0,53 | 0,84 |
| IP potenciado | 70,4% | 40 (33-47) | 187 (160-219) | 47 (37-55) | 4,17(3,37-5,22) | 111 (88-135) | 120 (110-133) | 53,5% | 1,5% |
| Otro TAR | 75,9% | 41 (34-48) | 185 (162-210) | 47 (40-58) | 3,86(3,13-4,73) | 112 (90-135) | 125 (116-138) | 54,8% | 3,3% |
| p | 0,14 | 0,23 | 0,28 | 0,12 | 0,01 | 0,92 | <0,001 | 0,79 | 0,29 |
| IP potenciado con dosis altasa | 66,1% | 40 (32-47) | 194 (164-229) | 45 (38-53) | 4,34(3,48-5,38) | 110 (90-138) | 120 (110-130) | 52,7% | 2,7% |
| Otro TAR | 75,9% | 41 (34-48) | 185 (161-211) | 47 (39-57) | 3,91(3,16-4,80) | 112 (89-135) | 125 (114-137) | 44,1% | 2,7% |
| p | 0,04 | 0,10 | 0,02 | 0,17 | 0,005 | 0,78 | 0,01 | 0,11 | 1 |
| IP potenciado con dosis bajasb | 72,9% | 41 (35-48) | 181(159-213) | 46 (37-55) | 4,02(3,35-4,94) | 114 (86-134) | 120 (11-137) | 41,5% | 1,7% |
| Otros TAR | 74,5% | 41 (34-47) | 187 (163-214) | 47 (39-57) | 3,93(3,16-4,94) | 111 (90-136) | 124 (114-136) | 46,5% | 3,0% |
| p | 0,72 | 0,37 | 0,45 | 0,28 | 0,46 | 0,99 | 0,20 | 0,35 | 0,75 |
| ITINAN | 74,9% | 41 (34-48) | 188 (164-213) | 48 (41-59) | 3,80(3,09-4,68) | 112 (90-136) | 125 (116-138) | 44,3% | 3,4% |
| Otro TAR | 73,2% | 41 (34-47) | 183 (158-214) | 44 (36-54) | 4,17(3,42-5,22) | 111 (89-133) | 122 (110-135) | 47,3% | 1,8% |
| p | 0,64 | 0,41 | 0,44 | <0,001 | <0,001 | 0,68 | 0,05 | 0,46 | 0,32 |
TAR: tratamiento antirretroviral; IP: inhibidores de la proteasa; ITINAN: inhibidores de la transcriptasa inversa no análogos de nucleósidos; RIC: rango intercuartílico.
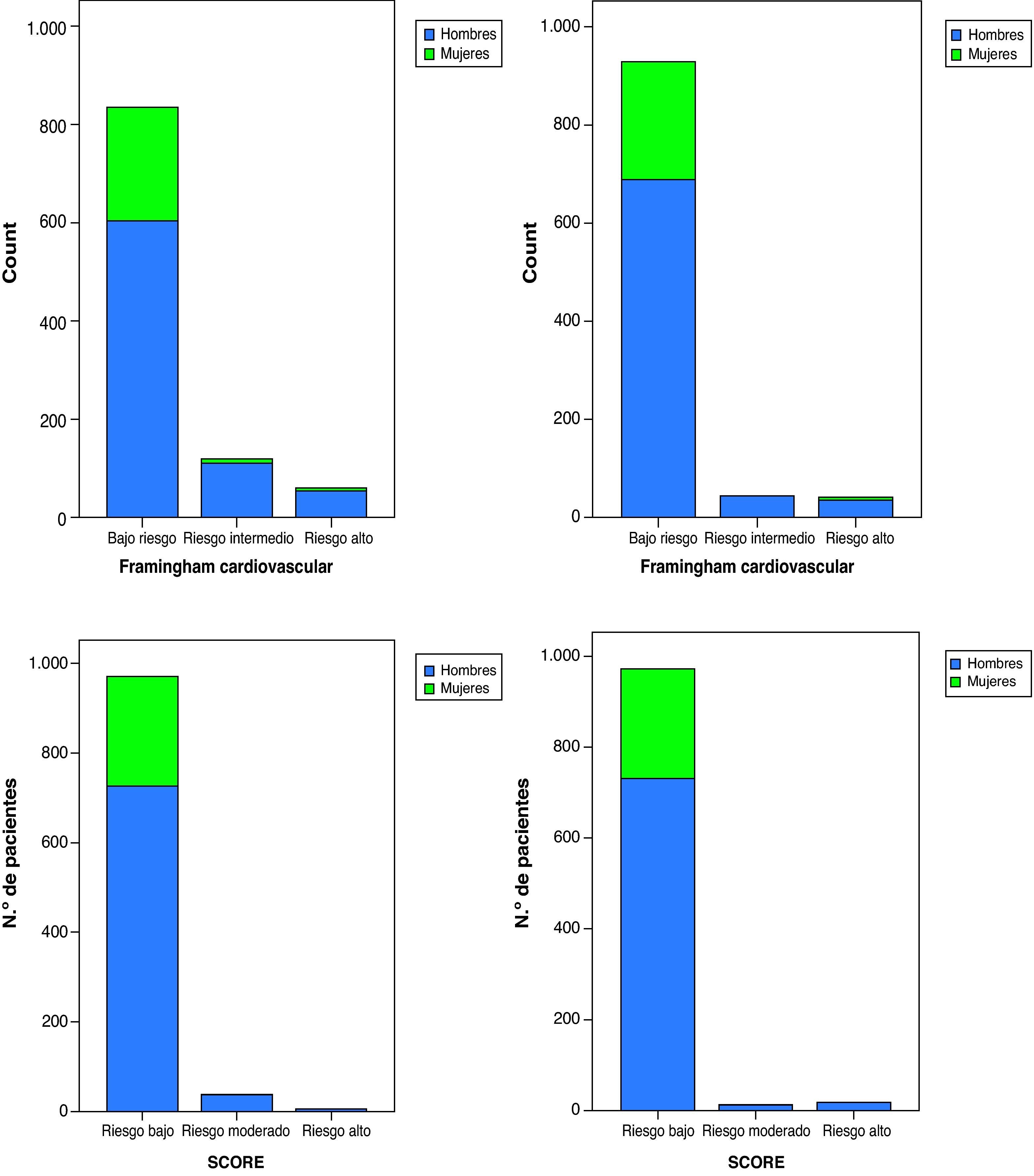
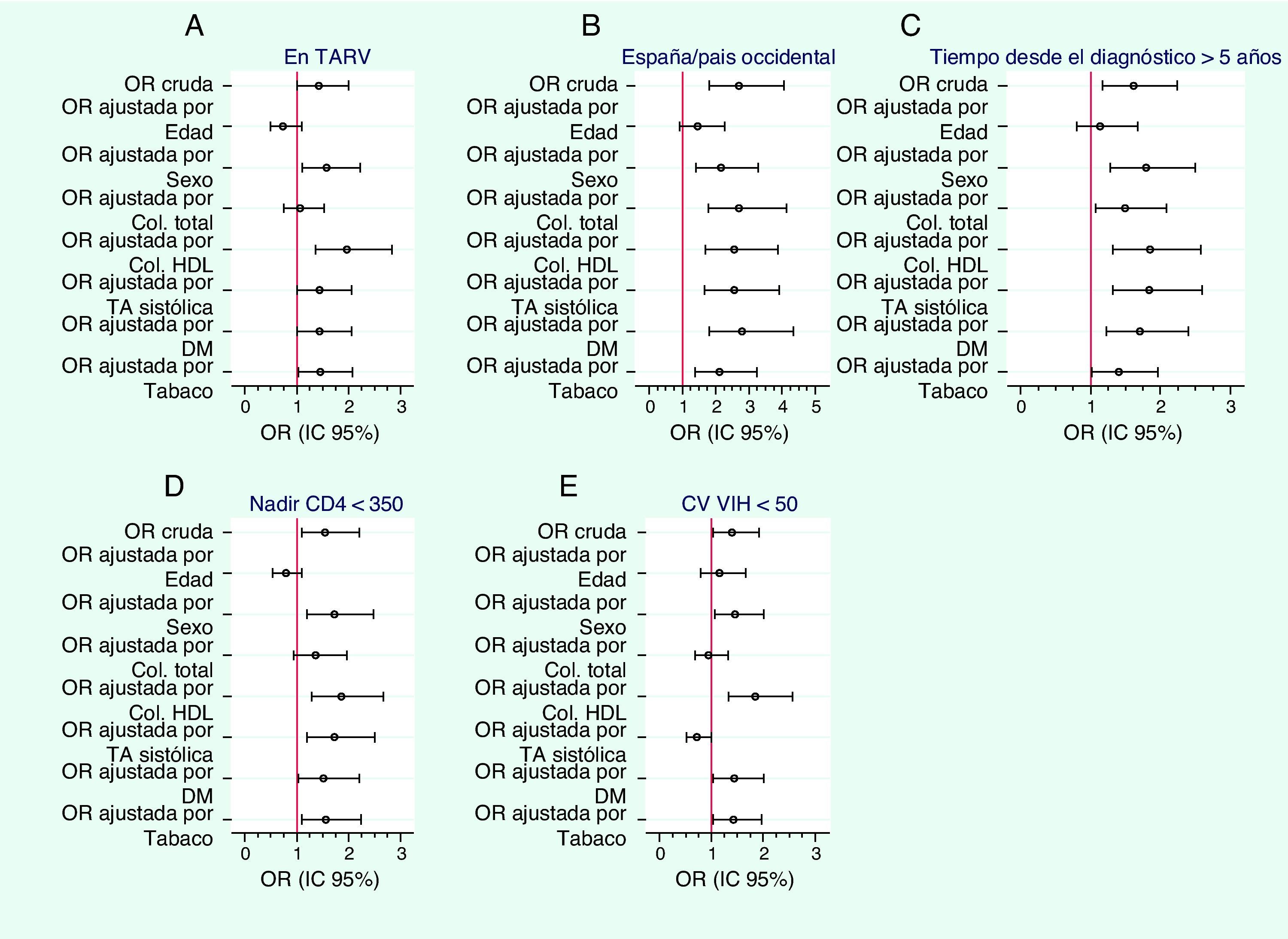
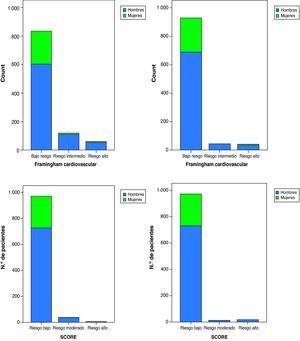
La mediana (RIC) del Framingham cardiovascular fue de 4,25% (2,14-7,71%), Framingham coronario 2,06% (1,0-4,33%), REGICOR 0,84% (0,49-1,65%) y SCORE 0,12% (0,02-0,49%) (tabla 2). Se incluyeron en el grupo de «riesgo moderado-alto» según Framingham cardiovascular, coronario, REGICOR y SCORE el 17,6, el 8,3, el 4,2 y el 3,1% de los pacientes, respectivamente (fig. 1). El RCV medido por todas las escalas fue significativamente más alto en los varones que en las mujeres. En el análisis univariante, la puntuación con todas las escalas fue mayor en los pacientes españoles y procedentes de países occidentales, en los que la infección se había diagnosticado más de 5 años antes, en los que habían tenido un nadir de CD4 <350células/mm3, en los que estaban virológicamente suprimidos y en los que recibían TAR (tabla 5). La puntuación con la escala de Framingham fue significativamente menor en los pacientes con menor nivel de estudios y con vía de transmisión heterosexual. No hubo diferencias en los factores asociados a un mayor RCV en el grupo de hombres respecto al conjunto de la población, mientras que en las mujeres solo se asociaron con una mayor puntuación en la escala de Framingham la procedencia de un país occidental y un nadir de CD4 <350células/μl. Cuando se evaluó por regresión logística el peso de cada uno de los factores de RCV tradicionales por separado en la asociación de una mayor puntuación en la escala de Framingham con los grupos mencionados, el principal determinante del riesgo más elevado fue la edad, ya que en todos los grupos la asociación con un mayor riesgo desapareció al ajustar por esta variable (fig. 2). En los pacientes con un nadir de CD4 <350células/mm3, en los que tenían una carga viral del VIH suprimida y en los que recibían TAR, la asociación con un mayor RCV desapareció al introducir en el modelo de regresión el C-total. A su vez, en un modelo de regresión lineal ajustado por edad y sexo para conocer los factores que se asociaban de forma independiente con mayores cifras de C-total entre recibir TAR, carga viral del VIH, nadir de CD4, vía de transmisión y duración de la infección por el VIH, los factores independientes en el modelo fueron recibir TAR (coeficiente no estandarizado, 18,9; p<0,001), un menor nadir de CD4 (coeficiente no estandarizado, 0,02; p=0,006) y la vía de transmisión (coeficiente no estandarizado 5,0; p=0,003). Por último, después de la edad y el C-total, el siguiente factor en importancia determinante del mayor riesgo fue el tabaco, que fue el que más redujo la odds ratio de tener un mayor RCV en la mayoría de los grupos.
Puntuación de las escalas de riesgo en relación con diferentes características de los pacientes
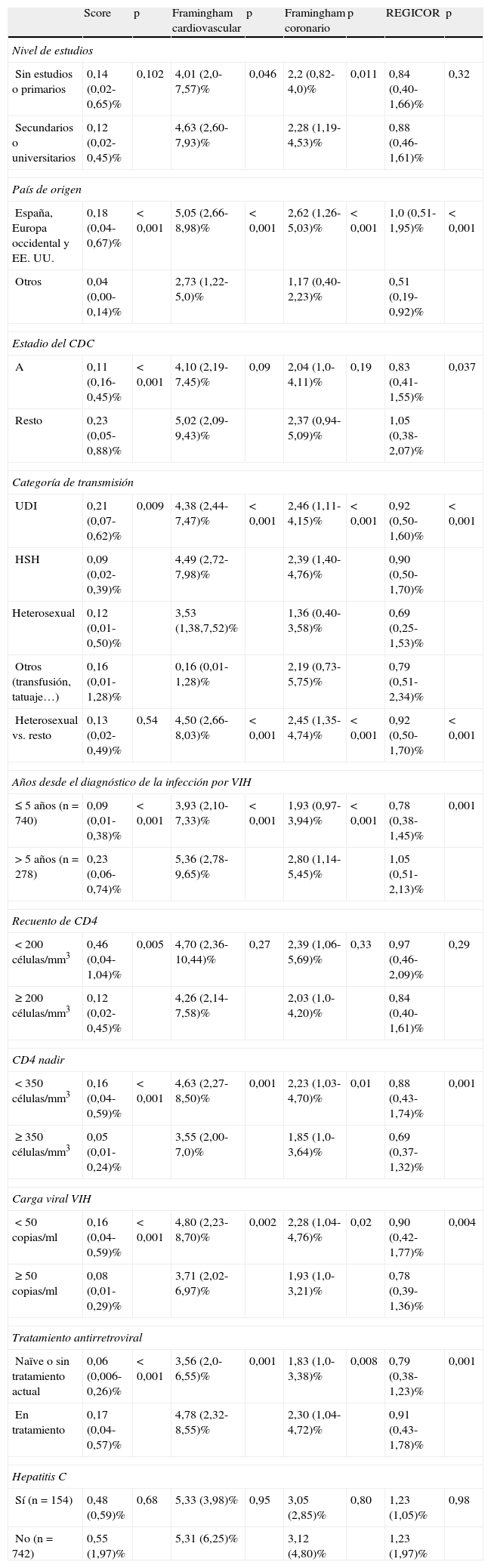
| Score | p | Framingham cardiovascular | p | Framingham coronario | p | REGICOR | p | |
| Nivel de estudios | ||||||||
| Sin estudios o primarios | 0,14 (0,02-0,65)% | 0,102 | 4,01 (2,0-7,57)% | 0,046 | 2,2 (0,82-4,0)% | 0,011 | 0,84 (0,40-1,66)% | 0,32 |
| Secundarios o universitarios | 0,12 (0,02-0,45)% | 4,63 (2,60-7,93)% | 2,28 (1,19-4,53)% | 0,88 (0,46-1,61)% | ||||
| País de origen | ||||||||
| España, Europa occidental y EE.UU. | 0,18 (0,04-0,67)% | <0,001 | 5,05 (2,66-8,98)% | <0,001 | 2,62 (1,26-5,03)% | <0,001 | 1,0 (0,51-1,95)% | <0,001 |
| Otros | 0,04 (0,00-0,14)% | 2,73 (1,22-5,0)% | 1,17 (0,40-2,23)% | 0,51 (0,19-0,92)% | ||||
| Estadio del CDC | ||||||||
| A | 0,11 (0,16-0,45)% | <0,001 | 4,10 (2,19-7,45)% | 0,09 | 2,04 (1,0-4,11)% | 0,19 | 0,83 (0,41-1,55)% | 0,037 |
| Resto | 0,23 (0,05-0,88)% | 5,02 (2,09-9,43)% | 2,37 (0,94-5,09)% | 1,05 (0,38-2,07)% | ||||
| Categoría de transmisión | ||||||||
| UDI | 0,21 (0,07-0,62)% | 0,009 | 4,38 (2,44-7,47)% | <0,001 | 2,46 (1,11-4,15)% | <0,001 | 0,92 (0,50-1,60)% | <0,001 |
| HSH | 0,09 (0,02-0,39)% | 4,49 (2,72-7,98)% | 2,39 (1,40-4,76)% | 0,90 (0,50-1,70)% | ||||
| Heterosexual | 0,12 (0,01-0,50)% | 3,53 (1,38,7,52)% | 1,36 (0,40-3,58)% | 0,69 (0,25-1,53)% | ||||
| Otros (transfusión, tatuaje…) | 0,16 (0,01-1,28)% | 0,16 (0,01-1,28)% | 2,19 (0,73-5,75)% | 0,79 (0,51-2,34)% | ||||
| Heterosexual vs. resto | 0,13 (0,02-0,49)% | 0,54 | 4,50 (2,66-8,03)% | <0,001 | 2,45 (1,35-4,74)% | <0,001 | 0,92 (0,50-1,70)% | <0,001 |
| Años desde el diagnóstico de la infección por VIH | ||||||||
| ≤5 años (n=740) | 0,09 (0,01-0,38)% | <0,001 | 3,93 (2,10-7,33)% | <0,001 | 1,93 (0,97-3,94)% | <0,001 | 0,78 (0,38-1,45)% | 0,001 |
| >5 años (n=278) | 0,23 (0,06-0,74)% | 5,36 (2,78-9,65)% | 2,80 (1,14-5,45)% | 1,05 (0,51-2,13)% | ||||
| Recuento de CD4 | ||||||||
| <200 células/mm3 | 0,46 (0,04-1,04)% | 0,005 | 4,70 (2,36-10,44)% | 0,27 | 2,39 (1,06-5,69)% | 0,33 | 0,97 (0,46-2,09)% | 0,29 |
| ≥200 células/mm3 | 0,12 (0,02-0,45)% | 4,26 (2,14-7,58)% | 2,03 (1,0-4,20)% | 0,84 (0,40-1,61)% | ||||
| CD4 nadir | ||||||||
| <350 células/mm3 | 0,16 (0,04-0,59)% | <0,001 | 4,63 (2,27-8,50)% | 0,001 | 2,23 (1,03-4,70)% | 0,01 | 0,88 (0,43-1,74)% | 0,001 |
| ≥350 células/mm3 | 0,05 (0,01-0,24)% | 3,55 (2,00-7,0)% | 1,85 (1,0-3,64)% | 0,69 (0,37-1,32)% | ||||
| Carga viral VIH | ||||||||
| <50 copias/ml | 0,16 (0,04-0,59)% | <0,001 | 4,80 (2,23-8,70)% | 0,002 | 2,28 (1,04-4,76)% | 0,02 | 0,90 (0,42-1,77)% | 0,004 |
| ≥50 copias/ml | 0,08 (0,01-0,29)% | 3,71 (2,02-6,97)% | 1,93 (1,0-3,21)% | 0,78 (0,39-1,36)% | ||||
| Tratamiento antirretroviral | ||||||||
| Naïve o sin tratamiento actual | 0,06 (0,006-0,26)% | <0,001 | 3,56 (2,0-6,55)% | 0,001 | 1,83 (1,0-3,38)% | 0,008 | 0,79 (0,38-1,23)% | 0,001 |
| En tratamiento | 0,17 (0,04-0,57)% | 4,78 (2,32-8,55)% | 2,30 (1,04-4,72)% | 0,91 (0,43-1,78)% | ||||
| Hepatitis C | ||||||||
| Sí (n=154) | 0,48 (0,59)% | 0,68 | 5,33 (3,98)% | 0,95 | 3,05 (2,85)% | 0,80 | 1,23 (1,05)% | 0,98 |
| No (n=742) | 0,55 (1,97)% | 5,31 (6,25)% | 3,12 (4,80)% | 1,23 (1,97)% | ||||
UDI: usuario de drogas intravenosas; HSH: hombres que practican sexo con hombres.
Los valores representan la mediana (rango intercuartílico).
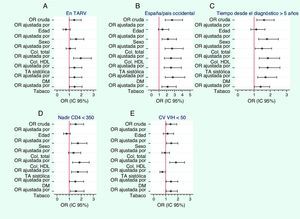
Relación entre un riesgo coronario >5% según la escala de Framingham y diversas características de los pacientes. Odds ratios crudas y ajustadas por cada uno de los factores clásicos de riesgo cardiovascular por separado. A) Riesgo coronario en pacientes en tratamiento antirretroviral. B) Riesgo coronario en pacientes españoles y procedentes en países occidentales. C) Riesgo coronario en pacientes con una duración de la infección por VIH >5 años. D) Riesgo coronario en pacientes con nadir de CD4 <350/mm3. E) Riesgo coronario en pacientes con carga viral <50 copias/ml. OR: odds ratio; Col.: colesterol; TA: presión arterial; DM: diabetes mellitus; TARV: tratamiento antirretroviral; CV: carga viral.
En los 183 pacientes con RCV moderado o alto según al menos una de las escalas, de los que el 91,8% eran varones, los factores de RCV más frecuentes fueron edad >45años en el 70,5%, tabaquismo en el 61,7%, C-total >200mg/dl en el 48,6%, C-HDL <40mg/dl en el 44,3%, PA sistólica >140mm Hg en el 36,6% e hipertensión arterial en el 19,1%. En el grupo de mujeres con RCV moderado o alto, los factores de riesgo más frecuentes fueron edad mayor de 45 años (12/15), C-total >200mg/dl (9/15) y tabaquismo (8/15).
DiscusiónEn este estudio multicéntrico contemporáneo de pacientes con infección por el VIH incluidos en CoRIS, los factores de RCV más frecuentes fueron el tabaquismo, presente en casi la mitad de los casos, y la dislipemia, detectada en aproximadamente una tercera parte de los pacientes, a expensas de un colesterol HDL bajo y un C-total elevado. La evaluación del RCV global con las escalas comúnmente empleadas en la práctica clínica identificó una proporción relativamente pequeña de personas con riesgo moderado o alto. El principal responsable de la mayor puntuación en la escala de Framingham fue la edad, seguida de las concentraciones de C-total.
La prevalencia de algunos factores de RCV fue relativamente elevada, aunque con diferencias significativas en relación con las características sociodemográficas e inmunovirológicas de los pacientes y con el TAR que recibían. El tabaquismo continúa siendo el factor de RCV más frecuente, sobre todo en el grupo de españoles y procedentes de países occidentales, y en los que tienen un menor nivel de estudios, con un consumo, por el contrario, más bajo en las personas que habían adquirido el VIH por vía heterosexual. Sin embargo, la prevalencia actual, inferior al 50%, es llamativamente más baja que la de estudios previos españoles, en los que se describían frecuencias del 67-77%18,19,25. Es probable que la reciente prohibición del consumo de tabaco en locales cerrados en España, la mayor insistencia para el cese del consumo por parte de los médicos y el aumento de población inmigrante, con menor frecuencia fumadora, hayan contribuido a este descenso. A pesar de esto, la proporción de fumadores en personas seropositivas sigue siendo muy superior a la de las seronegativas26,27. Otro hábito tóxico habitualmente más frecuente entre los pacientes con infección por el VIH y que no está reflejado en las escalas de riesgo, a pesar de su relevancia en la ECV, es el consumo de cocaína, que fue del 7% en nuestra cohorte y significativamente mayor en hombres que en mujeres.
La dislipemia, definida por niveles bajos de C-HDL o elevados de C-total, fue el segundo factor de riesgo más frecuente en este estudio. Más de una tercera parte de los pacientes tenía niveles bajos de C-HDL. El análisis por subgrupos puso de manifiesto una aparente relación de los niveles más bajos del C-HDL con un estadio más precoz de la infección por el VIH, ya que se asociaron con una menor duración de la infección, un mayor nadir de CD4, con la categoría A del CDC, con no haber iniciado TAR y, por tanto, con una mayor carga viral del VIH. Por el contrario, los niveles más altos de C-total se encontraron en todos los subgrupos de pacientes que representaban un estadio más evolucionado de la infección por el VIH. Estas diferencias se debieron en parte al TAR, que se asoció con niveles de C-HDL y de C-total más altos y con un menor cociente C-total/C-HDL. Es interesante destacar que el análisis por grupos de tratamiento puso de manifiesto diferencias en los lípidos entre las diferentes pautas de TAR. Los pacientes que recibían IP potenciados con dosis altas de ritonavir tenían niveles más altos de C-total y del cociente C-total/C-HDL que el resto de los pacientes tratados, incluso a pesar de la mayor proporción de mujeres en este grupo. Estas alteraciones lipídicas no se detectaron en los pacientes tratados con IP potenciados con dosis bajas de ritonavir y, como es conocido, fueron opuestas a las encontradas en los pacientes con ITINAN28. Aunque en la interpretación de los resultados del colesterol y sus fracciones hay que tener en cuenta que no se recogió información sobre la terapia hipolipemiante, en este estudio coetáneo los datos sugieren que el TAR, especialmente algunas pautas, podría asociarse con un perfil lipídico más favorable que el no recibir tratamiento. El uso creciente de los nuevos antirretrovirales con un perfil metabólico más benigno y de IP potenciados con bajas dosis de ritonavir es probable que conduzca en el futuro a un claro efecto neto beneficioso del TAR sobre los lípidos.
La prevalencia de otros factores de RCV, como hipertensión arterial y diabetes, fue más baja. Como era de esperar, dadas las características de la cohorte, hubo una frecuencia muy baja de lipodistrofia, aunque el 11% de los pacientes presentaba síndrome metabólico y el 25% de las mujeres en las que se midió la cintura tenía criterios de obesidad abdominal. Cuando se seleccionó a los pacientes de CoRIS con RCV moderado o alto, tanto el tabaquismo como los niveles más altos de C-total y más bajos de C-HDL continuaron siendo, después de la edad, los factores de RCV más frecuentes. Por tanto, a pesar de que el control de algunos de los factores de RCV haya mejorado, puede ser necesaria una intervención más enérgica sobre los factores modificables para mejorar el pronóstico de los pacientes.
El RCV medido por las escalas de riesgo fue, en general, bajo en los pacientes de esta cohorte multicéntrica española comparado con estudios previos realizados en España18,19. Aunque la edad media de los pacientes era similar, en esta cohorte la prevalencia de algunos factores de RCV, como el tabaquismo, fue menor. Otro probable motivo es que CoRIS es una cohorte reciente integrada por pacientes naïve al TAR, lo que implica un estadio más precoz de la infección y una mayor proporción de pacientes tratados con nuevos antirretrovirales, cuyo perfil cardiovascular es en general más favorable que el de los fármacos anteriores. Por tanto, era esperable una menor prevalencia de alteraciones metabólicas, como hiperlipemia, resistencia insulínica, síndrome metabólico o lipodistrofia, que la asociada a los tratamientos del pasado. No obstante, es importante reconocer que ninguna de las ecuaciones de riesgo incorpora variables que pueden influir en el RCV asociado a la infección por el VIH, como el grado de replicación vírica, el estado proinflamatorio y la activación inmune asociados. En un estudio reciente6, después de ajustar por todos los factores de RCV y por la raza, la infección por el VIH seguía asociándose con un mayor riesgo de desarrollo de infarto de miocardio. Diversos estudios han llamado la atención sobre la importancia y las posibles consecuencias de la inflamación asociada a la infección por VIH en la aterogénesis, y sugieren que determinados marcadores biológicos de inflamación, activación endotelial y trombosis podrían tener utilidad para evaluar el riesgo y predecir la existencia de arteriosclerosis preclínica29-33.
Aunque algunas características de los pacientes se asociaron con una mayor puntuación en las escalas de riesgo, cuando se ajustó por los factores tradicionales se encontró que la edad era el principal determinante en todos los grupos del riesgo más elevado en la escala de Framingham. En los pacientes en TAR, en los que tenían la carga viral suprimida y en los que habían tenido un nadir de CD4 más bajo, el C-total fue el otro factor de más peso en la mayor puntuación en la escala de Framingham.
Una limitación del estudio es que la cohorte CoRIS no es representativa de todo el espectro de pacientes que se atienden habitualmente en nuestro entorno, ya que no se incluyen personas con enfermedad de larga evolución, expuestos durante mucho tiempo al TAR y, en general, de mayor edad que los pacientes con diagnóstico más reciente. Por tanto, la puntuación en las escalas podría ser mayor en los pacientes con infección por VIH que no pertenecen a CoRIS. Incluso el RCV del grupo analizado podría haber sido menor que el del resto de CoRIS, ya que la proporción de mujeres era mayor en el primer grupo. La definición de diabetes empleada para el estudio puede haber infraestimado la prevalencia al excluir algunos de los pacientes cuya enfermedad estaba controlada exclusivamente con dieta. Por otro lado, la selección de los pacientes incluidos fue consecutiva en función del interés de determinados investigadores de CoRIS sin predeterminar el tamaño muestral de cada centro y de cada comunidad autónoma. No obstante, la muestra incluida en el estudio tiene una distribución geográfica amplia, a diferencia de los estudios anteriores, e incluye un número elevado de pacientes sin TAR y un espectro amplio en lo referente a la situación inmunológica y virológica, que ha permitido caracterizar grupos diferenciados en cuanto a sus características de RCV.
En resumen, en los pacientes con infección por VIH de CoRIS, la prevalencia de factores de riesgo modificables es todavía elevada. Predominan el tabaquismo y la dislipemia, fundamentalmente a expensas de un C-HDL bajo y un C-total alto. El principal determinante del RCV elevado evaluado por las escalas es la edad. Dado que se está produciendo un envejecimiento gradual en el colectivo de personas con infección por el VIH, es esperable que la enfermedad cardiovascular adquiera una relevancia progresivamente mayor con el tiempo y que, por tanto, el control de los factores de riesgo modificables sea crucial para prevenir el desarrollo de futuras complicaciones.
FinanciaciónFinanciado parcialmente por la Red Temática de Investigación Cooperativa en VIH/sida del FIS (ISCIII-RETIC RD06/0027). Mar Masiá y Félix Gutiérrez han recibido becas de investigación de las siguientes entidades: FIS (PI081893), FIBELX (05/05; 20/07; 10/11; 10/12; 10/13), FIPSE (12532/05; 12655/07) y Generalitat Valenciana (PI051338,083/05, AP-091/07; AP-087/10).
AutoríaMar Masiá y Félix Gutiérrez son los autores principales del artículo.
Conflicto de interesesLos autores declaran que no existe ningún conflicto de intereses.
Este estudio no habría sido posible sin la colaboración de todos los pacientes, médicos, enfermeras y gestores de datos que han participado en el proyecto.
Comité Ejecutivo de CoRIS: Juan Berenguer, Julia del Amo, Federico García, Félix Gutiérrez, Pablo Labarga, Santiago Moreno y María Ángeles Muñoz.
Trabajo de campo, gestión y análisis de datos de CoRIS: Ana María Caro-Murillo, Paz Sobrino Vegas, Santiago Pérez-Cachafeiro, Victoria Hernando Sebastián, Belén Alejos Ferreras, Débora Álvarez, Susana Monge, Inma Jarrín, Mónica Trastoy.
BioBanco: M. Ángeles Muñoz-Fernández, Isabel García-Merino, Coral Gómez Rico, Jorge Gallego de la Fuente y Almudena García Torre.
Centros participantes en el Grupo de Estudio del Riesgo Cardiovascular y coautores del artículo:
Hospital Universitario de Canarias (Santa Cruz de Tenerife): Juan Luis Gómez Sirvent, Patricia Rodríguez Fortúnez, María Remedios Alemán Valls, María del Mar Alonso Socas, Ana María López Lirola, María Inmaculada Hernández Hernández, Felicitas Díaz-Flores.
Hospital Carlos III (Madrid): Vicente Soriano, Pablo Labarga, Pablo Barreiro, Mariola López Vázquez, Carol Castañares, Pablo Rivas, Andrés Ruiz, Francisco Blanco, Luz Martín Carbonero, Eugenia Vispo, Carmen Solera.
Hospital Donostia (San Sebastián): José Antonio Iribarren, Julio Arrizabalaga, María José Aramburu, Xabier Camino, Francisco Rodríguez-Arrondo, Miguel Ángel von Wichmann, Lidia Pascual Tomé, Miguel Ángel Goenaga, M. Jesús Bustinduy, Harkaitz Azkune Galparsoro.
Hospital General Universitario de Elche (Elche): Félix Gutiérrez, Mar Masiá, José Manuel Ramos, Sergio Padilla, Andrés Navarro, Fernando Montolio, Yolanda Peral, Catalina Robledano García.
Hospital Universitari de Tarragona Joan XXIII, IISPV, Universitat Rovira i Virgili (Tarragona):
Francesc Vidal, Joaquín Peraire, Consuelo Viladés, Sergio Veloso, Montserrat Vargas, Miguel López-Dupla, Montserrat Olona, Joan-Josep Sirvent, Alba Aguilar, Antoni Soriano.
Hospital Universitario La Fe (Valencia): José López Aldeguer, Marino Blanes Juliá, José Lacruz Rodrigo, Miguel Salavert, Marta Montero, Eva Calabuig, Sandra Cuéllar.
Hospital San Pedro-CIBIR (Logroño): José Antonio Oteo, José Ramón Blanco, Valvanera Ibarra, Luis Metola, Mercedes Sanz, Laura Pérez-Martínez.
Hospital San Pedro II (Logroño): Javier Pinilla Moraza.
Hospital Universitario Mutua de Terrassa (Terrassa): David Dalmau, Angels Jaén Manzanera, Mireia Cairó Llobell, Daniel Irigoyen Puig, Laura Ibáñez, Queralt Jordano Montañez, Mariona Xercavins Valls, Javier Martinez-Lacasa, Pablo Velli, Roser Font.
Hospital de Navarra (Pamplona): Julio Sola Boneta, Javier Uriz, Jesús Castiello, Jesús Reparaz, María Jesús Arraiza, Carmen Irigoyen, David Mozas,
Hospital Parc Taulí (Sabadell): Ferrán Segura, María José Amengual, Eva Penelo, Gemma Navarro, Montserrat Sala, Manuel Cervantes, Valentín Pineda.
Hospital Reina Sofía (Murcia): Alfredo Cano Sánchez, Enrique Bernal Morell, Ángeles Muñoz Pérez.
Hospital San Cecilio (Granada): Federico García García, José Hernández Quero, Alejandro Peña Monje, Leopoldo Muñoz Medina, Jorge Parra Ruiz.
Centro Sanitario Sandoval (Madrid): Jorge Del Romero Guerrero, Carmen Rodríguez Martín, Teresa Puerta López, Juan Carlos Carrió Montiel, Paloma Raposo, Cristina González.
Hospital Son Dureta (Palma de Mallorca): Melchor Riera, Javier Murillas, Maria Peñaranda, Maria Leyes, M. Angels Ribas, Antoni Campins, Concepcion Villalonga.