En enero de 2010, la FDA alertó del aumento del riesgo de mortalidad con el uso de la tigeciclina frente a otros antibióticos para el tratamiento de infecciones graves1. El mayor aumento de mortalidad se observó en pacientes con neumonía nosocomial (14,1%), especialmente aquella asociada a ventilación mecánica (19,1%), indicación no aprobada para tigeciclina (off-label). Tras este comunicado, la EMA completó otra revisión y emitió unas conclusiones similares a las de la FDA2. Ambas agencias concluyeron que la mayoría de estas muertes podrían estar relacionadas con una progresión de la infección en pacientes tratados con este antibiótico1,2.
Los perfiles microbiológico y farmacológico de tigeciclina hacen que pueda ser prescrito en indicaciones no aprobadas, especialmente contra infecciones producidas por patógenos multirresistentes frente a las que muestra actividad in vitro3. Un ejemplo es Stenotrophomonas maltophilia, bacilo gram negativo asociado a infecciones nosocomiales graves como la bacteriemia y la neumonía. El tratamiento de infecciones producidas por este microorganismo resulta complicado debido a que presenta resistencia intrínseca a múltiples antibióticos. Farrel et al. analizaron la sensibilidad antimicrobiana de aislamientos de S. maltophilia (51% de hemocultivos y 37% de origen respiratorio) frente a diferentes antimicrobianos4. Tigeciclina demostró una actividad antibiótica in vitro similar frente a estas cepas y entre el 94,5 al 98,5% de los aislamientos fueron inhibidos a concentraciones de 2mg/L. Los autores concluyeron que tigeciclina podía considerarse un candidato potencial para investigaciones clínicas en infecciones de S.maltophilia.
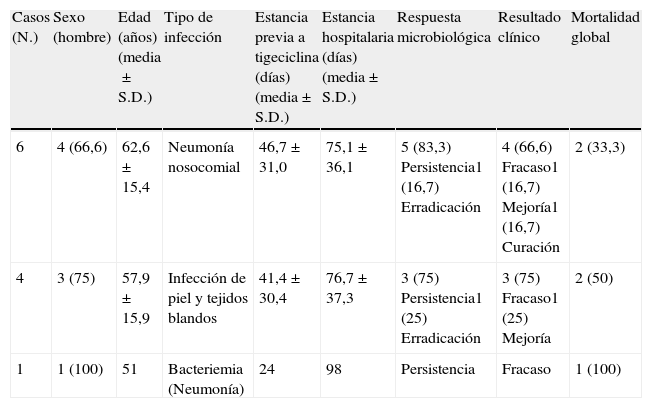
Por otro lado, un trabajo que evaluó el uso de tigeciclina en la práctica clínica y analizó la adherencia a un protocolo de uso de tigeciclina en un total de 103 pacientes5. Entre otras variables, se recogieron datos sobre resultado microbiológico incluyendo la aparición de flora emergente. Los resultados mostraron que algunos microorganismos sensibles a tigeciclina se aislaron como persistencia de la infección primaria y como flora emergente. La tabla 1 muestra los tipos de infección y el resultado clínico de los 11 pacientes con infección causada por S.maltophilia tratados con tigeciclina. Todos estos pacientes recibieron tratamiento con tigeciclina como terapia de rescate y tras una hospitalización prolongada. Se evidenció fracaso clínico y persistencia de S.maltophilia tanto cuando tigeciclina se utilizó fuera de indicación (neumonía nosocomial y bacteriemia) como también en indicaciones aprobadas (infección de piel y tejidos blandos). La mortalidad global fue del 26,2% (4,9% con infección por S.maltophilia). Además, hubo casos de aislamiento de flora emergente: 10 casos (52,6%) de Candida spp., 7 casos (36,9%) de Pseudomonas aeruginosa, 3 casos (15,8%) de Escherichia coli y 2 casos (10,5%) de S. maltophilia. Esta flora emergente se aisló mayoritariamente de pacientes ingresados en UCI con infecciones graves. La presencia de S. maltophilia como flora emergente se consideró mayoritariamente como colonización.
Características demográficas, clínicas y microbiológicas y evolución clínica de los pacientes con infección causada por S.maltophilia y tratada con tigeciclina
| Casos (N.) | Sexo (hombre) | Edad (años) (media±S.D.) | Tipo de infección | Estancia previa a tigeciclina (días) (media±S.D.) | Estancia hospitalaria (días) (media±S.D.) | Respuesta microbiológica | Resultado clínico | Mortalidad global |
| 6 | 4 (66,6) | 62,6±15,4 | Neumonía nosocomial | 46,7±31,0 | 75,1±36,1 | 5 (83,3) Persistencia1 (16,7) Erradicación | 4 (66,6) Fracaso1 (16,7) Mejoría1 (16,7) Curación | 2 (33,3) |
| 4 | 3 (75) | 57,9±15,9 | Infección de piel y tejidos blandos | 41,4±30,4 | 76,7±37,3 | 3 (75) Persistencia1 (25) Erradicación | 3 (75) Fracaso1 (25) Mejoría | 2 (50) |
| 1 | 1 (100) | 51 | Bacteriemia (Neumonía) | 24 | 98 | Persistencia | Fracaso | 1 (100) |
NOTA. Los datos se expresan como n.o (%) de pacientes a no ser que se indique lo contrario.
S.D.: desviación estándar.
En una extensión de este estudio a un total de 150 pacientes3, el aislamiento de S. maltophilia fue observado más frecuentemente cuando tigeciclina se utilizó fuera de indicación ([10{21,7%} vs. 2{1,9%}; p>0,001]). Además, la mortalidad fue superior en el grupo de pacientes tratados con tigeciclina fuera de indicación. Siete de los 11 pacientes con infección por S.maltophilia fueron tratados de neumonía nosocomial (uno con bacteriemia), indicación no autorizada para tigeciclina. Estos casos no pudieron ser tratados con cotrimoxazol (tratamiento de elección) debido a historia de hipersensibilidad previa (7/11) o a falta de sensibilidad según antibiograma (4/11).
Cuando se estudiaron los factores predictores de supervivencia6, se determinó únicamente la falta de aislamiento de S.maltophilia (OR 23,1; p=0,001) y el SAPS<40 al inicio del tratamiento con tigeciclina.
Algunos autores apuntan que dosis más altas de tigeciclina (p. ej., carga inicial de 200mg y 100mg cada 12 posteriores) podrían ser adecuadas en indicaciones no aprobadas. Sin embargo, se necesitan estudios controlados para evaluar la eficacia y el perfil de seguridad en estas indicaciones. Las conclusiones de un meta-análisis reciente destacan que tigeciclina no debería ser utilizado en monoterapia frente a infecciones graves y debería ser reservado únicamente como última alternativa7.
Así pues, teniendo en cuenta los hallazgos observados y las alertas de las agencias reguladoras, la recomendación del uso de tigeciclina en pacientes con infección de S.maltophilia podría cuestionarse y debería ser refrendada por nuevos estudios clínicos, más aún tras la observación de la presencia de aislamientos de S.maltophilia como flora emergente en pacientes tratados con este antibiótico.