Hemos leído con interés la carta de Marco et al.1 en referencia a la baja sensibilidad de los test rápidos antigénicos (TRA) para cribar la infección por SARS-CoV-2.
Los autores reportan un brote de SARS-CoV-2 ocurrido en un módulo penitenciario, tras diagnosticar tres casos por TRA, realizan un cribado a un total de 81 reclusos, con una incidencia (por TRA) de infección por SARS-CoV-2 del 11% (9/81). Entre tres y cinco días más tarde un nuevo cribado por PCR en tiempo real (rt-PCR) a los 72 casos inicialmente negativos reporta una positividad del 37% (27/72). Los autores identifican los resultados previos de TRA como falsos negativos, concluyen que dada la baja sensibilidad de los TRA para el cribado del SARS-CoV-2, debería usarse la rt-PCR como técnica preferente.
Es vital comprender algunos puntos importantes de las estrategias de cribado con TRA, como la correcta interpretación del resultado, el momento adecuado para realizarlos y las ventajas de estos test sobre la rt-PCR.
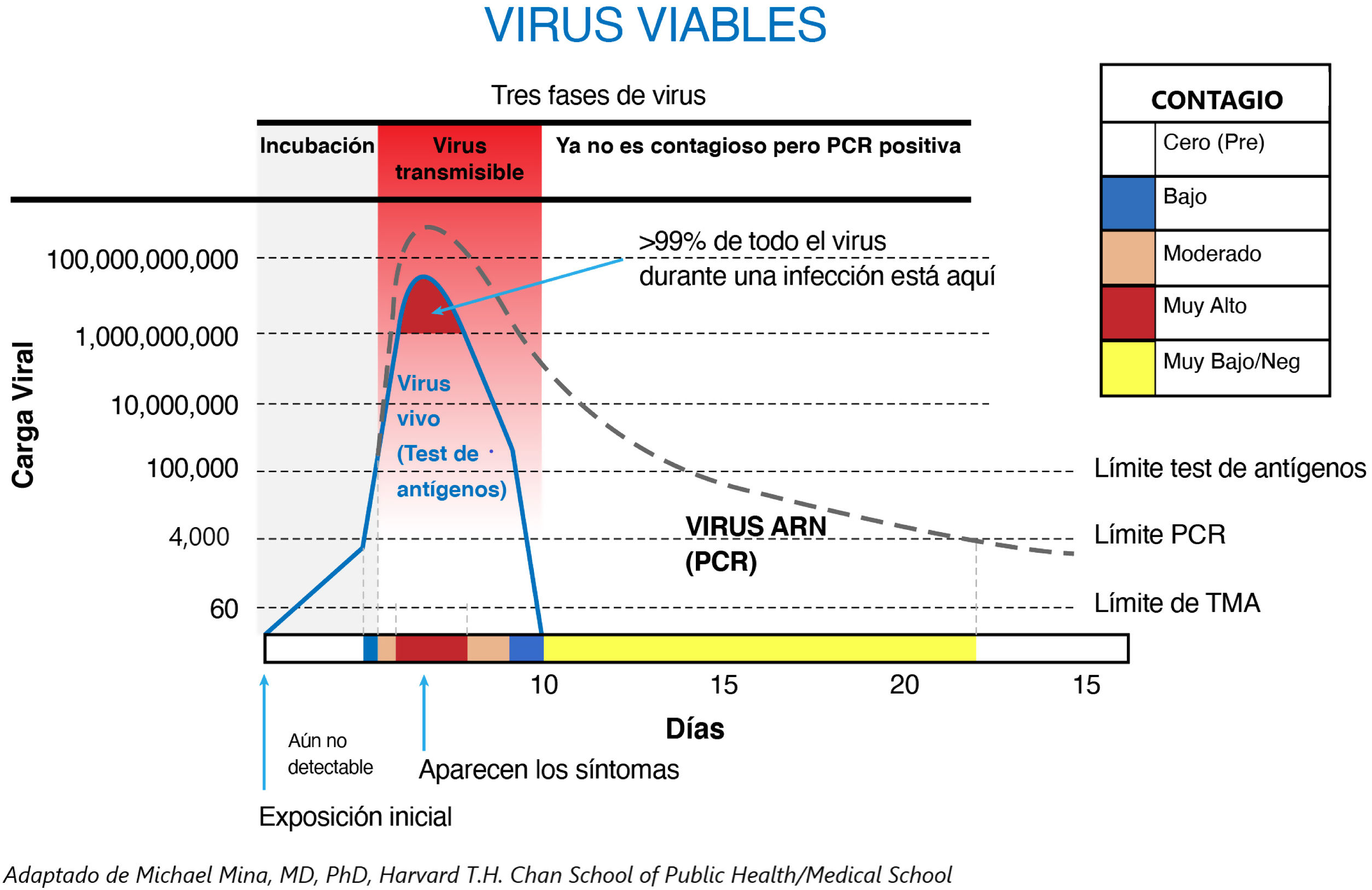
Los TRA tienen una alta sensibilidad para detectar a las personas con elevada carga viral y potencial de transmisión del virus (sintomáticos y asintomáticos)2. Esta capacidad está relacionada con la carga viral del paciente, que podría relacionarse con el «cycle threshold» (Ct) de las rt-PCR, un marcador indirecto de la carga viral en un sujeto infectado. Los TRA son eficaces para diagnosticar infectados con Cts < 25, que se correlacionan con virus que crecen en cultivos celulares y son transmisibles3,4, en estos casos los TRA han demostrado sensibilidades cercanas al 100%2. Los TRA por tanto podrían ser frecuentemente negativos a partir del 5° día de clínica (o 10° día de exposición) y universalmente en sujetos con baja carga viral.
El control con rt-PCR realizada entre tres y cinco días posteriores al cribado inicial reporta una tasa de positividad del 37% en sujetos con TRA negativo previo. La amplificación de ácidos nucleicos (NAAT) de SARS-CoV-2 con rt-PCR o TMA (transcription-mediated amplification) detecta resultados positivos hasta varios días o semanas, respectivamente, tras la resolución clínica, cuando los sujetos ya no tienen capacidad de generar transmisión.
Por tanto, TRA y rt-PCR capturan escenarios distintos de la enfermedad. Los TRA ofrecen resultados positivos durante un período menor de tiempo, con relación a la fase aguda de la infección.
Si analizamos la cinética viral del SARS-CoV-2 (fig. 1), observamos que las estrategias de cribado frecuente con test de antígenos son igual de eficaces para detectar a las personas contagiosas del virus, que una más espaciada basada en una rt-PCR5. La diferencia se debe a las características de cada test, los TRA con test «versátiles» que pueden ser utilizados en cualquier entorno, tienen un coste bajo y tienen la ventaja de dar un resultado en 15 minutos, al contrario de la rt-PCR. Aplicar una estrategia de cribado con TRA podría identificar el mismo número de personas trasmisoras del virus comparada con rt-PCR.
Volviendo al reporte de Marco et al., sería útil conocer las Cts de las muestras positivas por rt-PCR a los tres y cinco días del testado inicial, sobre todo para saber el real riesgo de contagiosidad de estos pacientes. Las Cts superiores a 25-30 tienen un riesgo bajo de trasmisión viral y una alta probabilidad de resultar negativas en un TRA, con independencia de la presencia o ausencia de síntomas. La negatividad en TRA y positividad en rt-PCR posterior en sujetos ya aislados, básicamente sugiere que el Ct es elevado y estamos capturando la fase final o una infección ya resuelta.
Esto es especialmente cierto con TMA, una técnica ultrasensible que detecta hasta 60 copias de SARS-CoV-2 (en lugar de las 3.000-5.000 copias de la rt-PCR)6. La TMA es la técnica más habitualmente usada en la actualidad en grandes estrategias de cribado, por la posibilidad de agrupar muestras en el laboratorio (pooling) y se puede mantener positiva hasta más allá de las ocho semanas del contagio.
En resumen, creemos que TRA y NAAT (rt-PCR o TMA) capturan fenómenos distintos. Cuando se desee identificar de una manera sencilla sujetos con potencial de transmisión de SARS-CoV-2, los TRA son la herramienta idónea. Cuando se desee un cribado para una cohorte transversal que identifique al mayor número posible de sujetos infectados (actual o recientemente), la NAAT será la técnica que capturará el mayor número de casos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.