Sr. Director:
Presentamos el caso de un varón de 63 años, hipertenso de años de evolución, sin tratamiento farmacológico, fumador y bebedor moderado. Episodio de cólico nefrítico hace 20 años sin otros antecedentes de interés.
Ingresó en diciembre del año 2006 por insuficiencia renal severa de causa no filiada y se realizó hemodiálisis urgente. Tras objetivarse proteinuria de Bence-Jones positiva con cadenas Kappa 288 mg/dl y banda monoclonal IgA 1,89, se realizó un aspirado de médula ósea y se confirmó el diagnóstico de mieloma múltiple de Bence Jones (+), con infiltración plasmocitaria de médula ósea > 70 %. En la serie ósea se observó una lesión lítica en 7.a costilla sacra derecha y en el cráneo, sugestivas de afectación ósea por mieloma.
Se mantuvo la terapia renal sustitutiva con hemodiálisis a días alternos, presentando una aclaramiento de creatinina de 4,8ml/min y función renal residual (1.000 ml/24 h).
Se inició tratamiento con dexametasona, seguido de ciclos de quimioterapia tipo VAD. Tras el cuarto ciclo presentó una respuesta parcial a nivel hematológico (descenso de cadenas kappa a 12 mg/dl) y se decidió realizar un autotrasplante de médula ósea con MF 140 mg/m2 y soporte de CPSP (julio de 2007).
El período de aislamiento tras el TMO se caracterizó por:
- –
Ambiente próximo a la esterilidad.
- –
Necesidad de monitor de diálisis que no precisara conexión a red de agua.
- –
Monitor Fresenius Multifiltrate.
- –
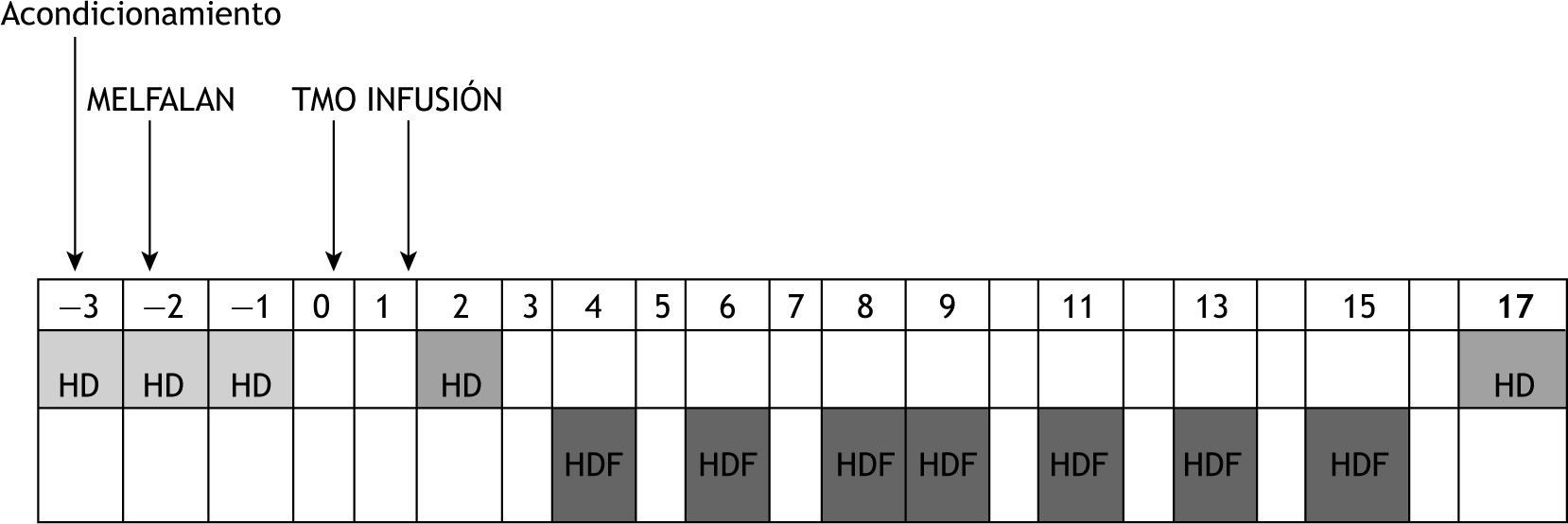
Inicio de HDFVVC el día (+) 4 post.: pauta: catéter Hickman yugular derecha. Qs 300 ml/min. QLD 1.000 ml/h. QLR 2000 ml/h. Q Hep 0,8-1 cc/h (800-1.000 U/h). UF según balances hídricos.
En análisis del desarrollo de HDFVV durante el trasplante y posterior aplasia medular se presenta en la figura 1.
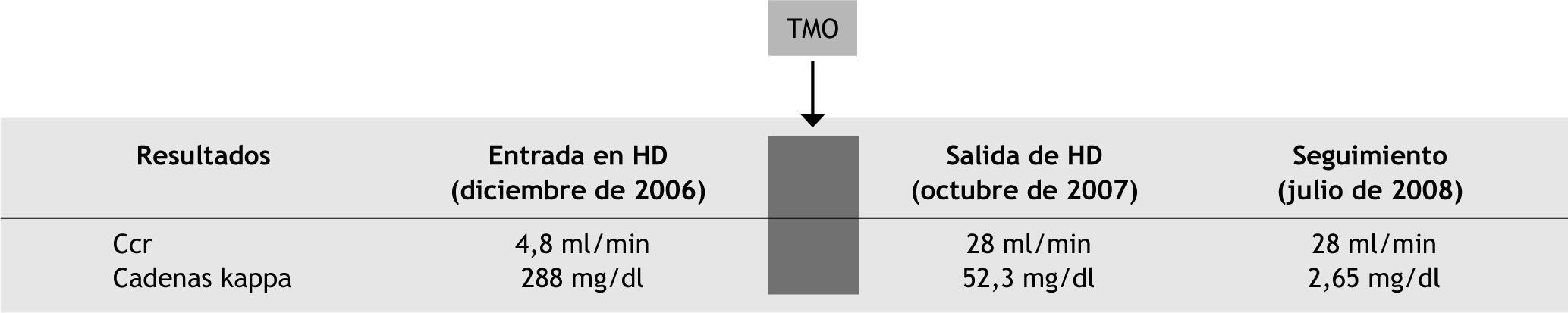
Se presentaron las incidencias siguientes: síndrome febril con foco en catéter central de sueroterapia (positivo a Staphylococcus epidermidis), cultivos del catéter Hickman negativos, buena evolución (antibioterapia según protocolo de hematología); sin complicaciones en relación a técnica de HDFVV; la función renal residual permitió buen control de volumen durante la terapia y la pauta de HDF a días alternos (fig. 2).
Podemos concluir que la HDFVV es un tratamiento eficaz como terapia sustitutiva en la insuficiencia renal a pacientes que precisan aislamiento protector porque:
- –
Se aplica de manera individualizada.
- –
Es una terapia bien tolerada hemodinámicamente.
- –
Es imprescindible la coordinación de los servicios implicados.
- –
Existen experiencias previas en la misma línea con resultados positivos en cuanto a mejoría de la función renal tras TMO, sin especificar en dichos estudios los métodos de diálisis empleados no se han especificado.
Comunicaciones de los médicos residentes a la Sociedad Norte de Nefrología. Noviembre, 2008. Pamplona. Coordinador: Nuria García.