Introducción: La radioterapia de intensidad modulada (IMRT) es una técnica de radioterapia conformal, la cual genera distribuciones de dosis muy alta y conformada en el volumen blanco (PTV) y dosis reducidas en los órganos a riesgos (OAR). El propósito de este artículo, es presentar la experiencia con IMRT en el tratamiento de los tumores del sistema nervioso central (SNC).
Material y métodos: Entre septiembre del 2006 a septiembre del 2009, un total de 32 pacientes con diagnóstico de tumores del SNC, fueron tratados mediante la técnica de IMRT, en la unidad de radioterapia del servicio de oncología del Hospital General de México (OD). Todos los pacientes fueron tratados con IMRT en un acelerador lineal Varian 21eX, las dosis variaron de acuerdo a la entidad tratada, siendo las variables estudiadas: sexo, edad, Karnosfky, etapa clínica, reporte histopatológico del primario, dosis al volumen grueso tumoral (GTV), dosis al volumen tumoral (CTV), dosis al volumen tumoral planeado (PTV), dosis a los distintos OAR, respuesta clínica y toxicidad. Siendo este un estudio de tipo observacional, retrospectivo longitudinal, descriptivo, para el análisis de la morbilidad aguda y crónica, fueron evaluadas de acuerdos a los criterios de toxicidad de la Radiation Therapy Oncology Group (RTOG).
Resultados: Del total de 32 pacientes (20.0%) con diagnóstico de tumores del SNC, en 12 casos se administró IMRT con fraccionamiento convencional, y en 20 se realizó Radiocirugía de Intensidad Modulada (IMRS). Del grupo de IMRT con fraccionamiento convencional, seis correspondieron a meningioma, cuatro a cordoma, un caso de oligodendroglioma y otro de prolactinoma. Respecto al grupo de IMRS, 12 son meningioma, tres adenomas de hipófisis, dos Malformaciones Arteriovenosas (MAV), un oligoastrocitoma, un neurinoma del acústico y un caso de epilepsia refractaria a manejo médico. En todos nuestros pacientes, se realizaron el análisis de los histogramas dosis volumen (DVH), en los distintos volúmenes de tratamiento GTV, CTV, PTV y en los OAR, siguiendo y cumpliendo con las recomendaciones de las distingas guías, de acuerdo al subsitio tumoral tratado.
Conclusiones: La IMRT proporciona una excelente cobertura del volumen blanco de tratamiento, depositándose altas dosis en dicho blanco y al mismo tiempo proteger o administra dosis en los distintos órganos de riesgo muy por debajo de la dosis tolerancia de cada uno de ellos.
Introduction: The intensity modulated radiotherapy (IMRT) is a new technique of conformal radiotherapy which distributes very high doses in target volume and small doses in the organ at risk (OAR). The objective of this article is to show the experience with IMRT in the treatment of several neoplasias such as: central nervous system (CNS).
Material and Methods: From September 2006 to September 2009, 32 patients with different cancer sub-sites diagnoses were treated with the IMRT in the Radiotherapy Service at Hospital General de Mexico (OD). All the patients were treated with IMRT with lineal accelerator Varian 21eX, the variation of doses is related to the disease, taking into account the next variables: sex, age. Karnosfky, clinic stage, hystopahologic report of the primary tumor, doses at gross tumor volume (GTV), doses at clinical target volume (CTV), doses at planning target volume (PTV), doses at the different OAR, clinic evaluation and toxicity were evaluated. This is an observational study, retrospective, longitudinal, descriptive for the analysis of AGUDE mobility and late that were evaluated according to the Radiation Therapy Oncology Group (RTOG).
Results: Of 32 patients included, 12 received IMRT with fractionated conventional radiotherapy and 20 with intensity modulated radiosurgery (IMRS). In the first group 6 were meningioma, 4 chordoma, 1 oligodrendoglioma, 1 case of prolactinoma. The group of IMRS 12 were meningioma, 3 adenoma of hypophysis, 2 arterio-venous malformations (MAV), 1 oligoastrocytoma, 1 acusticus neurynoma, 1 case of epilepsy refractory to medical treatment. In all the patients the analysis of hystogram dose volume were realised (DVH) in the different volumes of treatment (GTV, CTV, PTV) and in the organs at risk with the recommendations of the international guides in relation with the sub-site treated.
Conclusions: The IMRT brings and excellent volume target, placing high doses in the target, and at the same time sparing and protecting the different OAR at very low doses of the tolerance each one.
¿ INTRODUCCIÓN
La ventaja de la Radioterapia de Intensidad Modulada (IMRT) sobre las técnicas de radioterapia convencional, es la optimización en la cobertura del volumen tumoral. La IMRT es un avance de la Radioterapia Conformada (3DRTC), utiliza haces de intensidad no uniforme, para lo cual la optimización del cálculo que realizan los programas especiales indispensable, para lograr una distribución de dosis muy superior.1,2
En la IMRT se busca distribuciones de dosis homogéneas y/o heterogéneas, con gradientes acelerados, empleando haces de radiación de intensidad no uniforme, en los que se modula o controla la intensidad del haz de radiación, para lograr altas dosis en el tumor y al mismo tiempo, minimizar la dosis en los tejidos sanos adyacentes.3-8
El empleo de la IMRT ha llegado a ser especialmente importante en el manejo de los tumores del área de cabeza y cuello, seguido por próstata, en donde la comparación de planes entre la radioterapia convencional con la RT-3D y la IMRT, muestra una clara ventaja dosimétrica a favor de la última, más recientemente la IMRT ha comenzado a ser utilizada en las lesiones del Sistema Nervioso Central (SNC),9-13 e incluso con esquemas de fraccionamiento modificado como es el hipofraccionamiento,14,15 demostrándose un claro beneficio en los aspectos dosimétricos con una mejor conformidad y con una mayor cantidad de tejido normal o crítico, que puede ser fácilmente mantenido por debajo de la dosis de máxima tolerancia.
En nuestro país, la primera Institución en iniciar procedimientos de IMRT, fue la Unidad de Radioterapia del Servicio de Oncología del Hospital General de México (OD). En este artículo se presenta la experiencia obtenida en el manejo de estos primeros pacientes, específicamente en los tumores del SNC, haciendo énfasis en los detalles y consideraciones técnicas del procedimiento y su correlación clínica.
¿ MATERIAL Y MÉTODOS
De septiembre del 2006 a septiembre del 2009, un total de 32 pacientes con diagnóstico de tumores del SNC, fueron tratados en la Unidad de Radioterapia del Servicio de Oncología del Hospital General de México (OD). Todos los pacientes fueron tratados con IMRT con un acelerador lineal Varian 21 EX, las dosis variaron de acuerdo a la entidad tratada, y se especificarán en los párrafos subsecuentes. Los equipos para el procedimiento de la IMRT consta de:
1. Tomógrafo GE multicorte.
2. Sistemas de fijación de acuerdo al subsitio de tratamiento.
3. Sistema de planeación Eclipse v.7.25, con sistema Somavisión v.7.25.
4. Acelerador lineal dual marca Varian 21 EX.
Para la planeación del tratamiento de la IMRT se realizaron fusiones de Imágenes por Resonancia Magnética (IRM) y/o PET-CT, con imágenes tomográficas simples y/o contrastadas, del caso o sitio a tratar.
Las variables estudias fueron:
a. Sexo.
b. Edad.
c. Karnosfky.
d. Etapa clínica.
e. Reporte histopatológico de acuerdo al sitio del primario.
f. Dosis al Volumen Grueso Tumoral (GTV).
g. Dosis al Volumen Tumoral Clínico (CTV).
h. Dosis al Volumen Tumoral Planeado (PTV).
i. Dosis a los distintos órganos a riesgos (OAR).
j. Tiempo total de tratamiento.
k. Respuesta clínica.
l. Respuesta radiológica post radioterapia.
m. Toxicidad aguda.
Siendo esta revisión un estudio de tipo observacional, retrospectivo longitudinal, descriptivo (promedio, media, rango). Para determinar la asociación entre dos variables se realizó la prueba de ji cuadrada para independencia. Para el análisis de control local, falla local, locoregional, metástasis a distancia y muerte fueron estimados por el método de Kaplan-Meier.
Respecto a la optimización del cálculo de la dosis, pruebas de aceptación, comisionamiento y de control de calidad, existen artículos de varias instituciones que avalan cada uno de estos parámetros.3,5-8 En nuestra institución, también se lleva al cabo cada uno de estos distintos programas y pruebas de control de calidad, mismos que ya fueron detallados en una publicación previa.4
Todos los pacientes fueron evaluados semanalmente durante el tratamiento de IMRT, al término del mismo, al mes y posteriormente cada dos meses, durante el primer año. Cada dos a tres meses, el segundo año y cada cuatro meses a partir del tercer año. Durante el seguimiento, se realizó exploración clínica, estudios de imágenes (TC, IRM) y pruebas de laboratorio En caso de surgir alguna duda que no se aclarara con los estudios ya señalados, se solicitó PEC-CT corporal. La tolerancia de los OAR para la dosis de radiocirugía se definió y analizó, de acuerdo a las recomendaciones de la literatura.17-20 Igualmente, al emplear fraccionamiento convencional o hipofraccionamiento, se analizaron las dosis en los distintos órganos de riesgos, dándose las restricciones correspondientes de acuerdo a la estructura involucrada. La morbilidad aguda y crónica fue evaluada de acuerdo a los criterios de toxicidad de la Radiation Therapy Oncology Group (RTOG).16
¿ RESULTADOS
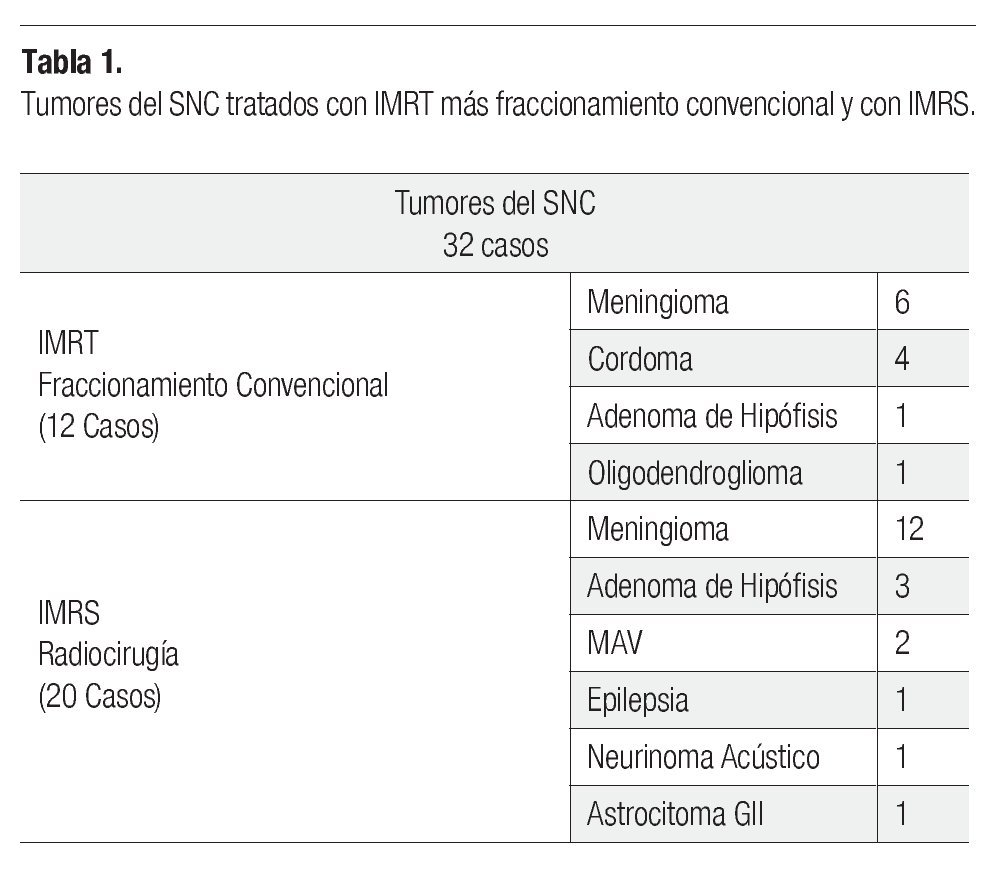
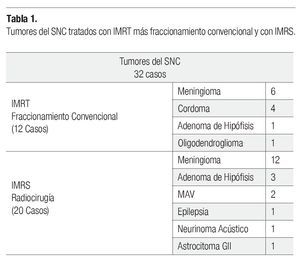
Un total de 32 procedimientos se realizaron en este grupo de neoplasias, en 12 casos se administraron IMRT con fraccionamiento convencional y en 20 casos, con Radiocirugía de Intensidad Modulada (IMRS). En la Tabla 1 se describen las distintas patologías que fueron tratadas, ya sea con IMRT más fraccionamiento convencional o con IMRS.
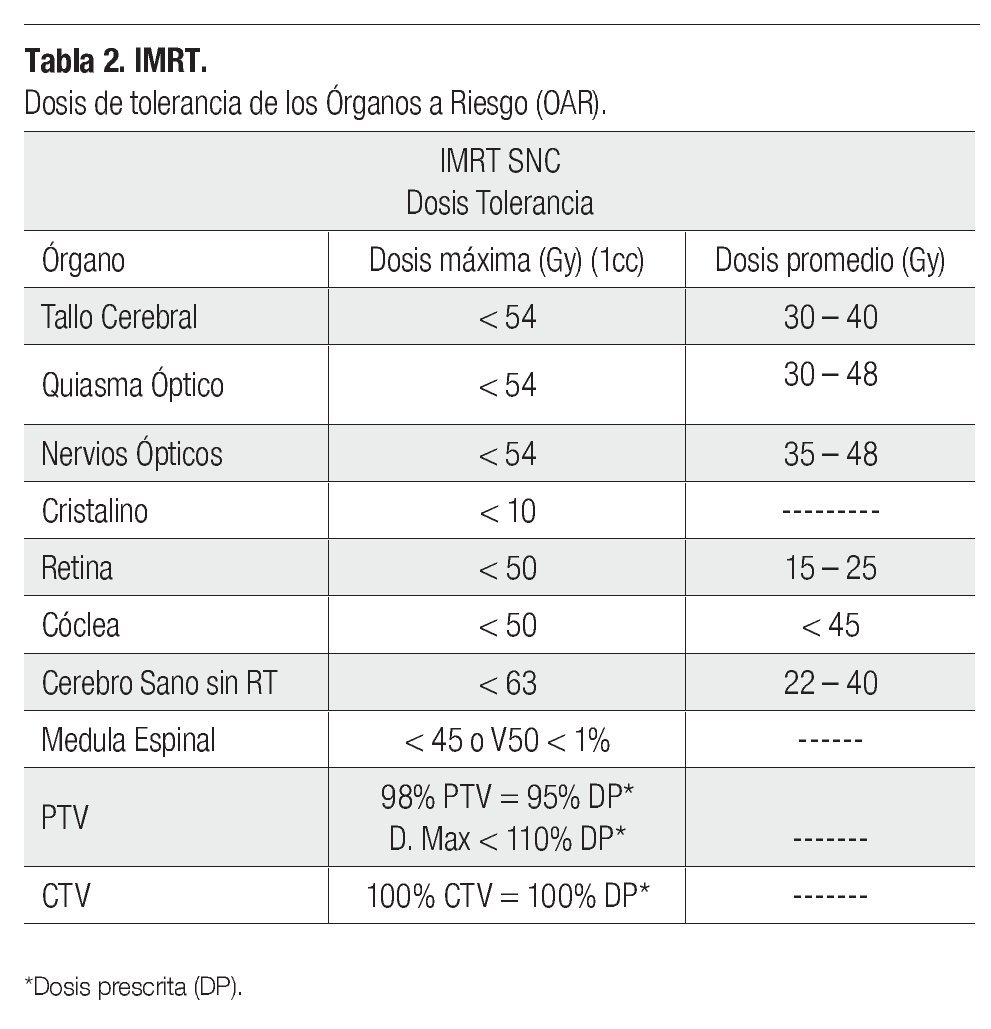
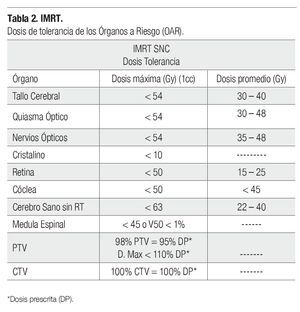
Del grupo de IMRT con fraccionamiento convencional, seis fueron meningioma (dos del ala del esfenoides, uno del seno cavernoso, quiasma óptico, órbita izquierda y fisura orbitaria superior derecha). Siendo la dosis administrada de 54 Gy en 30 fracciones, en cinco casos con márgenes quirúrgicos positivos o microscópicos y uno de 70 Gy, en 35 fracciones con resección parcial de la lesión en el ala del esfenoides derecho. En este grupo de neoplasias se definieron los distintos CTV, PTV y los OAR según el caso, en ninguno las dosis de tolerancia fue superada, sobre todo en los nervios ópticos y en el quiasma como se describe en la Tabla 2.
El estado actual de estos pacientes es el siguiente: dos están sin evidencia de actividad tumoral (SAT), en dos existe reducción del volumen tumoral en más del 50%, documentado por estudios de imágenes TC de cráneo o IRM. Un paciente presenta estatismo de la lesión en sus dimensiones, observándose en la imágenes de control, una importante zona central de necrosis tumoral, en otro caso hubo progresión y está muerto. El seguimiento promedio de este grupo es de 23.5 meses, con un rango de seis a 32 meses.
El cordoma fue la segunda neoplasia tratada, con cuatro casos (dos del ala del esfenoides y dos del clívus), siendo la dosis prescrita en dos casos de 70 Gy en 35 fracciones, otro con 60.20 Gy en 28 fracciones y otro con una presentación inusual del cordoma del clívus, con metástasis ganglionar en el Nivel II del cuello derecho. Corroborado lo anterior, con biopsia positiva para metástasis de un cordoma, la dosis administrada en este caso fue de 69.96 Gy en 33 fracciones al primario y de 59.40 Gy en 33 fracciones a la zona linfoportadora afectada. Dos pacientes están vivos sin AT (uno del ala del esfenoides, y el otro del clívus con metástasis ganglionar) y dos tuvieron progresión, uno está vivo con AT y el otro falleció. El seguimiento promedio es de 12 meses, con un rango de seis a 27 meses.
Las otras dos patologías tratadas con IMRT y fraccionamiento convencional fueron: un oligodendroglioma temporal izquierdo, recibiendo una dosis de 5400 cGy en 30 fracciones, a la fecha se encuentra sin evidencia de AT a 30 meses de seguimiento. Y un caso de adenoma de hipófisis productor de prolactina, que por cercanía del quiasma (1 mm), se le programó una dosis de 5400 cGy en 30 fracciones, a 29 meses de seguimiento se encuentra sin evidencia de lesión y con control bioquímico normal.
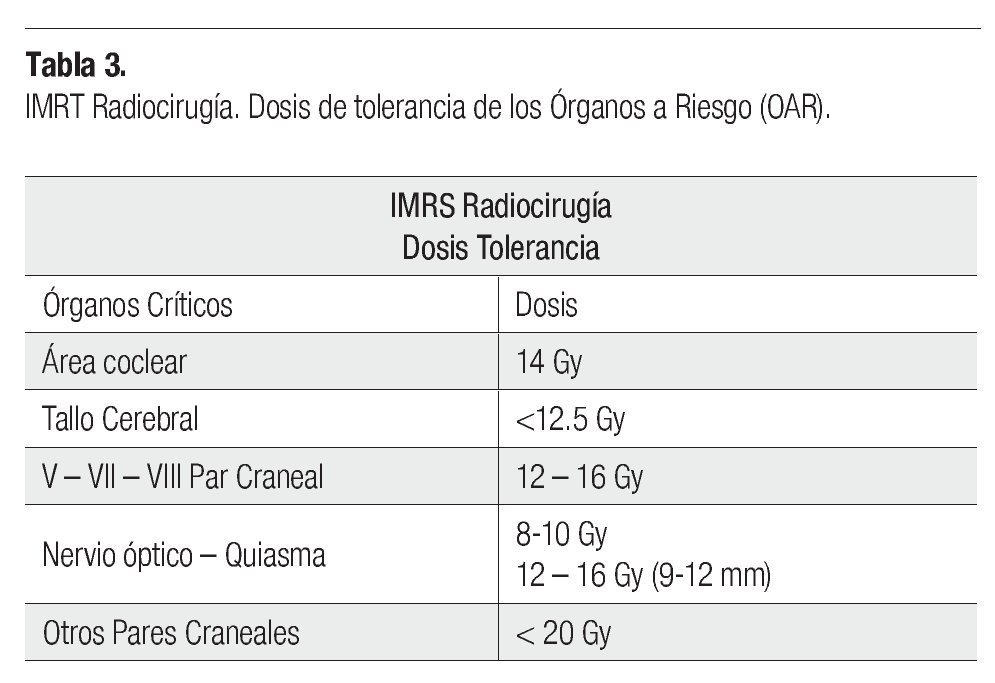
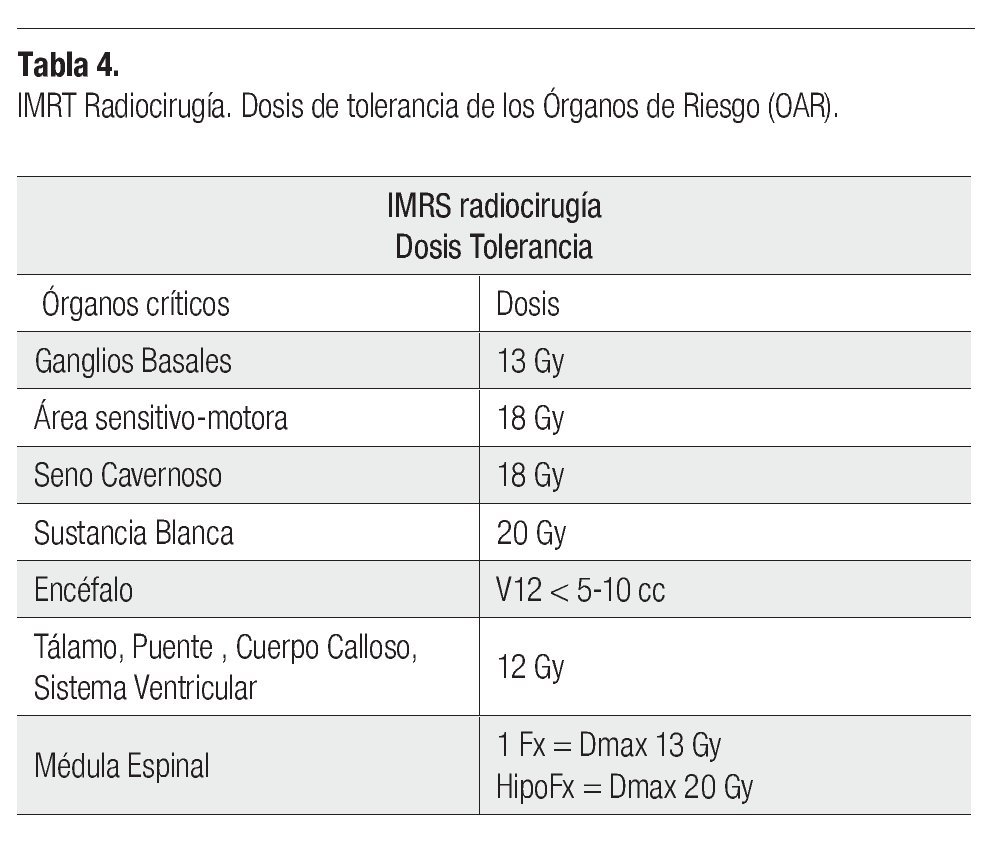
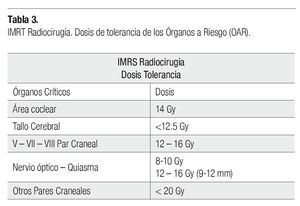
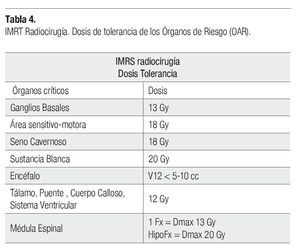
Respecto al grupo de IMRS, la patología que más se trató fue el meningioma con 12 casos, seguidos de tres adenoma de hipófisis, dos MAV, un oligoastrocitoma, un neurinoma del acústico y un paciente con epilepsia refractaria a manejo médico. La dosis administrada en 12 pacientes fue una dosis única, la cual dependió de la patología a tratar. En ocho pacientes se administraron un esquema de hipofraccionamiento dosis 3500 cGy en siete sesiones. Independiente de la administración con dosis única o con el esquema de hipofraccionamiento, el procedimiento realizado fue con el mismo criterio de radiocirugía, dosis única. La tolerancia de los OAR para la dosis de radiocirugía se describe en la Tablas 3 y 4.
De los 12 Meningiomas, seis se trataron con el esquema de hipofraccionamiento (dos del seno cavernoso, dos de la región petroclival, uno de la unión cráneo cervical y otro del ala del esfenoides). De estos pacientes, cuatro están con Respuesta Completa (RC), uno con Respuesta Parcial (RP), más del 50% (seno cavernoso) y el otro con RP menor del 50% (ala del esfenoides), con un seguimiento promedio de 25.2 meses (rango de seis a 38 meses).
Se trataron tres adenomas hipofisiarios, dos no productores y uno productor de Hormona del Crecimiento (HC). La dosis administrada fue en los dos adenomas no productores, uno con dosis de 3500 cGy en siete fracciones y otro con dosis de 20 Gy en una fracción. El productor de HC recibió una dosis de 3500 cGy en siete fracciones. El estado actual de estos pacientes, dos se encuentran sin evidencia de enfermedad, corroborado mediante imágenes TC de cráneo e IRM, que corresponde a los adenomas no productores. Respecto al adenoma productor de HC, éste se encuentra vivo, con una reducción del volumen tumoral en un 50% y con control bioquímico de la HC y de la somatomedina C, dentro de parámetros normales. El seguimiento de este grupo de pacientes es de 27.3 meses, con un rango de 19 a 38 meses.
Dos pacientes se trataron con diagnóstico de MAV, uno de la región parietal derecha y otro a nivel talámico derecho, siendo la dosis de 16 Gy en una fracción y 20 Gy en una fracción, respectivamente. En ambos casos, se encuentra con documentación radiológica (angiografía, angiotac) de obliteración del 100% de estas lesiones, el seguimiento promedio es de 26.5 meses, con un rango de 21 a 32 meses.
Un oligoastrocitoma anaplásico de la región parieto occipital derecha, recibió dosis complementaria con radiocirugía de 20 Gy en una fracción, después de haber administrado una dosis de 4500 cGy en 25 fracciones con radioterapia externa, conformada en 3D (RT-3D), la evolución de este paciente fue tórpida con progresión de la lesión y falleció al año de haber terminado su tratamiento.
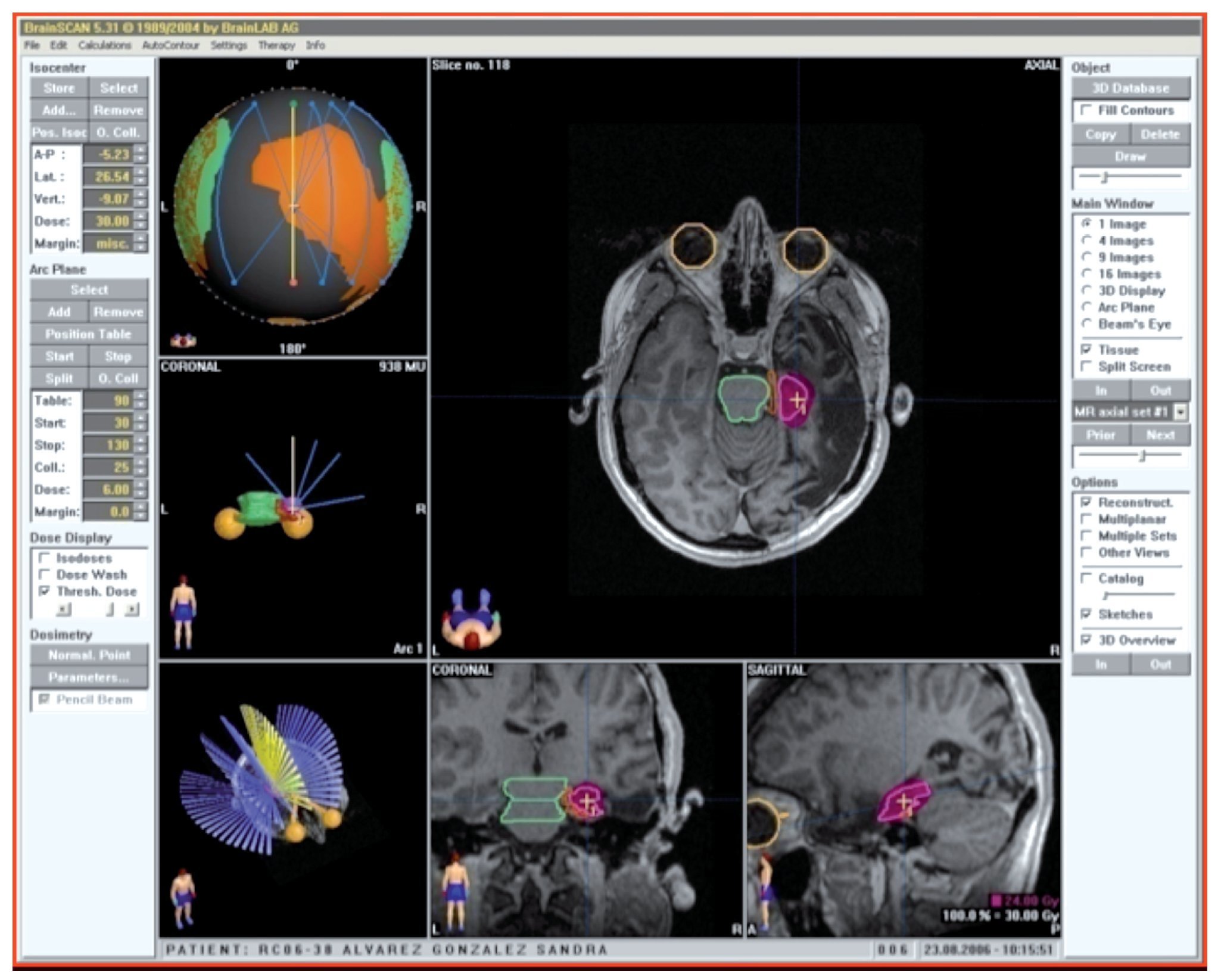
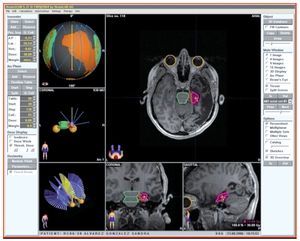
El paciente con diagnóstico de epilepsia del lóbulo temporal (hipocampo derecho), refractario a manejo médico y con convulsiones no controladas, fue ingresado a un protocolo de radiocirugía para este grupo de patología, programándose una dosis de 30 Gy en una fracción. En este caso en particular, la mejor planeación de radiocirugía se logró con IMRS (Figura 1), a 19 meses de seguimiento el número de convulsiones han disminuido, mejorando su calidad de vida.
Figura 1. Paciente con diagnóstico de epilepsia del lóbulo temporal (hipocampo derecho) con tratamiento de radiocirugía logrado con IMRS.
Por último, un paciente con diagnóstico de neuóstico de neustico de neurinoma del acústico izquierdo recibió una dosis, con el esquema de hipofraccionamiento con dosis de 3500 cGy en siete fracciones, a 13 meses de seguimiento se encuentra una reducción del volumen tumoral del 50% y con mejoría clínica respecto a la audición.
¿ DISCUSIÓN
Nuestro estudio confirma las observaciones de otras instituciones, respecto a las patologías que pueden ser abordadas por medio de la IMRT.7,21-22 Los tumores del área de cabeza y cuello, son el grupo más frecuentemente tratados con esta modalidad, en nuestra serie correspondieron a 60 pacientes (37.3 %), seguido por el cáncer de próstata con 55 casos (34.2%), en tercer lugar por las lesiones del SNC con 32 pacientes (19.9%), seguidos por los tumores ginecológicos ocho pacientes (5%).
La Radioterapia Estereotáxica (RTE) en los tumores del SNC se enfrenta a la dificultad de definir el volumen metabólicamente activo de la lesión, que puede tener una forma irregular y hasta tortuosa, rodeado de OAR que limitan la dosis administrable: cristalino, retina, nervio óptico, quiasma, tronco cerebral, hipófisis. Pero se tiene la ventaja de que el cráneo es fácilmente fijable y adaptable a técnicas de estereotaxia.4
Koo VS y colaboradores23 comparó planeaciones de pacientes con tumores cerebrales, realizadas con IMRT y con RTE conformada. Las planeaciones de IMRT eran ligeramente mejores en cuanto a la cobertura tumoral, con índices de homogeneidad y conformidad superiores, aunque con una mayor dosis sobre los nervios ópticos y tronco cerebral, pero por debajo del umbral de tolerancia.
Con el advenimiento de la TC, IRM que permite la visualización de la anatomía del paciente y los potenciales volúmenes blancos, la RTE conformada tridimensional (RT-3D), ha llegado a ser empleada ampliamente en el tratamiento de las lesiones en el SNC, debido a la mejoría en la conformidad de la dosis en el blanco tumoral, además de la separación de los OAR, al compararse con los campos de la RTE convencional.24
La IMRT en las lesiones del SNC tienen importancia, debido a la proximidad de estructuras críticas. Un detalle aún por definir y en especial en el tejido sano del SNC, es el incremento de la dosis total acumulada, que es conocida como dosis integral (DI). Algunos estudios han reportado un incremento de la DI con la administración de la IMRT,25,26 mientras que otros reportan, que no existe este incremento.27,28 Se sabe que con el incremento de la DI, un volumen de tejido sano se expone a dosis baja de radiación, esto es importante al tratar con IMRT en el SNC.24
Selek U y Chan EL realizan una revisión de las indicaciones de la IMRT en los tumores de base de cráneo y de la fosa posterior, dando pautas para la determinación de los distintos volúmenes blancos (GTV, CTV, PTV) para tumores como: meningioma, neuroestesioblastoma, cordoma, condrosarcomas, schwanomas, meduloblastomas.29
En recientes publicaciones, la IMRT ha sido investigada, su aplicación en los astrocitomas de alto grado24,30,31 e incluso esquema de hipofraccionamiento también ha sido explorado.32
Un total de 32 pacientes han sido tratados en nuestra serie, en 12 casos se administró IMRT con fraccionaó IMRT con fracciona- IMRT con fraccionamiento convencional, y 20 se trataron con dosis única mediante radiocirugía (IMRS). Del grupo de IMRT con fraccionamiento convencional, seis fueron meningioma, cuatro cordoma, un adenoma hipofisario y un oligodendroglioma. La eficacia y seguridad de la IMRT en el manejo de los meningioma ha sido recientemente demostrado.33,34 Uy NM y colaboradores reporta sus resultados con un control local del 93%, SVLE y SVG a cinco años del 88% y 89% respectivamente.33
De este grupo de pacientes, dos están vivos y sin datos de AT, tres están también vivos pero con persistencia de actividad tumoral, en dos de estos hay reducción del volumen tumoral en más del 50% y uno está con estatismo de la lesión, finalmente el sexto paciente falleció con AT.
El manejo inicial del cordoma es quirúrgico, pero esto no es factible en muchos casos, por lo que la radioterapia adyuvante es la recomendación para pacientes con márgenes quirúrgicos positivos y en caso de enfermedad residual.35,36 Varios investigadores recomiendan que el cambio de partículas (protón), sea el tratamiento ideal para el abordaje de los cordoma de base de cráneo.35,37
Los cuales reportan SVLE y SVG a cinco años del 63% y 68%, respectivamente. Sin embargo, otros autores reportan excelente resultados con la administración de altas dosis con RTE convencional, al administrar dosis post quirúrgicas, entre 60 a 70 Gy.38,39 El papel de la IMRT ha sido reciente investigado por Selek U y Chan E, que recomiendan dosis de 66 Gy con fraccionamiento convencional.29
De los cuatro cordomas de nuestra serie, dos se trataron con fraccionamiento convencional y dos con fraccionamiento alterado. Después de un seguimiento promedio de 12 meses (rango de seis a 27 meses), dos pacientes se encuentran vivos y sin AT.
Respecto al grupo de IMRS, de un total de 20 casos, la patología que más se trató fue el meningioma con 12 casos, seguidos de tres adenomas de la hipófisis, dos MAV, un oligoastrocitoma, un neurinoma del acústico y un paciente con epilepsia refractaria a manejo médico. La dosis administrada en 12 pacientes fue una dosis única, la cual dependió de la patología a tratar y en ocho casos se administró un esquema de hipofraccionamiento con dosis de 3500 cGy en siete sesiones.
La utilidad de la radiocirugía ha sido ampliamente documentada en diversas series, en que analizan los resultados en el meningioma,40,41 adenomas hipofisiarios,42,43 MAV,44-46 astrocitomas,47,48 neurinoma del acústico49,50 y en la epilepsia del lóbulo temporal refractaria a manejo médico.51,52
Más recientes esquemas de hipofraccionamiento, han sido investigados y aplicados en diversas patología del SNC (meningiomas, gliomas, adenomas hipofisiarios).14,15,32,53,54 Los resultados a largo plazo de la IMRT en los tumores del SNC, son limitados debido a lo relativamente reciente de su introducción en este grupo de patologías.
¿ CONCLUSIONES
La IMRT en comparación con otras técnicas de planeación, ofrece la mejor posibilidad de separar las estructuras críticas cercanas al volumen tumoral. Los resultados de estudios preliminares, que analizan las curvas de distribución de dosis en las planeaciones e independientes del subsitio tratado, está asociado con una sustancial reducción en la toxicidad asociada al tratamiento. La IMRT puede reducir los puntos calientes en forma significativa, en el tejido sano circunvecino y en la piel. El empleo de la IMRT en lesiones del SNC ha tomado auge, en los estudios en que reportan sus resultados señalan una reducción en la neurotoxicidad aguda y tardía con este procedimiento, sin embargo existe controversia en el análisis de la DI, en distintas regiones del cerebro.
Correspondencia: Dr. Pomponio José Luján-Castilla.
Dr. ATL. # 6 Manzana 3, Unidad Belisario Domínguez, Tlalpan, CP 14310, México D.F.
Teléfono: 55 5678 5918. Celular: 55 5452 3006.
Correo electrónico: pjlujanc@yahoo.com.mx