El objetivo de esta revisión es comprobar la posibilidad y plausibilidad de utilizar fármacos selectivos de receptores cannabinoides (CB) como antitumorales, dado que las células neoplásicas presentan una expresión alterada de estos ligandos. Partiendo del estudio del sistema endocannabinoide (SEC) y su relevancia como modulador homeostático en distintas funciones cerebrales superiores o cognitivas, se iniciaron diversas líneas de investigación relacionadas con los mecanismos de acción y los receptores celulares CB tipo 1 y 2. Se ha demostrado que fármacos agonistas (cannabiméticos) de los receptores CB son capaces de inhibir la mitosis de células carcinógenas. Múltiples estudios en distintas neoplasias, donde se realizan xenotrasplantes a ratas con células tumorales de humano, demuestran una disminución en su crecimiento celular, efecto dosis-dependiente, así como en la viabilidad de las células carcinógenas. Resulta totalmente alentador el estudiar más a fondo esta nueva aproximación terapéutica contra el cáncer, el impacto que podría tener implementa terapias sinérgicas basadas en cannabinoides y quimioterapia contra las neoplasias más prevalentes en el mundo, podría ofrecer un tratamiento más completo. Se abordan las neoplasias sensibles a esta terapia, el estado del SEC en el cáncer, los efectos adversos de los cannabinoides contra el cáncer, así como los estudios más relevantes que justifican esta nueva aproximación terapéutica contra el cáncer.
The objective of this review is to check the possibility and plausibility of using selective cannabinoid agonists/antagonists as antitumor drugs, because the neoplastic cells have demonstrated an altered expression of these ligands. Based on the study of the endocannabinoid system and its relevance as a superior homeostatic modulator in different brain functions or cognitive ones, various lines of research started studying the mechanisms of action and cellular response of the cannabinoid receptors type 1 and type 2. In this respect it has been shown that the cannabinoid receptor agonist drugs (cannabimemetic) are capable of inhibiting mitosis of cancer cells. Multiple studies in various cancer cells, where a xenotransplant is done in rats with tumor from human cells, they show a decrease in cell growth, dose-dependent effect, thus as on the viability of cancer cells. Is completely encouraging to study more thoroughly this new therapeutic approach against cancer, the impact that might have to deploy synergistic therapies based on cannabinoids and chemotherapy against the most prevalent malignancies in the world, could offer a more complete treatment. This review checks the neoplasm that are sensitive to be treated with cannabinoids, the endocannabinoide system in cancer, the adverse effects of the cannabinoids in cancer, and the most relevant studies that justify this new therapeutic approach against cancer.
Introducción
Desde hace tiempo, la Cannabis sativa y sus componentes activos han despertado mucho interés en el campo de la investigación, naciendo del hambre por conocimiento, se empezó a cuestionar los mecanismos por los cuales el fumar esta sustancia producía efectos psicoactivos en los seres humanos, así como efectos anecdóticos de sus consumidores, sin duda, el nuevo enfoque mundial en cuanto a la legalización de esta droga ha despertado y permitido a los científicos y la comunidad médica tener un mejor entendimiento de esta sustancia en su comportamiento, como quizás el descubrimiento más interesante y poco conocido en la actualidad.
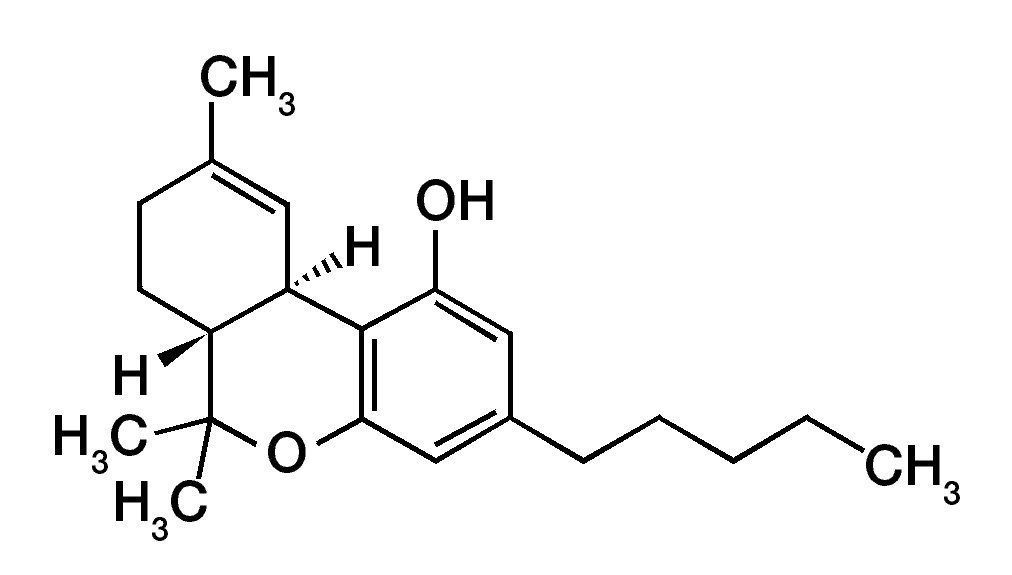
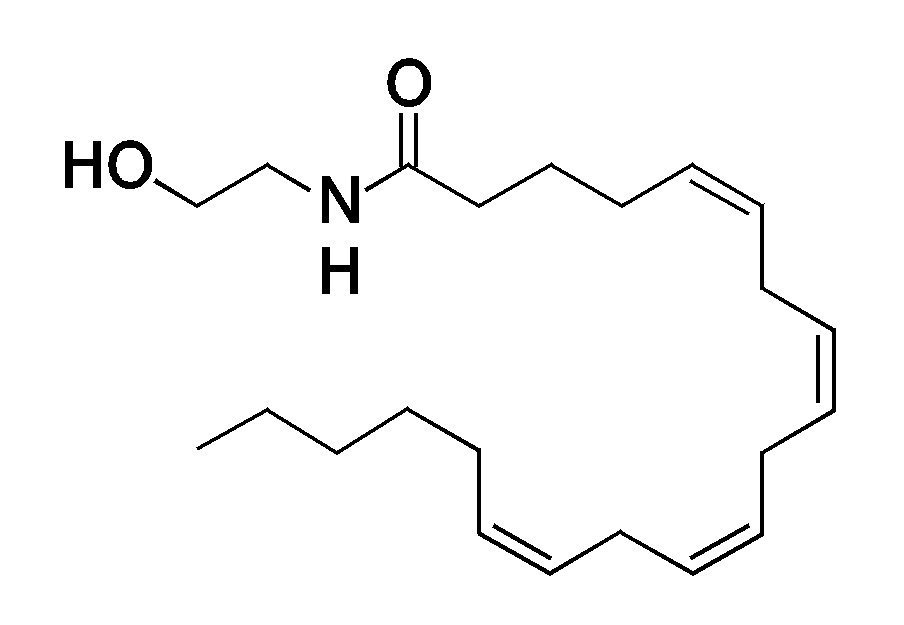
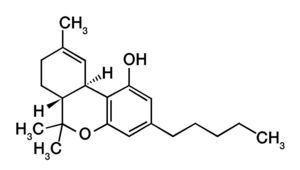
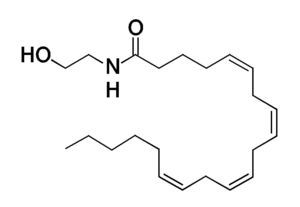
En 1964, se descubre el ¿9-THC (tetrahidrocannabinol) (fig. 1) componente principal de la Cannabis sativa1, de aquí nació el interés por buscar los mecanismos fisiológicos de esta sustancia en el compartimento humano, posteriormente se identifican los receptores celulares sensibles a Δ9-THC, los receptores a cannabinoides tipo 1 (CB1)2 y tipo 2 (CB2). Más interesante fue el descubrimiento de 2 ligando naturales de estos CB, la anandamida (AEA)3 (fig. 2) y 2-araquidonilglicerol, sin más, se estudió a detalle el proceso de síntesis, degradación y transportación de estos ligandos naturales, para así poder concluir con el descubrimiento del sistema endocannabinoide (SEC).
Figura 1 Composición molecular del fitocannabinoide más abundante en la planta Cannabis sativa: Δ9-tetrahidrocannabinol (¿9-THC).
Figura 2 Composición molecular del endocannabinoide más potente del ser humano: Anandamida.
El estudio farmacológico de sustancias 'cannabinoides' que no producen efectos psicoactivos, ha creado una nueva línea terapéutica contra múltiples patologías. El objetivo de esta revisión es aclarar su implementación en la terapia antitumoral.
El sistema endocannabinoide
Es impresionante describir la expresión que tiene el CB1 a nivel de sistema nervioso central4, resulta natural entender por qué el consumo de Cannabis sativa posee tan diversos efectos psicoactivos en el ser humano, sin dejar de lado que diversos mamíferos5 también presentan estos CB y éste se halla conservado evolutivamente. Si bien no se entiende aún muy bien la fisiología o su relevancia como modulador homeostático, se han descrito diversos mecanismos celulares a nivel de membrana celular por los cuales el agonismo de los CB desencadena una serie de reacciones de segundo mensajero asociado a una proteína6 G/i-α. Mencionar que este tipo de receptores tienen una densidad de expresión muy alta en el cerebro, incluso mayor que receptores de GABA y glutamato4.
A continuación describiremos la bioquímica de este sistema, su síntesis, su mecanismo de acción y degradación, para entender los efectos postagonismo de los receptores CB1, CB2 y su relación con la carcinogénesis; con especial interés en la AEA, el endocannabinoide más estudiado hasta ahora.
Los endocannabinoides son precursores fosfolipídicos de la membrana celular7, la AEA, se forma de la biosíntesis de 2 productos, esta reacción es catalizada por la N-acetiltransferasa, ubicua en la membrana celular, esta enzima mueve el ácido araquidónico de la fosfatidilcolina a la cabeza polar de la fosfatidiletanolamina, esto forma el precursor de la AEA, N-araquidonil-etanolamina (NAPE), éste se mantiene en la membrana hasta que como último paso, la fosfolipasa D, termina por catalizar el precursor y producir el endocannabinoide AEA, esta enzima es considerada de la familia de las metalohidrolasas de zinc, la cual se ve activada por una despolarización de la membrana o por la activación de receptores de membrana de glutamato (NMDA), receptores metabotrópicos de algunos neurotransmisores como dopamina o acetil-colina6. Por último hablaremos del proceso de captación y degradación del endocannabinoide, las cantidades liberadas de éstos, están controladas estrechamente por 2 mecanismos, uno es la captación de la célula y otro por hidrólisis de una enzima, el primero, describe un transporte intermembrana, el cual ha sido denominado transportador de anandamida.
Similar a otros receptores para la captación de lípidos, este receptor se puede saturar y algunas drogas lo inhiben, lo que puede terminar en un incremento en los niveles de AEA en el organismo. El otro mecanismo consiste en la hidrólisis por la enzima amida hidrolasa de ácidos grasos, esta enzima se encuentra en gran densidad en el cerebro, esta enzima cataliza la descomposición de la AEA en ácido araquidónico y etanolamida.
El mecanismo de acción de los endocannabinoides ha sido descrito poco tiempo atrás6, sin embargo, los mecanismos intrínsecos de la activación de CB1 y CB2 son tan variados y complejos que aún falta por describir en su totalidad este efecto agonista.
La AEA tiene un agonismo parcial de CB1 y CB2, sin embargo, presenta más actividad frente a los CB1 que CB2. Los receptores CB1 y CB2 están acoplados a proteína G/i-α, una vez en el receptor, los cannabinoides activan el receptor con la consecuente inactivación de la adenilato ciclasa, lo cual regula los niveles de cAMP, terminando en la inhibición de los procesos de fosforilación dependientes de algunas proteínas quinasa, como la PKA, MPKA, entre otras reguladoras de la transcripción genética6.
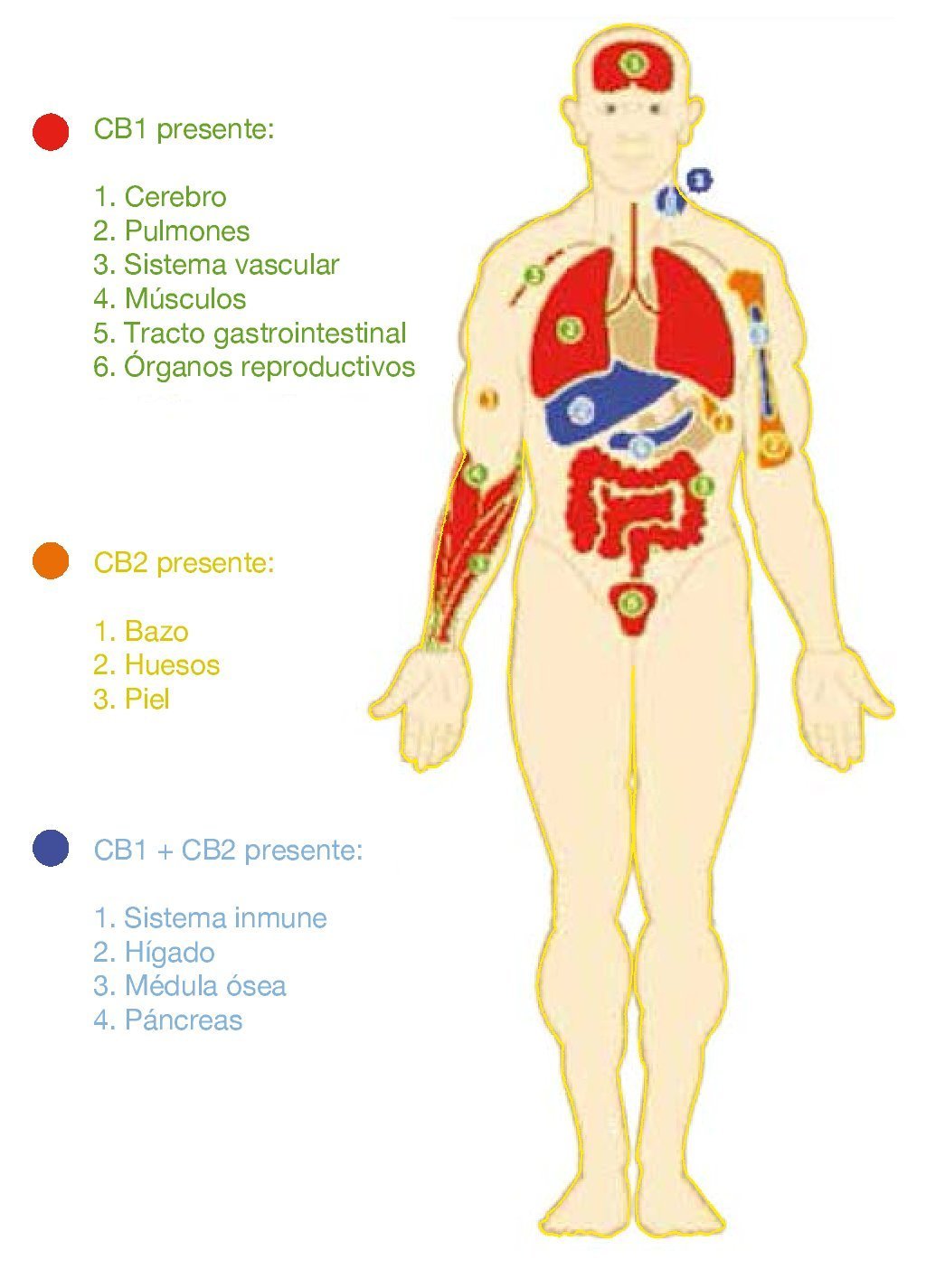
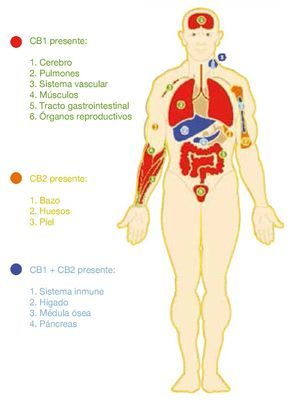
Se ha descrito la presencia de receptores CB reguladores homeostáticos en todos los sistemas corporales (fig. 3), por lo cual su alteración se encuentra relacionada con diversas patologías, en nuestra revisión hablaremos de la carcinogénesis.
Figura 3 Presencia de receptores cannabinoides reguladores homeostáticos en todos los sistemas corporales.
Farmacología en el sistema endocannabinoide
Una vez que la ciencia logró descifrar la existencia de los receptores CB1 y CB2, estos fueron clonados y estudiados, dilucidando su conformación proteica y mística celular, se lograron crear fármacos que tuvieran un efecto ligando-agonista en estos receptores8. Actualmente contamos con herramientas farmacológicas que nos permiten agonizar de manera selectiva y no selectiva a los CB, asimismo podemos farmacológicamente aumentar o disminuir la degradación de los endocannabinoides como la AEA.
¿Cuál sería el propósito de crear una nueva línea farmacológica que tuviera el mismo efecto de los endocannabinoides? Partiendo del hecho que estos receptores controlan distintas vías celulares de señalización, la activación farmacológica selectiva de los mismos podría llegar a modular alteraciones de la célula y crear un beneficio terapéutico.
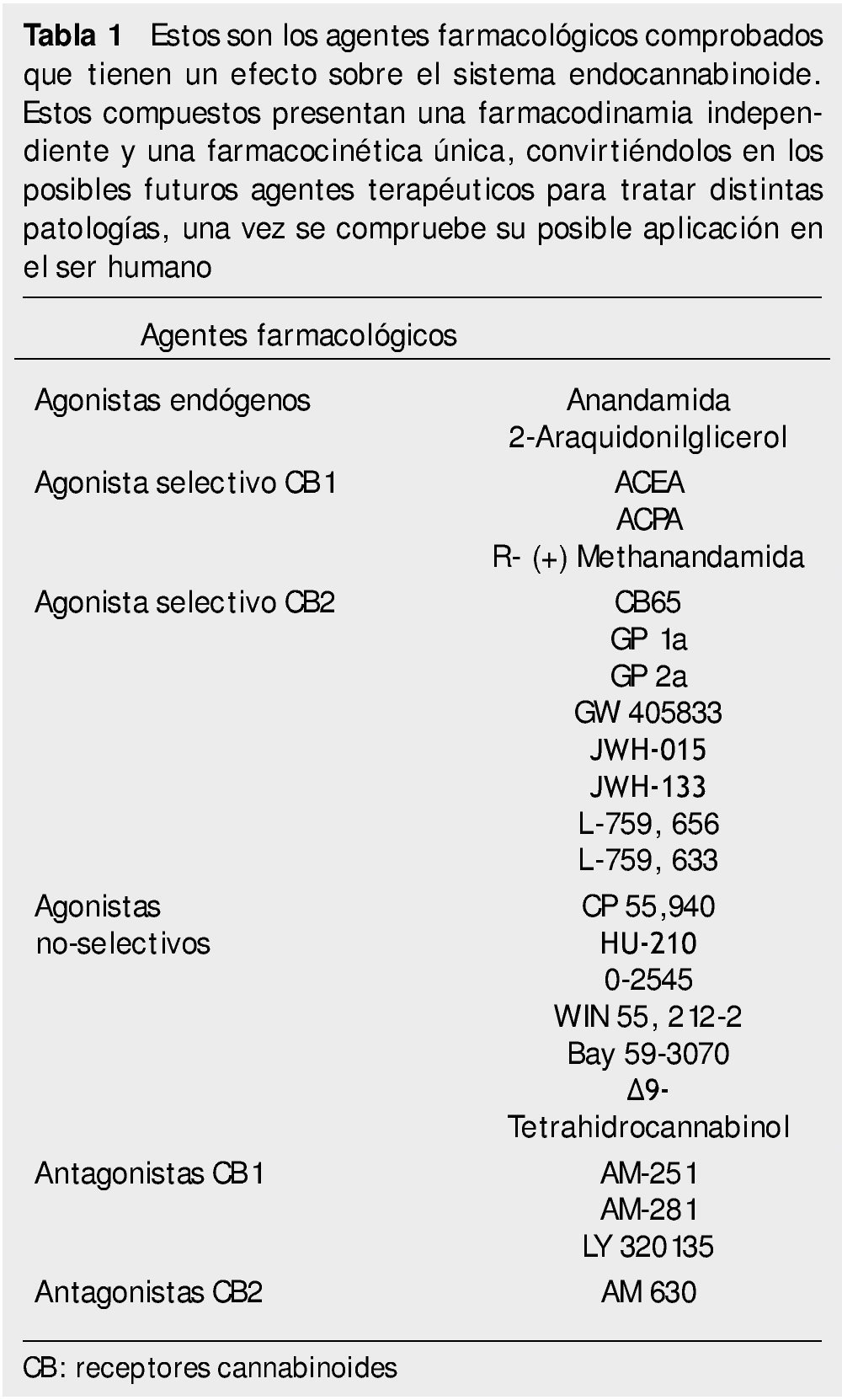
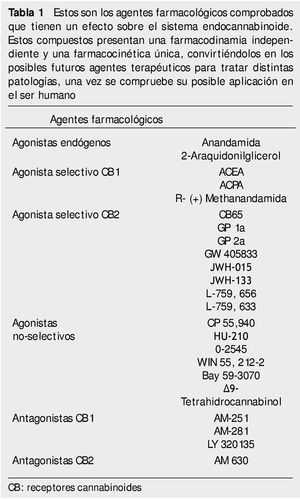
En la tabla 1 se ofrece una visión completa de los actuales fármacos que se encuentran en el mercado, cabe decir que estos agentes aún no han sido aprobados con fines terapéuticos, sino con fines experimentales.
Actualmente, existen estudios donde el agonismo de receptores CB con estos agentes cannabiméticos disminuye el tamaño tumoral, efecto que es revertido por el antagonismo de los mismos9, evidenciando la responsabilidad de los CB.
Otro punto interesante de aplicar fármacos derivados de CB, es que poseen un margen de seguridad bastante aceptable, es decir, los efectos adversos o no deseados ya se conocen. No es una sustancia nueva, pues su utilización es milenaria y se tiene bien documentado qué esperar tras su consumo, el mayor efecto no deseado podría ser el efecto psicoactivo que tiene el consumo agudo de Cannabis, en vista de esto, se aclara que los fármacos derivados exclusivamente de cannabidiol (CBD), el segundo cannabinoide más prevalente en los extractos de Cannabis sativa, poseen un agonismo inverso10 exclusivo por los receptores CB, esto implica que no se activen los CB1, los responsables de los efectos psicoactivos en los pacientes.
A su vez, el uso experimental en modelos in vivo, demuestran pocos efectos tóxicos en células normales, mientras que las células cancerígenas sí se ven afectadas por la aplicación de la sustancia, induciendo su apoptosis, se menciona incluso un efecto protector en células normales ante el estrés oxidativo11.
Estas características, entre otras, confieren a la terapia basada en cannabinoides un espectro farmacológico muy seguro.
El cáncer y su peso social en la actualidad
En nuestros tiempo, la fisiopatología de las neoplasias malignas ha sido muy bien descrita, mutaciones adquiridas en nuestro ADN, terminan por generar una célula defectuosa, donde sus mecanismos de replicación y proliferación se vuelven aberrantes. Una especie de célula zombi, cuyo único propósito es nutrirse de su hospedero. Este zombi, tiene la capacidad de generar su propia irrigación (angiogénesis), pues necesita mayor cantidad de oxígeno, igual va aumentando de tamaño conforme adquiriere mayor número de mutaciones, peor aún, tiene la capacidad de viajar por nuestro sistema linfático y generar un tumor secundario (metástasis), o como nos gusta decirlo, infectar a una célula vecina convirtiéndola en un zombi más.
Sin duda, las enfermedades neoplásicas se han vuelto un problema de salud mundial, las últimas estadísticas oficiales que arrojan datos confiables o al menos estimados en cuanto la incidencia y mortalidad de 27 neoplasias más prevalentes en 182 países, están actualizadas hasta el 2008 por la International Agency for Research on Cancer. En su estudio Global Biology of Cancer 2008 (GLOBOCAN)12 manifiesta la siguiente información: un total de 12.7 millones de casos nuevos al año de cáncer sin diferencia de sexo, alarmante las 7.6 millones de muertes responsables por el cáncer, a su vez, describen que el cáncer de pulmón sigue siendo la neoplasia más común en el mundo, tanto en incidencia (1.6 millones, 12.7%) como en mortalidad (1.4 millones, 18.2%), el segundo en incidencia es el cáncer de mama (1.4 millones, 10.9%), pero ésta es la quinta causa de muerte por cáncer (458,000, 6.1%), el tercero en incidencia es el colorrectal (1.2 millones).
Sin quitarle relevancia a las estadísticas epidemiológicos del cáncer, es importante recordar que la población mundial se está haciendo más anciana, es decir, el mundo se está preparando para tener más casos de cáncer, conforme la esperanza de vida aumenta, las posibilidades de presentar neoplasias también se incrementan. Esto definitivamente conlleva un desequilibrio para todas las familias, pues es bien sabido por la comunidad científica que muchas veces el cáncer se origina sin ningún tipo de antecedente familiar o exposición a factores de riesgo, éste sólo ocurre.
Ahora bien, en la actualidad cuando un paciente es diagnosticado con cáncer, ocurre en efecto dominó lo siguiente: se le notifica a éste de su condición, se le explican las posibles causas de su enfermedad, se le estadifica en cuanto al avance de su neoplasia y por último, se le platica sobre el tratamiento que recibirá. Estamos hablando de la quimioterapia y radioterapia, por no decir que la cirugía oncológica muchas veces es indicada demasiado tarde, pues ya existe metástasis.
También contamos con la nueva terapia molecular, fármacos con anticuerpos monoclonales dirigidos a inhibir procesos moleculares y de señalización celular, con un pequeño inconveniente, estos tratamientos son estratosféricamente caros y poco accesibles para la sociedad y los centros de salud, reconociendo el estado humilde en el cual la mayoría de la población vive, si bien pudieran acceder al tratamiento, éste les generaría un costo económico impresionante. El tratamiento antitumoral tiene 2 distintos objetivos: control local por medio de cirugía y radioterapia, y aquel que busca erradicar la enfermedad vía sistémica: quimioterapia, inmunoterapia, hormonoterapia y terapias blanco.
Desgraciadamente, la mayoría de las neoplasias son diagnosticadas en etapas avanzadas en las cuales ya solamente se puede ofrecer un tratamiento paliativo, es decir, no curará su condición, sólo retrasará el tiempo en el que éste termine con la vida de los pacientes.
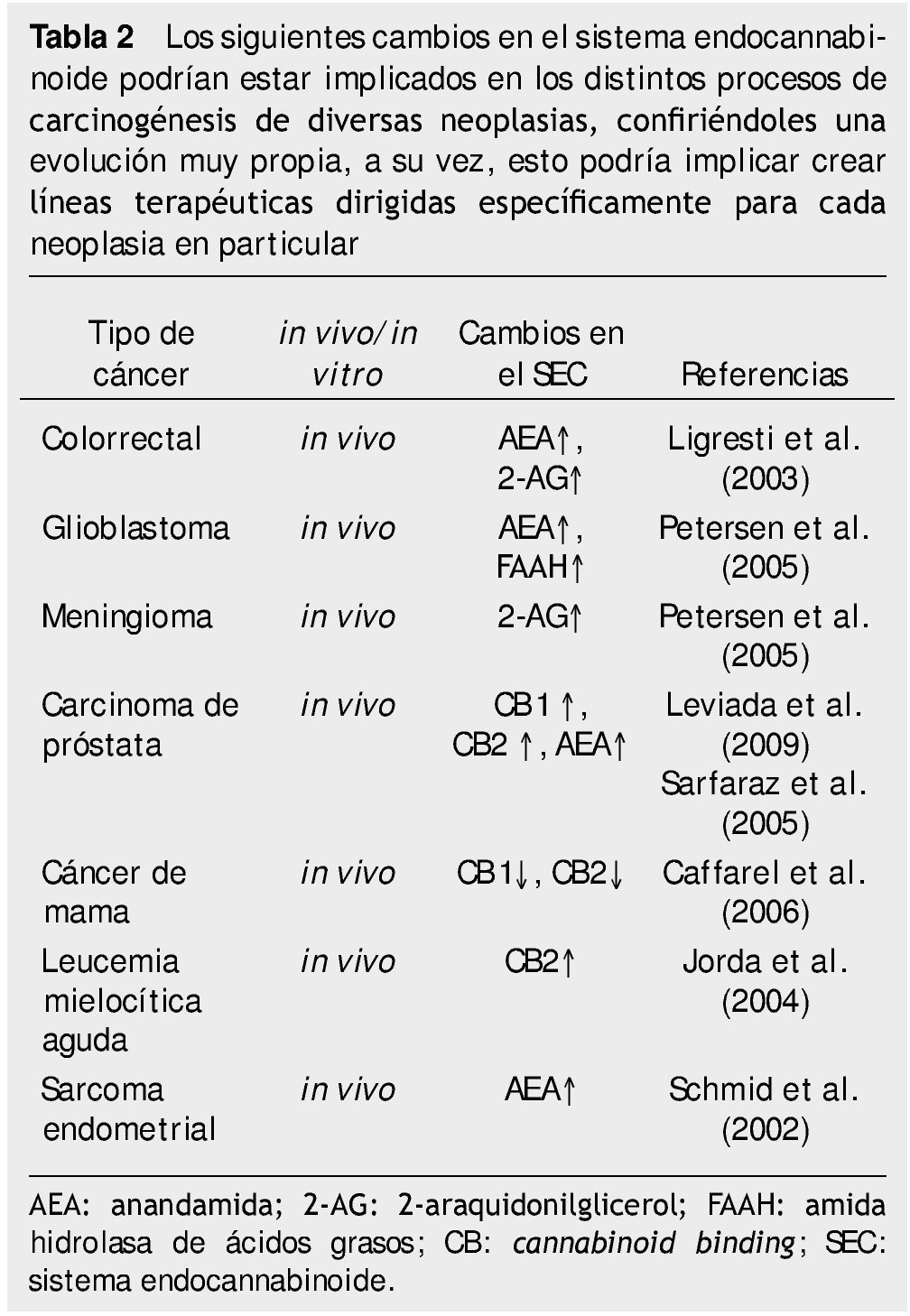
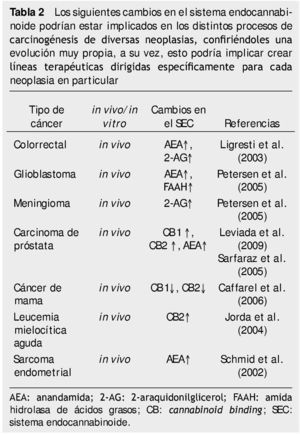
Entonces nace la pregunta, una que busca aportar algo distinto, algo nuevo, ¿si existiera algo inocuo en la célula?, ¿algo que siempre ha estado ahí y apenas lo descubrimos?, y quizá sea uno de los motivos por el cual la célula cancerígena es tan difícil de tratar. Varios estudios a la hora de demostrar la eficacia del tratamiento con CB, descubren que el SEC se encuentra alterado13, funciona mal, algunos mecanismo son, incremento en los niveles de receptores CB, disminución de la enzimas encargadas de degradar estos endocannabinoides, mayores niveles de AEA. Estos desordenes causan interés pues podrían estar involucrados en el proceso de carcinogénesis, algunos estudios que publican estas alteraciones se muestran en la tabla 2.
Por lo tanto, justificamos esta revisión, pues como ya está descrito, este sistema se encuentra encargado de manejar distintos mecanismos de señalización celular. Por mencionar las vías MAPK, CdC2, JunD, proteínas que se sabe tienen un efecto oncogénico a la hora de verse alteradas en células cancerígenas, entre muchas otras descritas en la literatura.
Lo que sabemos de la nueva terapia antitumoral con cannabinoides
Desde que se logró clonar y estudiar a los receptores CB, un exponencial número de estudios y experimentos comenzaron a dilucidar este nuevo SEC y su función como regulador homeostático. El tratamiento de la náusea, el vómito, la falta de apetito, la pérdida de peso y el dolor que las terapias antitumorales provocan en los pacientes, fueron las primeras ideas en revelar que el Cannabis y sus derivados podrían tener un verdadero efecto terapéutico14. Claro está, que la constante estigmatización de la sustancia Cannabis, ha impedido que se utilice en la práctica clínica, pero la ciencia cambia y evoluciona, así también, el concepto arraigado del Cannabis como una sustancia puramente destructiva. Tiempo pasó hasta que los científicos comenzaron a tratar cultivos celulares con cannabinoides y pudieron notar una disminución en el crecimiento tumoral, estamos hablando de Munson et al.15, que en 1975 demostró en ratas con implantación de carcinoma de pulmón humano, un retraso en el crecimiento tumoral tras la aplicación de distintos cannabinoides.
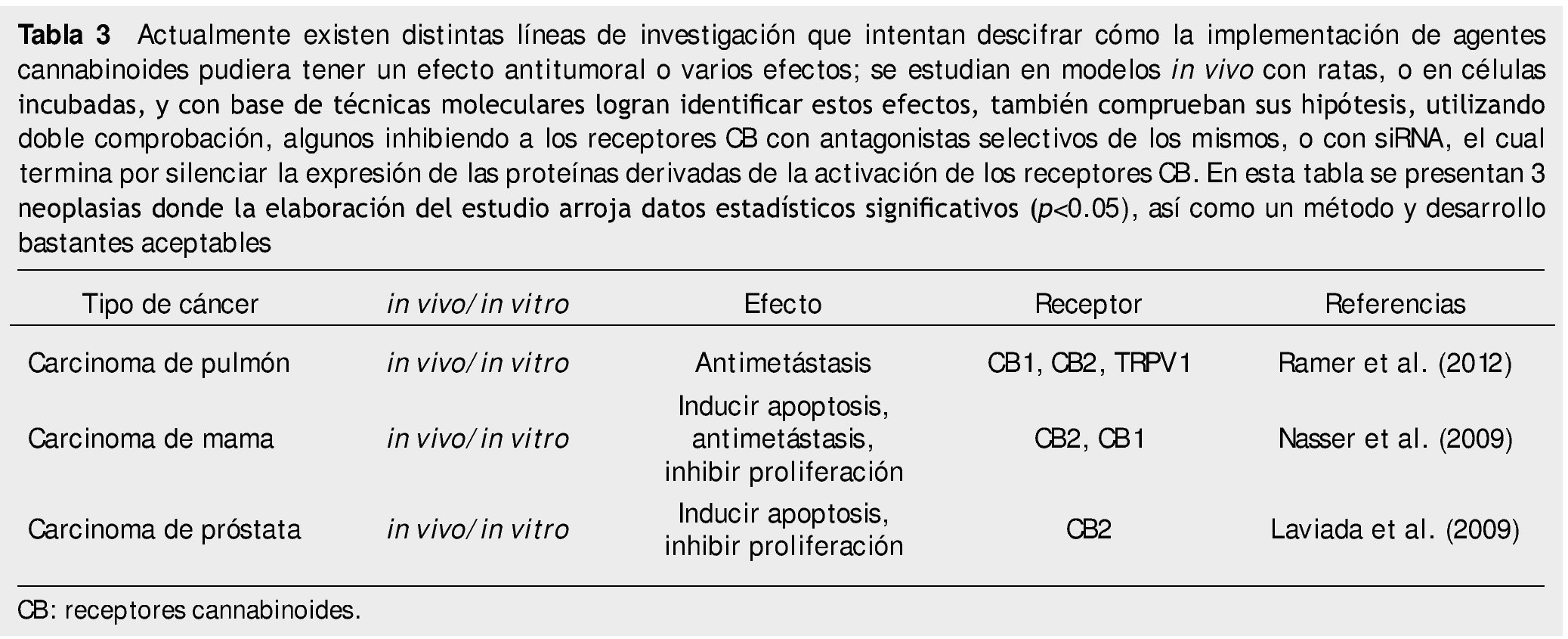
Pasó tiempo para que se realizará una nueva línea de investigación a nivel mundial, la cual estamos presenciando en la actualidad. En la tabla 3 están algunas neoplasias que ya está comprobado son sensibles a la utilización de cannabinoides como verdaderos fármacos antitumorales, estos realizados en cultivos celulares o ratas experimentales9,16, cabe decir que existen muchos estudios que investigan otros tipos de neoplasias, como leucemia, melanoma, glioma, colorrectal, hepatocarcinoma, páncreas, etc.
Entonces, ¿podrían o no los cannabinoides ser implementados como una nueva terapia antitumoral en la práctica clínica?, los estudios que avalan sus efectos antitumorales son bastantes, todos se basan en células cultivadas in vitro o in vivo en modelos murínicos; en sus conclusiones los autores sugieren como una constante, comprobar la eficacia de estos mecanismos antitumorales en estudios clínicos controlados. Quizá una de las razones por las que aún no vemos estos fármacos en la clínica, es por el intento de dilucidar los mecanismos moleculares que promueven la apoptosis, el arresto en fase de mitosis G0, inhibición de la angiogénesis y la posibilidad de la célula de hacer metástasis.
Esta información es necesaria para justificar el uso de componentes derivados de la Cannabis sativa en la clínica, así como aclarar los posibles efectos psicoactivos no deseados en los pacientes.
Visionariamente, realizaron en España17, el único estudio clínico con Δ9-THC que existe actualmente, en el 2006 consiguieron reclutar 9 pacientes con glioblastoma multiforme, un tumor cerebral muy agresivo y con pobre pronóstico de sobrevida en etapas avanzadas. Cabe decir que estos pacientes tenían un pronóstico menor a un año de vida, el estudio intento comprobar la reducción en el tamaño tumoral, después de realizar una resección en bloque del mismo tumor. Inyectaron THC intracranealmente, en varios ciclos con incrementos paulatinos en la dosis (10 μg-100 μg), para observar cómo controlaban el tamaño del tumor, los efectos adversos y la tolerancia a la sustancia, éstos fueron bien recibidos. Desafortunadamente, la muestra implicaba que los pacientes se encontraban en estado terminal y tenían un máximo de sobrevida de 24 semanas, 2 pacientes lograron sobrevivir hasta un año, si bien, no se obtuvieron resultados totalmente positivos, 2 pacientes por medio de resonancia magnética demostraron una regresión en el tamaño del tumor. El autor sugiere realizar nuevos estudios clínicos basados en la evidencia actual que se tiene respecto a los efectos antitumorales en otro tipo de neoplasias de reciente diagnóstico, instalar un estudio controlado con un abordaje y tratamiento distinto podrían bien demostrar datos más positivos.
Éste fue entonces, el primer estudio clínico con base en cannabinoides. Las distintas líneas de investigación en modelos murínicos, son el pivote para demostrar la eficacia de estas sustancias como agentes terapéuticos, los cultivos celulares con células cancerígenas son la herramienta para dilucidar los mecanismos moleculares en cuanto a la activación de los CB.
En este contexto, Petrocellis et al. 201218, utilizó células de carcinoma de próstata Lapa y 22RV (receptor andrógeno positivo) y DU-145 y PC-3 (receptor andrógeno negativo), en modelos in vitro e in vivo, para comprobar los efectos antitumorales previamente mencionados.
Cabe destacar que utilizaron distintos compuestos cannabinoides, excluyendo el THC, pues como ya mencionamos anteriormente, el THC tiene un fuerte agonismo por los CB1, los encargados de modular los efectos psicoactivos no deseados en esta terapia, por lo tanto utilizaron en mayor parte cannabidiol (CBD), un cannabinoide no psicoactivo. La relevancia de este estudio es que en sus modelos in vivo, usaron una terapia sinérgica con docetaxel, un quimioterapéutico antimitosis, aprobado por la FDA para el tratamiento de distintas neoplasias, como el cáncer de próstata. A su vez, un grupo de ratas fue tratado con un medicamento antiandrogénico que tiene especificidad por el receptor androgénico de las células de próstata, la bicalutamida.
Este estudio arrojó información que descifra distintos mecanismo antiproliferativos independientes del agonismo de CB, en dicho estudio encontraron un nuevo receptor encargado en la viabilidad de la célula de próstata, el TRPM819, un canal iónico que permite la entrada de Ca++ en la célula, necesario para generar mitosis. El CBD conseguía antagonizar y disminuir la expresión de este receptor. Se comprobó un aumento sinérgico en el grupo de ratas con Lapa tratadas con bicalutamida, es decir, el efecto de este fármaco se vio potenciado con el CBD. Concretamente, el tiempo de vida de este grupo de ratas fue mayor. Los autores concluyen que la terapia con cannabinoides no-THC tiene un importante efecto en la viabilidad de la célula, sobre todo porque induce la apoptosis (comprobado por ensayo TUNEL), así como promover el arresto de fase G1-S de la mitosis.
Es importante mencionar, que no todos los efectos antitumorales con la terapia cannabinoide son dependientes del agonismo de los CB y las distintas vías de señalización que regulan. Partiendo del descubrimiento del antagonismo del TRPM8, podemos concluir que existen otros mecanismos por los cuales los cannabinoides tienen un potencial antitumoral.
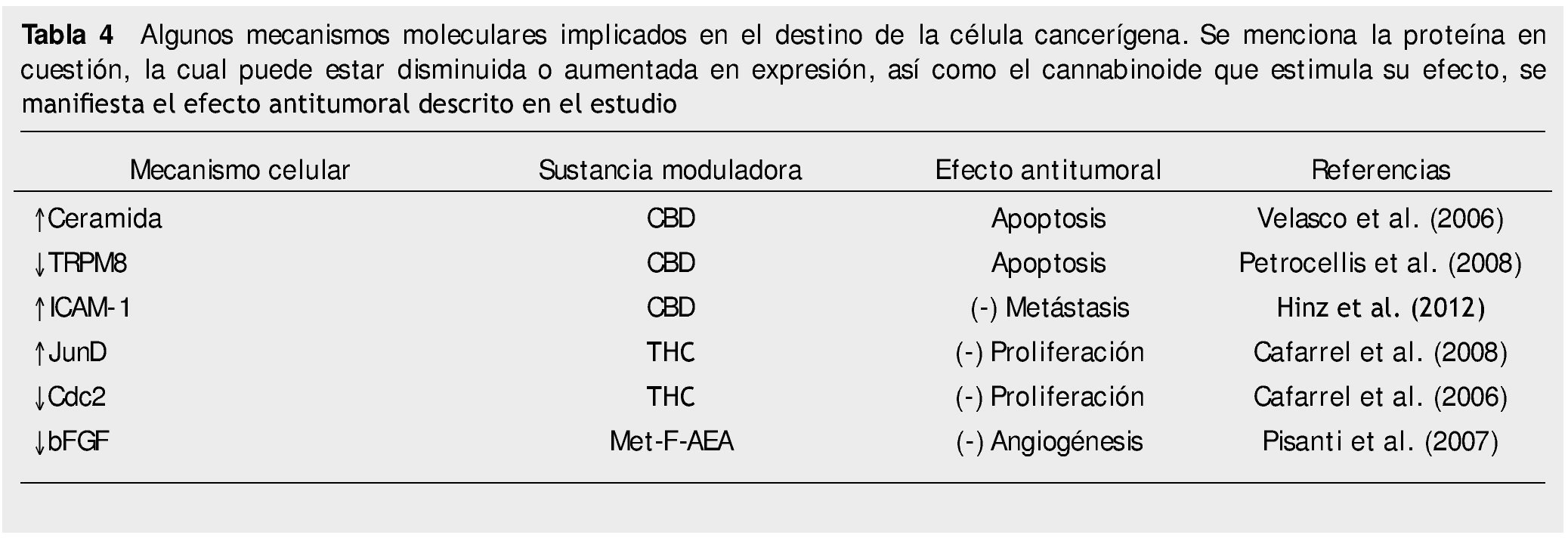
Por último, resumimos algunos mecanismos moleculares por los cuales la terapia con cannabinoides demuestra distintos efectos antitumorales20-22 (tabla 4).
Efectos adversos de la terapia antitumoral con cannabinoides
Pues bien, hasta ahora hemos descrito sólo algunos de los estudios más alentadores de esta nueva terapia antitumoral, sin embargo, otros estudios advierten sobre otros efectos no antitumorales, sino proliferativos23. Este estudio manifiesta el riesgo de sobreexpresión del HER-2 en las células con cáncer de mama, aclarando que su linaje celular no presentaba ninguna expresión de CB. Otro estudio manifiesta la inhibición de muerte celular24, este análisis descubrió un agonismo independiente de CB, asociado al receptor ligando de capsaicina, TRPV1, el cual promueve la aparición del receptor androgénico en células con cáncer de próstata, promoviendo su viabilidad.
Sin embargo, el error puede estar en la planificación del estudio, pues existe controversia a la hora de analizar las dosis de cannabinoide que utilizan, el tipo de linaje celular o al momento de realizar la comprobación por distintos métodos moleculares. De igual forma, esta terapia sigue teniendo un impacto científico muy importante, pues estamos ante la situación de que estos receptores CB, al final de cuentas, modulan el destino final de la célula.
Otro aspecto fundamental a tratar, es el efecto psicoactivo que tienen los cannabinoides en humanos25. Estos compuesto ejercen una variedad única de efectos excitatorios e inhibitorios en el sistema nervioso central, que pueden ser divididos en 4 grupos: afectivos, sensoriales, somáticos y cognitivos. Puesto que la localización de los receptores en el cuerpo humano es muy amplia, los cannabinoides pueden no sólo afectar al sistema nervioso central, sino también cualquier otro aparato o sistema de la economía, taquicardia, broncodilatación, relajación muscular e hipomotilidad intestinal, pudiendo constituir otro efecto de los cannabinoides.
Estos resultados pueden ser evidentes en aquellos fumadores recreativos de "marihuana", sin embargo, esto no implica que en estudios clínicos se presenten. De facto, un estudio26 donde se querían evitar los eventos de vómito y náusea, en pacientes que en el momento se encontraban bajo tratamiento con quimioterapia por presentar tumores sólidos, valoró los efectos de la aplicación de Sativex®vs. Ilacebo y midieron los efectos adversos, así como el control del vómito y la náusea durante 4 días, los resultados no demostraron ningún efecto adverso grave, más que los mencionados previamente. Resultaría benéfico implementar terapias con cannabinoides, teóricamente, uno estaría aminorando los efectos adversos de la quimioterapia y la radioterapia, como el dolor, la falta de apetito y la náusea, y a su vez tratando la patología de base. Por otro lado, la tolerancia generada ante estos efectos se genera muy rápido en humanos y animales, ya que el SEC se ve sensibilizado por el agonismo continuo, disminuyendo la expresión de los CB a nivel del sistema nervioso central.
Los cannabinoides son compuesto altamente liposolubles, por lo que sus metabolitos tienden a depositarse en el tejido adiposo y los niveles en plasma de cannabinoide permanecen durante al menos 2 meses tras retirar la sustancia, esto le confiere pocos síntomas de abstinencia, comparada con otras sustancias, que una vez es retirada del sistema, este mismo se ve afectado por la ausencia de la sustancia y genera síntomas.
En general, se cree que los cannabinoides como agentes terapéuticos, realmente son sustancias bastante seguras, ya que inclusive éstas no presentan toxicidad por las células normales del cuerpo, a comparación de su efecto antiproliferativo en células cancerígenas11.
La sugerencia es implementar verdaderos modelos clínicos controlados donde se evalúen los efectos adversos que podrían presentar los pacientes con terapia cannabinoide.
Conclusiones
El objetivo de esta revisión sigue siendo informar del avance científico que se tiene hasta la fecha del SEC y su importancia como regulador de muchas funciones fisiológicas en el ser humano, así como compartir datos precisos del panorama que se tiene como posible futura terapia antitumoral, esto justificado por la literatura y los estudios que informan sobre los mecanismos moleculares implicados en este efecto y donde sugieren la implementación de estudios clínicos controlados en pacientes que sufren de cáncer, para poder corroborar lo demostrado en modelos in vivo e in vitro.
No cabe duda que las terapias actuales basadas en ciclos de quimioterapia y radiación forman parte del tratamiento esencial en el cáncer, sin embargo, creemos que implementar terapias sinérgicas con agentes farmacológicos no psicotrópicos derivados de extractos de la Cannabis sativa y estas otras herramientas terapéuticas, podrían ser el nuevo abordaje terapéutico, uno que podría cambiar la evolución del cáncer, ofreciéndole a los pacientes un tratamiento más completo y esperanzador.
Conflictos de interés
Este trabajo fue presentado en las XXXVIII Jornadas Médicas Lasallistas, en la convocatoria de Trabajos Libres, realizadas en la Facultad Mexicana de Medicina de la Universidad La Salle, realizadas del 6 al 8 de marzo del 2014, el cual fue premiado con el primer lugar. No existió alguna relación económica o de otra naturaleza que afectara la realización de este artículo.
Financiamiento
Los autores no recibieron patrocinio para llevar a cabo este artículo.
* Autor para correspondencia:
Facultad Mexicana de Medicina, Universidad La Salle.
Fuentes N° 17 (esq. Av. San Fernando), Colonia Tlalpan,
Delegación Tlalpan, C.P. 14000, México D.F., México.
Teléfono: (55) 5914 9162. Celular: (664) 4061047.
Correo electrónico: zuniga_mario@live. Iom (Mario Zúñiga-Ayala).