Introducción: Los sarcomas de partes blandas de la pared abdominal y/o torácica para su resección tridimensional producen grandes defectos, su reconstrucción representa un reto. Para esto se ha utilizados colgajos locales de piel, mallas sintéticas o ambas, sin embargo sus complicaciones asociadas han limitado su éxito. Para evitar ese problema, el uso del colgajo pediculado de epiplón (omento) por su plasticidad, capacidad angiogénica, inmunológica y de reparación tisular, se ha utilizado como una alternativa segura y baja tasa de morbilidad.
Objetivo: Presentar nuestro abordaje quirúrgico de reconstrucción en sarcomas de partes blandas de pared abdominal, recidivantes a cirugía y radioterapia que condicionen grandes defectos en la misma, mediante la combinación de material sintético (malla) y el omento, como un colgajo pediculado interpuesto sobre la malla y el defecto propiamente dicho.
Conclusión: El colgajo pediculado de epiplón es una opción segura, por sus condiciones intrínsecas (plasticidad, angiogénesis, entre otras) cubre grandes defectos de pared, con una baja tasa de morbilidad y resultado estético adecuado.
Introduction: Tridimensional resection of soft tissue sarcomas from abdominal and chest wall led to large full thickness defects and represents a challenger for surgeons, several synthetic materials as Gore-Tex and local flaps skin has been used. However his limited successful is associated with complications, to avoid such problems, we use the omentum flap because have unique immunological and angiogenic properties and is well vascularized to facilitate wound healing and represent a safe alternative with low rate complications
Objective: To present our reconstruction surgical approach for recurrent soft tissue sarcomas from abdominal and chest wall that resection demand cover broad defects and we presents the combination use of Gore Tex mesh and omentum flap.
Conclusions: The combined use of Gore Tex mesh and omentum flap is safe and is possible cover broad of the abdominal and chest defects with low morbidity and acceptable static results.
¿ INTRODUCCIÓN
La reconstrucción de los defectos totales de la pared abdominal y/o torácica, por tumores (sarcomas y/o carcinomas metastásicos) de partes blandas de estas regiones, representan un reto para su reconstrucción.1-3 Debido a resecciones tridimensionales amplias, el uso de radioterapia previa,4 la poca elasticidad del tejido en esta área y la falta de tejido músculo-esquelético viable en la proximidad de estos defectos, ha fomentado el uso de materiales sintéticos, tales como Gore Tex (politetrafluoroetileno expandido). No obstante, las complicaciones tales como seroma, infección y extrusión están asociadas con estos materiales. Estas se incrementan en situaciones quirúrgicas, donde la falta de piel condiciona un cierre tenso, con un aumento en la morbilidad. Se sabe que para disminuir estas complicaciones, el recubrimiento del material sintético con un tejido blando bien vascularizado (omento), es vital para facilitar la cicatrización y prevenir la exposición del material sintético y permitir un adecuado cierre. El epiplón es conocido como el "policía del abdomen", un agente protector que se mueve alrededor de la cavidad peritoneal hacia las áreas donde "se está fraguando el delito".5 Ha sido reconocido como un órgano propio, con capacidad para atenuar la diseminación de la peritonitis, hasta ser fuente de factores angiogénicos y hemostáticos, involucrados en la reparación y curación tisular.6-9
El propósito de este artículo es presentar nuestro abordaje, usando una combinación de material sintético (malla) y el omento, como un colgajo pediculado interpuesto sobre la malla y el defecto propiamente dicho.
¿ HISTORIA, ANATOMÍA Y EMBRIOLOGÍA DEL OMENTO MAYOR (EPIPLÓN MAYOR)
El reconocimiento del epiplón mayor data desde los tiempos egipcios y fue llamado el gran epiplón por Aristóteles.10,11 Se origina embriológicamente del mesogastrio dorsal, y está divido anatómicamente en el epiplón mayor y menor. El epiplón mayor es una doble capa de peritoneo que desciende desde la curvatura mayor del estómago, recubre el intestino delgado y luego se dobla sobre sí mismo, para fusionarse con el peritoneo de la cara anterior del colon transverso. El epiplón menor se extiende entre el hígado y la curvatura menor del estomago formando el limite anterior de la bursa omentalis.12
El omento es un tejido altamente vascularizado, que fisiológicamente resiste muy bien a los procesos infecciosos y se adapta fácilmente a ambientes isquémicos, atribuibles al uso de radioterapia. Es una capa doble de peritoneo que cuelga de la curvatura mayor del estómago con dimensiones de 25 cm de largo en el hombre y 24 cm en la mujer, por 35 cm de ancho. Su vascularización depende de las arterias gastroepiploicas derecha e izquierda, dentro del epiplón propiamente se dividen en cuatro arcos principales: 1) arteria omental derecha, 2) arterial omental izquierda, 3) arteria omental media y 4) arterial omental accesoria (Figura 1). Aunque presenta cinco variaciones descritas por Alday y Goldsmith en 246 disecciones, la importancia de estas variantes es que podrían limitar la plasticidad de dicho tejido, ellas son: Tipo I (81.7%), existe una bifurcación de la arteria omental media en su tercio inferior. Tipo II (11%), existe una bifurcación arteria omental media en su tercio medio antes que se anastomose con los arcos derecho e izquierdo. Tipo III (4.5%), existe una bifurcación de la arteria omental media en su tercio superior en dos o tres ramas. Tipo IV (1.2%), ausencia de la arteria omental media y reemplazada por varios vasos omentales cortos. Tipo V (1.6%), la arteria omental izquierda no se une a la arteria gastroepiploica izquierda, aunque la derecha y la media si se unen a las arcadas principales.13
Figura 1. Anatomía del Omento Mayor: arteria omental derecha, izquierda y media.
El epiplón (omento) consiste en dos capas mesoteliales que encierran adipocitos y tejido conectivo laxo, con el agregado de células mononucleares fagocíticas.14, 15
Microscópicamente, la región adiposa es el hogar de las así llamadas manchas lácteas o taches laiteuses descritas por Ranvier, su función es la de depurar bacterias y es un sitio para la proliferación y maduración de macrófagos y células.16, 17
¿ TÉCNICA QUIRÚRGICA
Preoperatoriamente identificar cirugías abdominales previas del paciente, en donde el uso o resección del omento haya sido realizado, y por obvias razones limitar el uso del colgajo.18
1. Resección del tumor primario con los márgenes y principios oncológicos correspondientes.
2. La reconstrucción se debe adaptar al margen y tamaño tumoral, no a la conveniencia del cirujano. Iniciando con la medición del defecto con regla, identificar el omento mayor y su vascularización, a través del mismo defecto o de una incisión diferente.
3. Movilización del omento mayor, se realiza hacia el defecto de pared a reparar, conservando siempre al menos uno de los cuatro arcos principales. El omento mayor debe salir al exterior, a través de un orificio en la malla y se extenderá sobre ésta, cubriendo completamente la misma.
4. La colocación de la malla se realiza una vez que ya se movilizó y se verificó que el omento mayor cubre adecuadamente el defecto quirúrgico, la malla se fija de manera convencional a la aponeurosis y/o se fija mediante taladro al hueso (costillas, esternón, cresta ilíaca), para una mayor sujeción.
5. El cierre de estos defectos casi siempre implica la toma aplicación-injerto (TAI), debido a la resección amplia que incluye la piel, sobre el omento mayor que por su alta vascularización, asegura un éxito del 100% en su integración y cicatrización.19, 20
¿ CASO CLÍNICO
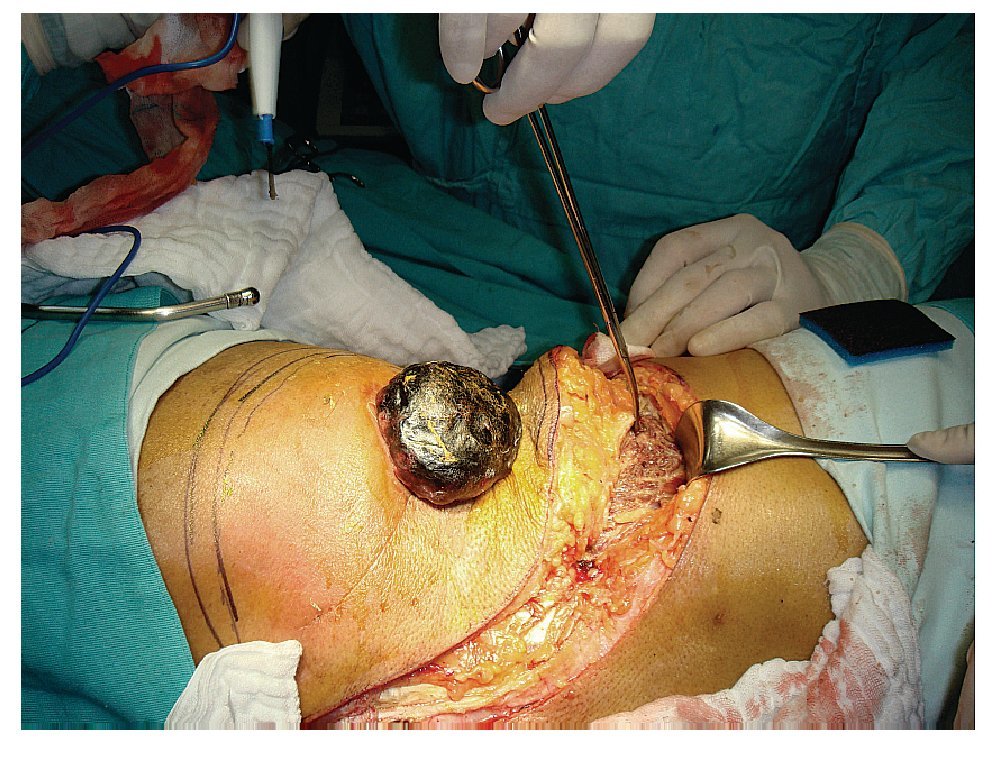
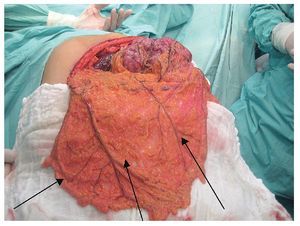
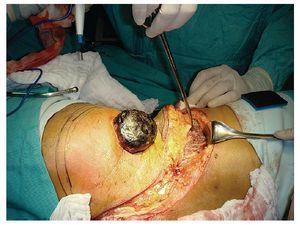
Masculino de 78 años de edad, hipertenso bien controlado, con diagnóstico de sarcoma (histiocitoma fibroso maligno) de pared abdominal, presente en el lado derecho, de cinco cm de diámetro, tratado inicialmente con resección quirúrgica amplia bajo cierre primario y radioterapia (60 Gy), en agosto del 2007. Posteriormente presenta recurrencia en enero del 2008, tratada nuevamente con resección amplia y material sintético. Para julio del mismo año, presenta nueva recurrencia local y tres nódulos tumorales (Figura 2) y sin datos de enfermedad a distancia. Se propone al paciente, resección de toda la pared lateral derecha abdominal, incluyendo su pared costal (dos costillas) y la resección parcial de la cresta ilíaca anterosuperior, por lo difuso de las lesiones tumorales.
Figura 2. Sarcoma recurrente de tejidos blandos en la pared lateral derecha abdominal.
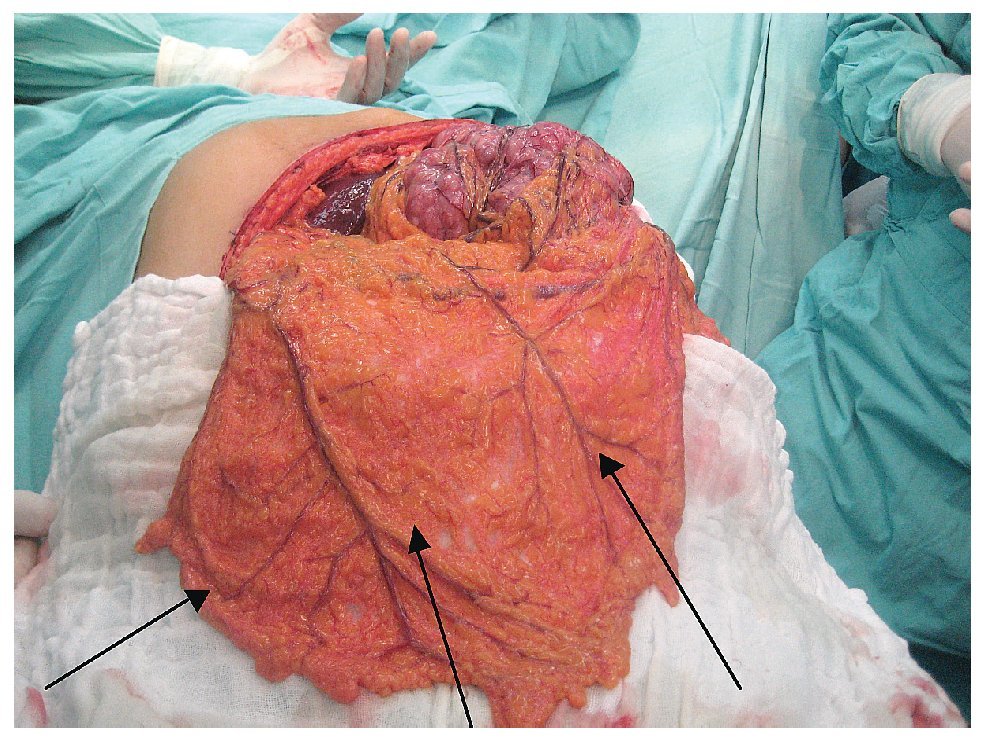
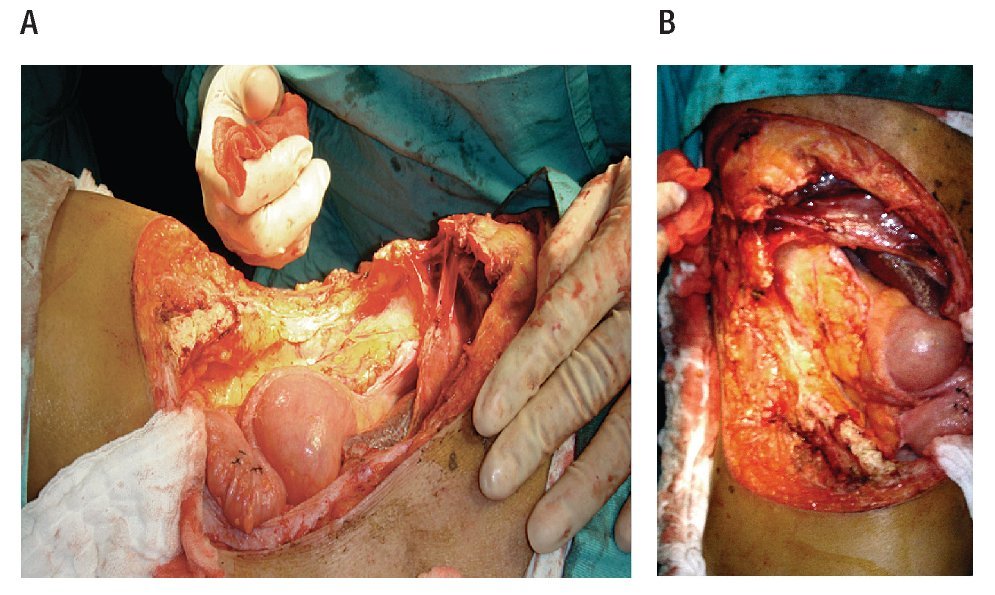
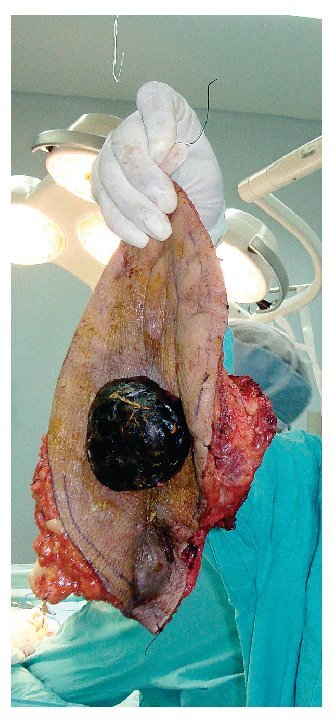
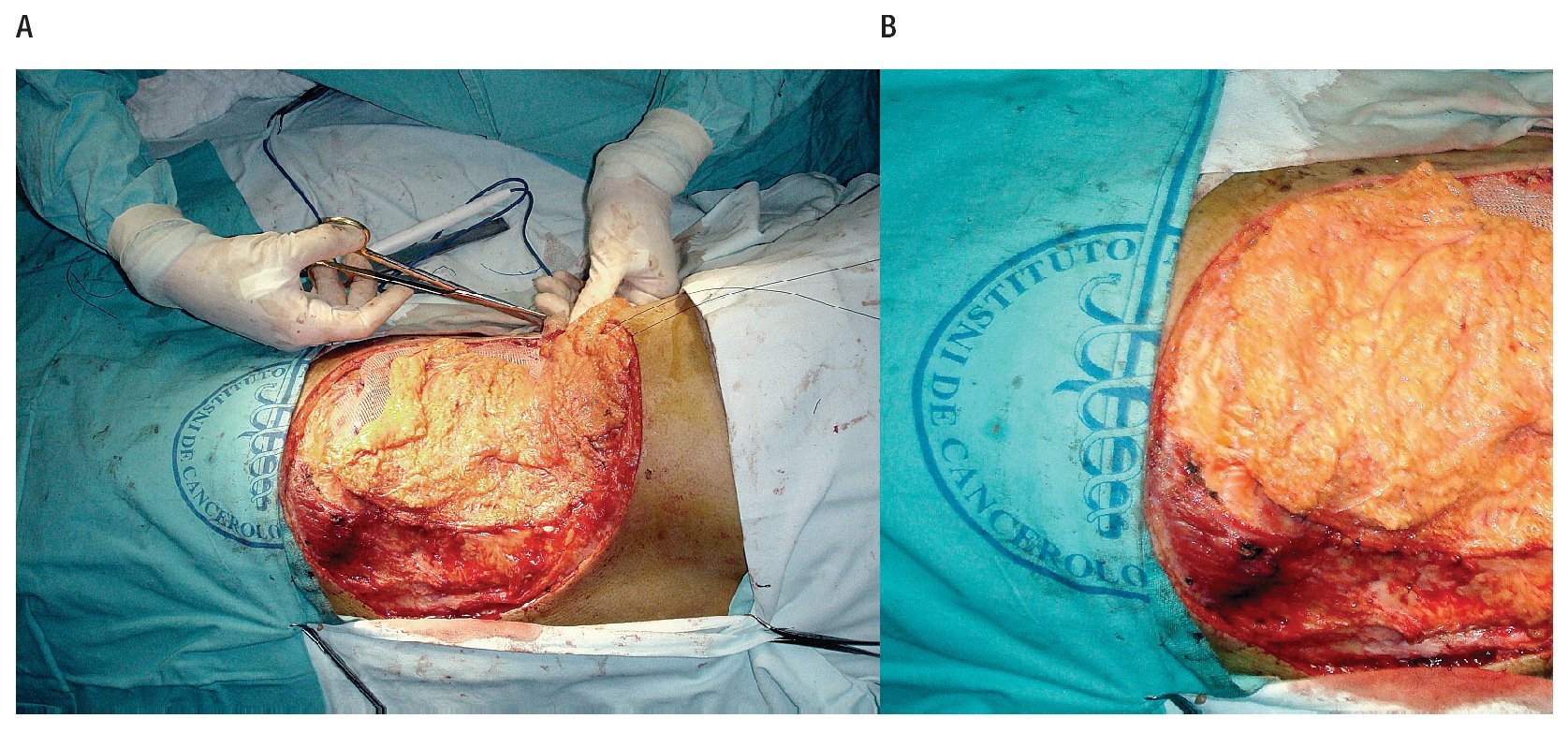
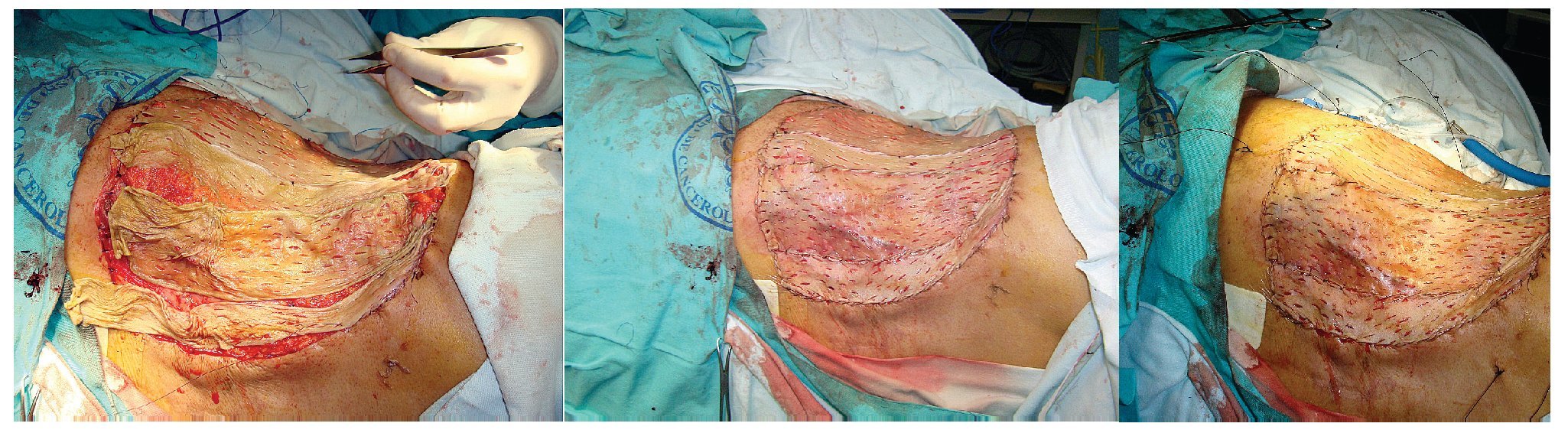
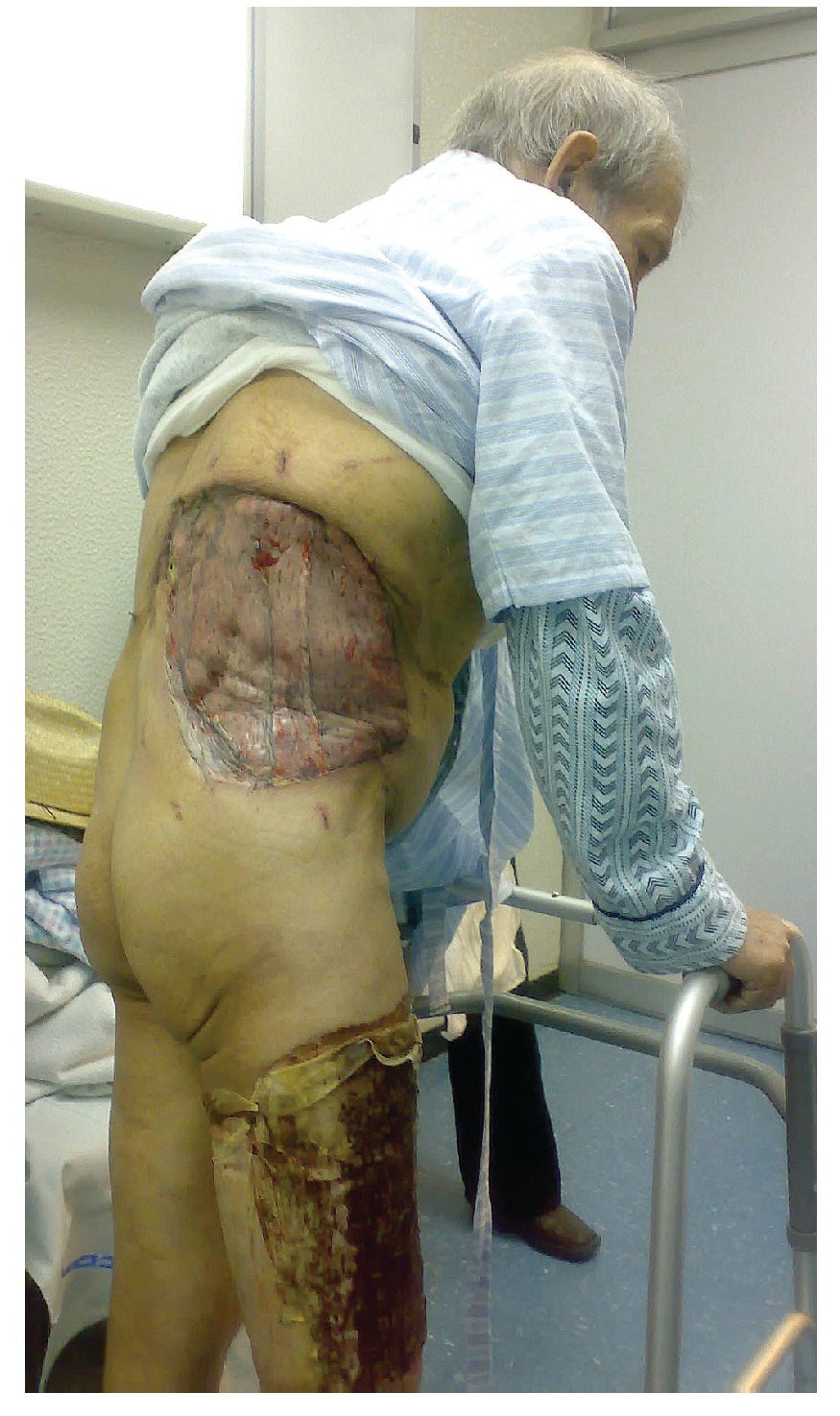
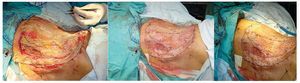
Se realizó la resección amplia tridimensional, resecando en bloque toda la pared abdominal derecha, exponiendo la cavidad abdominal y el retroperitoneo, dejando un defecto quirúrgico de 30 cm por 28 cm (Figura 3). Se envía la pieza quirúrgica a patología para estudio transoperatorio (Figura 4). Se reconstruye mediante el cierre primario del peritoneo, previa movilización del epiplón mayor identificando su irrigación y seccionado la arteria omental izquierda. Para su desplazamiento hacia la pared abdominal del lado derecho, se exterioriza sobre una malla de Gore Tex de 30 por 30 cm, mediante una apertura de tres cm en la parte más proximal de la malla, extendiendo y cubriendo en su totalidad el material sintético (Figuras 5 y 6). El defecto de piel se cubrió con injerto de espesor total de piel, más un tie over por cinco días. Se descubre el injerto al sexto día con una integración del 100%, presentando un evolución al mes y dos meses sin complicaciones, con una integración del injerto de 95% (Figura 7).
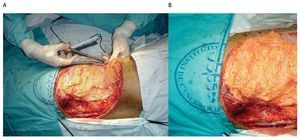
Figura 3. Resección de la pared lateral del abdomen: dos arcos costales, parte de cresta iliaca A), exposición del abdomen y retroperitoneo B).
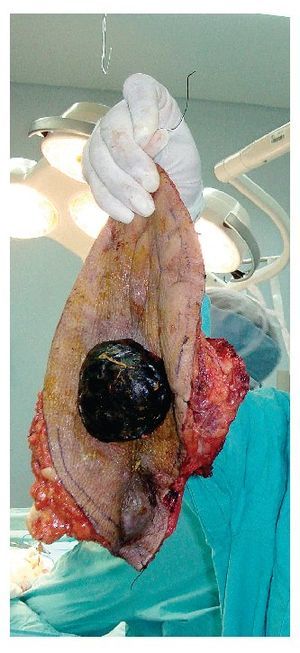
Figura 4. Pieza quirúrgica: Sarcoma de pared toracoabdominal resecado.
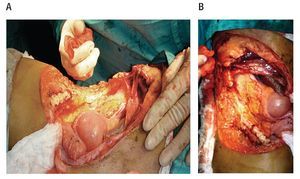
Figura 5. Movilización del omento mayor hacia el defecto de pared A) y su exteriorización a través de la malla B).
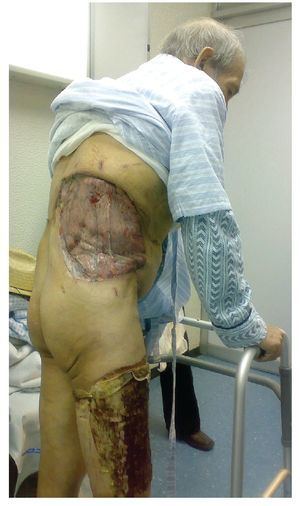
Figura 6. Toma y aplicación de injerto de piel de muslo hacia el defecto ya cubierto con malla y omento mayor
Figura 7. Injerto integrado al 100%, postoperatorio tardío (1 mes).
¿ DISCUSIÓN
Los defectos de la pared abdominal que resultan de la resección de tumores, son por lo general de difícil resolución, especialmente si estos son de espesor total e incluyen el peritoneo.21 El omento (epiplón) mayor debido a sus propiedades inmunológicas y angiogénicas es único en la economía del cuerpo humano, debido a su rica vascularización y plasticidad, su uso facilita el cierre de grandes defectos y promueva la integración del tejido blando al material protésico (malla).22 Además el colgajo pediculado de epiplón, alcanza a cubrir cuadrantes completos de la pared abdominal como en este paciente y cuando se necesita avanzar más el colgajo, el omento mayor se diseca del colon transverso y se rota al sitio deseado manteniendo su irrigación, mediante uno o ambos vasos gastroepiploicos.23,24 Otro punto importante es la selección del sitio por donde saldrá el colgajo de epiplón, para ser lo suficientemente justo, al evitar isquemizar el pedículo y prevenir la formación de hernia de la pared abdominal.25
Las ventajas del uso del omento en la reconstrucción, no sólo se reservan para cubrir grandes áreas de pared abdominal, sino también áreas o zonas que recibieron radioterapia o pacientes inmunocomprometidos (diabetes, cáncer, entre otros). Por tal motivo, las contraindicaciones sólo se limitan a procedimientos en los cuales, se halla resecado el epiplón previamente.26,27
El caso presentado consistía en un extenso defecto lateral de la pared abdominal, de espesor total de 30 cm Aproximadamente. Posterior a su resección, aislamiento del contenido abdominal y rotación del epiplón mayor hacia el defecto, simultáneamente una malla de polite-trafluoroetileno fue colocada sobre el defecto, fijada a los bordes del mismo para exponer el epiplón a través de la malla, para seguidamente extenderla sobre su superficie y finalmente colocar injertos de piel de espesor total. El paciente con una evolución buena y mínima morbilidad.
Correspondencia: Dr. Sergio Vásquez Ciriaco.
Cirujano Oncólogo. Calle Boulevard José Vasconcelos 208 b, Colonia América Sur, CP 68050, Oaxaca, Oaxaca.
Teléfono: 951 226 1993.
Correo electrónico:sergiovc10@hotmail.com