Se presenta el caso de un receptor de un trasplante hepático con la indicación de cirrosis hepática alcohólica y carcinoma hepatocelular en estadio inicial que presentó un rechazo celular agudo resistente a los corticoides demostrado por biopsia a los 3 meses del trasplante. Tras la ausencia de mejora analítica o histológica con 6-metil-prednisolona intravenosa y la conversión del régimen inmunosupresor a tacrolimus y micofenolato mofetil, se administraron 2 dosis de basiliximab intravenoso separadas por 4 días, asistiendo a la normalización clínica, analítica e histológica. No se detectaron episodios adversos relacionados con el tratamiento con basiliximab. El basiliximab puede representar una opción terapéutica en el rechazo celular agudo resistente a los corticoides tras el trasplante hepático, sin que se hayan observado infecciones, neoplasias ni otros efectos adversos potencialmente relacionados en este caso.
We present the case of a liver transplant recipient with alcoholic liver cirrhosis and early-stage hepatocellular carcinoma who developed biopsy-proven acute steroid-resistant rejection 3 months after liver transplantation. After the failure of immunosuppressive therapy with intravenous boluses of 6-methyl-prednisolone and switching of the immunosuppressive regimen to tacrolimus plus mycophenolate mofetil, two doses of intravenous basiliximab were administered four days apart. Clinical, analytical, and biopsy-proven histological response was complete. No basiliximab-related adverse events were detected. Basiliximab may represent an alternative in liver transplantation immunosuppression to treat acute steroid-resistant rejection, without increasing the incidence of infections, neoplasms, or other adverse events, as shown by this case.
El trasplante hepático constituye un tratamiento ampliamente consolidado en enfermedades hepáticas terminales agudas y crónicas de diferentes etiologías. La inmunosupresión en el trasplante de órganos sólidos continúa basándose en los inhibidores de la calcineurina (tacrolimus y ciclosporina) en asociación con corticoides1. A pesar de los recientes avances experimentados en la terapia inmunosupresora, el rechazo celular agudo continúa siendo una complicación frecuente en el período postrasplante. Los corticoides por vía intravenosa en altas dosis son el tratamiento de elección en el rechazo celular agudo. Sin embargo, el tratamiento del rechazo celular agudo resistente a los corticoides no ha sido todavía establecido. El objetivo de este artículo es comunicar la experiencia con el uso de basiliximab (Simulect®, Novartis Farmacéutica), un anticuerpo monoclonal quimérico dirigido contra la cadena alfa del receptor de la interleucina 2, en el tratamiento de un caso de rechazo celular agudo resistente a los corticoides tras un trasplante hepático.
Observación clínicaSe presenta el caso de un varón de 56 años que recibió un trasplante hepático con injerto de donante isogrupo en julio de 2006. Fue indicado tras el diagnóstico no invasivo de un carcinoma hepatocelular uninodular de 24mm injertado sobre una cirrosis hepática alcohólica con hipertensión portal clínicamente significativa y disfunción hepatocelular en grado moderado (8 puntos en la clasificación de Child-Pugh). La inmunosupresión de inducción se realizó con tacrolimus y corticoides (6-metil-prednisolona intravenosa y, posteriormente, deflazacort oral). En el período post-operatorio inmediato, el inhibidor de la calcineurina fue convertido a ciclosporina debido a un cuadro de neurotoxicidad atribuido a tacrolimus. A los 3 meses del trasplante el receptor presentó una elevación marcada de las transaminasas y enzimas de colestasis. Ello coincidió con un descenso brusco hasta valores infraterapéuticos de ciclosporina en probable relación con un fallo de adherencia al tratamiento. Una ecografía abdominal con Doppler no reveló lesiones vasculares ni anomalías en las vías biliares. Se realizó una biopsia hepática percutánea que mostró la presencia de un infiltrado inflamatorio en la mayoría de los espacios porta, ductos y vénulas portales compatibles con un rechazo celular agudo de grado II en la clasificación de Banff. Se inició terapia con altas dosis de corticoides por vía intravenosa (6-metil-prednisolona en dosis de 500mg una vez al día durante 3 días con reciclaje posterior) asociadas a un incremento en la dosis de ciclosporina. La terapia inmunosupresora fue posteriormente reconvertida a tacrolimus y micofenolato-mofetil al persistir, e incluso empeorar las alteraciones analíticas. Una semana después se realizó una segunda biopsia debido a la nula mejoría clínica y analítica, que mostró la persistencia de un rechazo celular agudo de grado II en la clasificación de Banff.
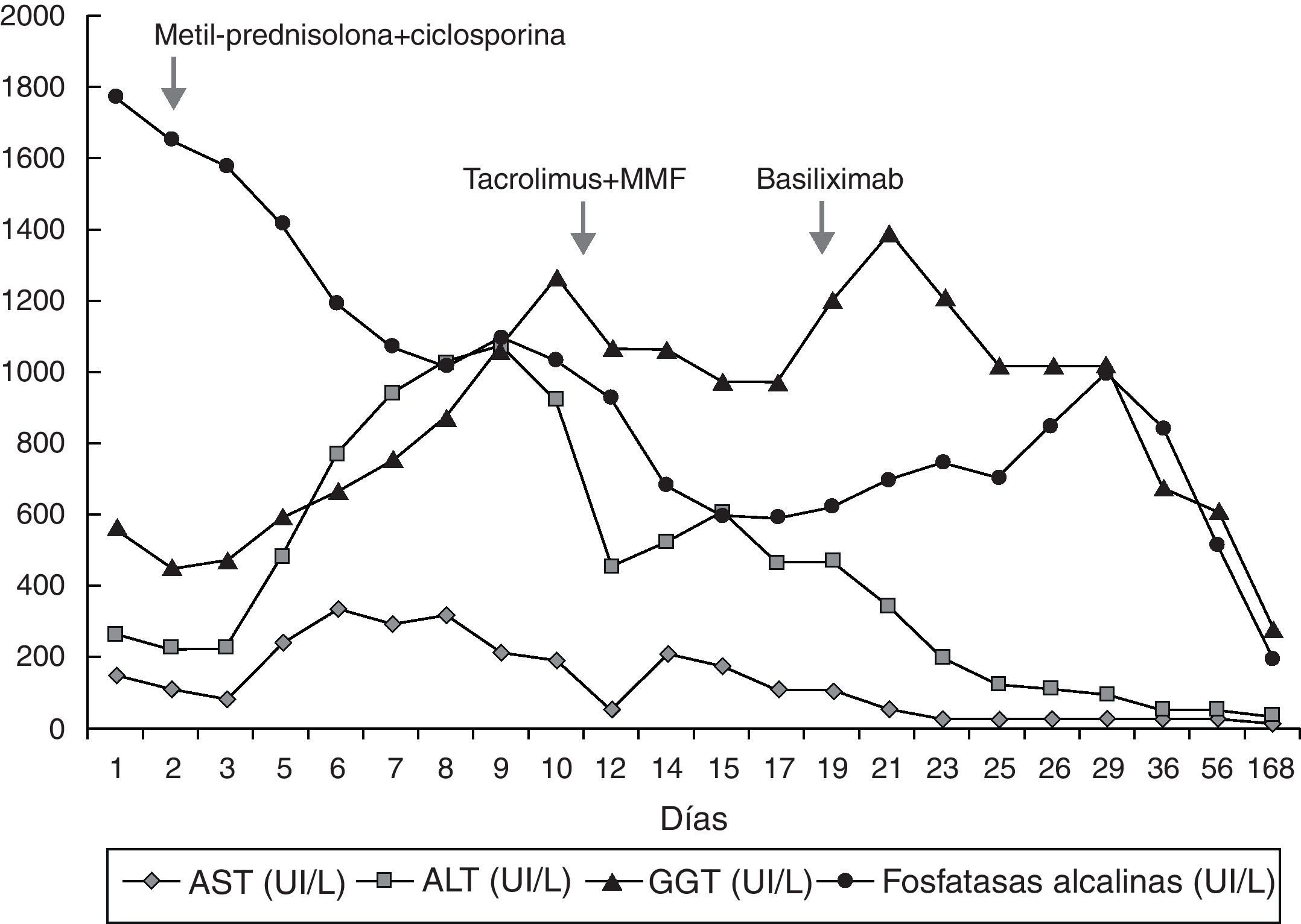
Con el diagnóstico de rechazo celular agudo resistente a los corticoides, se administraron 2 dosis de basiliximab de 20mg por vía intravenosa separadas por 4 días. Este tratamiento se siguió de la mejora progresiva y finalmente la normalización de los parámetros bioquímicos hepáticos, sin detectarse complicaciones potencialmente relacionadas con el mismo. Una tercera biopsia hepática realizada 6 meses después del alta mostró una histología del injerto prácticamente normal. El paciente permanece asintomático y con función del injerto conservada desde entonces. La evolución de los parámetros bioquímicos hepáticos del receptor y las intervenciones terapéuticas se muestran en la figura 1.
DiscusiónEl trasplante hepático constituye el tratamiento de elección en pacientes seleccionados con enfermedades hepáticas agudas y crónicas en fase terminal, cuando no existen otras posibilidades terapéuticas o estas han fracasado. A pesar de los avances en la terapia inmunosupresora experimentados en la última década y del reconocido privilegio inmunológico del hígado, el rechazo celular agudo sigue constituyendo una complicación frecuente tras el trasplante2,3. El diagnóstico rápido del mismo permite aplicar terapias que logran la resolución en la mayoría de los casos. La terapia estándar del rechazo celular agudo de grado leve y casos seleccionados de grado moderado consiste en el aumento en los valores de inmunosupresión basal, empleándose corticoides por vía intravenosa en altas dosis en los otros casos. En casos de rechazo resistente a los corticoides, más frecuente en receptores que hayan empleado corticoides antes del trasplante o en rechazos agudos graves, se han utilizado anticuerpos OKT3 y globulina antitimocítica, con el consiguiente riesgo de incrementar la aparición de infecciones, la recidiva de la infección por el virus de la hepatitis C sobre el injerto, y de neoplasias, sobre todo de origen linfoproliferativo4,5.
Basiliximab es un anticuerpo monoclonal quimérico que actúa como un antagonista del receptor de la IL-2 localizado en la superficie de los linfocitos T activados y, por consiguiente, inhibe la proliferación de los linfocitos T mediada por la IL-2. Varios estudios han demostrado la eficacia y seguridad del basiliximab asociado a los inhibidores de la calcineurina como terapia de inducción en el trasplante de órganos sólidos6–8, pero existe menos evidencia a la hora de evaluar su eficacia en el tratamiento del rechazo agudo, la mayoría en receptores de un injerto renal9. Únicamente 2 estudios describen el papel del basiliximab como terapia de rescate en el rechazo celular agudo resistente a los corticoides en receptores adultos de un trasplante de hígado10,11. El estudio de Orr et al.11 incluye 25 pacientes tratados con anti-IL-2 (daclizumab y basiliximab), de los cuales 12 (48%) se recuperaron del rechazo resistente a los corticoides, mientras que los otros 13 progresaron hacia disfunción del injerto, desarrollándose un rechazo crónico en 6 de ellos. Cinco sujetos presentaron complicaciones infecciosas, con evolución fatal en 2 de ellos. Estos resultados son comparables con series publicadas en receptores pediátricos. Aw et al.12 comunicaron la resolución del episodio de rechazo resistente a los corticoides en 5 de 7 pacientes tratados con basiliximab, desarrollándose un rechazo crónico en los 2 restantes. Adicionalmente, estos estudios señalan que el basiliximab posee un perfil de seguridad y una adecuada tolerancia, siempre y cuando se evite un estado de sobreinmunodepresión, especialmente en pacientes trasplantados por cirrosis por infección por VHC11.
En definitiva, aun en ausencia de estudios comparativos adecuados, el basiliximab podría representar una opción terapéutica válida en el rechazo celular agudo resistente a los corticoides tras el trasplante hepático, con un elevado grado de eficacia y una seguridad aceptable en relación con la gravedad del cuadro, debiéndose evitar en la medida de lo posible un estado de sobreinmunodepresión.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.