En los últimos años, la inmunoterapia ha revolucionado el tratamiento del cáncer. Entre los efectos secundarios destacan los denominados inmunomediados, fundamentalmente la toxicidad dermatológica y gastrointestinal1.
La colitis secundaria a este tratamiento es un efecto adverso frecuente que resulta complicado distinguir de una colitis ulcerosa primaria, tanto endoscópica como histológicamente, suponiendo un gran reto diagnóstico para el gastroenterólogo2.
Presentamos el caso de un paciente en tratamiento con pembrolizumab, tras diagnóstico de melanoma metastásico, quien desarrolló un cuadro de colitis con biopsias compatibles con colitis ulcerosa: ¿colitis ulcerosa o colitis-like?
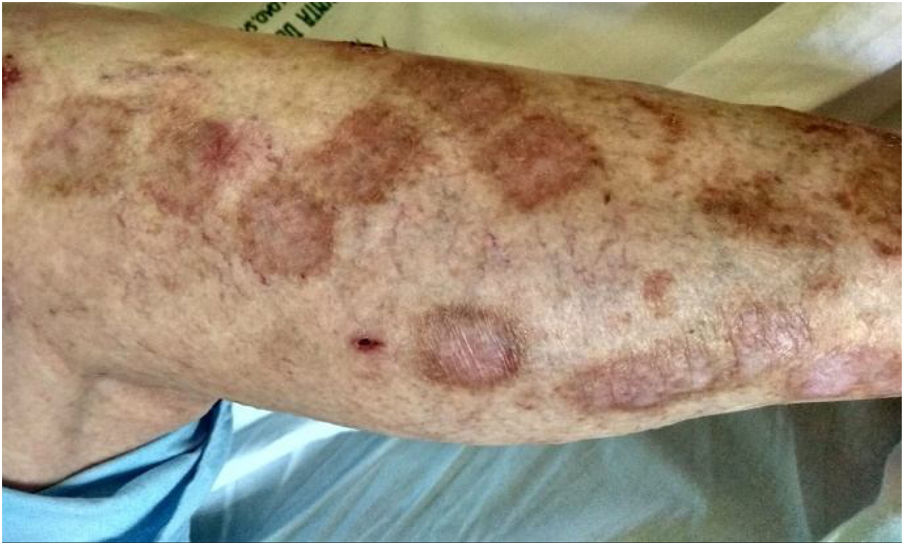
Caso clínicoVarón de 61 años con diagnóstico de melanoma con metástasis pulmonares. Tras iniciar tratamiento oncológico con pembrolizumab, consulta por la aparición de lesiones cutáneas eritematosas y anulares en extremidades (fig. 1), asociada a clínica de diarrea sanguinolenta con más de 15 deposiciones al día.
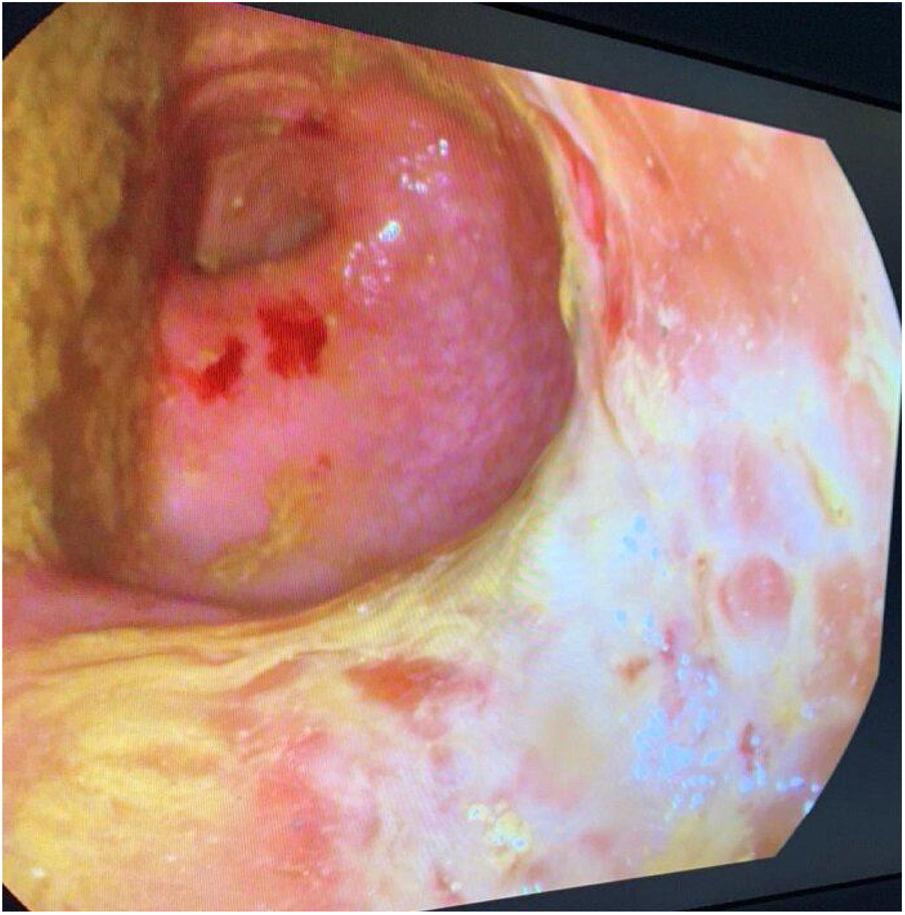
En la colonoscopia se observa una colitis izquierda con actividad severa, siendo las biopsias compatibles con una colitis ulcerosa (fig. 2). Ante la duda de origen tóxico o debut de enfermedad inflamatoria intestinal, se inicia tratamiento con corticoterapia con leve mejoría clínica, aunque finalmente precisa administración de infliximab por corticodependencia.
Ante el antecedente de melanoma, se decide administrar solo dos dosis de inducción con infliximab; sin embargo, al mes el paciente regresa a consulta con la misma clínica y se decide iniciar tratamiento con otro biológico, en este caso vedolizumab, por su perfil de seguridad en pacientes oncológicos.
Posteriormente, buena evolución clínica, manteniéndose asintomático, desde el punto de vista intestinal. A los dos meses, se objetiva en TC de control progresión tumoral con metástasis «en suelta de globos» pulmonares y metástasis óseas.
DiscusiónDentro del diagnóstico diferencial de la enterocolitis en paciente oncológicos incluimos las clásicas colitis asociadas a los antibióticos y las colitis neutropénicas; sin embargo, no siempre tenemos en cuenta otras etiologías, como pueden ser las secundarias a fármacos, en este caso, a inmunofármacos1.
El pembrolizumab es un inmunofármaco aprobado para el tratamiento del melanoma metastásico. Dado el mecanismo de acción que tiene este anticuerpo monoclonal, es lógica la aparición de efectos secundarios de tipo autoinmune, derivados de la producción de linfocitos T autorreactivos contra diferentes tejidos del organismo1,2.
La colitis inducida por este fármaco es muy poco prevalente (< 1%) y se manifiesta con diarrea que aparece entre las seis y 16 semanas desde que se inicia la terapia, afectando generalmente a colon descendente. Entre los efectos adversos gastrointestinales menos frecuentes se encuentran: las aftas, la esofagitis, la gastritis y la perforación2.
El tratamiento del «brote» se realiza con corticoides. Según la experiencia clínica, si tras tres días de tratamiento con corticoides intravenosos los síntomas no mejoran claramente, se puede considerar como colitis resistente a los corticoides. En estos casos, el tratamiento combinado con infliximab puede ser beneficioso3. Si los síntomas persisten tras la primera dosis, puede administrarse una segunda dosis transcurridas dos semanas. En algunas ocasiones se plantea como tratamiento de mantenimiento debido a los episodios de recaída observados, a pesar de la curación mucosa del colon3,4. Si los síntomas no mejoran tras la administración de infliximab o si está contraindicado el uso de anti-TNFα, debe contemplarse la posibilidad de usar vedolizumab4.
Aunque existen muy pocos casos descritos en la literatura, debido al auge de la inmunoterapia en los últimos años, la frecuencia de reacciones adversas puede aumentar y debemos tenerlas en cuenta. A pesar de que se ha observado una relación entre los efectos inmunomediados y una respuesta tumoral favorable5, en estos casos tendremos que suspender el tratamiento y tratar la toxicidad, ya que el pronóstico y la evolución pueden ser fatales.