Sr. Director: La leishmania es un protozoo con múltiples subespecies indistinguibles morfológicamente cuando parasitan los tejidos humanos, en los que adoptan la forma de amastigotes. Éstos son ovoides o redondeados, de 1,5-3 µm de diámetro, con fina membrana celular, núcleo relativamente grande y cinetoplasto característico en forma de barra que se tiñen bien con los métodos de hematoxilina-eosina (HE) y Giemsa. Los amastigotes, una vez inoculados en la piel por los insectos del género Lutzomyia o Phlebotomus (según el área geográfica) son captados por histiocitos en los que se multiplican por fisión binaria. La infección del insecto vector supone una conversión del amastigote en formas flageladas de mayor tamaño (leptomonas) en su tubo digestivo, que se inoculan en la picadura a distintos reservorios. Según la localización y la respuesta del huésped, se consideran varias formas de la enfermedad: cutánea, localizada o difusa, mucocutánea y visceral. La forma visceral es la menos común de las formas clínicas de leishmaniasis y presenta, a su vez, tres formas clinicoepidemiológicas: a) kala-azar infantil o esporádico, frecuente en el área mediterránea y cuyo reservorio es el perro; b) kala-azar hindú, que afecta principalmente a adolescentes y adultos jóvenes, y cuyos reservorios son ellos mismos, y c) kala-azar africano, propio de adultos, transmisible sólo en epidemias y cuyo reservorio es la rata1.
Actualmente, asistimos a un incremento de esta infección, sobre todo en relación con el síndrome de inmunodeficiencia adquiridaM hay escasas comunicaciones en la bibliografía de localizaciones excepcionales, entre ellas el aparato digestivo, en las que se ha identificado el parásito2-5.
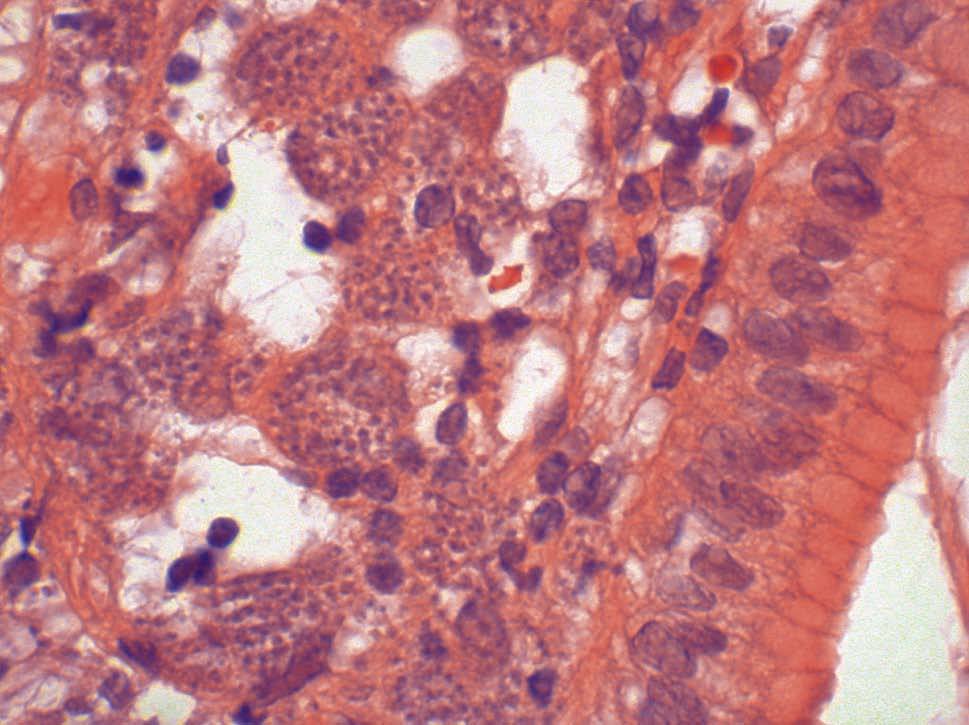
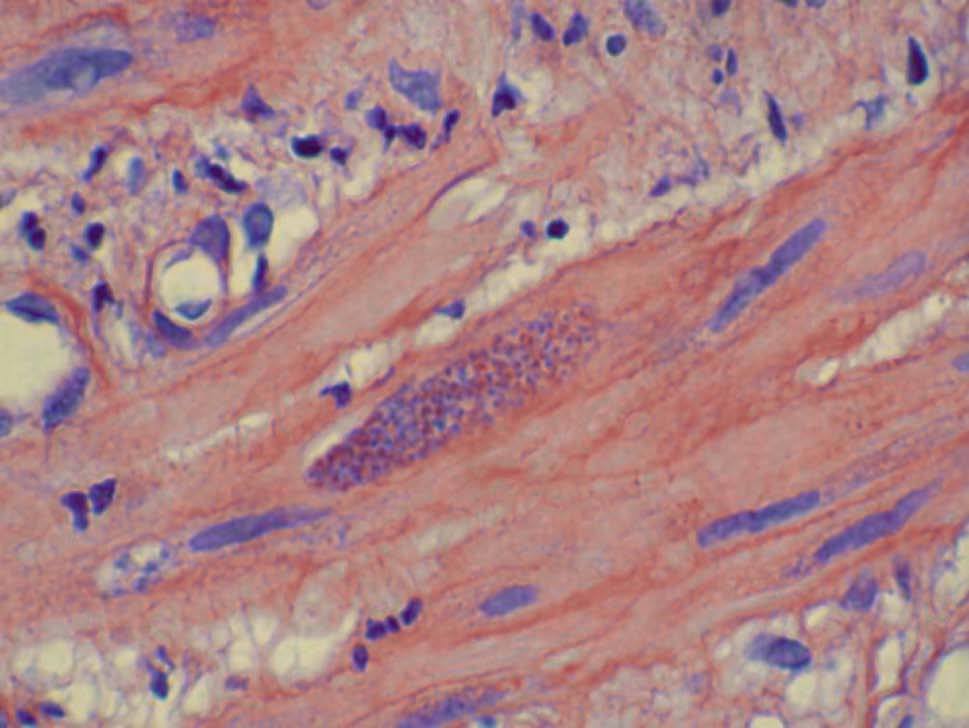
Presentamos dos casos de leishmaniasis visceral de localización extraordinariamente infrecuente: lámina propia de la mucosa gástrica (fig. 1) y muscular propia del esófago (fig. 2). En ambos casos el diagnóstico inicial se realizó en las biopsias obtenidas por endoscopia. Los pacientes eran varones, de 31 y 33 años, ambos con síndrome de inmunodeficiencia adquirida en fase avanzada, cuyo proceso se inició clínicamente con odinofagia y gastritis, respectivamente. En el caso de localización esofágica, la antropozoonosis estaba asociada a una úlcera mucosa inespecífica. En el caso de localización gástrica no se constataron lesiones asociadas.
Fig. 1.
Fig. 2.
El diagnóstico de leishmaniasis se basa en la identificación de los microorganismos en el tejido diana; generalmente, éstos se encuentran dentro del citoplasma de histiocitos, si bien no es infrecuente encontrar grupos extracelulares. El número de parásitos depende, en gran parte, del tiempo de evolución de la lesión y del estado inmunitario del huésped, y son más numerosos en las lesiones tempranas y en pacientes inmunodeprimidos. Los amastigotes, también llamados cuerpos de Leishman Donovan, presentan una localización preferentemente intracelular, y puede bservarse un núcleo redondo y un pequeño apéndice o cinetoplasto, ambos basófilos con HE, si bien su identificación se facilita con la tinción de Giemsa, con lo que el núcleo adquiere una tonalidad purpúrea y el cinetoplasto un color rojizo. El infiltrado inflamatorio acompañante compuesto por linfocitos, neutrófilos e incluso células plasmáticas puede en ocasiones dificultar la identificación de los microorganismos, sobre todo en casos con localización preferentemente extracelular.
La identificación de leishmaniasis en el tubo digestivo es excepcional, si bien en cuadros intensos pueden afectarse múltiples órganos y sistemas; en tales circunstancias se suele tener constancia de la parasitación, manifiesta en otras localizaciones. Es muy infrecuente el diagnóstico inicial de la enfermedad en el tubo digestivo, de ahí la rareza de los casos aquí presentados; se trata de un inicio clínico infrecuente que, sin embargo, permite un diagnóstico rápido y certero tras la realización de una biopsia mediante la identificación del parásito con técnicas de tinción convencionales (HE) y la asistencia de tinciones como la de Giemsa, que permite la observación de las leishmanias con mayor facilidad.
El diagnóstico diferencial debe establecerse con otras parasitasiones más o menos frecuentes en pacientes inmunodeprimidos, como la histoplasmosis o la tripanosomiasis. La simple histología o la aplicación de tinciones argénticas serán suficientes en la mayoría de los casos para realizar tal distinción si bien existen hoy día técnicas de reacción en cadena de la polimerasa (PCR) que permiten la certera identificación del parásito6,7.
Por tanto, es necesario tener en cuenta esta parasitación en el manejo de las biopsias de pacientes con sida, cualquiera que sea su localización. Con la presentación de 2 casos localizados en el aparato digestivo queremos recalcar la importancia que un estudio meticuloso de las biopsias endoscópicas tiene en este tipo de pacientes, pues de manera sencilla podemos hacer un diagnóstico que de otro modo puede conllevar un importante perjuicio para la salud del paciente.