Evaluar la eficacia y la seguridad de los sistemas de soporte hepático extracorpóreo Molecular Adsorbent Recirculating System (MARS®) y Prometheus® en el tratamiento de la insuficiencia hepática.
DiseñoRevisión sistemática de la literatura médica desde enero de 1999 hasta junio de 2009 en las bases de datos Medline, Embase, HTA, DARE, NHSEED, Cochrane Library Plus, Clinical Trials Registry y Health Services Research Projects in Progress. La selección de estudios se realizó mediante una serie de criterios de inclusión previamente establecidos, relativos al diseño del estudio, a la población, al tipo de intervención, al idioma y a las variables de resultado.
Pacientes e intervencionesPacientes con insuficiencia hepática aguda o insuficiencia hepática crónica agudizada en tratamiento con los sistemas MARS® o Prometheus®.
Variables de resultado: datos relativos a la seguridad, a la supervivencia a largo plazo, a los efectos clínicos y a las variables bioquímicas y hemodinámicas.
ResultadosSe seleccionaron 22 estudios que evaluaban la eficacia y la seguridad de los sistemas MARS® y Prometheus®. Se observó la existencia de heterogeneidad y limitaciones metodológicas que dificultó la correcta evaluación de estas técnicas.
ConclusionesLos sistemas de soporte hepático extracorpóreo son capaces de depurar tanto sustancias hidrosolubles como sustancias unidas a proteínas. Sin embargo, los datos actuales muestran que solo el sistema MARS® reduce la mortalidad en la insuficiencia hepática aguda y en la insuficiencia hepática crónica agudizada, aunque de forma no significativa. Estas técnicas pueden considerarse seguras, con efectos adversos similares a los del grupo control. Su principal indicación sería en la insuficiencia hepática grave de forma limitada en el tiempo, mientras se recupera el órgano o se produce su trasplante.
To evaluate the safety and efficacy of the MARS® and Prometheus® extracorporeal liver support systems in the treatment of liver failure.
DesignWe performed a systematic review of the literature from January 1999 to June 2009 in the Medline, Embase, HTA, DARE, NHSEED, Cochrane Library Plus, Clinical Trials Registry and HSRPROJ databases. Study selection was based on a series of previously established inclusion criteria related to the study design, population, type of intervention, language, and outcome measures.
Patients and interventionsPatients with acute liver failure or acute exacerbations of chronic liver failure treated with the MARS® or Prometheus® systems. Outcome measures: data on safety, long-term survival, clinical effects and biochemical and hemodynamic variables.
ResultsWe selected 22 studies evaluating the safety and efficacy of the MARS® and Prometheus® systems. Adequate evaluation of these techniques was hampered by the heterogeneity of the studies and their methodological limitations.
ConclusionsExtracorporeal liver support systems are able to purify both hydrosoluble and protein-bound substances. However, current data show that only the MARS® system reduces mortality in acute liver failure and in acute exacerbations of chronic liver failure, although this reduction is non-significant. These techniques can be considered safe, with adverse effects similar to those of the control group. Their main indication is severe liver failure, for short periods while the liver recovers or a liver transplant becomes available.
La insuficiencia hepática supone la incapacidad del hígado para llevar a cabo sus funciones metabólicas, de excreción y de detoxificación, debido a una disminución del número de hepatocitos o de su actividad funcional. Pueden aparecer grados variables de encefalopatía hepática (EH) por la llegada al cerebro de sustancias tóxicas que escapan al metabolismo hepático1,2.
La insuficiencia hepática aguda (IHA) se produce sin que exista enfermedad previa, mientras que la de tipo crónico es consecuencia de un daño hepático de larga evolución, independiente de su etiología y del tipo de lesión existente. Una forma de IHA es la hiperaguda o fulminante, en la que el cuadro clínico se instaura rápidamente, con encefalopatía progresiva y disfunción orgánica múltiple (edema cerebral, coagulopatía, insuficiencia renal aguda y deterioro hemodinámico. En estos casos, la mortalidad sin trasplante hepático es del 40–80%3,4. Por otra parte, cuando en un paciente con hepatopatía crónica se presentan una serie de factores precipitantes, como la hemorragia por varices esofágicas, la sepsis o el abuso de alcohol, la función hepática experimenta un deterioro agudo, y se habla, entonces, de insuficiencia hepática crónica agudizada (IHCA). Ambos tipos de insuficiencia hepática, IHA e IHCA, pueden ser reversibles y el hígado puede retornar a un nivel funcional similar al de antes de aparecer el factor precipitante.
El trasplante hepático es el único tratamiento que ha demostrado mejorar el pronóstico de los casos más graves de insuficiencia del órgano. Sin embargo, su coste y la escasez de donantes han obligado a buscar nuevos tratamientos de reemplazo que sirvan de «puente» para el trasplante o que faciliten la recuperación de las funciones de síntesis y depuración del hígado tras una IHA o una IHCA5. Los sistemas biológicos de depuración extracorpórea son técnicas experimentales que utilizan hepatocitos vivos a través de los que circula la sangre o el plasma del paciente, y pueden ser humanos —células de hepatoblastoma bien diferenciado— (extracorporeal liver assist device) o de cerdo (bioarthificial liver device)6.
Los primeros sistemas de depuración no biológicos o artificiales utilizados fueron la hemodiálisis, la hemofiltración y la hemoperfusión, sin lograr grandes resultados en la eliminación de toxinas unidas a proteínas. Desde hace algunos años se ha comenzado a utilizar albúmina en los sistemas de diálisis, debido a que es la principal proteína transportadora del plasma. Dentro de las diferentes técnicas existentes, la diálisis con albúmina de un solo paso ha demostrado su utilidad, pero a expensas de un elevado coste7, por lo que se ha propuesto disminuir la concentración de albúmina en el dializador, lo que parece no repercutir negativamente en la capacidad de depuración8. Sin embargo, los sistemas más utilizados en la actualidad se basan en la hemodiadsorción, que combina una diálisis convencional con una diálisis contra albúmina, que posteriormente se regenera, para reutilizarse mediante columnas de adsorción con carbón y resinas de intercambio iónico.
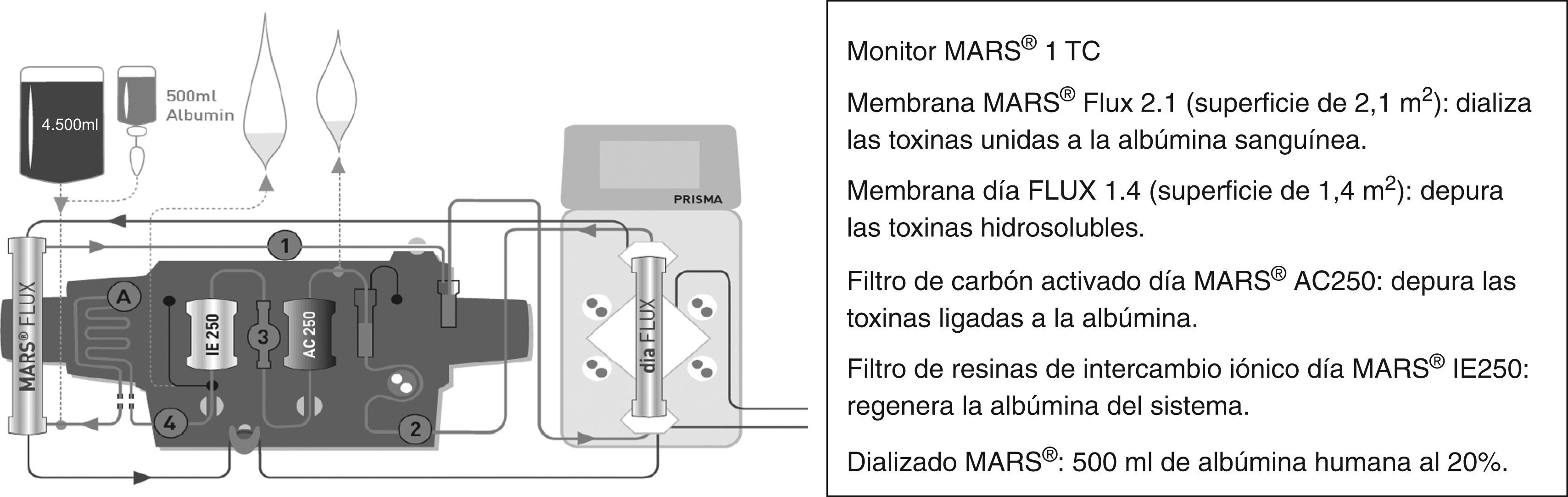
Molecular Adsorbent Recirculating SystemSe desarrolló en la Universidad de Rostock (Alemania) en la década de 1990 por parte de Stange et al9, y consiste en un sistema de hemodiálisis extracorpórea con 3 circuitos diferentes: sanguíneo, de albúmina y de diálisis de bajo flujo. El circuito sanguíneo utiliza un acceso venovenoso por catéter de doble luz y una máquina de hemodiálisis convencional propulsa la sangre hacia un filtro de alto flujo impermeable a la albúmina (Molecular Adsorbent Recirculating System [MARS®] Flux 2.1; Gambro®) (fig. 1). El líquido dializador es albúmina humana al 20% que, puesta en contacto con la sangre, hace que las sustancias con capacidad de unión atraviesen la membrana de polisulfona y se unan a ella.
La albúmina del circuito se regenera mediante el paso sucesivo por una columna de carbón activado por una segunda columna de resinas de intercambio iónico. Posteriormente, el dializado pasa a través de una membrana de diálisis convencional de bajo flujo, donde se dializa con un buffer de bicarbonato para eliminar las moléculas hidrosolubles (creatinina, urea y amonio).
Sistema Prometheus®El sistema Prometheus® (Fresenius Medical Care AG, Bad Homburg, Alemania) se introdujo en 1999 por parte de Falkenhagen et al10, y consta de un equipo de diálisis al que se le añade un módulo para la separación fraccionada del plasma y la adsorción (fig. 2). El mecanismo básico es la plasmaféresis o filtración de la albúmina del paciente, seguida de la adsorción. A través de un catéter de doble luz, la sangre del paciente se introduce en el circuito secundario, en donde se realiza una filtración selectiva de la albúmina a través de un filtro AlbuFlow® con un alto coeficiente de cribado (alrededor de 250kD), compuesto por membranas capilares de polisulfona (Fresenius Polysulfone®) de buena biocompatibilidad. A continuación, el plasma que contiene la albúmina pasa a través de 2 columnas de adsorción en serie, una de intercambio iónico y otra de resina neutra (Prometh® 01 y 02), donde las toxinas unidas a la albúmina se capturan por contacto directo con el material adsorbente. Posteriormente, el plasma sanguíneo y la albúmina detoxificada se devuelven al paciente, por lo que no se requiere albúmina externa para este proceso. Antes de la reentrada del dializado al paciente, este pasa a través de un filtro de helixona Fresenius® para eliminar las toxinas hidrosolubles.
El objetivo de este trabajo fue realizar una revisión sistemática de la utilización de los sistemas de soporte hepático extracorpóreo MARS® y Prometheus® en el tratamiento de la IHA y la IHCA, y evaluar la seguridad de estas técnicas, sus efectos clínicos o sobre las variables bioquímicas o hemodinámicas y los resultados de supervivencia a largo plazo.
Material y métodosSe realizó una revisión sistemática de la literatura médica con la siguiente metodología:
Estrategia de búsqueda: la búsqueda bibliográfica abarcó desde 1999 hasta junio de 2009. Las bases de datos utilizadas fueron las siguientes:
- •
Especializadas en revisiones sistemáticas: Cochrane Library Plus y la base de datos del NHS Centre for Reviews and Dissemination (HTA, DARE y NHSEED).
- •
Bases de datos generales: Medline y Embase.
- •
Bases de datos y repositorios de proyectos de investigación en curso: Clinical Trials Registry (National Institutes of Health, EE. UU.) y Health Services Research Projects in Progress.
- •
Buscadores generales: Google Académico.
Selección y análisis de estudios: el resultado de las búsquedas se volcó en un gestor de referencias bibliográficas (EndNote X.0.2) con el fin de eliminar los duplicados y facilitar la gestión documental. Tras la lectura de los resúmenes de los artículos, se realizó una selección de estudios mediante una serie de criterios de inclusión previamente establecidos y relativos al diseño del estudio, al tipo de intervención (tratamiento mediante los sistemas MARS® o Prometheus®), a la población del estudio (pacientes con IHA o IHCA), al idioma (sin restricción de idioma) y a las variables de resultado (datos relativos a mortalidad y seguridad, a supervivencia a largo plazo, a efectos clínicos y a variables bioquímicas o hemodinámicas). Dada la relativa abundancia de estudios que evaluaban el sistema MARS®, la búsqueda se limitó a ensayos clínicos, mientras que para el sistema Prometheus® se incluyeron tambien estudios observacionales. La extracción de datos se realizó siguiendo una metodología sistemática en hojas de extracción diseñadas específicamente para esta revisión. Los datos de los estudios incluidos se presentaron en forma de tablas de evidencia, y se prestó especial interés a aquellas variables de eficacia y seguridad. La calidad de la evidencia científica de los estudios se valoró según el diseño de estos, y se siguió una jerarquía de mayor a menor importancia de acuerdo con la escala de Jovell y Navarro-Rubio11.
Metaanálisis: se realizó un metaanálisis para evaluar la mortalidad, tanto en la IHCA como en la IHA, utilizando el programa informático Epidat versión 3.1. El estimador del efecto combinado se calculó como una media ponderada de los estimadores individuales de cada estudio, y se asignaron los pesos según el inverso de la varianza. La evaluación del grado de heterogeneidad de los estudios se llevó a cabo mediante la prueba de Dersimonian y Laird, y mediante los gráficos de L’Abbé y de Galbraith, que permiten inspeccionar visualmente la falta de homogeneidad entre los estudios incluidos. En caso de existir heterogeneidad entre estudios, se utilizó un modelo de efectos aleatorios, que considera tanto la variabilidad intraestudio como la variabilidad interestudio. Se realizó también un análisis de sensibilidad para estudiar la influencia individual de cada estudio en el resultado del metaanálisis.
ResultadosEstudios clínicos incluidosSe seleccionaron 8 ensayos clínicos aleatorizados12–19 y un metaanálisis20 que abordaban la eficacia y la seguridad del sistema MARS®, además de 2 estudios de coste-efectividad sobre la técnica21,22. Once estudios evaluaron el sistema Prometheus®: 6 eran series de casos23–28 y el resto, ensayos clínicos aleatorizados15,17,29–31. No se localizaron estudios que evaluasen la técnica de soporte hepático Prometheus® desde un punto de vista económico.
En la tabla 1 se muestran las principales características de los estudios incluidos en esta revisión.
Estudios incluidos en la revisión
| Estudio | Patología | Pacientes | Tipo de estudio | Grupos de estudio | Variables de resultado¿ |
| MARS® | |||||
| Mitzner et al (2000)18 | IHCA | 13 | ECA (MP), NE:III | MARS® (8) Control (HD) (5) | 1, 3, 4 |
| Heemann et al (2002)13 | IHCA | 24 | ECA (MP), NE:III | MARS® (12) Control (TME) (12) | 1, 2, 3, 4, 5 |
| Sen et al (2004)19 | IHCA | 18 | ECA (MP), NE:III | MARS® (9) Control (TME) (9) | 1, 3, 4, 5 |
| Hassanein et al (2007)12 | IHCA | 70 | ECA (MG), NE:II | MARS® (39) Control (TME) (31) | 1, 2, 3, 5 |
| Schmidt et al (2003)14 | IHA | 13 | ECA (MP), NE:III | MARS® (8) Control (TME) (5) | 1, 3, 4 |
| El Banayosy et al (2004)16 | IHA | 27 | ECA (MP), NE:III | MARS® (14) Control (HD) (13) | 1, 3 |
| MARS®- PROMETHEUS® (series de casos comparados y ECA) | |||||
| Evenepoel et al (2006)23 | IHCA | 18 | Serie de casos, NE:VIII | MARS® - Prometheus® (series comparadas) | 1, 2, 3 |
| Faenza et al (2008)25 | IHCA | 57 | Serie de casos NE:VIII | MARS® - Prometheus® (series comparadas) | 1, 2, 5 |
| Krisper et al (2005)29 | IHCA | 10 | ECA (MP), NE:III | MARS® - Prometheus® (diseño cruzado) | 1, 2, 3 |
| Laleman et al (2006)17 | IHCA | 18 | ECA (MP), NE:III | MARS® (6); Prometheus® (6); Control (TME) (6) | 2, 3, 4 |
| Stadlbauer et al (2006)30 | IHCA | 8 | ECA (MP), NE:III | MARS® - Prometheus® (diseño cruzado) | 1,2, 3 |
| Stadlbauer et al (2007)31 | IHCA | 8 | ECA (MP), NE:III | MARS® - Prometheus® (diseño cruzado) | 1,2, 3 |
| Dethloff et al (2008)15 | IHCT | 24 | ECA (MP), NE:III | MARS® (8); Prometheus® (8); Control (TME + HD) (8) | 1,2, 3, 4 |
| PROMETHEUS® | |||||
| Rifai et al (2003)26 | IHCA | 11 | Serie de casos NE:VIII | Prometheus® | 1,2, 3, 4, 5 |
| Rifai et al (2005)27 | IHCA | 10 | Serie de casos NE:VIII | Prometheus® | 2, 3, 4, 5 |
| Evenepoel et al (2005)24 | IHCA | 9 | Serie de casos NE:VIII | Prometheus® | 1, 2, 3, |
| Skwarek et al (2006)28 | IHA | 16 | Serie de casos NE:VIII | Prometheus® | 1, 3, 4 |
ECA: ensayo controlado y aleatorizado; ECA (MP): ECA de muestra pequeña; ECA (MG): ECA de muestra grande; IHA: insuficiencia hepática aguda; IHCA: insuficiencia hepática crónica agudizada; IHCT: insuficiencia hepática crónica terminal; HD: hemodiálisis; NE: nivel de evidencia; TME: tratamiento médico estándar.
Se realizó un metaanálisis con los datos de mortalidad existentes en los ensayos clínicos incluidos (tabla 2), que en el caso de la IHCA fueron 512,13,15,18,19 (fig. 3). La prueba de Dersimonian y Laird no mostró evidencia estadística de heterogeneidad (p=0,7917), si bien los gráficos de Galbraith y L’Abbé mostraron que los estudios podían no ser homogéneos, por lo que para obtener la estimación global del efecto se optó por utilizar el modelo de efectos aleatorios. Los resultados mostraron una reducción no estadísticamente significativa de la mortalidad en los pacientes tratados con el sistema MARS® (riesgo relativo [RR] de 0,78; intervalo de confianza [IC] del 95%: 0,58–1,03; p=0,1059). En el análisis de sensibilidad, ningún estudio modificó sustancialmente el resultado global al eliminarlo del metaanálisis.
Mortalidad en los estudios incluidos
| Estudio | Pacientes | MARS®, % | Control, % | Tiempo | RR |
| Insuficiencia hepática crónica agudizada | |||||
| Mitzner et al18 | 13 | 62,5 | 100 | 7 días | 0,63 |
| Heemann et al13 | 24 | 50 | 66,7 | 6 meses | 0,75 |
| Sen et al19 | 18 | 55,5 | 55,5 | 3 meses | 1 |
| Hassanein et al12 | 70 | 49 | 55 | NC | 0,89 |
| Dethloff et al15 | 24 | 25 | 50 | 6 meses | 0,50 |
| Insuficiencia hepática aguda | |||||
| Schmidt et al14 | 13 | 37,5 | 40 | NC | 0,94 |
| El Banayosy et al16 | 27 | 50 | 69,2 | NC | 0,72 |
NC: no consta; RR: riesgo relativo.
La supervivencia en pacientes con IHA se evaluó en los 2 ensayos clínicos existentes14,16 (fig. 4). La prueba de Dersimonian y Laird no mostró evidencia estadística de heterogeneidad (p=0,1749), y también se observó una reducción no estadísticamente significativa (RR de 0,75 [IC 95% de 0,42–1,35]; p=0,3427).
Sistema Prometheus®Los resultados sobre la supervivencia de los pacientes tratados con el sistema Prometheus® pueden verse en la tabla 3. De los ensayos aleatorizados incluidos, 3 de ellos eran de diseño cruzado y utilizaron los mismos pacientes29–31. En los 2 ensayos en los que se utilizó grupo control, no se encontraron diferencias significativas en la supervivencia de los diferentes grupos15,17.
Supervivencia observada en diferentes estudios tras tratamiento con el sistema
| Estudio | Enfermedad | Estudio controlado | Seguimiento | Supervivencia (%) |
| Rifai et al (2003)26 | IHCA | No | 30 días | 4/11 (36) |
| Skwarek et al (2006)28 | IHA | No | – | 8/16 (50) |
| Faenza et al (2008)25 | IHCA | No | Hasta trasplante | 7/10 (70) |
| Resto, a 3 meses | 2/6 (33,3) | |||
| Krisper et al (2005)29 | IHCA | Sí (diseño cruzado) | 30 días | 4/9 (44,4) |
| Stadlbauer et al (2006)30 | IHCA | Sí (diseño cruzado) | 30 días | 4/8 (50) |
| Stadlbauer et al (2007)31 | IHCA | Sí (diseño cruzado) | 30 días | 4/8 (50) |
| Laleman et al (2006)17 | IHCA | Sí | 7 días | 6/6 (100)¿ |
| Dethloff et al (2008)15 | IHC terminal | Sí | 6 meses | 5/8 (62,5)¿ |
IHA: insuficiencia hepática aguda; IHCA: insuficiencia hepática crónica agudizada.
En varios de los estudios incluidos en esta revisión no se mencionan efectos adversos, y en los que sí lo hacen, parecen ser similares a los del grupo control, con excepción de la trombocitopenia y la hemorragia, que parecen verse incrementadas con el sistema MARS®. Con el sistema Prometheus®, los efectos adversos se limitan también a casos de trombocitopenia, hemorragia y fugas del circuito de diálisis, y son escasos los de carácter grave. También se observó un incremento reversible del recuento leucocitario, sin asociarse a signos de infección sistémica.
Cambios en los parámetros hemodinámicos y clínicosEn 3 de los 5 ensayos incluidos se comprueba que el tratamiento con MARS® incrementa de forma significativa la presión arterial media (PAM) (tabla 4)13,14,17 y que, de forma paralela, se produce un incremento significativo del índice de resistencia vascular sistémica14,17 y disminuciones del índice y de la frecuencia cardíaca14.
Cambios en los principales parámetros hemodinámicos
| PAM | IRVS | IC | FC | |
| Sistema MARS® | ||||
| Mitzner et al (2000)18 | ↑ NS | |||
| Heemann et al (2002)13 | ↑ S | |||
| Schmidt et al (2003)14 | ↑ S | ↑ S | ↓ S | ↓ S |
| Laleman et al (2006)17 | ↑ S | ↑ S | ↔ | ↔ |
| Dethloff et al (2008)15 | ↑ NS | ↔ | ↔ | ↔ |
| Sistema Prometheus® | ||||
| Rifai et al (2003)26 | ↓ S | |||
| Rifai et al (2005)27 | ↔ | |||
| Skwarek et al (2006)28 | ↔ | |||
| Laleman et al (2006)17 | ↔ | ↔ | ↔ | ↔ |
| Dethloff et al (2008)15 | ↔ | ↔ | ↔ | ↔ |
FC: frecuencia cardíaca; IC: índice cardíaco; IRVS: índice de resistencia vascular sistémica; NS: no significativo; PAM: presión arterial media; S: estadísticamente significativo (p<0,05); ↑: aumento; ↓: disminución; ↔: sin cambios.
Con el sistema Prometheus® se observa una reducción reversible de la PAM26, aunque en los 2 ensayos aleatorizados en los que se comparó con el sistema MARS® no se observaron cambios significativos15,17.
Únicamente 3 estudios evaluaron el grado de EH antes y después de recibir tratamiento con MARS®, que mejoró en todos los casos de forma significativa12,13,19. Sen et al19 observaron una reducción significativa del Child-Pugh Score (p<0,01) a los 7 días de finalizar el tratamiento con el sistema MARS®, sin que se produjesen cambios en el grupo control. Sin embargo, al evaluar el Model for End-Stage Liver Disease Score, observaron reducciones significativas en ambos grupos, el grupo en tratamiento con MARS® y el grupo control (p<0,01 y p<0,05, respectivamente). No se observaron cambios significativos en el Child-Pugh Score con el sistema Prometheus®26,27.
Cambios en los parámetros bioquímicosLa bilirrubina total fue el único parámetro bioquímico analizado en todos los ensayos, y se encontró siempre disminuida en el grupo en tratamiento con MARS® (tabla 5) (en el estudio de El Banayosy et al16, los niveles se midieron a los 14 días de completar el tratamiento). Del resto de parámetros bioquímicos, únicamente existió consistencia en la creatinina y en la urea: se observó un descenso significativo de ambos parámetros.
Cambios en los parámetros bioquímicos
| Sistema MARS® | ||||||||
| Estudio | Bilirrubina | Creatinina | Albúmina | Urea | ALT | AST | Amonio | BUN |
| Mitzner et al (2000)18 | ↓ S | ↓S | ↑NS | |||||
| Heemann et al (2002)13 | ↓¿ | ↓S | ||||||
| Sen et al (2004)19 | ↓ S | ↓S | ↔ | ↔ | ||||
| Laleman et al (2006)17 | ↓ S | ↔ | ↔ | ↔ | ↔ | |||
| Hassanein et al (2007)12 | ↓ S | ↓S | ↓S | ↓S | ||||
| Schmidt et al (2003)14 | ↓ S | ↓S | ↔ | ↓S | ↓S | ↔ | ||
| El Banayosy et al (2004)16 | ↓ NS | ↓S | ↔ | ↔ | ↓S | |||
| Dethloff et al (2008)15 | ↓ NS | ↓S | ||||||
| Sistema Prometheus® | ||||||||
| Estudio | Bilirrubina | Creatinina | Albúmina | Urea | ALT | AST | Amonio | Ácidos biliares |
| Rifai et al (2003)26 | ↓ NS | ↓S | ↔ | ↓S | ↓S | ↓S | ||
| Rifai et al (2005)27 | ↓ NS | ↓S | ↔ | ↓S | ↓S | ↓S | ||
| Evenepoel et al (2006)23 | ||||||||
| Evenepoel et al (2005)24 | ↓ S | ↓S | ↓NS | ↓S | ↓S | |||
| Skwarek et al (2006)28 | ↓ S | -- | ↓S | ↓S | ↓S | |||
| Laleman et al (2006)17 | ↓ S | ↔ | ↔ | ↔ | ↔ | ↓S | ||
| Dethloff et al (2008)15 | ↓ NS | ↓NS | ||||||
AST: aspartato aminotransferasa; BUN: nitrógeno ureico en sangre; NS: no significativo; S: estadísticamente significativo (p<0,05); ↓: disminución; ↔: sin cambios; ALT: alanino aminotransferasa.
Respecto al sistema Prometheus®, en todos los estudios se pudo comprobar su capacidad para depurar tanto las sustancias hidrosolubles como las unidas a proteínas, y se observaron disminuciones significativas de las concentraciones de bilirrubina, ácidos biliares, amonio, creatinina y urea (tabla 5).
Cambios en los parámetros relacionados con la coagulaciónCon el sistema MARS®, los datos obtenidos son contradictorios. Así, mientras Mitzner et al18 encontraron un incremento significativo en la actividad de protrombina de los pacientes tratados con MARS®, otros autores no encontraron cambios13,17 e incluso un descenso, aunque no significativo.19. El INR no se vio modificado en los 3 ensayos que lo determinaron14,16,19, y el número de plaquetas disminuyó significativamente14,15 o incluso se vio incrementado, aunque de forma no significativa.16.
No se observaron modificaciones importantes con el sistema Prometheus® en los parámetros relacionados con la coagulación; únicamente cabe destacar el descenso significativo observado en el tiempo de protrombina23.
Resultados de los estudios económicosÚnicamente se seleccionaron 2 estudios de coste-efectividad del sistema MARS®, y no se localizó ninguno que abordase aspectos económicos del sistema Prometheus®.
El estudio de Hassanein et al21 analizó los costes en pacientes con IHCA aleatorizados para recibir MARS® o tratamiento médico estándar. El sistema MARS® produjo un menor número de fallecimientos hospitalarios y de complicaciones relacionadas con la enfermedad, con una importante reducción de costes que sirvió para contrapesar los asociados a este tratamiento extracorporal. Así, debido a que en el grupo control sobrevivieron 5 pacientes de un total de 11, cada superviviente tuvo un coste de 35.904 dólares, mientras que en el grupo tratado con MARS® sobrevivieron 11 de 12 pacientes, y el coste de cada uno de ellos fue de 32.036 $.
Por su parte, Hessel et al22 publicaron los resultados del seguimiento durante 3 años de una cohorte de 79 pacientes con IHCA, de los que 33 recibieron tratamiento con MARS® y 46, tratamiento médico estándar. La supervivencia fue del 67% en los pacientes tratados con MARS® y del 63% en el grupo control, que se redujo al 58 y al 35%, respectivamente, al año de seguimiento, y al 52 y al 17%, respectivamente, a los 3 años. Los costes de hospitalización del grupo en tratamiento con el sistema MARS® fueron mayores que los del grupo control (31.539 vs. a 7.543 €) y de igual manera los costes directos durante el seguimiento de 3 años (8.493 vs. a 5.194 €). Sin embargo, después de ajustar los datos por la mortalidad, el coste por año de cada superviviente fue de 5.827 € en el grupo MARS® y de 12.092 € en el grupo control; la razón coste-efectividad incremental de los pacientes del grupo MARS® fue de 31.448 € y el coste por año de vida ajustado por calidad fue de 47.171 €.
DiscusiónMetodología de los estudios y limitaciones de la evaluaciónA pesar del relativo gran número de estudios acerca de la utilización del sistema MARS® en la insuficiencia hepática, la mayoría se trata de series descriptivas de casos en las que no existe un grupo control. En esta revisión únicamente se consideraron estudios de calidad metodológica, es decir, que abordasen la eficacia y seguridad del sistema MARS® con un diseño de ensayo clínico controlado y aleatorizado. El único estudio incluido que no cumple totalmente estos criterios es el de Schmidt et al14, con un diseño cuasiexperimental en el que los pacientes se asignaron de forma consecutiva al grupo de intervención o al grupo control, y la decisión de incluirlo se debe a haberlo hecho previamente Khuroo et al en su metaanálisis20.
Por el contrario, la escasez de estudios en los que se aborda la utilización del sistema Prometheus® en la insuficiencia hepática hizo necesario ampliar los criterios de selección, e incluir también series descriptivas de casos. Los 5 ensayos aleatorizados evaluados fueron de pequeño tamaño muestral y 3 de ellos de diseño cruzado con los sistemas MARS® y Prometheus®29–31. En este tipo de estudios en los que cada paciente es su propio control, es muy importante que las intervenciones en estudio estén separadas por un período de tiempo suficiente para que desaparezca el efecto de la intervención anterior. Sin embargo, en estos ensayos no se describe la existencia de este «período de lavado». Por otra parte, ningún ensayo se diseñó para analizar la supervivencia y solo 2 estudios compararon los sistemas MARS® y Prometheus® con tratamiento convencional15,17, ya que el resto utilizaron como comparador únicamente el sistema MARS®, que parece considerarse el gold standard. Por último, en 3 ensayos clínicos29–31 y en 2 series de casos23,24 se utilizaron los mismos pacientes.
Se observaron diferentes limitaciones metodológicas en los estudios incluidos; las más importantes fueron el escaso tamaño muestral mencionado anteriormente, la falta de homogeneidad de los grupos de estudio, la inadecuada descripción de los resultados y la no estratificación de los pacientes por la gravedad de su enfermedad. La duración y el número de sesiones de tratamiento difiere también de unos estudios a otros, lo que puede explicar la inconsistencia de los hallazgos bioquímicos o hemodinámicos, y algunos estudios no exponen claramente todos los tratamientos adyuvantes recibidos por los pacientes. Es importante también tener en cuenta la existencia de potenciales conflictos de interés, dado que la industria fabricante de la tecnología ha financiado muchos de los estudios.
Efecto del soporte hepático extracorpóreo sobre la supervivenciaEl metaanálisis de Khuroo et al20 incluyó 4 ensayos aleatorizados13,14,16,18, y no observó que el sistema MARS®, en comparación con el tratamiento estándar, produjera una mayor supervivencia de los pacientes. En el metaanálisis realizado en esta revisión sistemática se incluyeron 7 ensayos clínicos aleatorizados, 5 para evaluar la mortalidad en los pacientes con IHCA y 2 en pacientes con IHA. En ambos casos, los resultados combinados mostraron una reducción de la mortalidad, aunque no significativa estadísticamente, los pacientes en tratamiento con MARS®, si bien cabe la posibilidad de que el reducido número de casos incluidos en los estudios no sea capaz de conseguir la suficiente potencia estadística para detectar diferencias significativas entre ambos grupos de tratamiento. De todas formas, la heterogeneidad en el número de sesiones de tratamiento y en la gravedad de la enfermedad hepática de los pacientes incluidos hace difícil evaluar el efecto del sistema MARS® sobre la supervivencia. Además, aunque este sistema depura la sangre de toxinas ligadas a la albúmina y disminuye los niveles de bilirrubina, es difícil comprender los mecanismos que hacen que se incremente la supervivencia.
Respecto al sistema Prometheus®, no existen suficientes datos para valorar el efecto sobre esta variable de resultado.
Efectos adversos de las técnicasA pesar de que en muchos estudios que evalúan los sistemas de soporte hepático extracorpóreo no se mencionan los efectos adversos, en los que sí lo hacen parecen ser similares a los del grupo control, con excepción de la trombocitopenia y la hemorragia, que se ven incrementadas. También, el International MARS® Registry, con datos de más de 500 pacientes, aunque patrocinado por la empresa fabricante, muestra que los efectos adversos observados son similares a los del grupo control32,33.
De todas formas, en estos pacientes gravemente enfermos es difícil discernir entre complicaciones de la propia enfermedad y efectos adversos secundarios a la técnica. Por último, cabe reseñar el incremento reversible del recuento leucocitario observado con el sistema Prometheus® que, sin asociarse a signos de infección sistémica, podría deberse a una activación leucocitaria tras el contacto con la membrana de diálisis34,35.
Cambios en los parámetros hemodinámicos y bioquímicosEn la insuficiencia hepática es frecuente encontrar una disminución de la PAM como resultado de la presencia de vasodilatación periférica, por lo que es necesario, en ocasiones, administrar un tratamiento vasopresor, especialmente si se asocia a un síndrome de respuesta inflamatoria sistémica. La normalización de este parámetro hemodinámico es importante en el tratamiento de la EH debido a la correlación existente entre la PAM y el flujo sanguíneo cerebral en la IHA36 y a que su caída puede originar fracaso multiorgánico por hipoperfusión tisular.
En 3 estudios se comprueba que el tratamiento con MARS® incrementa de forma significativa la PAM, aunque de forma transitoria (tabla 4), ya que a los 7 días sus cifras no difieren de las obtenidas antes de iniciar el tratamiento19. La reducción significativa observada en las concentraciones sanguíneas de renina, aldosterona, noradrenalina, vasopresina y nitratos podría explicar los cambios hemodinámicos anteriormente descritos17.
Parece existir un comportamiento diferente de la PAM según el sistema de depuración hepática extracorpórea que se utilice, ya que en series de casos se observó que el sistema Prometheus® produce una disminución reversible de la PAM26,28. Se ha especulado que una posible causa podría ser el paso de la albúmina del paciente por el circuito secundario del sistema Prometheus®, lo que provocaría cambios en la presión osmótica por disminución de la albúmina sérica17,29. Otra posible causa sería la capacidad de depurar metabolitos del óxido nítrico (nitratos) mediante el sistema MARS®, pero no mediante el sistema Prometheus®, y podría radicar en esto el efecto marcadamente diferente sobre la hemodinámica sistémica. De todas formas, el efecto del sistema Prometheus® sobre la hemodinámica del paciente no está completamente establecido.
En todos los estudios se pudo comprobar la capacidad de los sistemas MARS® o Prometheus® para depurar tanto las sustancias hidrosolubles como las unidas a proteínas, y se observaron disminuciones significativas de las concentraciones de bilirrubina, ácidos biliares, amonio, creatinina y urea. Un hecho esperado es que, tras cesar las sesiones de diálisis, los niveles de bilirrubina vuelvan a los niveles previos17. A pesar de la reducción significativa de las concentraciones de amonio, no se observó que el sistema Prometheus® produzca un menor grado de EH26,27, al contrario que el sistema MARS®, que sí lo produce. En estos pacientes, la mejoría del estado neurológico se relaciona con la eliminación de productos tóxicos del metabolismo12,13,19.
Eficacia en el grado de depuración de la técnicaEl estudio de Krisper et al29 muestra que el sistema Prometheus® produce un aclaramiento significativamente mayor que el sistema MARS® tanto de las sustancias hidrosolubles como de las unidas a la albúmina, lo que resulta en una mayor capacidad depuradora de este sistema de diálisis. En ese estudio llama la atención que la bilirrubina no conjugada únicamente se aclaró por el sistema Prometheus®, aunque esto no tiene por qué suponer un beneficio clínico. Otros autores también observaron que el cociente de reducción de toxinas hidrosolubles y de toxinas unidas a la albúmina fue significativamente mayor con el sistema Prometheus® y que esta superioridad fue mayor para la bilirrubina23. A diferencia del aclaramiento de las sustancias hidrosolubles, que se produce de forma constante, el aclaramiento de la bilirrubina y de sus fracciones disminuye durante el transcurso del tratamiento con ambas técnicas, lo que indicaría una saturación de los adsorbentes35.
Aspectos éticos y posibles indicaciones de la técnicaUna cuestión clave es la incertidumbre existente sobre sus resultados. Así, a pesar de que los estudios muestran posibles beneficios en los pacientes tratados con esta tecnología, no existen datos acerca de si se mantienen a largo plazo.
Por otra parte, a pesar de la posible mayor supervivencia de estos pacientes, no existen datos acerca de su calidad de vida, dato de gran importancia. Es difícil realizar una elección entre cantidad y calidad de vida, y, en su caso, debería hacerse por parte de los propios pacientes y sus familiares, con el apoyo de los profesionales sanitarios.
En líneas generales, el principal objetivo de los sistemas de soporte hepático extracorpóreo es el mantenimiento de aquellos pacientes con insuficiencia hepática grave, mientras se recupera el órgano o se produce su trasplante, por lo que su utilización debería ser siempre limitada en el tiempo. Además, los pacientes susceptibles de este tratamiento no deberían tener contraindicaciones para el trasplante hepático. Las posibles indicaciones serían la IHCA, la IHA (por fármacos o tóxicos, viral e isquémica) y la disfunción del injerto tras un trasplante hepático.
ConclusionesA pesar de que podría existir un efecto favorable de la utilización del sistema MARS® en pacientes con insuficiencia hepática, los escasos estudios de calidad hacen que los resultados no puedan considerarse concluyentes. Por este motivo, la utilización de esta técnica debería ser muy restringida y previamente deberían establecerse criterios estrictos de selección, tanto de los centros hospitalarios como de los pacientes, y mediante la elaboración de un protocolo de seguimiento, registro y evaluación de los resultados alcanzados. Respecto al sistema Prometheus®, la literatura médica existente no permite establecer conclusiones avaladas por la evidencia científica, por lo que debe considerarse un tratamiento de carácter experimental hasta que estén disponibles más datos sobre su eficacia y seguridad. Por último, son necesarios estudios de calidad, de suficiente consistencia estadística, homogéneos respecto a los pacientes y a la técnica, y que aporten datos definitivos sobre la eficacia y la seguridad de estas técnicas.
A Dña. Carmen Bouza Álvarez, del Instituto de Salud Carlos III y a D. Pedro Rascado Sedes, del Complejo Hospitalario Universitario de Santiago, por su colaboración desinteresada en la revisión de este manuscrito y por los comentarios aportados.