En 1980, Gauderer y Ponsky describieron la colocación por vía endoscópica y percutánea de un tubo de Pezzer de 14 French como sonda de gastrostomía1,2. Desde entonces, la utilización y colocación de sondas de gastrostomía por vía endoscópica y percutánea (GEP) ha tenido una gran difusión. La indicación principal de la colocación de una sonda de gastrostomía es la de mantener una nutrición enteral en pacientes con sistema digestivo indemne pero que, por problemas de deglución, obstrucción u otras causas, no pueden mantener dicha nutrición por vía oral, y en los que se presupone que dicho soporte nutricional deberá mantenerse por un período superior a las 3-4 semanas3.
TÉCNICA
Desde la descripción inicial, la técnica se ha comercializado con la aparición de múltiples equipos comerciales con diversas variaciones en la forma de colocación de la GEP. La más extendida es la denominada técnica pull (tracción), que es una ligera variación sobre la original descrita por Gauderer y Ponsky1,2. La guía es introducida en el estómago a través de una punción en la pared abdominal (una vez identificado por transiluminación y presión con el dedo un punto de contacto entre el estómago y la pared abdominal), retirada por vía endoscópica y atada al dispositivo de la sonda, estirando del cabo distal de la guía desde la pared anterior del abdomen, para arrastrar la guía y la sonda por faringe, esófago, estómago, pared gástrica y abdominal. La técnica tipo push (empujar) consiste en empujar la sonda por la guía hasta que aparece por la pared abdominal la punta del dilatador, estirando desde este punto4. Otra innovación descrita por Russell et al5 es una variación de la técnica de Seldinguer según la cual se introduce una guía en estómago, se dilata el trayecto y posteriormente se pasa la sonda. No existen diferencias significativas en cuanto a resultados o complicaciones respecto a la utilización de las diferentes variacio- nes en 2 estudios comparativos publicados6,7, aunque se comunica una mayor mortalidad en un estudio comparativo retrospectivo con la utilización de la técnica de Russell et al en comparación con la técnica de tracción8. En nuestra experiencia, la técnica de tracción es la de elección por su sencillez y facilidad de aplicación.
COMPARACIÓN CON OTRAS TÉCNICAS
Las alternativas a la GEP son la gastrostomía quirúrgica, la gastrostomía percutánea no endoscópica y la utilización de la sonda nasogástrica (SNG).
En cuanto a la gastrostomía por vía quirúrgica, se han publicado varias series que comparan ambas técnicas. Estudios retrospectivos ponen de manifiesto una disminución de la morbimortalidad asociada a la técnica en pacientes con GEP en relación con los de gastrostomía quirúrgi-
ca9-11. Sin embargo, diferentes trabajos prospectivos no confirman estas diferencias en cuanto a morbilidad y mortalidad. No obstante, la utilización de la GEP es más económica, disminuye el tiempo de intervención, las necesidades de anestesia y el tiempo de recuperación en la mayoría de los casos. Asimismo, la posibilidad de reiniciar la nutrición a las 24 h permite disminuir el tiempo de ingreso12-14. Por todo ello, se considera que la GEP es preferible a la gastrostomía quirúrgica clásica. Con el desarrollo de la laparoscopia, la cirugía ofrece una nueva alternativa a la colocación de la sonda de gastrostomía15,16, incorporando a las ventajas de una técnica quirúrgica poco agresiva la de poder realizar cirugía antirreflujo asociada17.
La colocación de la gastrostomía por vía percutánea sin la utilización de endoscopia y con control radiológico tiene como ventajas sobre la GEP el precisar menos sedación y evitar las molestias y riesgos de la endoscopia. Diversos trabajos en los que se comparan los resultados de la utilización de la GEP con la colocación de la gastrostomía bajo control radiológico ponen de manifiesto resultados similares en cuanto a efectividad, con menor número de complicaciones con la técnica radiológica18-22. Por tanto, ésta es una buena alternativa a la GEP y tiene, además, indicaciones específicas, como las estenosis faringoesofágicas no franqueables. Sin embargo, la radiología intervencionista está poco difundida en nuestro medio y es raro contar con la posibilidad de utilizar las dos técnicas en el mismo centro.
La otra vía para mantener una nutrición enteral prolongada es la utilización de una sonda nasogástrica (SNG). Hay pocas publicaciones que comparen la utilización de la GEP con la alimentación por SNG. Aunque en un primer estudio publicado por Fay et al23 no se aprecian diferencias en cuanto a la utilización de las dos técnicas, en un estudio aleatorizado posterior publicado por Park et al24, se objetivó que los pacientes alimentados por GEP presentaban una recuperación de peso estadísticamente significativa y se les administraba una proporción mayor de la dieta. Un segundo estudio, de Norton et al25, confirma dichas diferencias y además demuestra una mortalidad mayor en el grupo de SNG a las 6 semanas. En otro trabajo, de Wicks et al26, al suspender la alimentación por SNG e iniciarla por GEP se demostró un aumento significativo de la curva ponderal y masa corporal. Por último, en un cuarto estudio aleatorizado en 90 pacientes27, se observó un mismo número de fracasos en la colocación de la sonda y de aspiración posterior y que los problemas de úlceras nasales (13%) y dolor a la deglución (17%) en el grupo SNG eran equiparables en frecuencia al dolor abdominal (12%) después de colocar la GEP. Sin embargo, en el 22% de los pacientes del grupo SNG frente a sólo el 7% en los del grupo GEP hubo que efectuar procedimientos de inmovilización para evitar la extracción de las sondas27. Este es un punto importante, pues nuestro objetivo no debe ser solamente alimentar al enfermo, sino intentar mejorar o mantener la calidad de vida del mismo. También en el enfermo consciente y colaborador la GEP es más cómoda que la SNG, que repetidamente se obstruye, es movilizada o se extrae de manera inadvertida y que por motivos estéticos provoca en ocasiones un innecesario aislamiento del paciente en su domicilio. En el citado estudio aleatorizado, 8 pacientes (20%) del grupo SNG tuvieron que interrumpir la nutrición por problemas de la sonda frente a ninguno en el grupo GEP. Por último, tanto los enfermos como las enfermeras que participaron en el estudio puntuaron la comodidad y utilización de la técnica, siendo la diferencia entre ambos grupos estadísticamente significativa en favor de la GEP. A raíz de estos estudios, la GEP es la alternativa de elección cuando se presuma que un paciente precisará soporte nutricional y tenga una expectativa de vida superior a un mes, y también en caso de supervivencia inferior, si la utilización de la GEP va a mejorar la calidad de vida del enfermo.
INDICACIONES
Nutrición
Como ya se ha comentado, la GEP se indica para mantener un acceso con el fin de nutrir a pacientes con sistema digestivo funcionante pero con incapacidad de tomar el alimento. Existen diversos tipos de indicaciones según la situación del enfermo y varias formas de clasificarlas.
Si miramos la indicación según la etiología de la enfermedad que produce la necesidad de colocar una vía de acceso para la nutrición, la causa más frecuente (90% de indicaciones) es la disminución de la capacidad de ingesta e incluye procesos neurológicos que producen disfagia neuromotora (demencia senil, accidentes vasculares, enfermedad de Alzheimer, esclerosis lateral amiotrófica, esclerosis múltiple, enfermedad de Parkinson, encefalopatía postanoxia, tumores y traumatismos craneales o parálisis supranuclear progresiva), enfermedades de la cavidad orofaríngea (tumores, quemados, traumatismos), enfermedades del esófago (tumores, fístulas, estenosis, cáusticos) y cuadros de anorexia28.
Un segundo grupo es el de los pacientes con requerimientos nutricionales aumentados o alterados que no se pueden suministrar por vía oral, como en politraumatismos29, grandes quemados30, enfermedad inflamatoria intestinal31 o fibrosis quística32.
Un tercer grupo de indicaciones lo constituyen alteraciones del sistema digestivo y de la absorción que se bene fician de una nutrición enteral (síndromes de intestino corto, enfermedad inflamatoria intestinal, pancreatitis crónica o enteritis actínica)33.
Finalmente, el cuarto grupo de indicación de la nutrición es una miscelánea formada por pacientes con enfermedad cardíaca congénita, insuficiencia renal crónica, metabolopatías congénitas, vómitos incoercibles (hiperemesis gravídica), enfermos con sida34 o epidermólisis bullosa con afectación esofágica.
En todos los posibles grupos o clasificaciones podemos distinguir, además, cuatro subgrupos según la intención de tratamiento. Un primer subgrupo de pacientes con enfermedad aguda, potencialmente recuperable, y en los que se prevé que el soporte nutricional se ha de mantener durante un período superior a las 3-4 semanas: éste sería el caso de traumatismos y hemorragias cerebrales, insuficiencias respiratorias que precisan traqueostomía e intubación por períodos prolongados, grandes quemados, procesos tumorales bucofaríngeos que recibirán radioterapia o enfermedades del sistema digestivo que se benefician de dietas elementales por períodos prolongados como enfermedad inflamatoria intestinal, síndrome de intestino corto o pancreatitis crónica. La expectativa en este grupo de pacientes es poder retirar la GEP al solucionarse el proceso que había motivado su colocación y reiniciar la dieta por vía oral. Sin embargo, esto sólo se consigue en un 6-21% de los casos28,35-37.
Un segundo subgrupo, seguramente el más numeroso, es el de los pacientes con enfermedades mayoritariamente neurológicas, progresivas y que producen disfagia neuromotora u obstructiva, en los que la GEP se coloca con carácter definitivo al ser procesos irreversibles. Serían los pacientes con esclerosis lateral amiotrófica, esclerosis múltiple, enfermedad de Alzheimer, arteriosclerosis, neoplasias faringoesofágicas, enfermedad de Parkinson, demencia senil o cuadros de caquexia terminal como en algunos pacientes con sida, en los que la gastrostomía contribuye a mejorar su calidad de vida.
Un tercer subgrupo, más conflictivo, formado por pacientes con un proceso patológico crónico no evolutivo con estados vegetativos, como postaccidentes vasculares o postanoxia o por encefalitis u otras causas, en los que la gastrostomía no sólo es definitiva sino contribuirá de forma significativa a mantener o alargar la expectativa de vida de estos enfermos. En estos casos, la indicación debe ser estudiada e individualizada y la decisión consensuada, valorando que si se decide mantener una nutrición enteral, en el ámbito asistencial, para familiares, enfermeras o cuidadores, la GEP es claramente más cómoda, fácil de cuidar y con menos complicaciones a largo plazo que los otros sistemas.
El cuarto subgrupo sería el de los pacientes con enfermedad crónica estable, pero esperanza de vida larga y adecuada calidad de vida, como disfagias neuromotoras post accidentes vasculares y estenosis esofágicas benignas refractarias a tratamiento. En este subgrupo, sin discusión, la GEP es la técnica de elección.
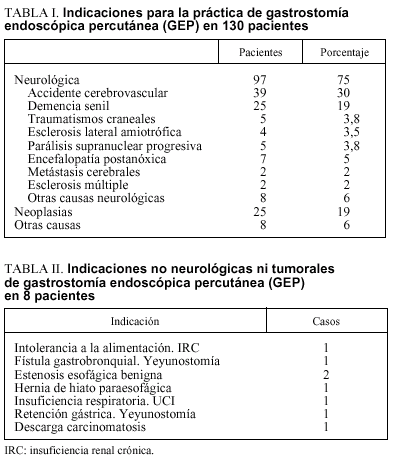
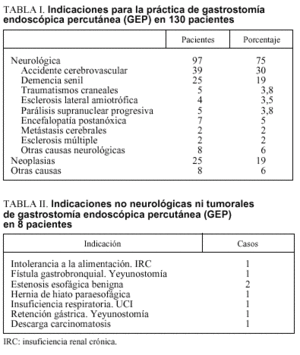
En nuestro centro, donde desde 1990 hemos colocado 130 GEP, las indicaciones (tabla I) siguen la tendencia de la mayoría de las series descritas. La indicación de nutrición más frecuente fue la enfermedad neurológica (74% de los casos). Un porcentaje importante tenía neoplasias orofaríngeas y esofágicas (25 pacientes, 19%). Finalmente, un pequeño grupo (tabla II) tenía indicaciones varias, entre las que destacan 2 pacientes con estenosis esofágica benigna refractarias a tratamiento endoscópico y no candidatas a tratamiento quirúrgico.
Un punto y aparte es la población pediátrica, en la que podemos encontrar indicaciones diferentes y la GEP ocupa un lugar importante para mantener el desarrollo y crecimiento de los pacientes. En la serie de Gauderer de 220 gastrostomías en niños37, las indicaciones fueron variadas. En 159 pacientes (72%) la indicación fue la incapacidad de tragar por anoxia cerebral, malformaciones orofaríngeas y laringotraqueales, cirugía facial, traumatismos faciales, alteraciones cromosómicas y metabólicas, miopatías y otras alteraciones neurológicas en los restantes casos. En 41 niños (18%) se utilizó para proporcionar suplementos alimentarios porque, a pesar de que los pacientes podían tragar, no recibían la alimentación suficiente. En este grupo se incluían pacientes con déficit de crecimiento, enfermedad cardíaca congénita, displasia broncopulmonar, neoplasias, atresia biliar, sida y alteraciones de la motilidad esofágica. En 13 pacientes (6%) la causa fue intestinal: enfermedad de Crohn, malabsorción, seudoobstrucción intestinal. En 5 niños con el síndrome de Alagille y en 2 con insuficiencia renal la GEP se colocó para la administración de la medicación. Finalmente, en un solo caso se utilizó la GEP como descompresión.
Indicaciones anecdóticas
Se han descrito múltiples indicaciones de las sondas de gastrostomía que no dejan de ser situaciones aisladas o anecdóticas, aunque eficaces en cada circunstancia. La más descrita es su utilización como sonda de descarga en obstrucciones intestinales (carcinomatosis peritoneal)38 o asociada a una yeyunostomía como descarga en estenosis gastroduodenales33, como sistema de fijación en vólvulos gástricos39, para ingerir medicaciones con mala tolerancia40,41, para reinfusión de bilis42 o como vía de abordaje para la práctica de endoscopia terapéutica43.
Neumonías por aspiración y yeyunostomía
Una indicación a comentar de forma individual es la de los pacientes referidos para GEP por presentar neumonías de repetición por aspiración, habitualmente en el contexto de una demencia senil o alteración neurológica. En este grupo hay que diferenciar si la aspiración se produce durante la ingestión, en cuyo caso la GEP puede ayudar en algunos casos a solucionar el problema aunque persistirá la aspiración de saliva44, o si se trata de aspiraciones por reflujo o vómito, en cuyo caso la colocación de una GEP no las evitará. Existen dos estudios que comparan la frecuencia de aspiración pulmonar antes y después de la colocación de la GEP. Olson et al45 estudiaron a 46 pacientes mediante gammagrafía antes y 7 días después de la colocación de la GEP y no encontraron cambios significativos. La mayoría de los pacientes presentaron el mismo patrón de reflujo antes y después de la GEP. En otro estudio, Hasset et al46 estudiaron a 87 enfermos. Veintinueve habían tenido neumonías por aspiración antes de la GEP y 35 tuvieron neumonía después de la colocación de la GEP. Dieciocho de los 29 con neumonías previas (62%) siguieron presentando neumonías posteriormente, así como 17 de los 58 que no la habían tenido con anterioridad (29%). La alternativa de colocar una sonda de yeyunostomía a través de la GEP, como medida para evitar las aspiraciones, no ha demostrado ser mejor que la GEP simple en la mayoría de los estudios realizados45,47-49, seguramente debido a que, por dificultades en la colocación de la sonda, ésta queda situada en duodeno proximal o por los frecuentes problemas de obstrucción y descolocación de la sonda que determinan su migración al estómago o bulbo. Existen evidencias de que, además, la presencia de una GEP favorece la retención gástrica50. Trabajos más recientes, sin embargo, demuestran que con una correcta colocación de la sonda en yeyuno o duodeno distal no existe reflujo y desaparece el riesgo de aspiración51. Esta técnica permite, además, mantenersimultá neamente una aspiración gástrica en casos de hipereme sis52, obstrucción o gastroparesia gástrica y la nutrición enteral. Posteriormente, se ha desarrollado, debido a las dificultades comentadas con anterioridad, la yeyunostomía endoscópica percutánea directa utilizando endoscopios largos (colonoscopio pediátrico) para alcanzar el yeyuno y colocar directamente la sonda en el mismo, una vez pasado el ángulo de Treitz. La yeyunostomía no se asocia a reflujo de alimento a estómago ni alteración de la motilidad gástrica53. Se puede asociar a una GEP para aspiración gástrica si la indicación es por obstrucción o dificultad de vaciado gástrico54.
CONTRAINDICACIONES
No existen contraindicaciones absolutas a la colocación de la GEP, aunque existe un grupo de enfermedades asociadas que debido al riesgo de complicaciones inmediatas y de fracaso de la técnica se catalogan como contraindicaciones relativas. Según la Asociación de Endoscopia Digestiva Americana55 éstas serían la presencia de ascitis significativa, obesidad mórbida y neumonía por aspiración secundaria a reflujo gastroesofágico. Otras contraindicaciones relativas que mencionan la mayoría de los autores son la presencia de coagulopatía, hipertensión portal y cirugía gástrica previa.
En un 2-8% de los casos, la GEP no se puede realizar al no conseguir transiluminar o identificar el estómago situado directamente sobre pared anterior de abdomen, debido a interposición de otras vísceras (hepatomegalia, colon), situación anómala del estómago, cirugía previa, malformaciones, ascitis u obesidad mórbida28,35,36. La gastrostomía bajo control radiológico o quirúrgica son las alternativas en estos casos.
COMPLICACIONES
Complicaciones graves
Las complicaciones asociadas a la GEP son en general leves y fácilmente tratables. La incidencia de complicaciones menores es de un 4-25% según las series. La incidencia de complicaciones más graves es de un 1-4%. La mortalidad relacionada con la técnica es inferior al 1%56. En nuestra experiencia hemos registrado un 10% de complicaciones tanto inmediatas como en el seguimiento (tabla III)35,57. Las complicaciones más severas son la broncoaspiración, peritonitis, hemorragia, fascitis necrohemo rrágica y aparición de fístulas gastrocólicas. La aspiración broncopulmonar puede ocurrir en cualquier momento durante la colocación de la GEP o al iniciar la alimentación. La aspiración inmediata tiene una incidencia de un 0,7-1,6% y se acompaña de una mortalidad del 50%10,28. La prevención desempeña aquí un papel principal. La exploración debe realizarse en el menor tiempo posible, evitando la sedación excesiva y con aspiración de secreciones durante la realización de la prueba y posteriormente. Si la sedación se realiza con midazolán su reversión con flumazenilo favorece el período de recuperación del paciente. Es importante asegurarse de que no existe un íleo paralítico o retención gástrica antes de iniciar la dieta, y se debe mantener al paciente en una inclinación de 30 grados para evitar el reflujo. La neumonía por aspiración no inmediata ocurre hasta en un 35% de los pacientes y es una de las causas principales de muerte55. La presencia de neumonías previas y de esofagitis por reflujo son los únicos factores de riesgo identificados en 2 estudios44,58. Como ya hemos comentado anteriormente, la colocación de una sonda de yeyunostomía, tanto directa como a través de la GEP, son las alternativas cuando exista el antecedente de neumonía por aspiración, aunque su utilidad aún no esté totalmente probada. En nuestra serie, la neumonía ha sido la complicación más frecuente y temible. De los pacientes referidos para la colocación de una GEP, 44 habían tenido previamente uno o más episodios de neumonía por aspiración (30%). Hubo 6 neumonías por aspiración en el seguimiento de estos enfermos durante los primeros 30 días y cuatro de ellos fallecieron. Todos habían presentado neumonías previas a la GEP. Sólo en un caso la aspiración se produjo el día de la prueba, seguramente secundaria a un exceso de sedación; el resto de las aspiraciones por reflujo se produjeron en el proceso de alimentación del paciente.
En la población pediátrica, la aparición de reflujo gastro esofágico no detectado previamente ocurre hasta en un 24% de los pacientes al colocar la GEP59 y un porcentaje significativo de éstos precisará la realización de cirugía antirreflujo para su control37,59.
La peritonitis ocurre en un 0-1,2%, y está relacionada con el momento de la colocación de la GEP o provocada por el arrancamiento precoz de la sonda antes de que se forme el trayecto fistuloso, es decir, antes de los primeros 14-20 días28,56,60,61. La colocación endoscópica precoz de una nueva sonda de GEP por el trayecto de la anterior, en los casos de autoextracción precoz de la sonda, previene la aparición de peritonitis y la necesidad de cirugía. Pasado este tiempo, el tracto fistuloso permite la extracción de la sonda y la introducción de una nueva con poco riesgo de perforación y de peritonitis. En pacientes agitados, en los que existe el riesgo de autoarrancamiento, se debe mantener la sonda tapada durante los primeros días. También es importante no confundir la presencia de un neumoperitoneo, hecho bastante frecuente (36-38%)62 después de la colocación de la GEP y que se resuelve espontáneamente, con un cuadro de peritonitis. Si existen dudas se debe realizar un estudio radiológico con contraste antes de intervenir al paciente.
La hemorragia es una complicación poco frecuente y se relaciona en general con la formación de úlceras en el lugar de la gastrostomía debidas a un exceso de tracción de la sonda63. La endoscopia para confirmar el diagnóstico y terapéutica, además de aflojar el tope externo suele ser suficiente en la mayoría de los casos.
La fascitis necrosante, aunque infrecuente y descrita en muy pocos casos, es una complicación grave64-65. Se caracteriza por necrosis importante de las capas superficiales de la fascia. Si no se diagnostica y se trata agresivamente mediante desbridamiento quirúrgico conlleva una alta mortalidad. Aparece a los 4-14 días de la intervención con fiebre, dolor, celulitis, edema de piel y ocasionalmente crepitación. Se ha descrito en pacientes malnutridos o con diabetes, enfermedad cardíaca u obesidad. La falta de profilaxis antibiótica, la realización de una incisión abdominal demasiado pequeña, dejar la GEP fijada con demasiada tensión, y la obesidad se han descrito como otras posibles etiologías contribuyentes64-66.
La fístula gastrocólica es otra complicación poco frecuente pero grave, debida a la inadvertida interposición del colon entre el estómago y la pared abdominal. No se detecta hasta meses después de la colocación de la GEP, con frecuencia con el primer recambio de sonda. Se manifiesta por diarrea o por aspiración de contenido fecaloide por la sonda. Normalmente con la retirada de la sonda se soluciona el problema67, la mejor forma de evitarla es realizar todos los pasos de la técnica correctamente, en especial el mantenimiento de la máxima insuflación del estómago durante todo el proceso de punción.
Otra complicación, que precisa en ocasiones de tratamiento quirúrgico, es el denominado en términos anglosajones buried bumper syndrome, que consiste en la incarceración submucosa o en el tracto fistuloso del tope interno de la sonda debido a excesiva tracción, en ocasiones como consecuencia del aumento progresivo de peso y de grosor de la pared abdominal del paciente, sin que éste se acompañe de una disminución de presión entre los topes. Esta complicación era especialmente frecuente con un determinado equipo comercial, el cual ya ha sido retirado del mercado. La utilización de sondas extraíbles por tracción, sin endoscopia hacen que la solución de este problema sea fácil, pues basta retirar la sonda traccionándola y recambiarla.
Complicaciones leves
Entre las complicaciones leves debemos destacar la infección de la herida como la más frecuente. Su incidencia varía según las series del 0 al 30%28,35,52,56,61. La utilización de antibióticos de forma profiláctica es discutida. Un estudio controlado demostró que la administración de 1 g de cefazolina 30 min antes de la prueba se asociaba a la disminución en la aparición de infección de la herida de un 30 a un 7,4%68. Otros estudios sin embargo, no demuestran una menor tasa de infección después de la utilización de los mismos antibióticos69,70. La mayoría de las bacterias aisladas en los cultivos de la herida son estafilococos, pseudomonas y otros bacilos grampositivos que colonizan la faringe de los enfermos hospitalizados y que son arrastrados por la sonda. Con la utilización de una pomada triantibiótica para lubrificar la sonda de gastrostomía a su paso por faringe y realizando una incisión amplia para evitar acumulación o retención de secreciones hemos conseguido mantener unas tasas de infección por debajo del 5%35. El tratamiento de la infección de la herida de la gastrostomía es en principio médico, con antibióticos dirigidos por cultivos y antibiograma, disminuyendo la presión entre los topes de la sonda, limpiando bien la herida y, si es preciso, ampliando la incisión. El desbridamiento quirúrgico y la retirada de la sonda se realizan cuando con estas medidas no podemos solucionar la infección y existe celulitis y absceso de pared. La sonda de gastrostomía se ha identificado como lugar de colonización Staphylococcus aureus meticilín-resistente71.
Otras complicaciones leves asociadas a la técnica son la presencia de íleo paralítico que se resolverá espontáneamente en 48-72 h, fiebre, dolor abdominal y formación de un hematoma en la pared abdominal. Todas ellas ocurren en menos de un 1% de los casos. Tardíamente se describen con más frecuencia la obstrucción de la sonda y la salida de alimentación o secreción gástrica por los bordes de la herida, así como el deterioro de la sonda, que obligan a su recambio.
Se han comunicado varios casos de metástasis de tumores ORL o esofágicos en el estómago o el trayecto de la gastrostomía. En todos los casos se había utilizado la técnica de tracción72.
MORTALIDAD Y FACTORES DE RIESGO
La mortalidad asociada a la técnica de colocación de la GEP es de un 0,6-1% y se relaciona con hipersedación, aspiración, laringospasmo, peritonitis e insuficiencia cardíaca8,28,35,60,61,73-75. La mortalidad a los 30 días varía entre un 10 y un 26%8,28,35,60,61,73-76, siendo la aspiración que co mo hemos comentado aparece hasta en el 35% de los casos la causa principal. Taylor et al76 realizaron un estudio controlado en un grupo de población con 97 enfermos remitidos para GEP. La probabilidad de supervivencia a los 30 días era del 78%. Identificaron la edad avanzada, el sexo masculino y la diabetes como factores de riesgo. En otro estudio, Light et al77 analizan los factores predictivos de mortalidad mediante análisis multivariado de regresión logística en 416 pacientes a los que se les colocó una GEP. La mortalidad a los 7 y 30 días fue de 9,4 y del 23,3%, respectivamente. La presencia de aspiración previa e infección de orina eran factores de riesgo a los 7 días, de forma que los pacientes con ambos factores tenían un riesgo del 48,8% de mortalidad en este período de tiempo frente al 4,3% de los que no tenían ninguno. Ambos factores y la edad superior a 75 años eran factores predictivos de mortalidad a los 30 días. Los pacientes con los tres factores tenían una mortalidad del 76,1% a los 30 días frente a un 10% los que no tenían ningún factor. Parece prudente, por tanto, no realizar una GEP a pacientes de edad con antecedentes de aspiración y que tengan una infección activa. En estos casos, nosotros los mantenemos 3-4 semanas con sonda nasogástrica y revaluamos la presencia o persistencia de infección, colocando la GEP si se ha resuelto la misma. Otros 2 estudios posteriores identifican una cifra baja de albúmina sérica como el único factor de riesgo de mortalidad a los 30 días78.
CONCLUSIÓN
En conclusión, la GEP es una técnica sencilla de realizar, fácil de aprender, con poca morbilidad y baja mortalidad inmediata. Debe considerarse como técnica de elección en pacientes incapaces de alimentarse o mantener sus necesidades nutricionales por vía oral con sistema digestivo indemne, y en los que se presupone que necesitarán el soporte nutricional durante un período de más de 4 semanas. En todos los casos debe individualizarse la indicación, proporcionarse una amplia explicación al paciente y familiares y valorarse los factores de riesgo de presentar complicaciones. La neumonía por aspiración es la complicación más frecuente, especialmente en los pacientes referidos para la colocación de una GEP que presenten una historia de aspiraciones previas. Se deben realizar estudios controlados para valorar el papel y utilidad de la yeyunostomía endoscópica directa en estos pacientes.
Correspondencia: Dr. J.I. Arenas Miravé. Servicio de Aparato Digestivo. Hospital Aránzazu. San Sebastián.