La infección por el virus de la hepatitis A (VHA) se transmite principalmente por vía fecal-oral; mientras que en regiones endémicas el virus se adquiere en la niñez, en países desarrollados la infección suele adquirirse en la edad adulta en relación con la ingesta de agua o alimentos contaminados, viajes a áreas endémicas o prácticas sexuales de riesgo. La clínica de la hepatitis aguda A es indistinguible de otros tipos de hepatitis aguda; en casos excepcionales puede evolucionar a hepatitis fulminante aunque lo más habitual es que se resuelva de forma espontánea, sin tratamiento específico y sin secuelas1.
La vacuna anti-VHA es altamente eficaz. En Cataluña está vigente un programa piloto desde el curso escolar 1998-1999 hasta el 2013-2014 por el que se administra la vacuna anti-hepatitis A (combinada con la B) a los niños2.
Presentamos el caso de una paciente de 15 años, correctamente vacunada según el calendario vigente, que presentó una hepatitis aguda A.
Mujer de 15 años de edad sin alergias conocidas, hábitos tóxicos ni antecedentes patológicos de interés. Se comprobó la correcta vacunación anti-VHA en el medio escolar mediante la presentación del carné de vacunación debidamente cumplimentado.
La paciente debutó con fiebre hasta 39°C de 2 semanas de evolución y de predominio vespertino, síndrome constitucional, vómitos posprandiales y aparición de odinofagia. Posteriormente presentó ictericia motivo principal por el cual acudió a urgencias.
En el momento del ingreso presentaba ictericia en piel y mucosas, sin lesiones cutáneas. Se observó eritema faríngeo, pequeñas placas de 1-2mm de diámetro blanquecinas de forma bilateral y adenopatías en la región laterocervical, axilar izquierda e inguinal derecha. En la exploración abdominal destacaba una discreta esplenomegalia no dolorosa. En la analítica se halló: bilirrubina total de 8,27mg/dl, GGT 165U/l, FA 511U/l, GOT 284U/l, GPT 253U/l, leucocitos 12.790/mm3 (68% de linfocitos), Hb 9,9g/dl y TP 72,7%. En la ecografía abdominal se identificó la presencia de hepatoesplenomegalia, sin otros hallazgos significativos. Las determinaciones de anticuerpos heterófilos, citomegalovirus (IgG<4 UI/ml, IgM 0,49 UI/ml), VHC, virus de la inmunodeficiencia humana (VIH), HBsAg y HBcAc (IgM) fueron negativas; el anticuerpo IgM del VHA resultó positivo. Se comunicó el caso al Área de Vigilancia Epidemiológica del Departamento de Salud de la Generalitat de Catalunya.
Al segundo día de ingreso la paciente presentó una reacción cutánea caracterizada por lesiones papulares pruriginosas de 1-2mm de diámetro que afectaban a cara, tronco y las 4 extremidades (fig. 1). Se orientó como una reacción «Gianotti-Crosti-like». En el momento del alta, el perfil hepático había mejorado de forma significativa. En el control postalta al cabo de un mes la paciente estaba asintomática y el perfil hepático se había normalizado por completo.
España es un país de baja endemicidad para la hepatitis A. La prevalencia de anticuerpos anti-VHA en Cataluña es de 34-49% para individuos entre 20-29 años y del 42-59% para aquellos entre 30-39 años3. Las tasas de incidencia en Barcelona ciudad oscilaron entre 4,7-6,9 casos/100.000h entre 2006-2010.
La vacuna anti-VHA se administra en 2 dosis. En la población general el 95% desarrollan niveles protectores de anticuerpos tras la primera dosis y un 100% tras la segunda4. Sin embargo, en pacientes infectados por el VIH, el porcentaje disminuye sensiblemente (entre 52-94%). La mayoría de los datos sugieren que, en los casos en los que la viremia del VIH está controlada, la cifra de CD4 no influye en la eficacia de la vacuna5. Factores como la edad, el sexo y la obesidad pueden afectar a la inmunogenicidad de la vacuna anti-VHA aunque, en la mayoría de los casos, se alcanzan títulos protectores sin que la eficacia se vea comprometida. Alteraciones en la conservación de la vacuna, pautas incompletas o la urgencia de mutantes de escape son otras causas que se han implicado en el fracaso de la misma1.
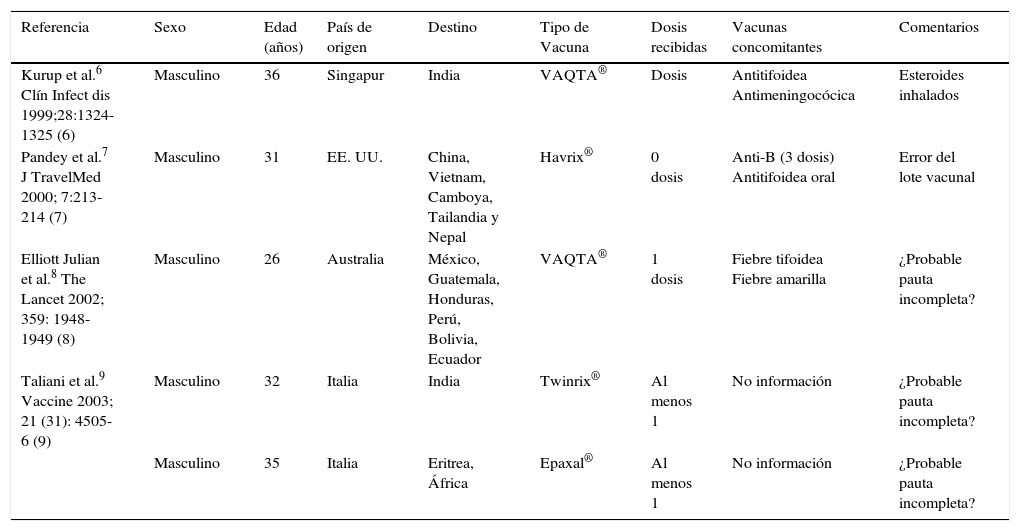
Hasta la fecha se han publicado muy pocos casos de fracaso de la vacuna anti-VHA6–9 (tabla 1). En todos menos uno, se trata de varones jóvenes que viajan a países endémicos y desarrollan síntomas al regreso de su viaje. Solo en uno de ellos se demostró un error en el lote vacunal, de manera que el paciente realmente no había recibido ninguna dosis7. En el resto, existe la sospecha de que la pauta de vacunación fuera incompleta. El único de los casos descritos que no corresponde a un viajero es el de un varón homosexual, VIH positivo, que había sido vacunado correctamente. A posteriori se averiguó que no había desarrollado anticuerpos protectores10.
Casos descritos de fallo de vacuna anti-VHA en viajeros a zonas endémicas
| Referencia | Sexo | Edad (años) | País de origen | Destino | Tipo de Vacuna | Dosis recibidas | Vacunas concomitantes | Comentarios |
|---|---|---|---|---|---|---|---|---|
| Kurup et al.6 Clín Infect dis 1999;28:1324-1325 (6) | Masculino | 36 | Singapur | India | VAQTA® | Dosis | Antitifoidea Antimeningocócica | Esteroides inhalados |
| Pandey et al.7 J TravelMed 2000; 7:213-214 (7) | Masculino | 31 | EE. UU. | China, Vietnam, Camboya, Tailandia y Nepal | Havrix® | 0 dosis | Anti-B (3 dosis) Antitifoidea oral | Error del lote vacunal |
| Elliott Julian et al.8 The Lancet 2002; 359: 1948-1949 (8) | Masculino | 26 | Australia | México, Guatemala, Honduras, Perú, Bolivia, Ecuador | VAQTA® | 1 dosis | Fiebre tifoidea Fiebre amarilla | ¿Probable pauta incompleta? |
| Taliani et al.9 Vaccine 2003; 21 (31): 4505-6 (9) | Masculino | 32 | Italia | India | Twinrix® | Al menos 1 | No información | ¿Probable pauta incompleta? |
| Masculino | 35 | Italia | Eritrea, África | Epaxal® | Al menos 1 | No información | ¿Probable pauta incompleta? |
La peculiaridad de nuestro caso radica en que se trata de una adolescente correctamente vacunada y que no presenta ninguno de los factores de riesgo que se han relacionado con el fallo vacunal. Se comprobó el lote vacunal y se investigó si había habido más casos en su colegio. Este caso demuestra que, ante un cuadro clínico y analítico compatible, debemos descartar la hepatitis aguda A a pesar de una pauta de vacunación correcta. La comunicación de los casos a las autoridades sanitarias permitirá establecer la frecuencia de estos fallos vacunales y la necesidad de cambiar las pautas de profilaxis en colectivos de riesgo.