Sr. Director: Bupropión es un antidepresivo monocíclico cuyo mecanismo de acción está basado en inhibir la recaptación neuronal de catecolaminas e indolaminas1. Se utiliza principalmente en el tratamiento de la depresión y la dependencia al tabaco2. Se desconoce el mecanismo por el cual bupropión potencia la actividad de los pacientes a abstenerse de fumar. No obstante, se supone que en esta acción intervienen mecanismos noradrenérgicos y/o dopaminérgicos.
Presentamos un caso de hepatitis aguda por bupropión.
Varón de 48 años de edad, que consultó por presentar ictericia cutaneomucosa y coluria en los últimos 4 días. Entre sus antecedentes personales destacaba: etilismo crónico y fumador de 20 cigarrillos al día.
Dos meses antes había comenzado un tratamiento con disulfiram y naltrexona para la deshabituación del alcohol. Además, en el segundo mes añadió bupropión como tratamiento deshabituador del tabaco. Inició con 150 mg de bupropión diarios, que aumentó al doble al cabo de 15 días. A los 15 días del aumento de la dosis presentó una ictericia cutaneomucosa, que motivó su consulta. La exploración física mostró una hepatomegalia de 2 cm e ictericia mucocutánea.
Los hallazgos analíticos relevantes fueron: ALT 1.405 (valores normales [VN], 10-40 U/l), AST 473 (8-30 U/l), GGT 647 U/l (10-30 U/l), FA 803 (90-360 U/l), billirrubina total/directa 12,14/6,2 mg/dl, actividad de protrombina 68%, ANA positivo 1/80, y AMA positivo 1/80. Hemograma, α1-antitripsina y ceruloplasmina normales. SMA negativo. La serología para virus A, B, C y VIH fue negativa. La ecografía abdominal fue normal, con la excepción de hepatomegalia homogénea. En la tabla I se muestra la evolución de las alteraciones analíticas, con normalización de las transaminasas y bilirrubina a los 77 días del inicio del cuadro. Actualmente, el paciente sigue tomando alcohol y presenta una ligera elevación de los parámetros hepáticos con negativización de ANA y AMA.
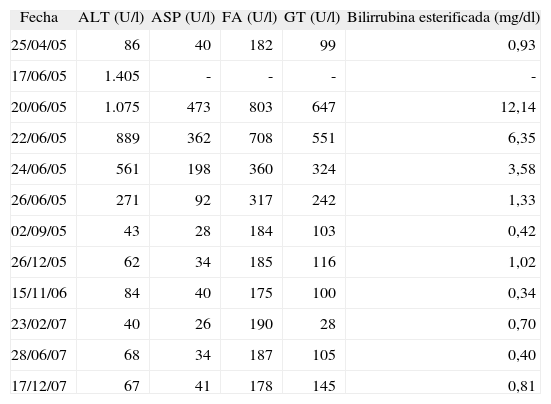
Evolución de los valores de transaminasas y bilirrubina
| Fecha | ALT (U/l) | ASP (U/l) | FA (U/l) | GT (U/l) | Bilirrubina esterificada (mg/dl) |
| 25/04/05 | 86 | 40 | 182 | 99 | 0,93 |
| 17/06/05 | 1.405 | - | - | - | - |
| 20/06/05 | 1.075 | 473 | 803 | 647 | 12,14 |
| 22/06/05 | 889 | 362 | 708 | 551 | 6,35 |
| 24/06/05 | 561 | 198 | 360 | 324 | 3,58 |
| 26/06/05 | 271 | 92 | 317 | 242 | 1,33 |
| 02/09/05 | 43 | 28 | 184 | 103 | 0,42 |
| 26/12/05 | 62 | 34 | 185 | 116 | 1,02 |
| 15/11/06 | 84 | 40 | 175 | 100 | 0,34 |
| 23/02/07 | 40 | 26 | 190 | 28 | 0,70 |
| 28/06/07 | 68 | 34 | 187 | 105 | 0,40 |
| 17/12/07 | 67 | 41 | 178 | 145 | 0,81 |
Bupropión se considera un agente antidepresivo seguro y bien tolerado. Ensayos preclínicos anteriores realizados en animales, que recibían altas dosis de bupropión durante prolongados períodos, mostraron alteraciones hepáticas reversibles tras el cese del tratamiento. Ensayos clínicos de precomercialización mostraron una incidencia < 1% en la alteración de las enzimas hepáticas3–5. Otros 2 ensayos clínicos aleatorizados sobre la terapia con bupropión para dejar de fumar no mostraron ningún efecto adverso hepático durante las 7 y 9 semanas que duró el tratamiento6.
No se conoce el mecanismo por el cual se produce el daño hepático. Describimos el caso de un paciente que tenía una ligera hipertransaminasemia y que desarrolló una hepatitis aguda a las 4 semanas de iniciar el tratamiento con bupropión con posterior normalización de los parámetros hepáticos tras la suspensión; además, hemos descartado de forma razonable otras etiologías.
Una búsqueda bibliográfica en MEDLINE nos permitió encontrar otros 4 casos de hepatitis aguda producida por bupropión desde el comienzo de su uso. Los 2 primeros7,8 se caracterizaban, al igual que el nuestro, por un aumento de las transaminasas y la bilirrubina a los 54 y 41 días de iniciar tratamiento, valores que se normalizaron a los 10 y 11 días, respectivamente, de su suspensión. Además, en el caso de Oslin, el paciente fue nuevamente tratado con bupropión, con lo que se produjo un nuevo aumento de las transaminasas al cabo de 4 días, valores que se normalizaron a los 35 días de suspenderlo. El tercer caso9 destacó por ser el primero de una hepatitis colestásica secundaria a bupropión con unos valores de bilirrubina que fueron anormales, aun después de suspender el tratamiento. Este caso, junto con el segundo y el nuestro, además se caracterizó por la presencia en sangre de anticuerpos ANA, que desaparecieron al cesar el tratamiento. El último y más reciente episodio10 ocurrió tras 6 meses de tratamiento con bupropión y es el único que ha tenido un desenlace fatal.