Sr. Director: El infliximab está indicado como tratamiento de inducción y de mantenimiento en la enfermedad de Crohn fistulizante y en los brotes moderados-graves refractarios a la terapia habitual1,2. También está demostrada su efectividad en el tratamiento de la artritis reumatoide3, la psoriasis, la artritis psoriásica y la espondilitis anquilosante4. A pesar de su seguridad probada, tiene un amplio perfil de efectos secundarios, y la hepatotoxicidad es uno de los menos frecuentes4,6-10. Exponemos el caso de una paciente que presentó toxicidad hepática tras la tercera infusión de infliximab y tras la reintroducción de este fármaco 5 meses después.
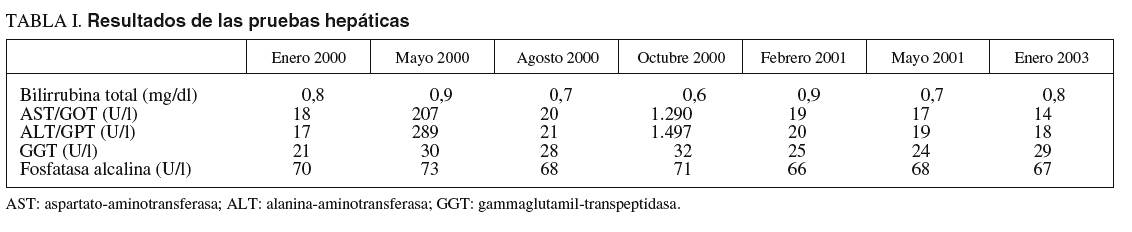
Mujer de 43 años, diagnosticada de enfermedad de Crohn con afección cólica de 10 años de evolución, en tratamiento con mesalazina desde el momento del diagnóstico y corticodependiente desde 1998, con dosis mínima necesaria de 15 mg/día de prednisona, a pesar de la cual presentaba 2-3 episodios anuales de reagudización de su enfermedad. Inició tratamiento con azatioprina en enero de 1999, presentando tras la segunda dosis un cuadro de pancreatitis aguda que obligó a su suspensión. Un mes después inició un tratamiento con metotrexato a dosis de 25 mg/semana por vía intramuscular, a pesar de lo cual no pudo retirar el tratamiento esteroideo ni prevenir la aparición de nuevos brotes, presentando una fístula rectovaginal de alto débito en enero de 2000. Se suspendió el metrotexato y se inició tratamiento con infliximab a dosis de 5 mg/kg en infusiones a las 0,2 y 6 semanas (la primera dosis se administró en abril de 2000). Tras la tercera infusión presentó un cuadro de ligera elevación de transaminasas (tabla I) que se autolimitó al cabo de 3 meses. Los fármacos concomitantes en aquel momento eran mesalazina (1 g/8 h v.o) y prednisona (15 mg/día v.o). La paciente se encontraba asintomática y la exploración física no mostró hallazgos de interés. Se descartó por la historia clínica la ingesta de alcohol, otros fármacos o tóxicos, u otros antecedentes epidemiológicos de interés. Las serologías virales, los autoanticuerpos, el metabolismo cúprico, férrico, alfa-1-antitripsina, anticuerpos antiendomisio, y el estudio de profirinas en heces y orina fueron negativos. La ecografía abdominal fue normal. La respuesta al fármaco fue parcial pero permitió una reducción notoria en el débito y la sintomatología de la fístula rectovaginal, volviendo a empeorar al cabo de 5 meses de la última dosis. Se reintrodujo el tratamiento con infliximab en octubre de 2000, y tras la primera infusión presentó una notable elevación de las transaminasas (tabla I) acompañada de astenia y malestar general sin ictericia, lo que obligó a suspenderlo, normalizándose la analítica en febrero de 2001. De nuevo el estudio etiológico de la hipertransaminasemia fue negativo. La paciente se negó a la realización de biopsia hepática. En los sucesivos controles analíticos practicados desde entonces no se ha vuelto a constatar ninguna alteración significativa en la bioquímica hepática, y en la actualidad la paciente sigue tratamiento con leucoaféresis.
El infliximab se ha demostrado eficaz como tratamiento en los brotes moderados-graves de la enfermedad de Crohn resistentes a la terapia convencional, tanto en la inducción como en el mantenimiento de la remisión, y en la enfermedad fistulizante1-3. En la actualidad se estudia su utilidad en el tratamiento de algunas manifestaciones extraintestinales de la enfermedad de Crohn2,3, como la espondilitis anquilopoyética, la sacroileítis, el pioderma gangrenoso, la artritis, la enfermedad perineal, orofacial y esofágica y la pouchitis. El infliximab es un fármaco seguro y bien tolerado, pero no está exento de efectos secundarios1-4,6-10. Se han descrito reacciones postinfusión, de hipersensibilidad, infecciones (oportunistas, reactivaciones tuberculosas...), artromialgias, formación de anticuerpos anti-ADN, ANA, síndrome lupus-like, etc. Entre los efectos adversos gastrointestinales, podemos destacar los siguientes: náuseas, vómitos, dolor abdominal, meteorismo, colecistitis, suboclusión intestinal y estomatitis.
Existen pocos casos recogidos en la bibliografía sobre la hepatotoxicidad en relación con infliximab, la mayoría de ellos en pacientes con enfermedades reumatológicas3,4,7 y/o reactivaciones de hepatopatías virales subyacentes8,9. Las hepatitis secundarias a anticuerpos anti-TNF en pacientes con enfermedad de Crohn sin ninguna enfermedad reumatológica asociada ni hepatopatía de base, como en el caso que presentamos, son muy poco frecuentes6,10. El hecho de que en nuestra paciente la hipertransaminasemia recidivara tras la reintroducción del fármaco, y con mayor gravedad, pone de manifiesto una evidente relación causa-efecto entre la infusión de las dos últimas dosis del infliximab y la aparición de toxicidad hepática, lo que se confirma al aplicar la escala de probabilidad modificada de Naranjo6; todo esto implica al infliximab como el factor etiopatogénico más probable en el desarrollo de la hepatotoxicidad en nuestra paciente.