La supervivencia del cáncer colorrectal es del 57% a los 5 años, en parte debido a un diagnóstico tardío por una baja participación en los programas de cribado. Son necesarios instrumentos que analicen las causas de participación.
ObjetivoComprobar la validez y consistencia interna de la versión en castellano del cuestionario de Rawl para el cribado de cáncer colorrectal con sangre oculta en heces.
Tipo de estudioMetodología de validación de cuestionarios.
LocalizaciónTres centros de salud de Valencia.
VariablesEdad, sexo, estado civil, nivel de estudios, clase social, consumo de tabaco, alcohol, índice de masa corporal, antecedentes personales y familiares de cáncer.
ResultadosSe estudiaron 408 individuos (237 casos y 171 controles). La edad media fue de 59,45 (DE 5,17) años. La consistencia interna de todas las variables alcanzó una alfa de Cronbach de 0,796. El alfa de Cronbach de la dimensión beneficios del cribado fue de de 0,871 y para la dimensión barreras al cribado fue de 0,817. Los coeficientes de correlación intraclase del test-retest para la dimensión de los beneficios del cribado fue de 0,809 (IC 95% 0,606-0,913) y de 0,499 (IC 95% 0,126-0,750) para las barreras.
ConclusiónLa versión en castellano del cuestionario Rawl es válido, fiable y reproducible. Con lo que disponemos de un elemento validado en España con el que objetivar barreras y beneficios percibidos en un programa de cribado poblacional.
Colorectal cancer 5-years-survival is 57%, partway due to a low rate of participation in screening programmes. Instruments analyzing causes of low adherence are needed.
ObjectiveTo evaluate the validity and internal consistency of the Spanish version of Rawl's Questionnaire for the screening of colorectal cancer by faecal occult blood testing.
Type of studyQuestionnaire validation methodology.
LocationThree Primary Care Centres in Valencia.
VariablesAge, sex, civil status, educational level, social class, smoking, alcohol consumption, body mass index, personal and family history of cancer.
ResultsWe analyzed 408 individuals (237 cases and 171 controls). Mean age was 59.45 years (SD 5.17). Internal consistency of all variables reached a Cronbach's alfa of 0.796. The Cronbach's alfa benefit dimension of the screening was 0.871 and for the barrier dimension of the screening it was 0.817. Intraclass correlation coefficients of the test-retest for the benefit dimension of the screening was 0.809 (CI 95% 0.606-0.913) and 0.499 (CI 95% 0.126-0.750) for the barrier dimension.
ConclusionThe Spanish version of Rawl's Questionnaire is valid, reliable and reproducible, so we have this validated instrument with which to identify barriers and benefits in a colorectal screening programme in Spain.
El cáncer colorrectal (CCR) en España, representa la segunda causa de muerte por cáncer, registrándose más de 15.000 muertes por año1. En incidencia, es también la segunda neoplasia más frecuente, después del cáncer de próstata en el hombre y del cáncer de mama en la mujer, pero ocupa el primer lugar si no se hace distinción de sexo, estimándose 44.231 nuevos casos en el 20202.
La supervivencia media del CCR en nuestro país es tan solo del 57% a los 5 años del diagnóstico. La supervivencia de los pacientes con CCR detectados dentro de un programa de cribado es superior a la de los pacientes diagnosticados por síntomas3. En el cribado para la población de riesgo medio (individuos mayores de 50 años sin factores de riesgo adicionales) la estrategia utilizada es la detección de sangre oculta en heces (SOH) bianual4. Aunque la cobertura de los programas de cribado es prácticamente universal en nuestro país, la participación en los mismos sigue siendo inferior al 50% y la mayor parte de los CCR en nuestro medio se siguen diagnosticando fuera de los programas de cribado5.
Existen tres grupos de factores asociados a la adhesión: relacionados con la organización del programa de cribado6, relacionados con factores sociales7 y dependientes de la visión del sujeto. En este último factor se han adoptado diferentes modelos teóricos en un intento de entender los elementos subjetivos del individuo que influyen en la participación. El modelo más estudiado es el Modelo de Creencias en la Salud o Health Belief Model (HBM) descrito por Rosenstock8,9.
Este modelo describe varios conceptos cognitivos que predicen el comportamiento en actividades preventivas: susceptibilidad percibida, severidad percibida, autoeficacia, beneficios y barreras10. En este sentido Jacobs adaptó para el cribado del cáncer colorrectal el cuestionario que Champion inicialmente había desarrollado para el cribado de cáncer de mama11. Rawl validó en Estados Unidos un cuestionario específico para cada prueba de cribado: SOH, sigmoidoscopia y colonoscopia12. El cuestionario de Rawl basado en el HBM se validó en diversos países y en distintas poblaciones y es el más difundido en la bibliografía13–15.
En el momento actual, existen escasos datos sobre los posibles factores favorecedores o limitadores de la participación en un programa de cribado poblacional de CCR en España. Es necesario tener instrumentos que midan con fiabilidad estas variables. Por ello, el objetivo de este estudio es comprobar la validez y consistencia de la versión en castellano del cuestionario Rawl de cribado de CCR con SOHi.
Material y métodosEste es un estudio de validación de cuestionario, incluido dentro de un estudio más amplio de casos y controles. Se ha realizado en los centros de salud Chile, República Argentina y Serrería II de la ciudad de Valencia. Para una prevalencia esperada de bajo apoyo social del 30%, un intervalo de confianza del 95%, una potencia del 80% y una odds ratio de 2, el número necesario de individuos a incluir en el estudio era de 404. Por lo que se realizó un muestreo aleatorizado simple confiando encontrar un número similar de casos y controles, dado que la participación en estos programas de cribado ronda el 50%.
El criterio de inclusión fue que los individuos hubieran sido invitados a participar en el Programa de Cribado de Cáncer Colorrectal de la Comunitat Valenciana, en el cual se invita a todos los individuos entre 50 y 69 años que no tengan síntomas y que no presenten ninguno de los criterios de exclusión permanente para participar en los programas de cribado de CCR (antecedentes personales de CCR, enfermedad inflamatoria intestinal, poliposis colorrectal, adenoma colorrectal, colectomizados, comorbilidad grave o antecedentes familiares de poliposis adenomatosa familiar u otros síndromes polipósicos hereditarios, cáncer colorrectal hereditario no asociado a poliposis, dos o más familiares de primer grado con CCR o un familiar de primer grado con CCR diagnosticado antes de los 60 años).
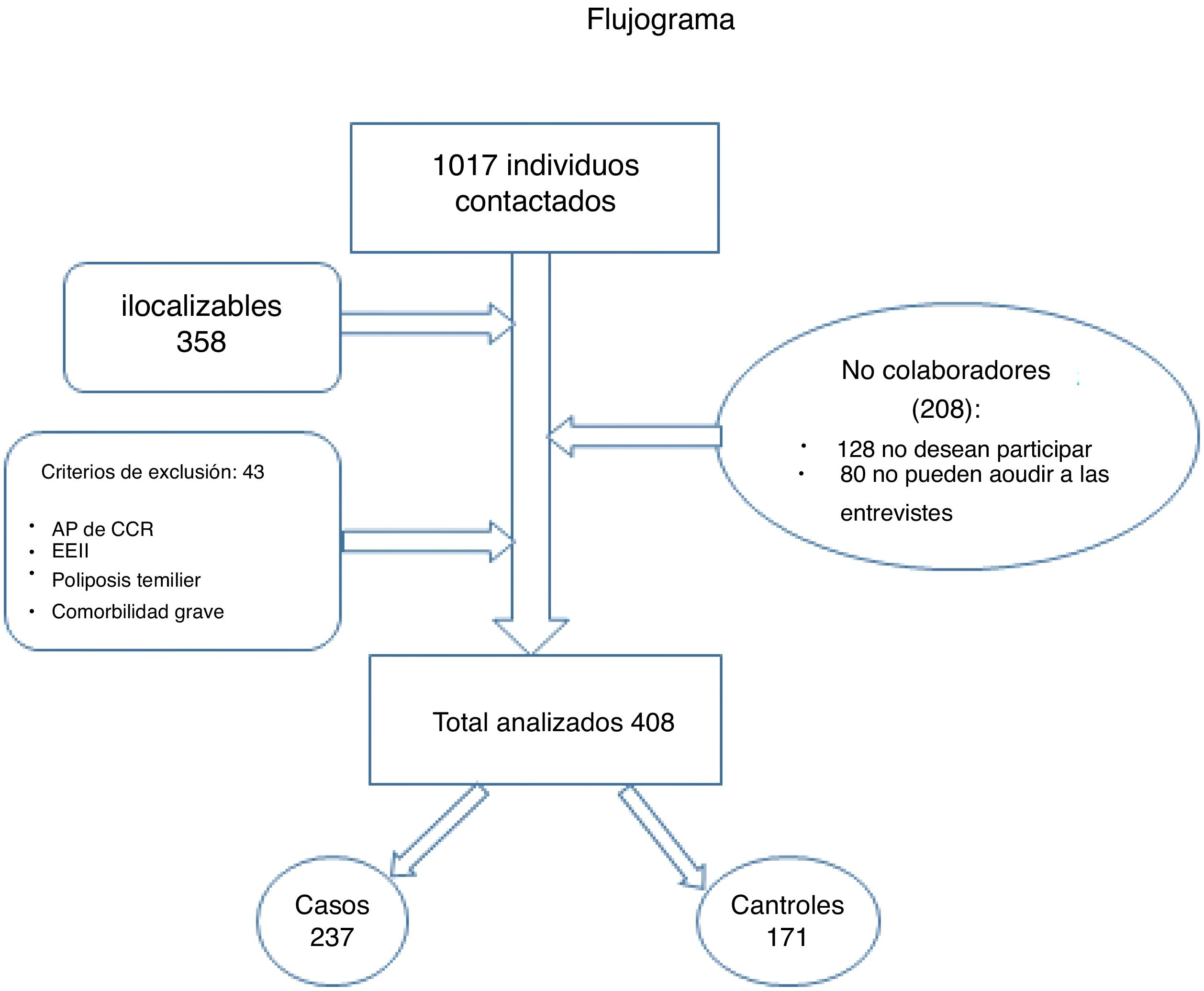
Tal como se puede ver en la figura 1, de marzo a septiembre de 2019, contactamos telefónicamente con 1017 pacientes. De ellos 358 fueron ilocalizables, 128 no quisieron participar y 80 no pudieron hacerlo al no poder acudir a las entrevistas. Cuarenta y tres pacientes no cumplieron los criterios de inclusión. Finalmente, incluimos en el estudio a un total de 408 pacientes, que se dividen en 237 casos y 171 controles, los cuales fueron entrevistados por uno de los investigadores previamente entrenados.
Definimos como casos a aquellos individuos que participaron en alguna ronda del programa de cribado de cáncer colorrectal. Se definieron como controles, los individuos que no entregaron la muestra de heces tras ser invitados a participar.
El cuestionario Rawl para el cribado de cáncer colorrectal está basado en el modelo teórico del comportamiento humano denominado HBM. La versión del año 2010 del cuestionario consta de 12 ítems que explora los beneficios y las barreras para realizar el cribado con sangre oculta en heces, se evalúa con una escala de Likert16. El cuestionario se cumplimenta de manera autoadministrada en aproximadamente 10 min.
Traducción-retrotraducciónPreviamente a la traducción y validación del instrumento se solicitó el permiso de la autora. El cuestionario fue traducido por dos personas bilingües que obtienen una primera versión. Esta versión fue retrotraducida por otros dos individuos bilingües e independientes que obtienen una versión preliminar. Finalmente tras las revisiones por pares se estableció la versión definitiva del cuestionario por consenso de todo el equipo. Con esta versión se realizó una prueba piloto con 10 pacientes para asegurar la compresión y viabilidad del cuestionario final (anexo).
Validez del constructoTras haber comprobado que se cumplen los supuestos del análisis factorial, el valor del estadístico KMO fue de 0,818 y la prueba de esfericidad de Barlett mostró significación estadística (p<0,001), en el análisis exploratorio se identificaron 2 dimensiones del cuestionario que explicaban el 52,25% de la variabilidad total (19,43% y 32,82%, respectivamente).
En el análisis factorial confirmatorio se utilizó el método de máxima verosimilitud. La puntuación de cada dimensión se calculó mediante la suma de los ítems que la componían, estableciéndose a mayor puntuación mayores beneficios y barreras percibidos. Así mismo, se calculó el efecto techo (número de respuestas con la mayor puntuación posible) y efecto suelo (número de respuestas con la menor puntuación posible).
Análisis de la fiabilidadPara el análisis de la consistencia interna del instrumento se calculó el coeficiente alfa de Cronbach total y para cada una de las dimensiones identificadas del cuestionario. Se descartaron los coeficientes de correlación menores de 0,1. Así mismo se calculó la media y la varianza si el ítem era eliminado. Se consideraron aceptables valores del alpha de Cronbach de 0,7 o superiores.
Test-retestPara observar la estabilidad del cuestionario en el tiempo se seleccionaron 23 individuos a los que se les repitió el test al cabo de 15 días calculando el coeficiente de correlación intraclase de cada dimensión.
Análisis descriptivoSe realizó un análisis descriptivo en el que las variables categóricas se resumieron en términos de frecuencia absoluta y porcentajes, las variables cuantitativas mediante valores medios y desviación típica, mediana y rango intercuartílico. Todos los test se realizaron con un planteamiento bilateral. Se consideraron significativos valores de p<0,05.
Para la realización del análisis estadístico se utilizó el programa BM SPSS Statistics for Windows, Version 22.0. Armonk, NY: IBM Corp y el programa Epidat 4.2 (Ministerio de Sanidad, Gobierno de Galicia [Consellería de Sanidade, Xunta de Galicia] en colaboración con el Organización Panamericana de la Salud [Organización Panamericana de la Salud, OPS-OMS])
Áspectos éticosEste estudio cuenta con la aprobación del Comité Ético de Investigación de la Dirección General de Salud Pública y Centro Superior de Investigación en Salud Pública de Valencia (CEIDGSP-CSISP) con número de registro 20190301/04. Todos los participantes firmaron el consentimiento informado. El proyecto se desarrolló conforme a la Declaración de Helsinki, las International Guidelines for Ethical Review of Epidemiological Studies, la regulación europea y española sobre investigación biomédica, y la regulación europea (General Data Protection Regulation 2016/679; GDPR-2016) y española (Ley Orgánica 3/2018, de 5 de diciembre, de Protección de Datos Personales y garantía de los derechos digitales; LOPDP-2018) sobre protección de datos personales.
Los investigadores firmaron un compromiso de confidencialidad e igualmente se adoptaron medidas específicas para mantener la integridad y seguridad de los datos y evitar el acceso de terceros a cualquier dato personal identificado o identificable. Ninguna publicación o informe derivados del estudio utilizará o contendrá datos o imágenes identificadas o identificables.
El autor para la correspondencia, en nombre del resto de las personas firmantes, garantiza la precisión, transparencia y honestidad de los datos y la información contenida en el estudio; que ninguna información relevante ha sido omitida; y que todas las discrepancias entre autores/autoras han sido adecuadamente resueltas y descritas.
El estudio se ha realizado sin financiación externa.
Todos los autores manifiestan no tener ningún conflicto de intereses.
ResultadosLa edad media fue de 59,45 (DE 5,17) años. El 54,20% fueron mujeres, el 72,30% no fumaban y el 25,40% eran abstemios. El índice de masa corporal medio fue de 26,01 (DE 4,41). El 20,10% tenían antecedentes familiares de CCR, el 55,60% antecedentes familiares de otras neoplasias y el 11% antecedentes personales de neoplasias distintas del CCR.
El cuestionario se completó de manera autoadministrada en el 87,8% de los casos frente al 12,20% en el que fue dirigida, no encontramos diferencias estadísticamente significativas entre ambas formas de cumplimentar el cuestionario. El 58,8% tenían estudios superiores frente al 22,50% con bachiller, el 17,60% con estudios primarios y el 1% eran analfabetos. El 72,10% tienen pareja, 70,80% estaban casados. Respecto de la clase social el 43,90% eran directivos o gerentes, el 37,20% tenían ocupaciones intermedias, el 10,30% eran obreros cualificados y el 8,60% obreros sin cualificar.
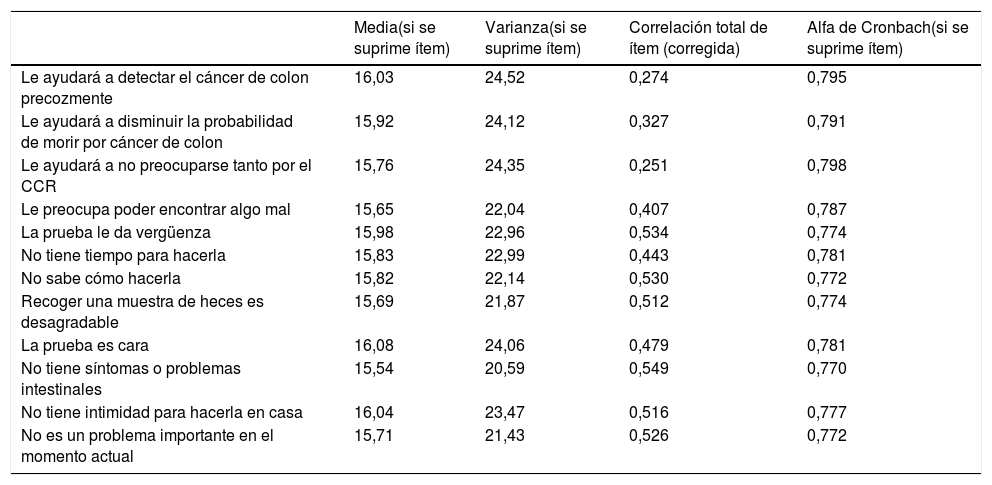
Al analizar todas las variables agrupadas, la consistencia interna del cuestionario alcanzó una alfa de Cronbach de 0,796. En la tabla 1 figuran las diferentes correlaciones resultantes tras eliminar alternativamente cada uno de los ítems del instrumento.
Consistencia interna del cuestionario de Rawl para el cribado con sangre oculta en heces
| Media(si se suprime ítem) | Varianza(si se suprime ítem) | Correlación total de ítem (corregida) | Alfa de Cronbach(si se suprime ítem) | |
|---|---|---|---|---|
| Le ayudará a detectar el cáncer de colon precozmente | 16,03 | 24,52 | 0,274 | 0,795 |
| Le ayudará a disminuir la probabilidad de morir por cáncer de colon | 15,92 | 24,12 | 0,327 | 0,791 |
| Le ayudará a no preocuparse tanto por el CCR | 15,76 | 24,35 | 0,251 | 0,798 |
| Le preocupa poder encontrar algo mal | 15,65 | 22,04 | 0,407 | 0,787 |
| La prueba le da vergüenza | 15,98 | 22,96 | 0,534 | 0,774 |
| No tiene tiempo para hacerla | 15,83 | 22,99 | 0,443 | 0,781 |
| No sabe cómo hacerla | 15,82 | 22,14 | 0,530 | 0,772 |
| Recoger una muestra de heces es desagradable | 15,69 | 21,87 | 0,512 | 0,774 |
| La prueba es cara | 16,08 | 24,06 | 0,479 | 0,781 |
| No tiene síntomas o problemas intestinales | 15,54 | 20,59 | 0,549 | 0,770 |
| No tiene intimidad para hacerla en casa | 16,04 | 23,47 | 0,516 | 0,777 |
| No es un problema importante en el momento actual | 15,71 | 21,43 | 0,526 | 0,772 |
Valores medios y varianza de la escala si la pregunta es eliminada, índice de homogeneidad corregido (correlación total de elementos corregida). Alpha de Cronbach si se elimina el ítem.
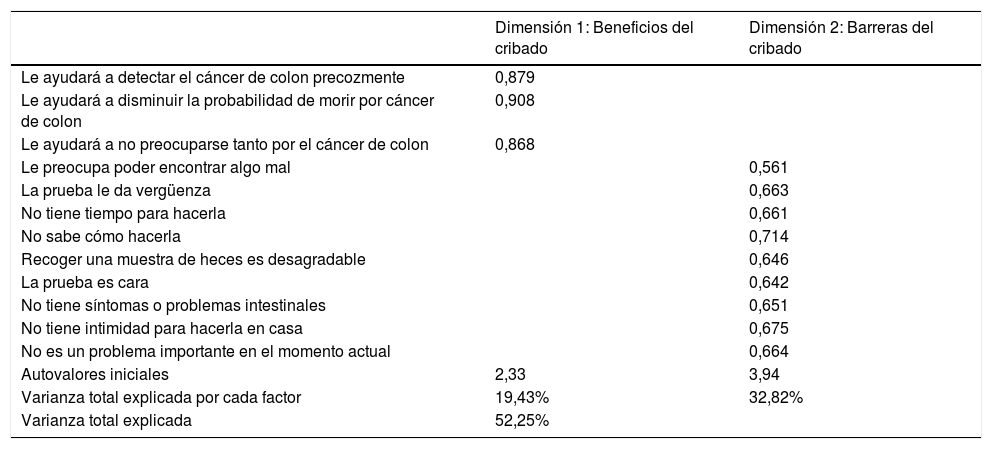
En el análisis factorial exploratorio se identificaron 2 dimensiones del cuestionario que explicaban el 52,25% de la variabilidad total (19,43% y 32,82%, respectivamente). El valor del estadístico KMO fue de 0,818 y la prueba de esfericidad de Barlett mostró significación estadística (p<0,001).
La dimensión 1 corresponde a las 3 primeras preguntas del cuestionario y la dimensión 2 a las preguntas de la 4 a la 12. Se calculó la consistencia interna de cada una de las dimensiones encontradas siendo el alfa de Cronbach de la dimensión 1 de 0,871, que identifica los beneficios del cribado con sangre oculta en heces. Para la dimensión 2, que explora las barreras al cribado, el alfa de Cronbach fue de 0,817 (tabla 2).
Validez del cuestionario Rawl para el cribado de cáncer colorectal: análisis factorial exploratorio y confirmatorio
| Dimensión 1: Beneficios del cribado | Dimensión 2: Barreras del cribado | |
|---|---|---|
| Le ayudará a detectar el cáncer de colon precozmente | 0,879 | |
| Le ayudará a disminuir la probabilidad de morir por cáncer de colon | 0,908 | |
| Le ayudará a no preocuparse tanto por el cáncer de colon | 0,868 | |
| Le preocupa poder encontrar algo mal | 0,561 | |
| La prueba le da vergüenza | 0,663 | |
| No tiene tiempo para hacerla | 0,661 | |
| No sabe cómo hacerla | 0,714 | |
| Recoger una muestra de heces es desagradable | 0,646 | |
| La prueba es cara | 0,642 | |
| No tiene síntomas o problemas intestinales | 0,651 | |
| No tiene intimidad para hacerla en casa | 0,675 | |
| No es un problema importante en el momento actual | 0,664 | |
| Autovalores iniciales | 2,33 | 3,94 |
| Varianza total explicada por cada factor | 19,43% | 32,82% |
| Varianza total explicada | 52,25% |
Factores identificados, autovalores, variabilidad total explicada.
Tras analizar la frecuencia de las respuestas de cada pregunta del cuestionario según las dimensiones definidas, se observó que, para la dimensión beneficios el porcentaje de efecto suelo fue del 3,5% y el porcentaje de efecto techo fue 2,5%. Para la dimensión barreras, un 0,2% de los participantes obtuvieron la puntuación mínima (efecto suelo) y un 0,2% la puntuación más alta (efecto techo).
Para ver la estabilidad del cuestionario se realizó un análisis test-retest repitiendo, al cabo de 15 días, el cuestionario a 23 pacientes. Encontramos unos coeficientes de correlación intraclase para la dimensión de los beneficios del cribado de 0,809 (0,606-0,913) y de 0,499 (0,126-0,750) para las barreras.
DiscusiónNuestro estudio ha validado la escala de Rawl, basada en el Modelo de Creencias en la Salud, al español para evaluar los beneficios y las barreras que perciben los pacientes en un programa de cribado de CCR basado en el test de SOHi. Determinar esto, es muy importante para conseguir el objetivo de una participación mayor del 65% en los programas de cribado, eliminando barreras y potenciando los beneficios percibidos por la población.
El primer cuestionario que adaptaba el modelo teórico del HBM al cribado del CCR lo llevó a cabo Jacobs11. En el 2001 Rawl lo validó en pacientes afroamericanos16 y posteriormente valida una nueva versión en el año 2010. La mayor parte de las validaciones publicadas hasta el momento son en población de bajos ingresos y bajo nivel sociocultural16–18. Hay estudios validados de trabajadores manuales y otros en empleados de fábricas de automoción19. Se han hecho validaciones en población turca13, china14 e iraní17. También están publicadas adaptaciones del modelo HBM en inmigrantes coreanos en Estados Unidos y en afroamericanos18,20,21.
Rawl encuentra un 74% de antecedentes familiares de CCR en su validación sobre pacientes afroamericanos16; en nuestra muestra solo el 20% de los pacientes tenían antecedentes familiares de CCR. Pensamos que esta diferencia puede deberse a factores raciales, ya que la población negra es la que mayor incidencia tiene de CCR20, y a que la muestra de Rawl se hacía sobre pacientes que no habían participado en el programa de cribado.
La población de nuestra muestra es de extracción urbana y de clase social media/alta, mientras que la mayoría de las publicaciones son en población de bajos ingresos y de menor nivel sociocultural16–18. También hay algún estudio que se ha llevado a cabo en trabajadores manuales22. El cuestionario demuestra ser un buen instrumento para objetivar los beneficios y barreras que presentan los individuos al someterse al cribado de CCR, al estar validado en poblaciones con diferentes perfiles sociales, culturales y económicos.
Sabiendo que el valor mínimo aceptable del alfa de Cronbach se sitúa por encima del 0,7, nosotros obtenemos una consistencia interna del 0,796 al agrupar todas las variables. Asimismo obtenemos una alfa de Cronbach de 0,871 y 0,817 en cada una de las dimensiones encontradas (beneficios y barreras respectivamente). Esto confiere gran fiabilidad al cuestionario. Incluso son mejores que los valores de la validación inicial del año 2001 (alfa de Cronbach 0,65 y 0,72) y de la versión actualizada del año 2010 (alfa de Cronbach 0,76 y 0,82) donde también se identificaban las dos dimensiones. En nuestro caso estas dos dimensiones explican el 52,5% de la variabilidad total frente al 34% de la varianza explicada en la validación original de Rawl12.
El cuestionario Rawl fue validado en personas de distintas razas. Ozsoy et al. llevaron a cabo la validación en población turca cuantificando una alfa de Cronbach de entre 0,58 a 0,8813. Leung adaptó el cuestionario en población china con un alfa de Cronbach de entre 0,74 a 0,8814. Existe otra validación en Taiwan23. También están publicadas adaptaciones en inmigrantes coreanos en Estados Unidos y en afroamericanos21. Existe una versión persa que presenta buenos datos de fiabilidad17. Recientemente Tahmasebi et al. encuentran un alfa de Cronbach de 0,78 al adaptar la escala en población iraní15. En España no encontramos cuestionarios, basados en el HBM, validados para el cribado de CCR; aunque sí los hay para el cribado de cáncer de mama24. Existe un cuestionario en español aplicado al cribado de CCR pero está basado en el Modelo Teórico de los Determinantes Sociales de la Salud, consta de 23 ítems obtenidos tras investigaciones cualitativas, no encontramos datos de su validación en la bibliografía25,26.
Existen otros modelos de cuestionarios validados sobre el cribado de CCR para conocer las actitudes y conocimientos de las personas pero están menos difundidos que los basados en el modelo teórico del HBM27.
Para la interpretación de la reproducibilidad de cuestionarios se consideran adecuados valores de coeficientes de correlación intraclase por encima de 0,428; en nuestro caso, los valores en las dos dimensiones analizadas superan ese dintel. Los datos de reproducibilidad de las validaciones turca13, iraní17 y de Taiwan23 son similares. Con lo que podemos afirmar que el instrumento de medición tiene estabilidad en el tiempo.
Nuestro estudio aporta conocimiento y transculturalidad, en un sector poblacional poco estudiado, a la hora de objetivar las barreras y beneficios que perciben los pacientes al realizar el cribado de CCR. Esto es clave para individualizar y priorizar medidas por parte de las autoridades sanitarias que consigan aumentar la participación en los programas de cribado.
Como limitaciones de nuestro estudio podríamos decir que únicamente analizamos el comportamiento de pacientes con riesgo medio de padecer CCR, no es extrapolable a población institucionalizada u hospitalaria al haberse realizado en Atención Primaria, ni a pacientes con alto riesgo de CCR o que hayan realizado el cribado con otras técnicas diferentes a la SOHi. Nosotros no incluimos el nivel de ingresos económicos de los pacientes como hacen otros autores14,16,20, ya que esto tiene una gran implicación en los sistemas sanitarios donde el paciente debe de costearse la prueba, pero no en el español. Por otro lado, algunos autores desarrollan instrumentos más específicos para explorar condicionantes como la privacidad, las creencias comunitarias o la vergüenza en la realización de la prueba que no están incluidas en el instrumento que nosotros validamos29,30. Es necesario también tener en cuenta la población ilocalizable de nuestro estudio pues podría conferir un sesgo por pérdidas, aunque no encontramos diferencias en cuanto a la edad y el sexo con la población incluida. Por todo ello, son necesarios nuevos estudios en el futuro que analicen estas variables y tengan en cuenta estas limitaciones.
No encontramos en la bibliografía validaciones del cuestionario Rawl en Europa, a excepción de una validación en las islas Baleares para el cáncer de mama, que tuvo un resultado negativo por baja correlación. Sí existe bibliografía en EE. UU., Turquía, Irán, China, Taiwán o Corea. Fundamentalmente en ámbito laboral, veteranos de guerra, atención primaria, en consulta externas hospitalarias, centros comerciales o a través de entrevistas telefónicas.
Como conclusión, es importante resaltar la necesidad de disponer de un instrumento validado en nuestro medio que objetive las barreras y beneficios percibidos por la población al decidir su participación o no en un programa de cribado. Esto permitirá diseñar estrategias de información que potencien los beneficios percibidos y adapten las técnicas de cribado para disminuir las barreras que sienten los pacientes. Con todo ello, podremos acercarnos al objetivo de una participación mínima del 65% que consiga disminuir la mortalidad por CCR.
Con este estudio, hemos validado la versión en castellano del cuestionario Rawl. Es un cuestionario fiable y reproducible que permitirá determinar los factores subjetivos asociados a la participación en programas poblacionales de cribado de CCR en España.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.