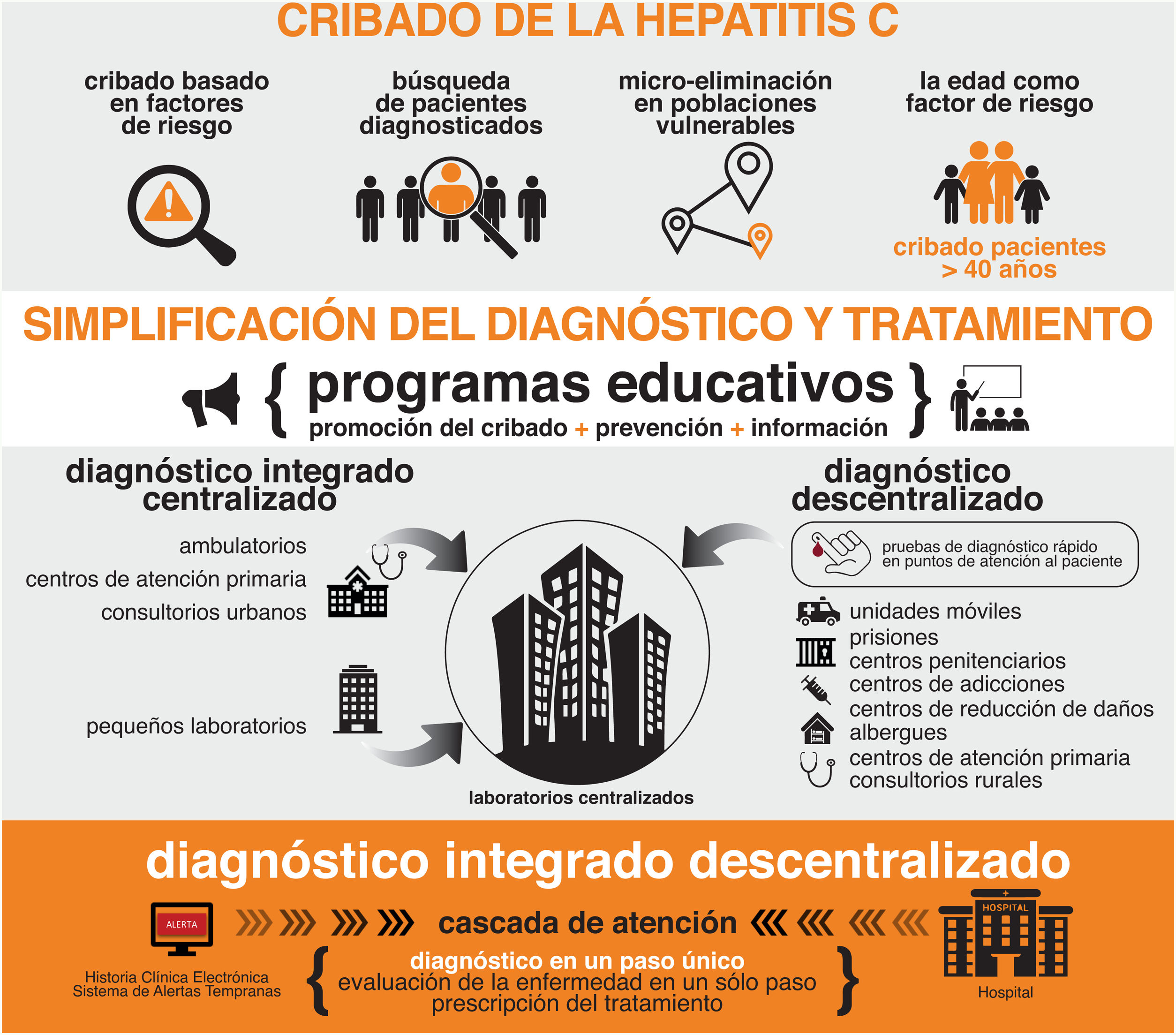
La Asociación Española para el Estudio del Hígado (AEEH) está convencida de que la eliminación de la hepatitisC en España es posible siempre y cuando seamos capaces de emplear los recursos y las herramientas necesarias para la misma. Este documento refleja la posición de la AEEH respecto a la eliminación del virus de la hepatitisC (VHC), estableciendo una amplia serie de recomendaciones que se pueden agrupar en cinco categorías: 1)cribado del VHC en función de la edad, de la existencia de factores de riesgo clásicos de adquisición de la infección, búsqueda activa de pacientes diagnosticados con anterioridad y desarrollo de estrategias de microeliminación en poblaciones vulnerables; 2)simplificación del diagnóstico del VHC (diagnóstico en un solo paso y diagnóstico en el punto de atención del paciente); 3)simplificación del tratamiento de los pacientes y mejora de los circuitos asistenciales; 4)medidas de política sanitaria, y, finalmente, 5)establecimiento de indicadores de eliminación del VHC.
The Spanish Association for the Study of the Liver (AEEH) is convinced that the elimination of hepatitisC virus (HCV) in Spain is possible as long as we are able to use the resources and tools necessary for it. This document reflects the position of the AEEH regarding the elimination of HCV, establishing a wide range of recommendations that can be grouped into five categories: 1)Screening of HCV according to age, of the existence of classic acquisition risk factors of infection, active search of previously diagnosed patients and development of micro-elimination strategies in vulnerable populations; 2)Simplification of HCV diagnosis (one-step diagnosis and diagnosis at the point of patient care); 3)Simplification of patient treatment and improvement of care circuits; 4)Health policy measures, and, finally, 5)Establishment of HCV elimination indicators.
La hepatitis C es un problema de salud pública global. Según los últimos datos publicados, afecta a más de 70 millones de personas, lo que supone el 1% de la población mundial1,2. Estudios recientes efectuados en España durante los últimos 3años estiman que la seroprevalencia de anti-virus de la hepatitisC (VHC) oscila entre el 0,8 y el 1,2% de la población adulta, mientras que entre el 0,2 y el 0,4% muestran una infección activa por el VHC y, por lo tanto, están en riesgo de desarrollar a medio-largo plazo una cirrosis hepática y las complicaciones asociadas a ella3-6. Una parte importante de estos sujetos ya han sido diagnosticados y tratados, aunque existe un número relativamente elevado de pacientes que desconocen que tienen una hepatitisC, sobre todo en pacientes mayores de 50años, como nos muestra el estudio de seroprevalencia del Ministerio7. En resumen, los resultados definitivos de la encuesta efectuada por el Ministerio de Sanidad7, en una muestra de 9.103 de sujetos de población general, es el siguiente: 9.002 fueron negativas y se detectaron 66 muestras anti-VHC positivas 0,69%). De estas, en 17 se detectó ARN del VHC 0,17%. No se encontró ningún caso confirmado de hepatitisC en menores de 20años. De igual modo, la prevalencia de viremia fue residual en menores de 40años. La prevalencia de viremia aumentó en las cohortes de 40 a 49 (0,14%), de 50 a 59 (0,50%) y de 60 a 69 (0,34%), particularmente en hombres. Esta prevalencia, claramente más baja que la demostrada en estudios previos, probablemente sea consecuencia del enorme esfuerzo terapéutico efectuado en nuestro país durante los últimos 4años. Otro estudio muy reciente, procedente de Navarra, aporta datos similares8,9.
A pesar de la importante reducción del número de pacientes infectados desde el año 2015, la infección por el VHC continúa siendo una causa frecuente y evitable de cirrosis hepática y hepatocarcinoma. Y pese al marcado descenso del VHC como causa de trasplante, se observa una estabilización en los últimos 2años, siendo la causa de cerca del 20% de los trasplantes, a expensas probablemente del desarrollo de carcinoma hepatocelular sobre cirrosis por VHC, una vez erradicado este10. La Organización Mundial de la Salud (OMS), en sintonía con otras instituciones sanitarias y gobiernos, estableció en el año 2015 una estrategia global en el sector sanitario en hepatitis virales con el objetivo de conseguir su eliminación como problema de salud pública para el año 203011. Dicha estrategia define la eliminación como una reducción del 80% en las nuevas infecciones por VHC y una reducción del 65% en la mortalidad por VHC. Como resultado de este compromiso global, diferentes gobiernos han puesto en marcha planes de acción específicos contra la hepatitisC. En el caso particular de España, el Plan Estratégico Nacional para el Abordaje de la HepatitisC en el Sistema Nacional de Salud (PEAHC)12 estableció cuatro líneas de acción: cuantificar la magnitud de la hepatitisC; definir el acceso al tratamiento con agentes antivirales directos (AAD); establecer mecanismos de coordinación para implantar la estrategia, y fomentar el avance en el conocimiento de la prevención, diagnóstico y tratamiento de la hepatitisC en el Sistema Nacional de Salud (SNS) mediante actuaciones en I+D+i. Desde su inicio en abril de 2015 hasta mayo del 2019, en España se han tratado con AAD más de 130.000 pacientes con hepatitisC, lo que representa la práctica totalidad de los pacientes diagnosticados y en seguimiento. A estos pacientes se deben sumar los miles de enfermos tratados con regímenes basados en interferón en las últimas dos décadas, lo que probablemente supone cerca de 150.000 pacientes curados3. Este plan, pionero a nivel mundial, ha permitido poner a España en el foco de los países que más han avanzado para conseguir los objetivos marcados por la OMS para la eliminación de la hepatitisC en el año 203013. Pero pese a esos excelentes datos, se estima que en el ámbito de la población general que acude a la atención primaria hay todavía 76.500 personas virémicas. Por otro lado, en España la tasa de diagnóstico de esta enfermedad no es todavía satisfactoria y el número de sujetos adultos que desconocen que están infectados por el VHC se estima en alrededor de 22.500, a los que habría que sumar también todos los pacientes que, pese a estar diagnosticados, no se están tratando7. Esta inadecuada tasa de diagnóstico puede deberse a que existe un número no determinado de pacientes que no acuden al sistema sanitario por pertenecer a grupos sociales vulnerables y en riesgo de exclusión, como lo son los sujetos condenados a penas privativas y no privativas de libertad (ya en exclusión antes de su entrada en prisión) o las personas que consumen drogas (PQCD), y las que tienen dificultades de acceso (inmigrantes). En otras ocasiones se trata de sujetos con temor a la estigmatización social que escapan voluntariamente del sistema. Finalmente, existen personas que desconocen los factores de riesgo y, por lo tanto, la posibilidad de estar infectadas; suelen pertenecer a cohortes de edad en las que se ha demostrado que la prevalencia de infección activa es superior a la media. Estos sujetos pueden transmitir la infección mediante prácticas de riesgo, y un porcentaje variable pueden desarrollar fibrosis hepática avanzada, cirrosis y finalmente hepatocarcinoma. La identificación de estos sujetos y su tratamiento es una buena inversión de salud, tal como demuestran diversos estudios realizados por miembros de la Asociación Española para el Estudio del Hígado (AEEH), aunque los estudios se han efectuado con prevalencias superiores a las actuales14-16.
En cuanto a promover el diagnóstico precoz en poblaciones prioritarias definidas por la pertenencia del individuo a una población vulnerable, la recomendación actual es hacer cribado en estos grupos. Varios estudios recientes han demostrado que el cribado poblacional asociado a tratamiento es coste-efectivo en diferentes franjas de edad y en la población adulta general4,17,18. Por este y por otros motivos, tanto la AEEH como otras sociedades científicas, como la Sociedad Española de Patología Digestiva, así como la Alianza para la Eliminación de las Hepatitis Víricas en España (AEHVE), abogan por la realización de planes para establecer estrategias de cribado y programas de microeliminación de la hepatitisC, que básicamente consisten en segmentar y dividir la estrategia global de eliminación focalizándola en distintos programas dirigidos a focos primarios de la infección.
Por último, el tratamiento está indicado en todos los pacientes infectados19-22. Conocemos con detalle la historia natural de la enfermedad y sabemos que un tratamiento adecuado evita la progresión a estadios avanzados e impide la transmisión de la infección. El tratamiento consigue un beneficio individual sobre la propia enfermedad hepática, disminuye la mortalidad de cualquier causa23, mejora la calidad de vida y evita el desarrollo de manifestaciones extrahepáticas24,25; en los casos con fibrosis avanzada previene las complicaciones de la cirrosis20, y en pacientes en lista de espera de trasplante hepático incluso puede suponer evitar el procedimiento26. Además, produce diferentes beneficios colectivos, como la reducción de nuevas infecciones o el incremento de la facilidad en el acceso al trasplante hepático de otros pacientes.
Por estos motivos, la AEEH estima que ha llegado el momento de efectuar un plan global para facilitar la eliminación de la hepatitisC (tabla 1, fig. 1). Este plan pretende ser un marco en el que tengan cabida todas las iniciativas potencialmente útiles para dicha eliminación. Se sustenta en los siguientes principios:
- –
Participación de un amplio grupo de profesionales que asegure la multidisciplinariedad.
- –
Basado en la mejor evidencia científica disponible.
- –
Búsqueda de la equidad en todas las medidas propuestas.
- –
Inclusivo, pues incorpora todas las medidas locales, regionales, nacionales e internacionales que han demostrado utilidad para eliminar el VHC y a todos los elementos de la cadena asistencial.
- –
La búsqueda de todas las herramientas que conduzcan a nuestro objetivo final: la eliminación de la hepatitisC como problema de salud pública en nuestro país.
- –
Plan universal y ejecutable por nuestras administraciones sanitarias.
Recomendaciones de la Asociación Española para el Estudio del Hígado para la eliminación del virus de la hepatitis C (VHC)
| Combinación de varios métodos de cribado del VHC |
| Cribado poblacional etario del VHC |
| Cribado basado en los factores de riesgo de adquisición la infección por el VHC |
| Búsqueda activa de pacientes diagnosticados con anterioridad pero que nunca han sido tratados o bien han sido tratados pero no han obtenido la curación |
| Estrategias de microeliminación en poblaciones vulnerables |
| Diagnóstico en un solo paso |
| Diagnóstico en el punto de atención al paciente |
| Vinculación del diagnóstico al tratamiento |
| Dispensación delegada |
| Desarrollo y utilización de marcadores de eliminación del VHC |
| Estricta vigilancia epidemiológica que permita el diagnóstico de las reinfecciones, etiología actual de la mayor parte de los casos incidentes |
| Incremento del conocimiento de la enfermedad por parte de profesionales de la salud y de la población general |
La AEEH está firmemente convencida de que la eliminación de la hepatitisC en España es posible. Pero para conseguir esta eliminación es imprescindible la puesta en marcha de las siguientes recomendaciones:
- –
Cribado de la hepatitisC, con la edad como factor de riesgo de infección por el VHC. Los resultados de los estudios económicos que evalúan la coste-efectividad del cribado recomiendan efectuarlo en la población de 20 a 79años de edad. No obstante, y dado que la mayoría de los casos no diagnosticados se concentran en el segmento de 40-70años, la AEEH recomienda la determinación de anticuerpos frente al VHC al menos una vez en la vida en este segmento de edad. Cada sistema de salud deberá ajustar la estrategia de cribado a su información epidemiológica local.
- –
Continuar la búsqueda activa del VHC en la población con factores de riesgo tanto a nivel hospitalario como de atención primaria.
- –
Programas enfocados a la microeliminación de forma simultánea al anterior, mediante la búsqueda activa del VHC en poblaciones vulnerables en todos los dispositivos asistenciales a los que acuden estas personas.
- –
Diagnóstico en un solo paso en todos los laboratorios de microbiología y/o de análisis clínicos del SNS.
- –
Adaptación de las técnicas de diagnóstico a la población diana, incluyendo medios de diagnóstico que faciliten el acceso a un diagnóstico y tratamiento para los colectivos vulnerables en riesgo de exclusión social y que habitualmente no contacta con los dispositivos asistenciales convencionales (atención primaria y/o hospitalaria). Entre estas, usar viremia en el punto de atención al paciente cuando la prevalencia de viremia en el grupo a cribar sea elevada, así como una adecuada vinculación a los procesos asistenciales del SNS.
- –
Vinculación del diagnóstico al tratamiento. Acceso equitativo y universal al cribado y a un tratamiento antiviral curativo.
- –
Ampliar la cobertura en centros de reducción de daños (para personas que consumen drogas por vía parenteral).
- –
Mejorar la continuidad asistencial en el proceso del abordaje global de la atención a los pacientes con hepatitisC.
- –
Dispensación delegada cuando ello facilite el acceso al tratamiento en los pacientes diagnosticados.
- –
Desarrollo y utilización de indicadores de eliminación del VHC a nivel del SNS.
- –
Estricta vigilancia epidemiológica que permita el diagnóstico de las reinfecciones, origen actual de la mayor parte de los casos incidentes, y que permita identificar correctamente los casos incidentes (agudos) de los casos crónicos (prevalentes), como recomienda el Centro Europeo para la Prevención y el Control de las Enfermedades (ECDC).
- –
Incremento del conocimiento de la enfermedad por parte de profesionales de la salud y de la población general.
El seguimiento de estas recomendaciones permitirá la identificación y el posterior tratamiento de los casos no diagnosticados en nuestro país, el diagnóstico de las reinfecciones, evitará el desarrollo de enfermedades hepáticas avanzadas relacionadas con la hepatitisC y, en suma, contribuirá de forma decidida a la eliminación de esta enfermedad a corto plazo entre nuestros conciudadanos.
Cribado del VHCLa edad como factor de riesgo de infección por el VHCEl cribado de una enfermedad determinada es un «servicio» de salud pública en el que los miembros de una población definida son invitados a someterse a preguntas o pruebas para identificar a los individuos con mayor probabilidad de obtener un beneficio que un perjuicio —causado por las sucesivas pruebas o el tratamiento— para reducir el riesgo de la enfermedad en estudio o de sus complicaciones25,26. La infección por el VHC cumple con todos los criterios exigibles de un programa de cribado27,28, de acuerdo con los criterios elaborados por nuestro Ministerio de Sanidad29 hace aproximadamente una década y que dividiremos en tres categorías:
- 1.
Características de la hepatitisC que sustentan considerar a la edad como factor de riesgo de infección por el VHC:
- –
La enfermedad está bien definida y se conoce su historia natural.
- –
El diagnóstico de la infección tiene unos criterios claros30. La determinación de anti-VHC es simple, segura, rápida, fácil de realizar, con alta sensibilidad, alta especificidad, alto valor predictivo positivo, bien aceptada por los profesionales y pacientes y con una excelente relación coste-efectividad.
- –
El tratamiento es extremadamente eficaz.
- –
Las evidencias que indican que un diagnóstico y un tratamiento precoces mejoran la evolución de la enfermedad son abrumadoras: previenen la evolución a cirrosis, reducen la transmisión y prácticamente anulan la incidencia de hepatocarcinoma31-33. Incluso un diagnóstico y tratamiento de la enfermedad en fases tardías disminuyen la mortalidad hepática, la mortalidad global, la necesidad de trasplante y la incidencia de hepatocarcinoma (European Association for Study of the Liver [EASL], American Association for the Study of Liver Disease [AASLD]). Además, evita o mejora las manifestaciones extrahepáticas relacionadas con la infección34,35.
- –
Es un problema de salud pública importante, como lo demuestran su notable impacto en términos de incidencia, morbilidad y mortalidad36 y los modelos predictivos de carga de la enfermedad.
- –
Se ha demostrado reiteradamente la relación coste-eficacia del cribado en población adulta37,38, aunque es cierto que se han efectuado teniendo en cuenta prevalencias superiores a las actuales.
- –
Es muy poco probable el desarrollo de una vacuna frente al VHC, al menos a medio plazo.
- 2.
Características de nuestro sistema sanitario que hacen posible llevar a cabo un programa de diagnóstico en función de la edad de la población a cribar:
- –
Atención sanitaria a todos los ciudadanos con carácter universal.
- –
Informatización de la historia clínica y desarrollo de los sistemas de información clínica y de los registros administrativos.
- –
No existe una alternativa al diagnóstico en población asintomática y sin claras conductas de riesgo, que no sea el cribado.
- –
Existencia de circuitos asistenciales adecuados que permiten un diagnóstico, un tratamiento y un seguimiento estandarizados.
- –
Es una oportunidad de salud para colectivos vulnerables con escaso acceso al sistema sanitario. El cribado del VHC mejora el acceso al diagnóstico de sujetos infectados por el virus de la hepatitis B (VHB), el virus de la inmunodeficiencia humana (VIH) y otros agentes infecciosos, mejora de forma directa la salud del individuo objetivo del programa e, indirectamente, de los sujetos que pudieran ser infectados por los primeros. Esta situación se produce de forma particular en algunos colectivos vulnerables, como las PQCD, los internos en centros penitenciarios, los hombres que tienen sexo con hombres (HSH), las personas sin hogar, inmigrantes y las personas con enfermedades psiquiátricas graves. No obstante, estos grupos no son homogéneos y, especialmente en los HSH, el riesgo está vinculado al consumo de drogas39.
- –
Dada la extraordinaria facilidad, sencillez y coste de la determinación de anticuerpos frente al VHC, la implantación completa del programa se puede hacer en un periodo no superior a los 3-5años, alcanzando la cobertura del total de la población diana en un plazo que evite la inequidad en el acceso40.
- –
Es un programa factible dentro del SNS que se debe acompañar de un sistema de información de promoción de la salud.
- –
El cribado como herramienta para alcanzar la eliminación solo tiene cabida en países en los que se haya aprobado el tratamiento para todos los pacientes, situación en la que se encuentra nuestro país.
- 3.
Consecuencias previsibles en el caso de que este programa de cribado no se efectúe:
- –
Diagnóstico de la hepatitisC en fases avanzadas de la enfermedad. Datos actuales recientemente comunicados en nuestro país demuestran que el 20% de los pacientes inician su tratamiento en fases avanzadas de la enfermedad41. Además, se produciría un agotamiento diagnóstico, previsto para el año 2022, causa actual —y sobre todo futura— de que los nuevos diagnósticos sin un cribado se efectúen en fases avanzadas de la enfermedad42,43.
- –
Una disminución lenta o muy lenta de la incidencia debido al contagio por personas no diagnosticadas ni tratadas.
- –
El elevado impacto negativo en colectivos como las PQCD, donde la incidencia está muy en relación a la prevalencia (que deber reducirse para evitar nuevos casos).
- –
Finalmente, se producirá un nuevo incremento de la morbimortalidad atribuible al VHC en los próximos años, con un recrudecimiento del número de ingresos por cirrosis descompensada y hepatocarcinoma, asociado a un incremento de la necesidad de trasplante hepático en estos pacientes44.
El cribado en sujetos mayores de 40años debe combinarse con la búsqueda activa de la infección por el VHC en las personas que presenten una o más de las siguientes características:
- –
En todos los pacientes con hipertransaminasemia o con una hepatopatía aguda o crónica. Idealmente, se debería efectuar de forma refleja, siempre que no se hubieran determinado antes los anticuerpos frente al VHC.
- –
Sujetos con riesgo elevado de infección por VHC por vía parenteral y/o percutánea:
- ∘
Antecedentes de transfusión de sangre o hemoderivados anteriores a 1992.
- ∘
Antecedentes de cirugía, procedimientos invasivos o intervenciones odontológicas antes de la utilización de material de inyección de un solo uso (1980).
- ∘
Pacientes sometidos en algún momento a hemodiálisis.
- ∘
Personas con antecedentes de tatuajes, piercings o procedimientos con instrumental punzante (manicura, pedicura, acupuntura, etc.) realizados sin la debida seguridad.
- ∘
Personal sanitario tras exposición accidental reconocida con material biológico posiblemente infectado.
- ∘
Personas que compartan utensilios personales, como por ejemplo, cepillos de dientes o cuchillas de afeitar.
- –
Personas con una mayor probabilidad de infección por presentar un riesgo más elevado de infección por vía sexual:
- ∘
Convivientes y parejas sexuales de personas infectadas por el VHC45.
- ∘
Personas que mantienen relaciones sexuales de riesgo, sin protección, especialmente HSH.
- ∘
Trabajadores sexuales.
- –
Recién nacidos de madres infectadas por VHC, a partir de los 18meses46.
- –
Otros colectivos en los que se debe descartar la infección por VHC de forma sistemática:
- ∘
Sujetos que hayan estado internados en instituciones penitenciarias.
- ∘
Sujetos condenados a penas no privativas de libertad.
- ∘
Infectados por VIH y/o VHB.
- ∘
Pacientes con infecciones de transmisión sexual, particularmente sífilis, gonococia, clamidia e infecciones por Mycoplasma genitalium, especialmente en localización anal.
- ∘
Inmigrantes procedentes de países de alta prevalencia (Europa del Este, en concreto Rumanía, Asia Central y Asia del Este, África y Oriente Medio)47-49. La población en España de países de alta prevalencia (por convención >3%) son: Rumanía, Ucrania, Rusia y procedentes del África Subsahariana. Es más apropiado hablar de Sur de Asia (Pakistán), y en cuanto a Oriente Medio, solo es importante a efectos de prevalencia la población egipcia, que en España no la hay.
- ∘
Personas que consumen drogas por vía inhalada y comparten instrumental.
- ∘
Personas sin techo50.
La detección de estas personas con factores de riesgo que utilizan el sistema sanitario podría potenciarse mediante dos estrategias, principalmente dirigidas a los profesionales de atención primaria:
- –
Establecer un sistema de avisos y/o alertas integrado en la historia clínica electrónica sobre la necesidad de realización de anticuerpos frente al VHC, a partir de datos clínicos registrados relacionados con el riesgo de infección por VHC.
- –
Búsqueda activa de personas con riesgo de adquisición de la infección por el VHC a partir de los sistemas de información clínica procedentes de la historia clínica electrónica.
Un número indeterminado de pacientes han sido testados y diagnosticados de hepatitisC (anti-VHC positivo y/o ARN VHC positivo) en algún momento de su vida y, por diferentes razones, no han sido tratados y se ha perdido su seguimiento dentro del sistema sanitario. Estos pacientes forman parte de uno de estos dos grupos: a)pacientes que presentan anticuerpos anti-VHC (anti-VHC), a los cuales no se les ha realizado la determinación del ARN del VHC, por lo que se desconoce si son virémicos, y b)pacientes en los que se ha confirmado que son ARN-VHC y que no se han tratado o no se curaron con regímenes basados en interferón o no han continuado seguimiento. La búsqueda activa de estos pacientes no constituye una herramienta de cribado propiamente dicha, pero contribuye al objetivo global de diagnosticar (y tratar inmediatamente después) al mayor número de pacientes posible. Estos pacientes se pueden encontrar en cualquier parte de nuestro sistema sanitario, tanto en centros de atención primaria como en centros de atención a drogodependientes (CAD), e incluso en el propio ambiente hospitalario50. Se han descrito diferentes estrategias para el afloramiento de estos pacientes:
- –
Revisión de casos con serología positiva a partir de sistemas de información de microbiología y/o laboratorios centrales51,52.
- –
Revisión de los registros de pacientes tratados mediante AAD (y basados en interferón) de nuestras farmacias hospitalarias.
- –
Revisión sistemática «convencional» de los registros de serologías positivas en los últimos años.
- –
Utilización de sistemas basados en herramientas de inteligencia artificial capaces de identificar en diferentes registros sanitarios la potencial existencia de una hepatitisC. Este tipo de aproximación se ha utilizado en las comunidades de Galicia y Castilla y León53.
- –
Implementación de alertas electrónicas en la historia clínica o en el informe de laboratorio50.
- –
Aunque los datos no son definitivos, la seropositividad de los pacientes ingresados en plantas de psiquiatría (agudos y subagudos) es cercana al 3%, por lo que parece razonable la búsqueda intencionada de infección por VHC en estos pacientes.
Para evitar que en el futuro se produzca esta situación es imprescindible:
- –
Desarrollo de una base de datos única de la información clínica en los diferentes sistemas de salud.
- –
Aumentar la vigilancia, fomentar la notificación obligatoria de casos de hepatitis por VHC y detección de casos producidos en el entorno sanitario.
- –
Aumentar el nivel de conocimiento de los profesionales sanitarios acerca de la necesidad de llevar a cabo una detección precoz de esta enfermedad.
- –
Garantizar que el diagnóstico precoz se acompaña de un acceso inmediato al tratamiento.
- –
Integrar la actividad de cribado precoz de hepatitis (VHB, VHC) y de VIH en la cartera de servicios de atención primaria.
El concepto de microeliminación, revisado recientemente54, consiste en segmentar la estrategia global de eliminación de la hepatitisC focalizándola en distintos programas dirigidos a focos primarios de infección (p.ej., internos en centros penitenciarios, consumidores de drogas por vía parenteral, etc.). En nuestro país existen múltiples experiencias exitosas de microeliminación, tanto en internos de instituciones penitenciarias como en usuarios de drogas por vía parenteral con o sin programas de reducción de daños55. En estos escenarios se han demostrado útiles para la microeliminación:
- –
La telemedicina en algunos centros penitenciarios, tanto españoles como internacionales56,57.
- –
El diagnóstico descentralizado, sea in situ o no.
La AEEH recomienda la combinación del cribado poblacional etario y la búsqueda activa de personas con factores de riesgo para la adquisición del VHC y de los pacientes diagnosticados con anterioridad pero que nunca han sido tratados con las estrategias de microeliminación. De forma específica:
- –
Implementar la realización de una única determinación de anticuerpos frente al VHC en todos los adultos entre 40 y 70años que no hayan sido examinados con anterioridad.
- –
Implementar programas de búsqueda activa del VHC en la población con factores de riesgo tanto a nivel hospitalario como de atención primaria, como se realiza actualmente en algunas comunidades, como Aragón y Cataluña.
- –
La búsqueda activa de pacientes diagnosticados con anterioridad pero que nunca han sido tratados, o bien han sido tratados pero no han conseguido la curación.
- –
Programas enfocados a la microeliminación de forma simultánea al anterior, mediante la búsqueda activa del VHC en poblaciones vulnerables en todos los dispositivos asistenciales a los que acuden dichos sujetos.
El acceso al tratamiento de todos los pacientes con hepatitisC es una prioridad en cualquiera de los planes de eliminación de la infección. En esta situación, la disponibilidad de pruebas para el diagnóstico de infección activa por el VHC en los servicios de microbiología y/o de análisis clínicos es fundamental. Adicionalmente, el alto porcentaje de pacientes ya tratados y curados condiciona que se deba tener acceso a sistemas de información ágiles que permitan discriminar este aspecto y evitar repeticiones innecesarias y costosas, evitando al mismo tiempo la remisión a consultas especializadas de pacientes en los que la infección ya ha sido curada y tratada.
En el documento de diagnóstico en un solo paso (DUSP) de la hepatitisC elaborado conjuntamente por la AEEH y otras sociedades se pueden observar cuáles son los marcadores del virus de la hepatitisC, así como la definición de infección activa58. El DUSP consiste en la investigación de viremia en todos los pacientes de nuevo diagnóstico serológico. Tras la solicitud de una determinación de un test de anticuerpos frente al VHC y una vez comprobado que se trata de la primera vez que se solicita y/o que no se ha efectuado un diagnóstico virológico previo, se debe proceder a la determinación de la viremia (sin mediar nueva petición clínica). Este DUSP es crítico, dado que disminuye el tiempo de acceso para el inicio del tratamiento y, lo que es más importante, evita una importante pérdida de pacientes durante el proceso diagnóstico59.
Pero además de alentar el diagnóstico en un solo paso, la AEEH promueve el diagnóstico en la comunidad descentralizado e integrado. En España estamos entrando en una nueva era con respecto al VHC: la era de la eliminación del VHC. La aparición de los AAD, que alcanzan tasas de curación superiores al 97%, ha convertido la eliminación del VHC en una posibilidad real. Y para conseguirla es necesario diagnosticar y tratar a todos los pacientes. Es probable que muchos de los no diagnosticados y/o no tratados formen parte de colectivos de pacientes que escapan al sistema, como ya mencionamos con anterioridad60. En estos colectivos es imprescindible facilitar el acceso al diagnóstico61. Por este motivo, además del diagnóstico en un solo paso comentado con anterioridad, es necesario:
- –
Flexibilizar y acercar al paciente las técnicas de diagnóstico, facilitando la implantación de métodos como los test de gota de sangre seca (TGSS) o los métodos de diagnóstico en el punto de atención al paciente.
- –
Avanzar desde el diagnóstico centralizado hacia un diagnóstico descentralizado e integrado en el sistema sanitario.
Podemos definir la atención centralizada como la que se practica en centros hospitalarios convencionales, donde se atiende al paciente, se diagnostica la infección por el VHC, se estadifica la enfermedad hepática y se inicia el tratamiento. Por el contrario, una atención descentralizada se caracteriza por un diagnóstico rápido de la infección por el VHC, se hace estadificación rápida de la enfermedad hepática y se inicia el tratamiento de forma inmediata (estrategia «test and treat»). La elección de un tipo u otro de asistencia sanitaria debe basarse en la prevalencia de la infección, el tipo de población y la existencia de barreras administrativas o geográficas62. Ambos tipos de atención presentan una clara diferencia: el diagnóstico centralizado permite un control epidemiológico óptimo; por el contario, un diagnóstico descentralizado incrementa la accesibilidad y disminuye las pérdidas. Sin duda, si queremos eliminar la hepatitisC debemos evolucionar hacia el diagnóstico descentralizado integrado, es decir, una combinación de ambos tipos de técnicas que finalmente confluyan para, de forma simultánea, lograr un excelente control epidemiológico y facilitar la accesibilidad. Pero un diagnóstico centralizado o descentralizado no significa, necesariamente, rapidez en el diagnóstico. En España disponemos de los siguientes sistemas de diagnóstico potenciales:
- –
Test clásicos de diagnóstico virológico.
- ∘
Detección de anticuerpos mediante enzima inmunoensayo (EIA).
- ∘
Detección de ARN mediante técnicas moleculares (PCR o TMA).
- ∘
Detección y cuantificación del antígeno del core del VHC.
- ∘
Determinación del genotipo y estudios filogenéticos.
- –
Test «atípicos» de diagnóstico virológico. Diagnóstico en el punto de atención al paciente. Conceptualmente podemos definirlo como una prueba diagnóstica que se efectúa muy cerca del entorno del paciente, que proporciona un resultado en un corto espacio de tiempo (habitualmente <1h) y que permite ofrecer una asistencia sanitaria a pacientes vulnerables que de otro modo no accederían al diagnóstico y tratamiento de su hepatitisC. La Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica (SEIMC) ha elaborado recientemente un documento para el uso del Point of care (POC; diagnóstico en el punto de atención al paciente)63. Entre estos podemos destacar:
- ∘
Test de gota de sangre seca (TGSS)64,65. Aunque no está normalizado, las muestras recogidas en una tarjeta de papel permiten la detección de anticuerpo, carga viral y genotipo y se pueden analizar en prácticamente cualquier equipo de sistema hospitalario, aunque en este momento este procedimiento no está normalizado y aprobado por los fabricantes de carga viral para el uso en sus equipos66,67.
- ∘
Sistemas de detección de anti-VHC en sangre capilar y/o saliva en aproximadamente 20min68.
- ∘
Sistemas de detección del ARN-VHC in situ, rápidos, individuales, como los sistemas basados en sangre capilar69.
- ∘
Sistemas POC para determinación de Ag Core.
Cualquiera de los sistemas utilizados para la detección del VHC, debe ser seguido de una política de comunicación efectiva. En este sentido, los sistemas informáticos de alerta incrementan significativamente las tasas de diagnóstico y derivación efectivas50.
La AEEH recomienda el diagnóstico en un único paso, pero también incluir los nuevos test diagnósticos descentralizados integrados o no en el sistema sanitario. Específicamente:
- –
Se recomienda efectuar una determinación de viremia en:
- ∘
Todos los pacientes con su primera serología positiva frente al VHC.
- ∘
En pacientes con infección resuelta que mantienen comportamientos de riesgo para la reinfección. En estos pacientes se debe evitar la repetición de anti-VHC, siendo recomendable la determinación de ARN del VHC con una periodicidad mínima anual.
- –
De forma general, no es imprescindible la determinación del genotipado viral.
- –
Dado que la principal barrera para la microeliminación consiste en el diagnóstico y la evaluación de los pacientes infectados, se debe usar el test que mejor se adapte a las peculiaridades del sistema sanitario, de la población o de la existencia de diferentes tipos de barreras (geográficas, culturales, etc.).
- –
Otra barrera importante es la vinculación a los centros terapéuticos.
- –
En un modelo descentralizado integrado, el TGSS resulta una buena alternativa.
- –
Disponer de un sistema de alertas integradas en la historia clínica electrónica, independientemente del tipo de test usado y del sistema de diagnóstico, facilita el acceso al tratamiento después del diagnóstico.
El tratamiento de la hepatitisC está indicado en los pacientes infectados por el VHC, independientemente del grado de fibrosis hepática o de la existencia de diferentes comorbilidades. El objetivo de este documento no es proporcionar al lector una guía del tratamiento de los pacientes con hepatitisC; en este sentido, les recomendamos consultar la guía de tratamiento de la hepatitisC de la AEEH. En la era de la eliminación, no solo es fundamental simplificar el diagnóstico de la infección, sino también abordar el tratamiento de la enfermedad de una forma sencilla para el paciente, que evite que se «escapen» pacientes, y esto solo se puede conseguir mediante circuitos asistenciales de máxima simplicidad. Para conseguir esta simplicidad podemos optar por la atención en uno de estos dos sistemas:
- –
Consultas de alta resolución hospitalarias, en las que a los pacientes se les valore la enfermedad hepática (fibrosis), sean atendidos por el especialista y se les prescriba y dispense la medicación de la forma más rápida y eficiente posible. En aquellos hospitales sin acceso inmediato a una elastografía de transición, el uso de índices indirectos de fibrosis como el FIB-4 u otros es una excelente alternativa70. Se puede definir como óptima la consulta de alta resolución en la que todo el proceso se efectúe en un solo día. Las consultas de alta resolución son importantes en los pacientes poco adherentes al sistema sanitario y en los que tienen fibrosis avanzada71,72.
- –
Desarrollo de dispositivos asistenciales no hospitalarios y en puntos de atención al paciente, especialmente para poblaciones vulnerables, donde se establezca el diagnóstico de forma rápida e inmediatamente se inicie el tratamiento64. Estas estrategias están especialmente indicadas en inmigrantes (sobre todo en zonas rurales), donde existan barreras geográficas, enfermos mentales, PQCD, alcohólicos, en centros penitenciarios de alta rotación y bajo tiempo de estancia, clínicas de atención sexual, centros de salud muy alejados o en centros de reducción de daños.
Los aspectos clave relativos al tratamiento que debemos recordar son:
- –
El tratamiento está indicado en todos los pacientes con una infección activa por el VHC. Se recomienda un régimen pangenotípico, de alta eficacia, independientemente del grado de fibrosis hepática.
- –
La duración del tratamiento debe ser de entre 8 y 12semanas y la vía de administración, oral.
- –
Durante el tratamiento no es necesario realizar visitas médicas de seguimiento, excepto en los pacientes con riesgo de complicaciones por su enfermedad hepática avanzada o en los que pueda existir duda del cumplimiento terapéutico.
- –
La evaluación de la enfermedad hepática, de la dispensación y de la prescripción idealmente se debe efectuar en una única visita.
- –
Dado que la prescripción de los AAD se debe efectuar en un hospital, abogamos por la coordinación de estos dispositivos asistenciales de diagnóstico y tratamiento in situ con centros hospitalarios donde se produzca la prescripción y, mediante una dispensación y custodia delegada, esta se efectúe en el centro periférico.
- –
Es necesario el establecimiento de sistemas de información y/o alertas adecuados que eviten la pérdida de continuidad entre diagnóstico y tratamiento.
- –
En cuanto al seguimiento de estos pacientes, es importante hacer una diferenciación entre la curación virológica (esta se alcanzará en la práctica totalidad de los pacientes) y la curación de la enfermedad.
- ∘
Los pacientes curados sin fibrosis o con fibrosis leve pueden ser dados de alta una vez que se confirme la respuesta virológica sostenida (RVS).
- ∘
Los pacientes con fibrosis avanzada y cirrosis deben ser seguidos de manera indefinida.
- –
Para evaluar de una forma consistente la incidencia de la reinfección debemos utilizar una única definición de recidiva y reinfección. Académicamente no es totalmente correcto, y la definición más operativa de reinfección es:
- ∘
Recidiva de la infección: reaparición de la viremia en cualquier momento entre el inicio del tratamiento y hasta 12semanas después de finalizado el mismo (incluso sin necesidad de hacer genotipado ni pre ni posterior al tratamiento).
- ∘
Reinfección: reaparición de la viremia en cualquier momento a partir de las 12semanas después de finalizado el tratamiento (sin necesidad de hacer genotipado ni pre ni posterior al tratamiento).
- ∘
No obstante, la definición anterior que diferencia entre recidiva y reinfección basada en el tiempo puede no ser totalmente adecuada. En nuestro medio es relativamente frecuente la reinfección entre el final del tratamiento y las 12semanas postratamiento en personas con conductas de riesgo.
- –
En los pacientes con una infección por VHC previa que continúan con exposición a factores de riesgo es necesaria la determinación anual de carga viral según recomiendan las guías clínicas. Es decir, el cribado de una potencial reinfección por el VHC no se debe hacer con anti-VHC sino con técnicas moleculares (PCR-VHC).
- –
Se debe facilitar la posibilidad de realizar una determinación de la viremia a todos los dispositivos asistenciales extrahospitalarios (atención primaria, agentes comunitarios) con los que interaccionan estas personas.
- –
Debemos reforzar la formación multidisciplinar y transversal de todos los colectivos que intervienen en la atención de poblaciones vulnerables con alto riesgo de infección por el VHC.
- –
Se debe incrementar el conocimiento de la hepatitisC en atención primaria para asegurar el adecuado manejo de los pacientes y la transmisión de una correcta información a ellos. Esta formación debe dirigirse a dos aspectos: el cuidado del paciente y evitar la transmisión.
- –
Fomentar el papel potencial de enfermeras consultoras, que pueden contribuir al seguimiento del paciente una vez el especialista haya indicado el tratamiento.
- –
En poblaciones alejadas de centros sanitarios (España vaciada), una alternativa puede ser la coordinación entre farmacias y centros de asistencia primaria para que la administración se realice allí.
- –
Se deben implementar planes de formación continuada para los profesionales sanitarios basados en el conocimiento de este plan u otros planes de eliminación del VHC con dos áreas de trabajo: formativa e informativa.
- –
Se debe hacer un plan integrado de información al paciente:
- ∘
Proporcionar información, unificada y consensuada por los distintos servicios de farmacia, de forma oral y escrita, sobre el tratamiento prescrito, así como un contacto directo con el servicio de farmacia (teléfono/correo electrónico) para la resolución de dudas.
- ∘
Fomentar la formación y la educación al paciente para propiciar un paciente motivado, comprometido, experto y activo con su autocuidado y con la importancia de cumplir su tratamiento.
- ∘
Información sobre el estilo de vida y la dieta.
- ∘
Facilitar webs de consulta de información fiables.
La AEEH recomienda:
- –
El tratamiento está indicado en todos los pacientes infectados por el VHC.
- –
Se debe facilitar la dispensación delegada en poblaciones vulnerables.
Un programa de eliminación no se puede llevar a cabo sin el apoyo de las instituciones sanitarias. En nuestra opinión, es imprescindible la actualización del PEAHC, que debe compatibilizarse con los planes regionales que adaptan ese plan nacional a la realidad de cada comunidad autónoma. En este sentido, ya contamos con los primeros planes autonómicos dirigidos a la eliminación del VHC. De esta forma se van añadiendo las políticas de «microeliminación regional» para conseguir la «eliminación nacional»: Plan Cantabria73, Plan Aragón74, Plan Galicia, Plan Canarias75, Plan Cataluña76, Plan Madrid77, Plan Murcia y Plan Navarra. Así mismo, es periódica la publicación de los planes de diferentes países: Australia78, Escocia79, Francia80, Egipto81, Grecia82, Holanda83, Islandia84, Suiza85, Tailandia86, Estados Unidos87, Ruanda88, Mongolia89, Pakistán90 o Georgia91. Si bien no disponemos de resultados actualizados de su puesta en marcha, algunos trabajan en su modelización para implantarlos. Para las sociedades científicas, como la AEEH, fomentar estos planes regionales es muy importante. Entre los diferentes objetivos de estos planes destacan:
- –
Definir y desarrollar estrategias de microeliminación en los focos primarios.
- –
Incidir en la educación para la salud para evitar reinfecciones en colectivos vulnerables.
- –
Instaurar programas de reducción de daños.
- –
Crear nuevos programas asistenciales específicos para los internos de centros penitenciarios y sujetos con penas no privativas de libertad.
- –
Abogar por el paso de las responsabilidades sanitarias de los centros penitenciarios y de los centros de tratamiento de adicciones al sistema público de salud, tal y como establece la ley (Ley 16/2003, de 28 de mayo, de cohesión y calidad del Sistema Nacional de Salud; BOE núm. 128, de 29/05/2003).
- –
Instaurar nuevas vías asistenciales en los colectivos alejados del sistema sanitario (grupos vulnerables).
- –
Creación de centros o referentes comunitarios de cribado para combatir los focos primarios.
- –
Garantizar la homogeneidad y la coordinación territorial en el abordaje de la hepatitisC.
- –
Desarrollar políticas de prevención que incidan en las prácticas de riesgo.
- –
Promover en el colectivo de hombres con prácticas homosexuales la adopción de prácticas de sexo seguro y la realización del test del VHC dentro del abordaje por factores de riesgo acordado en el plan autonómico.
- –
Colaborar con las ONG que trabajan en el ámbito de los HSH, programas de prevención de enfermedades de transmisión sexual, virus de la hepatitisA (VHA), VHB, sida, sífilis, etc.
- –
Mantener los criterios básicos para la selección de donantes de sangre y/o sus componentes.
- –
Reforzar y actualizar, en su caso, las recomendaciones para evitar riesgos biológicos en procedimientos diagnósticos y terapéuticos invasivos, así como los protocolos de actuación postexposición frente al VHC por exposición ocupacional.
- –
Revisar el cumplimiento de los mecanismos de control de establecimientos de piercing, tatuaje y micropigmentación.
- –
Desarrollar intervenciones que permitan reducir el riesgo poblacional.
- –
Incrementar el conocimiento sobre la hepatitisC en la población general, mediante campañas de información a través de carteles, folletos, medios de comunicación, redes sociales, etc., que de forma sencilla y clara lleven el conocimiento y el mensaje a la población sobre qué es y cómo se transmite la hepatitisC y, sobre todo, que transmitan el mensaje de que su tratamiento es efectivo en nuestros días y la hepatitisC es una enfermedad curable.
- –
Disponer de recursos de educación como guías disponibles para distintos tipos de usuarios: pacientes, asociaciones, grupos de trabajo, etc.
Estas intervenciones requieren metodologías muy dinámicas basadas en la interacción y el trabajo interdisciplinar de las asociaciones de pacientes, del personal sanitario y de los medios de comunicación, para conseguir que el mensaje llegue al mayor número de personas posible, asegurando que los mensajes sean accesibles desde el punto de vista cultural y lingüístico para las distintas poblaciones diana. En este punto es muy importante la colaboración con trabajadores sociales y estamentos (ONG) que conocen la idiosincrasia de las distintas poblaciones de riesgo y poblaciones específicas para permitir el acercamiento y el trabajo con ellas.
- –
Diseño de material específico que sirva de base para la realización de talleres en el ámbito sanitario y comunitario, así como para la realización de actividades en el ámbito de los programas de educación afectivo-sexual del ámbito escolar.
- –
Diseñar acciones para reducir el riesgo en el sistema de salud. A pesar de la implantación de medidas de seguridad en el medio sanitario, la incidencia de nuevos casos de hepatitisC continúa en este entorno, atribuido a prácticas inseguras o a un inadecuado control de la infección.
- –
El plan de acción para proteger a pacientes y trabajadores dentro del entorno sanitario deber incluir:
- ∘
Mejorar la vigilancia y la detección de casos producidos en el entorno sanitario.
- ∘
Disminuir el riesgo asociado a un manejo inadecuado de instrumental desechable y jeringas mediante la reducción de la exposición a instrumental percutáneo y la actualización de las guías para el manejo de la exposición a VHC en el entorno sanitario.
- ∘
Proveer la educación necesaria en los aspectos más importantes de esta infección para su adecuado control en centros sanitarios de agudos, de crónicos y en el control ambulatorio.
- ∘
Manipulación y eliminación segura de objetos afilados y desechos contaminados.
- ∘
Análisis de la sangre donada.
- ∘
Capacitación del personal sanitario: lavado de manos y uso de guantes, incluida la preparación de las manos para cirugía; limpieza segura de los equipos medicoquirúrgicos.
El objetivo global de eliminación del VHC precisa del desarrollo de diferentes indicadores que permitan evaluar los resultados en salud de las diferentes intervenciones que se vayan realizando, tanto a nivel de cribado como de microeliminación o de diagnóstico y tratamiento. Entre ellos pudieran efectuarse:
Indicadores de participación- –
Población diana de cada programa (macro y microeliminación).
- –
Tasa de detección de anti-VHC/PCR-VHC.
- –
Incidencia bianual/trianual de VHC. Repetición cada 2-3años de estudios de prevalencia.
- –
Ratio diagnóstico/diagnóstico de la infección en un solo paso.
- –
Ratio diagnóstico/diagnóstico no centralizado.
- –
Indicadores del impacto de diagnóstico y tratamiento a medio plazo: número de pacientes diagnosticados de hepatocarcinoma, número de ingresos hospitalarios por VHC, número de trasplantes por VHC, mortalidad por VHC.
- –
Porcentaje de pacientes con infección previa conocida/desconocida.
- –
Porcentaje de pacientes con enfermedad leve/avanzada.
- –
Enfermedad extrahepática.
- –
Coinfecciones: VIH, VHB.
- –
Forma de presentación de la enfermedad: precoz o tardía. Si es tardía: descompensación y tipo y hepatocarcinoma.
- –
Ratio diagnosticados/tratados.
- –
Ratio tratamientos instaurados en la primera consulta/tratamientos instaurados.
- –
Tratamientos empleados.
- –
RVS.
La AEEH recomienda:
- –
El uso de indicadores de resultados es crítico para la evaluación de la eliminación del VHC.
- –
No se ha demostrado la superioridad de unos sobre otros, por lo que es deseable la utilización de al menos un marcador de cada una de las categorías indicadas con anterioridad.
Coordinador: Javier Crespo.
Grupo redactor: Agustín Albillos, María Buti, José Luis Calleja, Javier García-Samaniego, Manuel Hernández-Guerra, Trinidad Serrano, Juan Turnes.
Grupo revisor: Enrique Acín García, Juan Berenguer, Marina Berenguer, Joan Colom, Inmaculada Fernández, Conrado Fernández Rodríguez, Xavier Forns, Federico García, Rafael Granados, Jeffrey Lazarus, José María Molero, Esther Molina, Fernando Pérez Escanilla, Juan Antonio Pineda, Manuel Rodríguez, Manuel Romero, Carlos Roncero, Pablo Saiz de la Hoya, Gloria Sánchez Antolín.
Este documento se publica simultáneamente en las revistas [Gastroenterología y Hepatología - https://doi.org/10.1016/j.gastrohep.2019.09.002] y [Revista Española de Enfermedades Digestivas - https://doi.org/10.17235/reed.2019.6700/2019], con el consentimiento de los autores y editores.