Aun siendo los anti-TNF fármacos eficaces y seguros se han comunicado diversas alteraciones hematológicas como la neutropenia que puede llevar a infecciones graves.
Presentamos el caso de una mujer de 30 años diagnosticada de enfermedad de Crohn a los 8 años de edad con patrón estenosante y localización ileo-cólica e intestino delgado, (previamente intervenida) y en tratamiento con Humira® 40mg cada 15 días desde 2007, intensificado en 2014 por pérdida de respuesta.
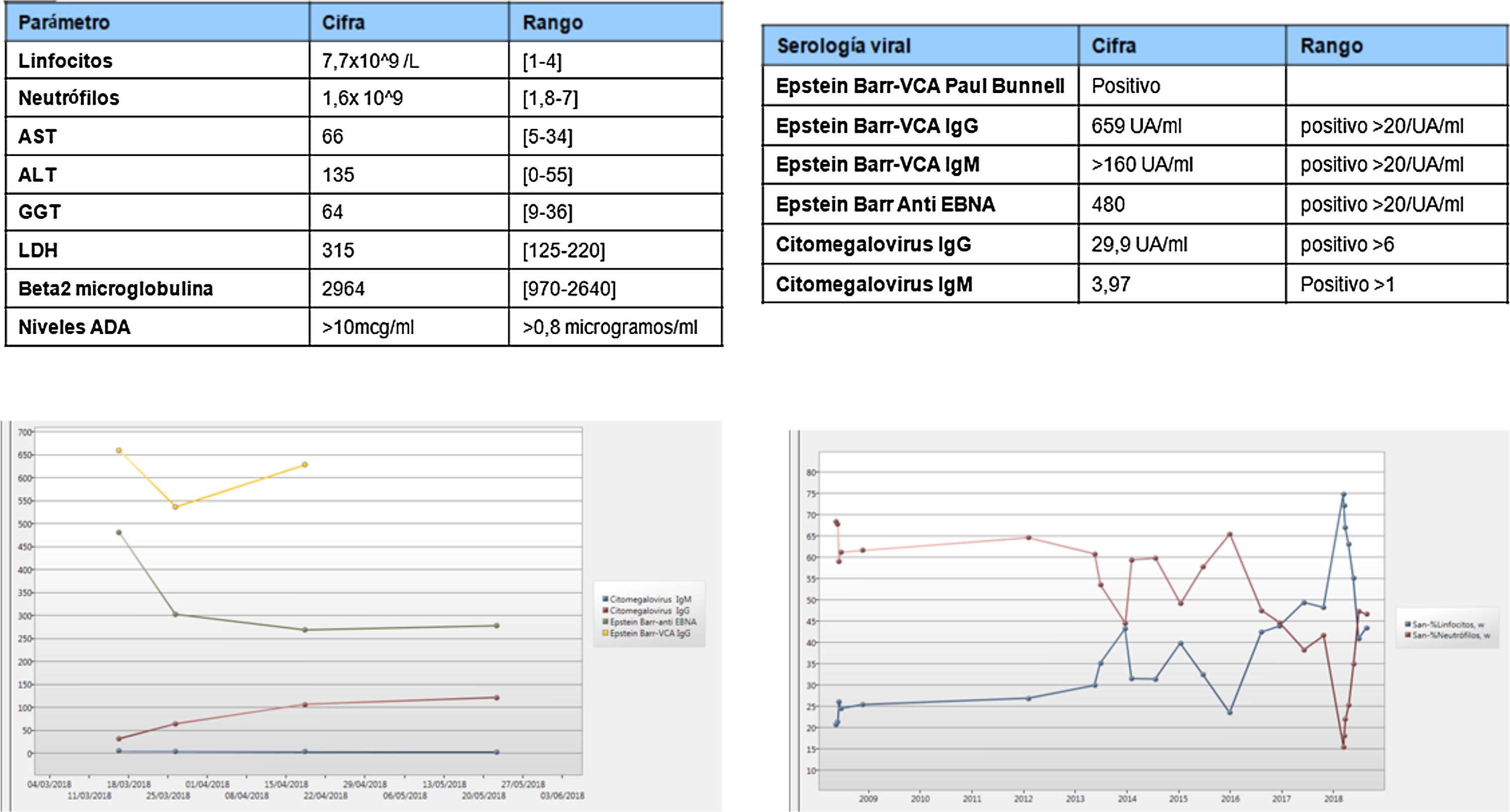
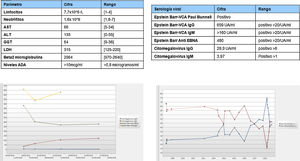
En noviembre 2017 se desintensifica por remisión clínica persistente realizándose analítica de control a los 4 meses con los resultados que se muestran en la (fig. 1A). La morfología linfocitaria estaba alterada con predominio de linfocitos grandes granulares (LGG). Se amplió analítica con serologías virales (fig. 1B) y ecografía abdominal identificando esplenomegalia.
Ante la sospecha de síndrome mielodisplásico se realizó citometría de flujo sin alteraciones de la clonalidad sugestivas de malignidad.
El cuadro se interpreta como secundario a ADA y reactivación viral posterior. Se decide suspender el fármaco y vigilancia posterior con seguimiento analítico a los dos meses (figs. 1C y 1D).
A los 3 meses de suspender la medicación presenta actividad clínica iniciando ustekinumab sin alteraciones analíticas posteriores hasta le fecha (semana 52).
A pesar de que los fármacos anti-TNF son seguros, por su acción, se ha descrito un mayor riesgo de infecciones y trastornos hematológicos como la neutropenia1.
El descenso de neutrófilos confiere riesgo de infecciones y puede deberse a causas primarias (procesos hematológicos malignos) o secundarias, la mayoría tóxicas asociadas a fármacos.
Los propios anti-TNF y alteraciones morfológicas linfocitarias secundarias como los LGG juegan un papel en la neutropenia asociada a anti-TNF pudiendo suprimir la hematopoyesis, pudiendo ser parte de un síndrome mielodisplásico inicial1–4
Los LGG son un subgrupo de linfocitos T dentro de las células Natural Killer que aparecen de manera normal en el 10-15% sangre periférica2,3.
Pueden tener origen monoclonal como en leucemia de linfocitos grandes granulares, síndromes mielodisplásicos, o no monoclonal secundaria a infecciones virales, trastornos hematológicos como el linfoma o autoinmunes.
Estudios de ensayos clínicos en EII y artritis reumatoide establecen una incidencia de neutropenia (<1000 en recuento) de 0,6%-0,9% para ADA y de 1,1-5,7% para Infliximab. A pesar de esto el 81% de los pacientes permanecieron con el mismo tratamiento mientras que el resto cambiaron de anti-TNF a pesar de lo cual el 62,5% tuvieron que suspenderlo por neutropenia recurrente1.
Se recomienda cese del fármaco en neutropenias severas (<500 en recuento) e investigar causas secundarias como trastornos hematológicos.
Con estos datos se sabe que la neutropenia transitoria o persistente asociada a anti-TNF está siendo infraestimada presentándose únicamente comunicaciones en forma de series de casos.
Debido a la inmunosupresión asociada a los anti-TNF como la neutropenia o los LGG, el riesgo de infecciones (tanto primoinfección como reactivación) sobretodo virales como el VEB puede inducir también cambios en la diferenciación celular de los linfocitos B o T pudiendo ser el precipitante de síndromes mielodisplásicos persistentes1,5.
Por tanto tenemos dos fenómenos concomitantes que inducen tanto neutropenia como LGG. En nuestro caso coexisten ambos fenómenos (ADA y sospecha de reactivación viral) así como la alteración linfocitaria. Cabría pensar cuál fue la causa inicial. Se conoce que la reactivación del VEB puede inducir cambios en serologías de CMV como en nuestra paciente y también que las reactivaciones virales en pacientes inmunodeprimidos pueden ser oligosintomáticas4,5. Probablemente al ser un evento asintomático, las cargas virales fuesen negativas en el momento de los análisis mientras que los cambios serológicos han persistido.
Tras la suspensión de la medicación la morfología de sangre periférica se normalizó en días mientras que las alteraciones serológicas han continuado alteradas por lo que parece que la presencia de los LGG se deba al fármaco anti-TNF y esto haya propiciado una reactivación viral.
En resumen tanto los anti-TNF que producen cambios en la médula ósea como los LGG, como el riesgo de reactivación de infecciones, principalmente el VEB, pueden inducir síndromes mielodisplásicos asociados.
En el caso de le EII estaría pendiente evaluar dicho riesgo ya que las guías de monitorización no incluyen la realización de serologías periódicas y la mayoría de estudios y series de casos descritos han sido en pacientes con enfermedades reumatológicas.