La medida de los resultados percibidos por el paciente en la asistencia de la enfermedad inflamatoria intestinal (EII) adquiere cada vez más importancia. Existe una herramienta sencilla y validada en inglés para este fin: el «IBD-Control». Nuestro objetivo es traducirlo al español, adaptarlo y validarlo.
Pacientes y métodosSe tradujo el IBD-Control, generando el instrumento en español «EII-Control», y se validó prospectivamente. Los pacientes cumplimentaban el EII-Control y otros cuestionarios que servían de comparadores de referencia. El gastroenterólogo realizaba una valoración global de la enfermedad, calculaba índices de actividad y registraba el tratamiento. Un subgrupo de pacientes repitió toda la valoración en una segunda visita. Se analizó también la utilidad de escalas resumidas del EII-Control (el EII-Control-8 y el EII-Control-EVA).
ResultadosSe incluyeron 249 pacientes con EII (101 repitieron la segunda visita). Estándares psicométricos del test: consistencia interna: α de Cronbach para EII-Control 0,83 con fuerte correlación entre EII-Control-8 y EII-Control-EVA (r=0,5); reproducibilidad: correlación intraclase 0,70 para EII-Control; validez de constructo: correlaciones de moderadas a fuertes entre EII-Control, EII-Control-8 y EII-Control-EVA frente a comparadores; validez discriminante: p <0,001; sensibilidad al cambio: misma respuesta que índice de calidad de vida. Sensibilidad y especificidad en el punto de corte 14 de 0,696 y 0,903, respectivamente, para determinar el estado quiescente.
ConclusionesEl EII-Control es un instrumento válido para medir el control de la EII desde la perspectiva del paciente en nuestro medio y cultura. Su simplicidad lo convierte en una herramienta útil para apoyar la asistencia.
Measurement of patient-perceived outcomes in inflammatory bowel disease (IBD) care is becoming increasingly important. A simple and validated tool exists in English for this purpose, the “IBD-Control”. Our aim is to translate it into Spanish, adapt and validate it.
Patients and methodsThe IBD-Control was translated into the Spanish instrument “EII-Control” and prospectively validated. Patients completed the EII-Control and other questionnaires that served as baseline comparators. The gastroenterologist performed a global assessment of the disease, calculated activity indices and recorded treatment. A subgroup of patients repeated the entire assessment at a second visit. The usefulness of IBD-Control summary scales (IBD-Control-8 and IBD-Control-VAS) was also analysed.
ResultsA total of 249 IBD patients were included (101 repeated the second visit). Psychometric standards of the test: internal consistency: Cronbach's α for EII-Control 0.83 with strong correlation between EII-Control-8 and EII-Control-EVA (r=0.5); reproducibility: intra-class correlation 0.70 for EII-Control; construct validity: moderate to strong correlations between IBD-Control, IBD-Control-8 and IBD-Control-VAS versus comparators; discriminant validity: P<.001; sensitivity to change: same response as quality of life index. Sensitivity and specificity at cut-off point 14 of 0.696 and 0.903, respectively, to determine quiescent status.
ConclusionsThe IBD-Control is a valid instrument to measure IBD-Control from the patient's perspective in our environment and culture. Its simplicity makes it a useful tool to support care.
La enfermedad inflamatoria intestinal (EII) es una dolencia crónica del tracto gastrointestinal que comprende 2 entidades principales: la enfermedad de Crohn (EC) y la colitis ulcerosa (CU), además de la colitis indeterminada o inclasificable, que es mucho menos frecuente1–3. La EII suele cursar con periodos de actividad y de remisión. Cuando la enfermedad se encuentra activa, las manifestaciones clínicas predominantes en la EC son el dolor abdominal y la diarrea, mientras que en la CU son la presencia de diarrea y rectorragia1,2. Estos síntomas afectan muy negativamente a la vida de los pacientes, con un componente individual subjetivo intrínseco que es importante (calidad de vida [CV] percibida). Es en este contexto donde surge el concepto de resultados percibidos por los pacientes (PRO, por patient reported outcomes), y su medida (PROM, por patient reported outcomes measurement) como evaluación de su propio estado funcional y bienestar.
Un objetivo muy importante del tratamiento de la EII es alcanzar y mantener su control sintomático para mejorar e idealmente normalizar su CV. Por lo tanto, evaluar el control de la EII desde la perspectiva del paciente es un aspecto básico en la toma de muchas decisiones terapéuticas. Esto explica el interés creciente por la medición de los PRO, tanto para los clínicos como para las agencias reguladoras y autoridades sanitarias4,5. Así, actualmente se incluyen sistemáticamente en la evaluación de los nuevos tratamientos, junto con las valoraciones más clásicas (índices clínicos, parámetros de laboratorio, biomarcadores o endoscopia)6–8. Merece la pena insistir en que los índices o variables clínicas no son objetivos y no evalúan la perspectiva del paciente sobre el impacto que tiene en él la enfermedad9, algo que sí hacen los PRO. También han empezado a tener un papel en auditorías y registros nacionales4. Para evaluar los PRO se dispone de cuestionarios estandarizados y validados. Su desarrollo viene esencialmente de la última década, y ha dado lugar al desarrollo de PROM de múltiples dominios, tanto específicos de enfermedad (síntomas) como generales (bienestar, energía o vitalidad, impacto en la esfera física, social y emocional)10–16.
De la misma forma que estos instrumentos se aplican cada día más en los ensayos clínicos11,15, aumenta el interés por su capacidad de aportar información para la asistencia práctica individual. Sin embargo, aún no se usan habitualmente en la práctica diaria. Uno de los motivos puede ser la carga en tiempo que supondría, para paciente y profesional sanitario, usar cuestionarios largos multidominio. Resulta lógico pensar que cuestionarios abreviados, si demostraran su utilidad, podrían incorporarse a nuestra práctica clínica17,18. El instrumento ideal debería ser sencillo de cumplimentar e interpretar, y aportar un valor añadido relevante en la asistencia práctica. Debería ser fiable (preciso en su medición) y válido (capaz de medir aquello para lo que se ha diseñado). Una herramienta así podría suponer un avance como personalización real del tratamiento.
En este sentido, Bodger et al. han desarrollado y validado un cuestionario en el Reino Unido, destinado a capturar rápidamente el control de la EII desde la perspectiva del paciente, que han denominado «IBD-Control»19. Los criterios seguidos en su elaboración fueron su brevedad y sencillez a la hora de cumplimentarlo e interpretarlo y ser «genérico» en su contenido, con el propósito de maximizar su potencial uso práctico y en el mayor espectro de pacientes con EII.
El interés de este índice para la práctica clínica es evidente, pero es muy recomendable su validación formal en otras poblaciones de EII antes de recomendar su uso. En español no disponemos de ningún instrumento similar. El objetivo de nuestro trabajo es traducir al español y validar el uso del IBD-Control en nuestro medio, para conseguir el primer cuestionario de PROM traducido y validado al español, que podría ser utilizado en investigación y en la práctica clínica.
MetodologíaEl objetivo de nuestro estudio es traducir al español el IBD-Control («EII-Control» en español) y demostrar su fiabilidad, validez y sensibilidad en la medición del control de la EII, tanto en la CU como en la EC en nuestro medio (entendido como un idioma y cultura). El proceso y metodología replican, salvo mínimas diferencias deliberadas, los llevados a cabo con el índice original.
Nuestra unidad de EII del Hospital Universitario Miguel Servet atiende a más de 1.500 pacientes, a los que proporcionamos tanto la atención ambulatoria como en sus ingresos. Nuestra unidad se ha acreditado, de acuerdo con los estándares de calidad del Grupo Español de Trabajo en Enfermedad de Crohn y Colitis Ulcerosa (GETECCU), como unidad de atención integral a pacientes con EII. Los profesionales que la integramos (facultativos y enfermeras) tenemos una amplia experiencia en el control de la EII.
Descripción breve del IBD-Control (original, en inglés): desarrollo y validaciónEl IBD-Control19 es un documento corto (una única carilla en formato A4) y simple, con 5 apartados. Los primeros 4 contienen 13 preguntas categóricas y el quinto es una escala visual analógica (EVA horizontal). Se pregunta al paciente sobre el control de la EII en las 2 últimas semanas. El«EII-Control-8» es una subpuntuación que se calcula con la suma de las puntuaciones de 8 preguntas. Se traduce en un intervalo de 0-16 (0=peor control). Tanto el IBD-Control-8 como la EVA tienen por objeto representar una medida resumen del mismo constructo.
Sus fases de desarrollo y validación fueron exhaustivas y rigurosas. Se utilizaron como comparador de referencia del IBD-Control varias mediciones, incluyendo índices de actividad clásicos de la EII, cuestionarios de calidad de vida genéricos y específicos, y la evaluación global del médico.
Traducción y validación del IBD-Control al español: el EII-ControlEstudio prospectivo, en un solo centro, con 2 fases: traducción y posterior validación prospectiva del cuestionario IBD-Control al español: el EII-Control.
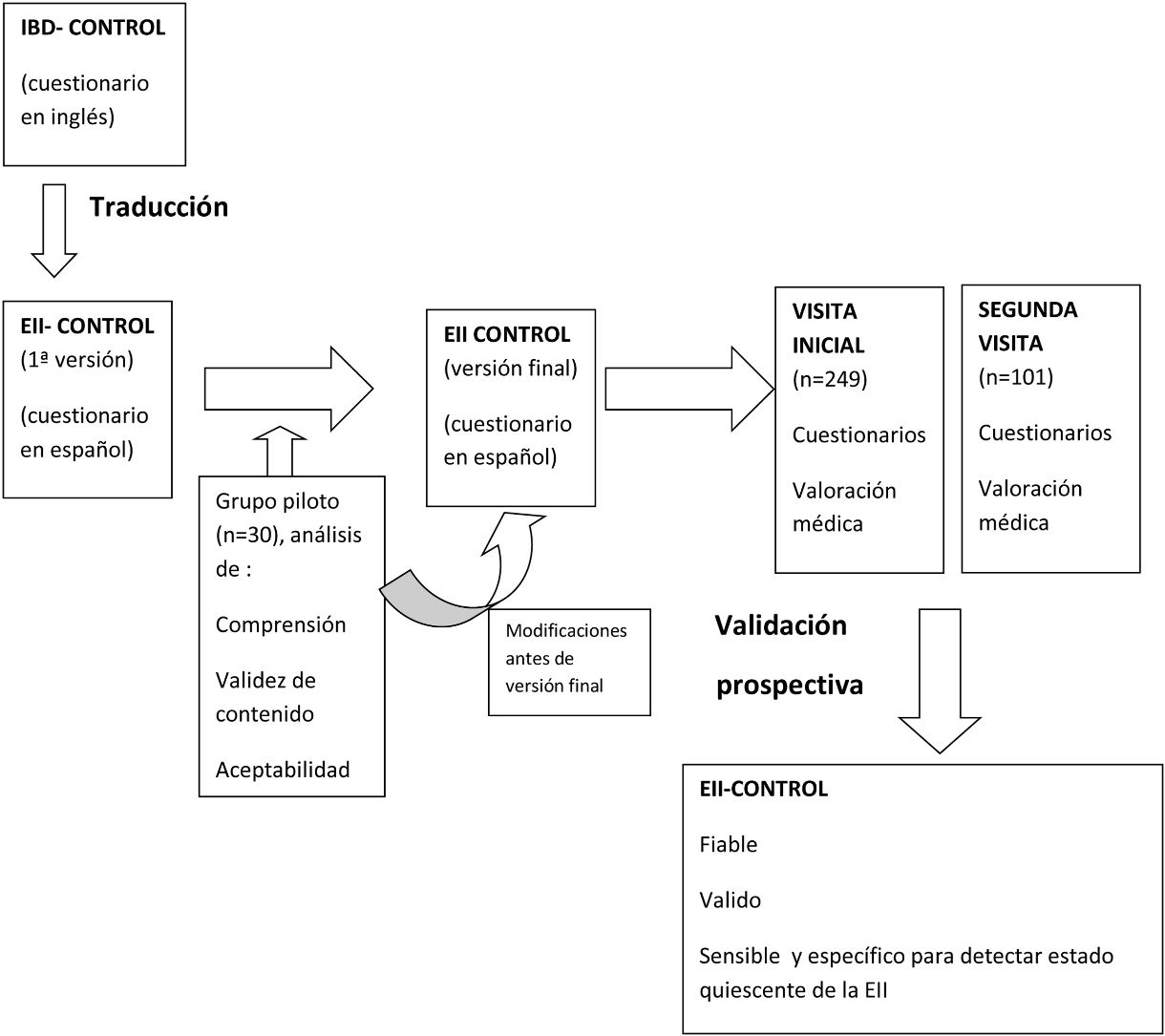
Traducción del cuestionario: el EII-ControlLa traducción fue realizada por miembros de nuestro grupo expertos en habla inglesa. Tras la traducción inicial, al igual que en el trabajo original, se determinó de forma estructurada su comprensión, validez del contenido y aceptabilidad, por un grupo de 30 pacientes al que llamamos «grupo piloto». Se les solicitó, tras leer el cuestionario traducido, sus anotaciones/comentarios/dudas en relación con el contenido y formato del mismo, aclarando con el equipo investigador todas ellas, e implementando sus cambios por consenso del grupo, lo que dio lugar a la versión final: el EII-Control.
Fase de validación prospectiva del cuestionario EII-ControlLos pacientes incluidos fueron valorados en 2 visitas sucesivas: visita inicial y segunda visita, bien de seguimiento programado, bien por necesidad ante la reactivación de la EII dentro del periodo de estudio, que comprendió desde el 1 de marzo de 2016 al 30 de septiembre de 2016. En ambas visitas se obtenía, como se detalla más adelante, el EII-Control, otros cuestionarios, índices de actividad y adicionalmente otras variables.
Población de estudioPacientes consecutivos atendidos en la consulta monográfica, diagnosticados de EII (EC, CU o colitis indeterminada), de acuerdo con los criterios habituales (Lennard-Jones), mayores de edad y que aceptaron participar en el estudio, tras su explicación detallada y la firma del consentimiento informado. Excluimos a personas con deterioro cognitivo o con incapacidad para entender o rellenar los cuestionarios. Disponemos y se recogieron también todos los datos relevantes sobre su EII (localización, extensión, fenotipo, existencia o no de enfermedad perianal, duración, número de hospitalizaciones previas y cirugías, presencia o no de estomas, tratamiento actual, comorbilidad y hábito tabáquico).
Evaluaciones realizadas en las visitasEn cada visita (inicial y segunda visita) se obtuvieron las evaluaciones necesarias para la validación del test.
- •
Cuestionarios: los pacientes cumplimentaron de forma autoadministrada los siguientes cuestionarios en una herramienta informática colocada para dicho fin en la sala de espera de consultas externas, siendo asistidos en su primer uso por la enfermera de investigación, y siempre en caso de necesidad.
- -
EII-Control (cuestionario a validar, anexo i).
- -
Cuestionario de calidad de vida específico para la EII en español, en su versión reducida: CCVEII-9.
- -
Cuestionario general de calidad de vida (EuroQol), versión española: EQ-5D24.
- -
Cuestionario de ansiedad (HAS) y depresión (HDS), versión española25.
- -
Escala de severidad de la fatiga (FSS), versión española; este cuestionario fue añadido en nuestro estudio, no estando incluido en el trabajo original de Bodger et al.19. Decidimos incluirlo, dada la importancia de este síntoma en los pacientes con EII.
- •
Índices de actividad y valoración por el médico: el médico que atendía al paciente calculaba los índices de actividad correspondientes (índice simple de actividad clínica para la CU y Harvey-Bradshaw para la EC) y establecía una valoración clínica global (remisión, leve, moderada o grave), de forma ciega respecto a los resultados de los cuestionarios completados por el paciente. Se registró el tratamiento que el paciente llevaba en ese momento y todo cambio terapéutico derivado de la consulta que implicaba un cambio en la situación del paciente (inicio de nuevos tratamientos, modificación o suspensión de las dosis de los fármacos previos o indicación de valoración/tratamiento quirúrgico).
- •
Analíticas, biomarcadores y otras exploraciones/pruebas diagnósticas: todos los pacientes disponían, en ambas visitas, de analíticas recientes (dentro del mes anterior a la visita), incluyendo biomarcadores y otras determinaciones relevantes.
Las propiedades psicométricas evalúan la fiabilidad (precisión de la escala de medida, es decir, determinación del mínimo error de medida) y la validez (capacidad del instrumento de medir aquellas características que pretende medir) del EII-Control. La fiabilidad incluye la consistencia interna (homogeneidad de los ítems que componen una escala; dado que pretenden medir un mismo concepto, es esperable que sus respuestas estén relacionadas entre sí) y la reproducibilidad/repetibilidad de las mediciones (grado en que la medida proporciona resultados idénticos o similares al usarla repetidamente en los mismos individuos cuando su condición de salud no ha cambiado). La validez incluye la validez de constructo (analizar si el cuestionario está relacionado con la medición deseada) y la capacidad de respuesta (detección en el tiempo de cambios relevantes), determinando los puntos de corte que discriminan enfermedad quiescente de activa. Veamos los detalles estadísticos de estas mediciones.
La consistencia interna se evaluó para las preguntas categóricas y las subescalas (EII-Control-8 y EII-Control-EVA, con el coeficiente α de Cronbach26 y con la correlación medida con el coeficiente de Spearman de cada una de las preguntas con la EVA del EII-Control y con el valor general del CCVEII-9.
La reproducibilidad/repetibilidad se evaluó con el coeficiente de correlación intraclase en primer lugar, en todos los pacientes que completaron las 2 valoraciones en la visita inicial y segunda visita, y en segundo lugar, únicamente con pacientes con enfermedad estable en la segunda visita, controlada por valores iguales en la pregunta 2 de EII-Control (respuesta «sin cambios») y variación de al menos 10 puntos en el CCVEII-9.
La validez de constructo se evaluó mediante análisis de correlación y regresión por comparación de las puntuaciones derivadas del cuestionario, con medidas externas independientes del estado de salud del paciente. Estas medidas incluyeron los cuestionarios: EQ-5D, CCVEII-9, HAS y HDS, y FSS; los índices de actividad clínica y la valoración global del médico. Valores elevados de los coeficientes de correlación y un adecuado ajuste a los cuestionarios validados indican una adecuada validez. Las correlaciones positivas con los indicadores de CV indicarán una adecuada validez del cuestionario a evaluar, al igual que las correlaciones negativas con elementos relacionados con la salud o gravedad de la enfermedad, como indicadores de ansiedad, depresión o gravedad. La relación EII-Control y sus subescalas con la valoración médica se compararon con la prueba del análisis de la variancia. Las correlaciones bivariantes se expresaron como coeficientes de correlación de Spearman y las puntuaciones medias entre grupos se compararon con la prueba t o el análisis de la variancia. Se usó la regresión lineal variable múltiple para examinar la fuerza relativa y la independencia de las preguntas individuales como predictores de las diversas medidas externas del estado de salud y para seleccionar los ítems a incluir en las subpuntuaciones.
Se analizó también la validez de la subescala EII-Control-8 mediante la relación de los valores del cuestionario EII-Control-8 agrupados de 2 en 2 con los valores de la puntuación del cuestionario EQ-5D.
Para analizar la capacidad de respuesta o de predecir respuesta se seleccionaron los pacientes que habían presentado una reducción en su CV medida por el cuestionario CCVEII-9, es decir, los pacientes con menor valor en la puntuación de este cuestionario en la segunda visita que en la visita inicial. Se ha calculado por medio de la diferencia de medias de EII-Control, EII-Control-8 y EII-Control-EVA en 3 grupos de pacientes definidos por tener una variación inferior a 10, igual a 10 o superior a 10 en el cuestionario CCVEII-9 en la segunda visita respecto a la visita inicial. Se calculó el tamaño del efecto en ambos cuestionarios y se compararon.
Para determinar los puntos de corte para detectar el estado «quiescente» se definió «estado quiescente» en los pacientes que cumplieron estas 4 condiciones:
- •
Criterio médico de enfermedad inactiva («remisión» en la valoración global del médico).
- •
No recibir en ese momento tratamiento oral con corticoides, inducción con biológicos, antibióticos por la EII, estar en lista de espera de tratamiento quirúrgico ni precisar de escalada del tratamiento derivada de la visita.
- •
Índice simple de actividad clínica de la CU (SCCAI)<4 o índice de Harvey-Bradshaw≤4 y puntuación total del CCVEII 9 < 90.
- •
Respuesta de 0 o 2 en la pregunta 2 del cuestionario EII-Control (indica que la enfermedad no ha cambiado o ha mejorado en las 2 últimas semanas, es decir, excluye a los pacientes que respondan que los síntomas intestinales son «peores»).
Los sujetos que cumplían los 4 criterios anteriores se consideraron bien controlados o «quiescentes», y aquellos que no lo hacían, «no quiescentes». Se utilizó el análisis de eficacia diagnóstica para evaluar el rendimiento del EII-Control como herramienta para identificar a los pacientes quiescentes. Dada la aplicación clínica prevista, definimos unas puntuaciones límite óptimas, centrando el énfasis en lograr una alta especificidad (≥85%) para minimizar el riesgo de falsos positivos (identificar a un paciente no quiescente como quiescente). Se seleccionó el valor de corte con el producto sensibilidad×especificidad más alto, de la forma descrita.
Cálculo del tamaño muestral y análisis estadísticoEl trabajo original está realizado con 300 pacientes en un área de población similar a nuestro centro (350.000-400.000 personas). El tamaño muestral calculado, con un margen de error de un 5%, un nivel de confianza del 95% y asumiendo una heterogeneidad de la muestra del 50%, es de 250-300, similar al del trabajo original.
En el estudio descriptivo se han calculado media, mediana, desviación estándar, mínimo y máximo de las variables cuantitativas, y frecuencias absolutas y relativas de las variables cualitativas. El estudio psicométrico se hizo con la metodología reflejada en cada apartado específico.
Los datos obtenidos fueron recogidos en una base de datos Excel® y analizados posteriormente con el software SPSS®, licencia de uso de la Universidad de Zaragoza, con un nivel de confianza del 95%, lo que equivale a un error tipo i del 5%.
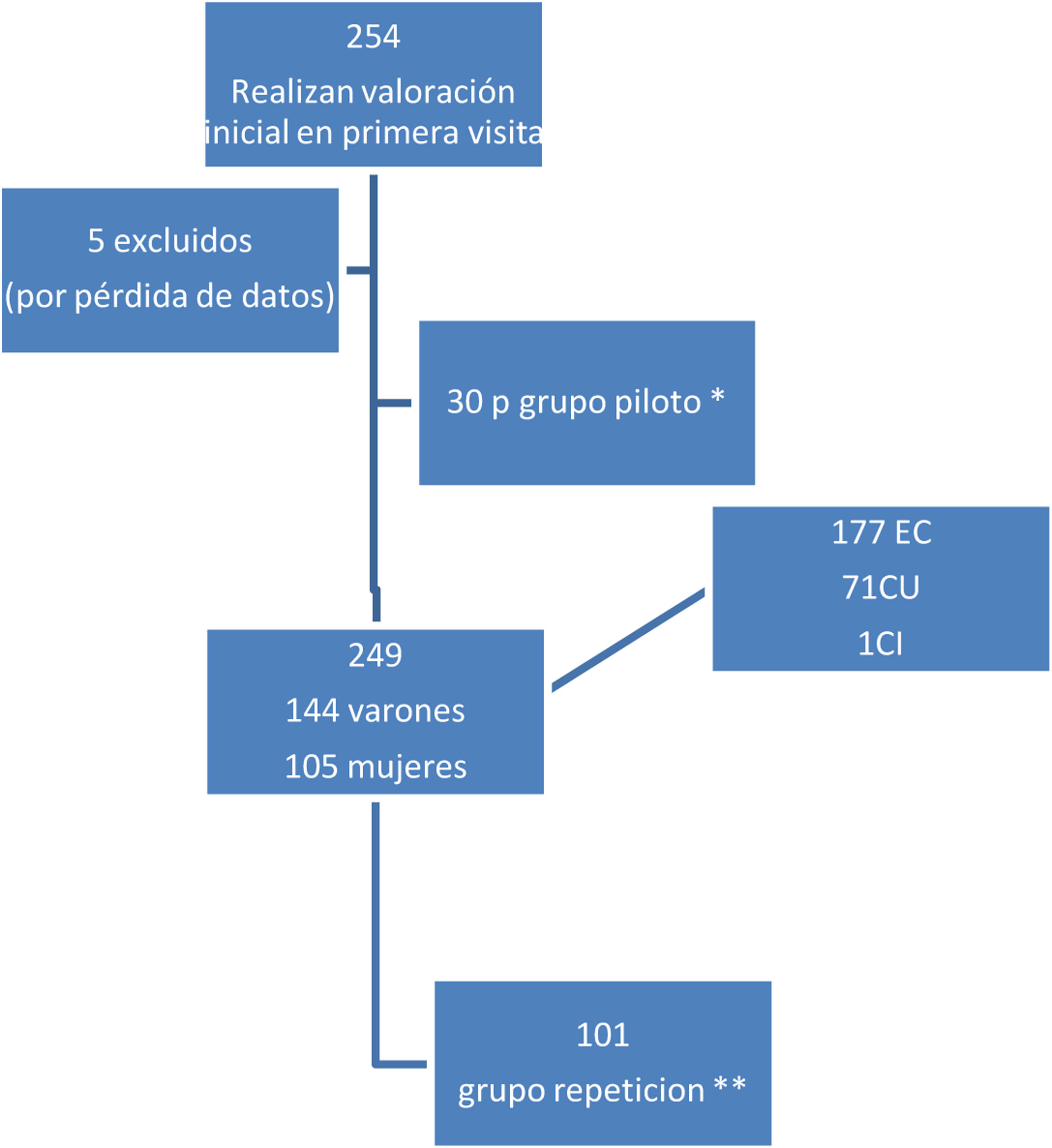
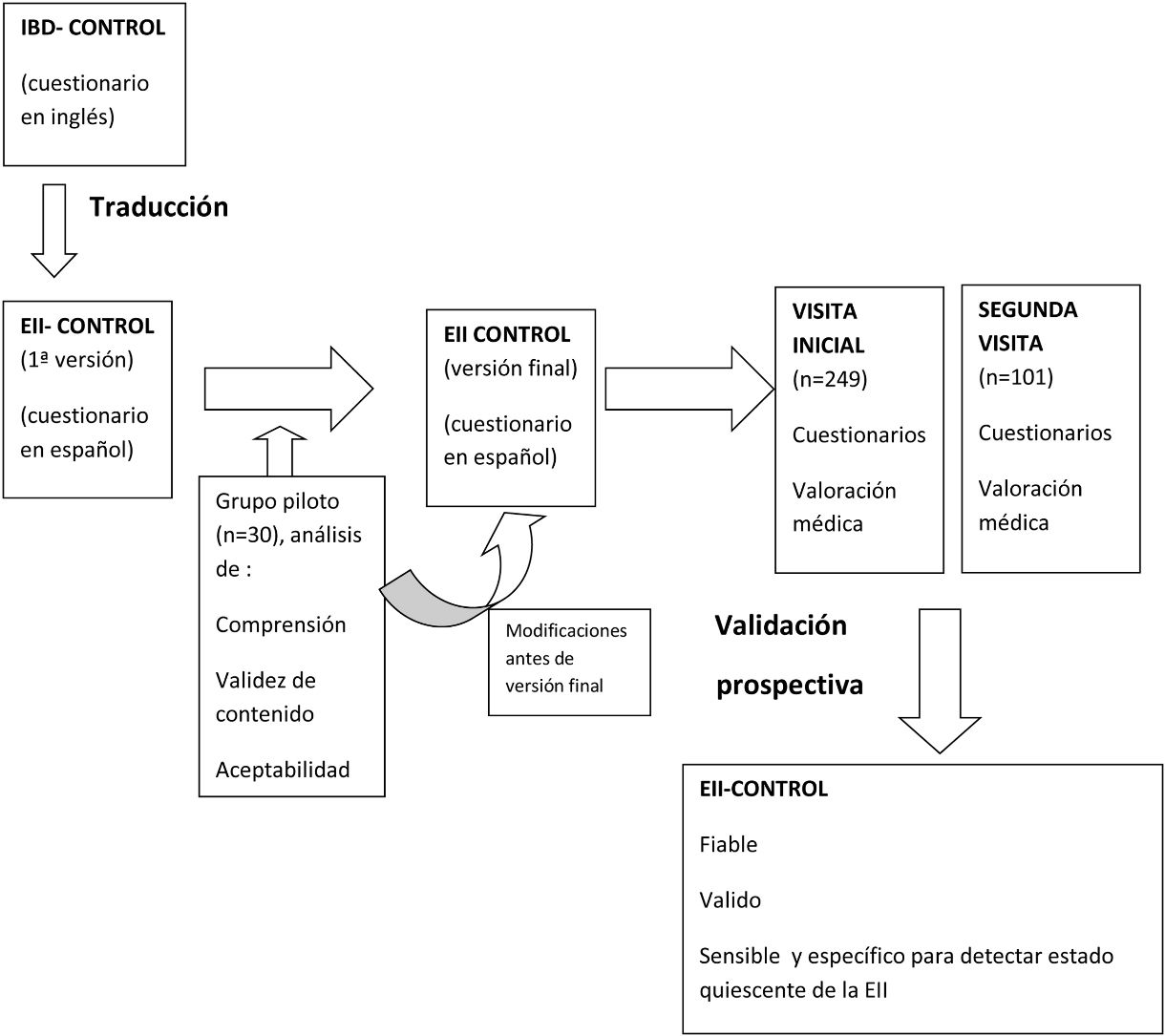
ResultadosEn la visita inicial se incluyeron 254 pacientes consecutivos, 5 de ellos excluidos del análisis por pérdida de los datos en su procesado (n primera visita=249 pacientes). Treinta pacientes formaron el grupo piloto para valorar la comprensibilidad del cuestionario una vez traducido. La segunda visita fue realizada por 101 pacientes (grupo de repetición) (fig. 1).
Flujo de pacientes. CI: colitis indeterminada; CU: colitis ulcerosa; EC: enfermedad de Crohn.
* Pacientes que leyeron el cuestionario tras su traducción para valorar la comprensión, validez del contenido y aceptabilidad, antes de la versión definitiva.
** Pacientes que repitieron toda la valoración en 2 visitas sucesivas ?visita inicial y segunda visita?, según práctica clínica.
El grupo piloto que leyó la primera versión del cuestionario una vez traducido al español estaba formado por 30 pacientes (17 mujeres y 13 hombres): 14 CU, 13 EC y una colitis indeterminada de entre 18 y 65 años. Tras revisarlo conjuntamente con los médicos y las enfermeras de la unidad, y establecida su adecuada comprensión y aceptación por parte de los pacientes, se generó la versión final del EII-Control.
Fase de validación prospectivaDatos de los pacientesSe incluyeron 249 pacientes en la visita basal, cuyas características se reflejan en la tabla 1. El 86% de los pacientes fueron de nacionalidad española. De la cohorte de pacientes evaluados en la vista inicial, 101 fueron nuevamente valorados en la segunda visita de control (sus características se muestran en la tabla 1).
Características de los pacientes
| Características | Todos los pacientes de la visita basal (n=249) | Pacientes de la segunda visita (grupo de repetición) (n=101) |
|---|---|---|
| Edad media, años | 46 | 43 |
| Tipo de enfermedad, n (%) | ||
| EC | 177 (71,08) | 71 (73,2) |
| CU | 71 (28,5) | 26 (26,8) |
| CI | 1 (0,4) | 0 |
| Sexo, n (%) | ||
| Varón | 144 (57,8) | 53 (54,6) |
| Mujer | 105 (42,2) | 44 (45,4) |
| Cirugía previa, n (%) | ||
| Cirugía abdominal | 41 (16,3) | 19 (19,6) |
| Cirugía perianal | 19 (7,6) | 6 (6,2) |
| No | 181 (72,6), | 69 (71,1) |
| Enfermedad perianal, n (%) | ||
| Sí | 40 (16,1) | 17 (17,5) |
| No | 209 (83,9) | 80 (82,5) |
| Estoma, n (%) | ||
| Sí | 3 (1,2) | 1 (1,04) |
| No | 246 (98,8) | 96 (98,96) |
| Tabaco, n (%) | ||
| No fumadores | 77 (33,6) | 32 (33) |
| Exfumadores | 106 (46,2) | 36 (37) |
| Fumadores | 46 (20,1) | 18 (18,5) |
| Desconocido | 20 | 11 (11,5) |
| Tratamientos, n (%) | ||
| Sin tratamiento | 27 (11,5) | 10 (2,06) |
| ASA-V | 71 (28,5) | 28 (28,86) |
| Corticoides orales | 3 | 0 |
| Inmunosupresores | 118 (50,0) | 50 (51,54) |
| Biológicos | 90 (37,2) | 46 (47,42) |
| Evaluación global del médico, n (%) | ||
| Inactivo | 101 (44,9) | 31 (31,9) |
| Leve | 80 (35,5) | 37 (38,1) |
| Moderado | 34 (15,1) | 20 (20,6) |
| Grave | 10 (4,4) | 5 (5,15) |
| Manifestaciones extraintestinales, n (%) | 63 (26,8) | 24 (23,7) |
| Cuestionarios de calidad de vida, media±DE | ||
| EQ-5D | 0,80±0,19 | 0,82±0,19 |
| EQ-5D-EVA | 69,6±21,2 | 72,9±20,8 |
| CCVEII-9 | 45,1±10,3 | 46,5±10,7 |
CCVEII-9: cuestionario reducido de la calidad de vida de enfermedad inflamatoria intestinal; CI: colitis indeterminada; CU: colitis ulcerosa; DE: desviación estándar; EC: enfermedad de Crohn; EQ-5D: cuestionario general de calidad de vida versión española; EVA: escala visual analógica.
La correlación de las diferentes preguntas categóricas individuales del cuestionario EII-Control con el valor de la subescala EII-Control-EVA, así como con el valor general del cuestionario CCVEII-9, fue analizada mediante el coeficiente de Spearman. Todas las correlaciones de las preguntas fueron estadísticamente significativas en comparación con ambos valores, lo que indica consistencia de las preguntas del EII-Control.
El grado de acuerdo de las 13 preguntas categóricas mediante el test α de Cronbach calculado en la primera y segunda realización de cuestionario obtuvo unos valores de 0,833 y 0,801, respectivamente. Además, se calculó el valor del coeficiente por cada pregunta del cuestionario, suponiendo que esta pregunta es eliminada, obteniendo valores muy similares entre ellas y el global. Todo esto proporciona información sobre la adecuada consistencia interna del cuestionario para el constructo «control de la enfermedad». Además de ello, la subpuntuación del EII-control-8 y la puntuación del EII-control-EVA mostraron una fuerte correlación positiva entre sí. Esto se confirmó en pacientes con EII global (r=0,502; p=0,047), y con EC (r=0,546; p<0,001) y CU (r=0,583; p<0,001) por separado.
ReproducibilidadEn el grupo de todos los pacientes que completaron las valoraciones en la visita inicial y segunda visita (n=101), no se detectaron diferencias significativas en las puntuaciones medias del EII-control y EII-control-EVA entre las visitas y sí una pequeña variación en EII-Control-8, no siendo así en el grupo de pacientes que no variaba su estado de enfermedad (enfermedad estable, n=40). Los coeficientes de correlación intraclase fueron elevados en ambos grupos de pacientes, situándose el de EII-Control en valores superiores a los de la escala EVA o EII-Control-8 (tabla 2).
Reproducibilidad de las puntuaciones totales y resumidas de EII-Control para el grupo de repetición y para los pacientes estables (coeficiente de correlación intraclase y diferencia de medias)
| CCI (IC 95%) | Media±DE, primera visita | Media±DE, visita de seguimiento | Diferencia de medias (IC 95%) | pa | |
|---|---|---|---|---|---|
| Total pacientes, n=101 | |||||
| EII-Control | 0,703 (0,560-0,800) | 16,04±6,33 | 16,62±5,95 | −1,079 (−2,202; 0,043) | 0,059 |
| EII-Control-EVA | 0,613 (0,426-0,739) | 75,16±22,88 | 77,66±19,087 | −3,069 (−7,281; 1,143) | 0,151 |
| EII-Control-8 | 0,580 (0,434-0,696) | 10,35±4,06 | 11,36±4,04 | −1,000 (−1,743; 0,276) | 0,007 |
| Pacientes con enfermedad estable, n=40 | |||||
| EII-Control | 0,862 (0,586-0,864) | 17,10±5,33 | 18,10±5,27 | −2,18; 0,181 | 0,095 |
| EII-Control-EVA | 0,526 (0,412-0,835) | 76,95±20,50 | 80,60±17,57 | −9,599; 2,299 | 0,222 |
| EII-Control-8 | 0,580 (0,434- 0,696) | 11,55±3,69 | 12,10±3,31 | −0,55 (−1,316; 0,216) | 0,155 |
CCI: coeficiente de correlación intraclase; DE: desviación estándar; EVA: escala visual analógica; IC 95%: intervalo de confianza al 95%.
Los resultados de los análisis de correlación del EII-Control y las variables de comparación se presentan en la tabla 3 en el grupo de 249 pacientes que realizaron la prueba al menos una vez. La correlación fue significativa en todos los casos tanto para el EII-Control como para el EII-Control-8 y para el EII-Control-EVA. Fue positiva con todas las escalas de CV y con la valoración médica y fue negativa con las de sintomatología. Ello indica una adecuada validez para el cuestionario EII-Control, ya que el valor de este varía en la misma dirección que CCVEII-9, EQ-5D y valoración clínica, es decir, al aumentar los valores de CCVEII-9 o EQ-5D o presentar una mejor valoración clínica, el valor de EII-Control también aumenta y viceversa. Por el contrario, la correlación es negativa con los cuestionarios HAS, HDS, FSS y con los índices simple de actividad clínica de la CU/Harvey-Bradshaw, lo que quiere decir que, con la evaluación negativa de la enfermedad, ansiedad, depresión o fatiga, el valor de EII-Control disminuye y viceversa. La pregunta 2, que relaciona la presencia de sensaciones de ansiedad o depresión, demostró una correlación estadísticamente significativa con el cuestionario HAS (r=−0,136, p=0,031), pero no con el HDS (r=0,072, p=0,258).
Validez de constructo: correlaciones entre el EII-Control y sus puntuaciones resumidas y medidas externas del estado de salud de los pacientes en la evaluación inicial
| Coeficiente (p) | CCVEII-9 | Evaluación clínicaa | EQ-5D-valor | EQ-5D-EVA | HAS | HDS | FSS | SCCAI | Harvey-Bradshaw |
|---|---|---|---|---|---|---|---|---|---|
| EII-Control | 0,774 (p<0,001) | 0,528 (p<0,001) | 0,614 (p<0,001) | 0,639 (p<0,001) | −0,600 (p<0,001) | −0,225 (p<0,001) | −0,477 (p<0,001) | −0,368 (p<0,0,04) | −0,524 (p<0,001) |
| EII-Control-8 | 0,812 (p<0,001) | 0,557 (p<0,001) | 0,812 (p<0,001) | 0,676 (p<0,001) | 0,672 (p<0,001) | 0,255 (p<0,001) | −0,497 (p<0,001) | −0,485 (p<0,001) | −0,574 (p<0,001 |
| EII-Control-EVA | 0,558 (p<0,001) | 0,416 (p<0,001) | 0,664 (p<0,001) | 0,639 (p<0,001) | −0,399 (p<0,001) | −0,218 (p<0,001) | −0,245 (p<0,001) | −0,385 (p<0,0,02) | 0,371 (p<0,001) |
CCVEII-9: cuestionario reducido de la calidad de vida para la enfermedad inflamatoria intestinal; EQ-5D: cuestionario general de calidad de vida versión española; FSS: escala de severidad de la fatiga; HAS: escala hospitalaria de ansiedad; HDS: escala hospitalaria de depresión; SCCAI: índice simple de actividad clínica de la colitis ulcerosa.
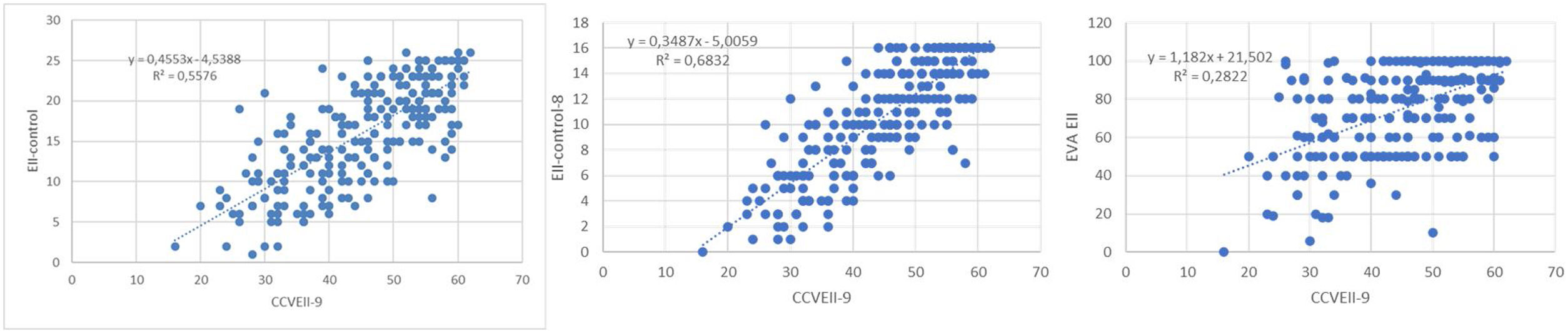
Los resultados de la regresión en los cuestionarios con correlación significativa se presentan en la figura 2. En ella se ve que la mayor correlación que presenta el EII-Control con CCVEII-9 se traduce en un mejor ajuste del modelo de regresión con un valor de R2 de 0,5985, lo que indica una fuerte relación entre ambos cuestionarios y que la variabilidad de CCVEII-9 puede predecir casi un 60% de la variabilidad de EII-Control.
En cuanto a la relación EII-Control con la valoración global del médico, los valores se han comparado con la prueba del análisis de la variancia. Los resultados indicaron siempre valores más elevados en la puntuación del EII-Control y sus 2 subescalas cuanto mejor era el estado del paciente (mayor puntuación en inactivos y menor puntuación en graves); se encontraron diferencias estadísticamente significativas entre grupos, p<0,001 en todos los casos.
En cuanto a la validez del cuestionario EII-Control-8 (subescala con las preguntas 1a, 1b, 3a, 3b, 3c, 3d, 3e y 3f), para analizar su capacidad de detectar el estado de salud, se relacionaron los valores del cuestionario EII-Control-8 agrupados de 2 en 2 con los valores de la puntuación del EQ-5D. Se observó que los valores más elevados de EII-Control-8 se relacionan con los valores de EQ-5D de forma creciente, lo que valida el cuestionario.
Además de ello, las correlaciones de EII-Control-8 con CCVEII-9, EII-Control-EVA o EQ-5D fueron siempre positivas y estadísticamente significativas: 0,851 (p<0,001), 0,560 (p<0,001) y 0,696 (p<0,001), respectivamente, lo que venía a demostrar también la validez de esta medida.
Capacidad de respuestaLa capacidad de respuesta de EII-Control fue comparable a la de CCVEII-9, ya que ambos presentaron diferencias estadísticamente significativas entre las 2 mediciones con media superior en la primera valoración, p<0,001 en ambos casos. De la misma manera, el tamaño del efecto fue reducido en ambos casos y coherente entre ambos cuestionarios: 0,14 en CCVEII-9 y 0,09 en EII-Control.
Asimismo, EII-Control, EII-Control-8 y EII-Control-EVA presentaron valores diferentes en 3 grupos de pacientes definidos por tener variación inferior a 10, igual a 10 o superior a 10 en el cuestionario CCVEII-9. Los tamaños del efecto fueron de tipo moderado (>0,3) o alto (>0,7) en los 3 casos.
Sensibilidad y especificidad del EII-Control en la identificación de pacientes «quiescentes» o inactivosDe los 249 pacientes incluidos en el estudio, se definieron 220 en estado quiescente, según los criterios seleccionados, en la visita inicial.
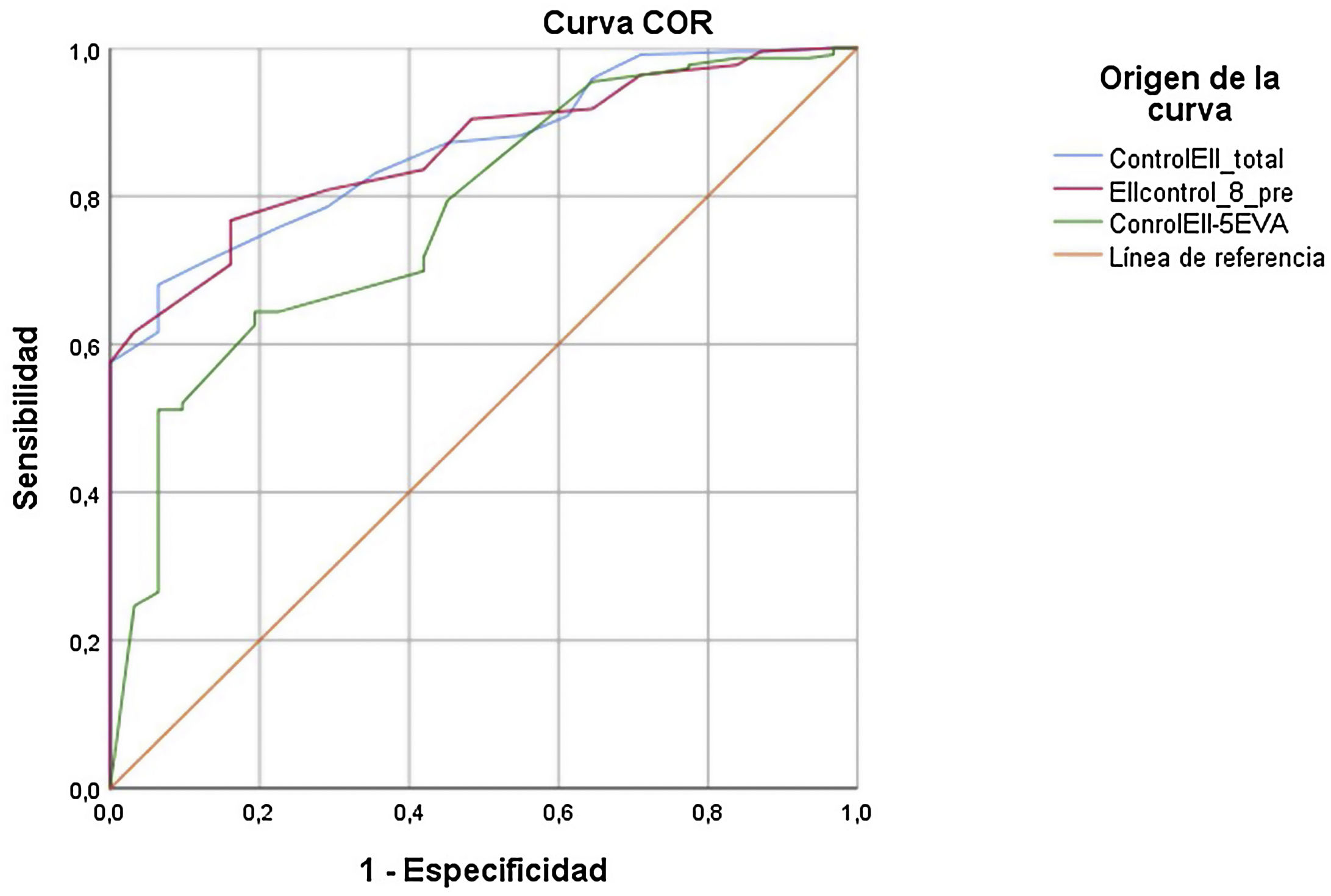
Los resultados de la curva COR de los cuestionarios EII-Control, EII-Control-8 y EII-Control-EVA se presentan en la figura 3. Los valores del área bajo la curva fueron 0,864 (IC 95% 0,811-0,916) para EII-Control, 0,862 (IC 95% 0,810-0,914) para EII-Control-8 y 0,776 (IC 95% 0,692-0,860) para EII-Control-EVA, p<0,001 en todos los casos. Es decir, todas las escalas tienen capacidad para detectar el estado quiescente, si bien la escala EVA presenta menor credibilidad. Los puntos de corte que alcanzaron mejores valores de sensibilidad y especificidad fueron 14 (sensibilidad 0,696 y especificidad 0,903) para EII-Control; 11 (sensibilidad 0,662 y especificidad 0,903) para EII-Control-8 y 82 (sensibilidad 0,516 y especificidad 0,903) para la escala EVA.
Estas puntuaciones de corte significarían que solo uno de cada 10 pacientes que no cumplan con nuestros estrictos criterios clínicos para la EII inactiva se clasificarían falsamente como inactivos, pero ninguno de estos «falsos positivos» requirió ningún cambio de tratamiento en el momento de la consulta y todos fueron considerados casos en remisión o solo levemente activos por el médico tratante. Estos datos confirman la posible aplicación clínica del EII-Control como una herramienta de clasificación rápida para determinar los pacientes de bajo riesgo (inactivos) adecuados para formas alternativas de seguimiento.
Se analizó, asimismo, si la presencia de la pregunta 2 en el estado de quiescencia influía en la capacidad de predicción en el cuestionario EII-Control, que también la incluye. El área bajo la curva fue el mismo al eliminar esta pregunta del estado quiescente, es decir, 0,731 (IC 95% 0,660-0,802).
DiscusiónEl cuestionario IBD-Control fue diseñado por Bodger et al. con el objetivo de ofrecer una valoración rápida y fácil de usar del control de la enfermedad desde la perspectiva del paciente. Se desarrolló con la participación de pacientes para definir el constructo de medición (es decir, ¿qué es control de la enfermedad?) y crear ítems centrados en el paciente. Los requisitos clave predeterminados fueron que el IBD-Control fuera aplicable a la asistencia clínica de rutina y que incluyera ítems relacionados con las 2 formas principales de EII (EC y CU). Los dominios identificados mediante discusión con pacientes sobre el control de la enfermedad y aquellos publicados en la literatura sobre CV en la EII10,27,28 tuvieron un consenso considerable; por tanto, un buen control desde la perspectiva del paciente implica la ausencia de repercusión de la enfermedad en las principales esferas de la vida del paciente (energía/vitalidad, capacidad de desempeñar las actividades cotidianas, el sueño, el estado de ánimo o la ausencia de dolor o malestar). Del IBD-Control se debe destacar el énfasis centrado en la implicación de los pacientes en la creación de los ítems y en el diseño del cuestionario, que complementó a la revisión de la literatura y la opinión clínica experta.
El estudio demostró que el IBD-Control fue muy bien aceptado por los pacientes, por la rapidez en completarlo y las elevadas tasas de cumplimentación, característica fundamental cuando se pretende emplearlo en la práctica clínica. Además, se demostraron sus potentes propiedades de medición (rango psicométrico), que cumplieron con las normas internacionales actuales20–22, siendo muy sólidas cuando se compararon con una amplia serie de medidas externas y la validación no se limitó solo a mostrar las correlaciones con las medidas de enfermedad tradicionales en la población de pacientes, sino que consideró el rendimiento de las puntuaciones resumen a nivel individual y para un propósito clínico específico.
Lógicamente, el estudio tiene algunas limitaciones, a pesar de lo riguroso de su proceso de desarrollo y validación. Así, los autores admiten alguna limitación, sobre todo la existencia de un posible sesgo de selección inevitable e inherente a la selección de pacientes deseosos de completar múltiples cuestionarios para un estudio de validación. Sin embargo, dado que su tamaño muestral era extenso e incluía sujetos con un amplio espectro de características demográficas y clínicas similares a su población de EII local23, este posible sesgo fue minimizado. En nuestro caso, la inclusión de los pacientes se hizo de forma consecutiva sin ninguna selección, siempre que cumplieran los criterios de inclusión y que firmaran el consentimiento informado, por lo que el sesgo de selección que comentan los autores es mínimo o inexistente. No obstante, y como mencionan los autores en su discusión, sería deseable realizar una validación adicional en otros ámbitos y en subgrupos específicos de pacientes. De forma similar, grupos diferentes de pacientes en cuanto a idioma y cultura requieren dicha validación.
Con este objetivo, validar el IBD-Control en nuestros pacientes españoles, con su más que probable utilidad para nuestra práctica, diseñamos el presente estudio. Es importante recordar que el español es el segundo idioma en el mundo, lo que recalca la importante de esta validación. Se partió del cuestionario IBD-Control, que se tradujo al español en un proceso estructurado, que generó el EII-Control. Posteriormente se realizó la validación prospectiva psicométrica de este EII-Control tal y como se realizó en el trabajo original, con tan solo mínimos cambios para mejorarlo (por ejemplo, incluir la escala FSS). Nuestros resultados concuerdan fuertemente con los de Bodger et al., de manera que tanto la validez como la fiabilidad presentan cifras muy superponibles, indicando que el cuestionario traducido al que hemos llamado EII-Control es válido también en los pacientes de nuestro medio. En este sentido, lo desconocemos, pero es posible que la complejidad de los pacientes del estudio original y del nuestro varíe, dado que los del estudio original son de base poblacional y en nuestra consulta monográfica se atiende a los pacientes más complicados del área, y aun así no se afectaron los resultados del test, lo que apoyaría la validez general del EII-Control en la EII en general. Otra de las diferencias de nuestro estudio, en relación con el trabajo original, fue que nosotros añadimos la evaluación de la relación entre la puntuación del EII-Control y el FFS. Como sabemos, uno de los síntomas más frecuentes, incluso en pacientes que consideramos en remisión, es la astenia o fatiga, limitando en ocasiones de forma importante la CV de los pacientes. La correlación que observamos entre el EII-Control y la escala FSS es muy alta, lo que apoya la validez del EII-Control. Un aspecto interesante tanto para los creadores del IBD-Control original como para nosotros es que la herramienta identifique de forma fiable a los pacientes en estado «quiescente», definido estrictamente con un conjunto de criterios. Esto resulta interesante para su potencial aplicación en modelos de asistencia que buscan reducir la necesidad de consultas presenciales a favor de consultas clínicas virtuales o telemáticas. Si este enfoque de control y seguimiento estaba cobrando importancia en los últimos años, actualmente, en la «era COVID», aún es de mayor trascendencia y actualidad. La teleasistencia se ha convertido, en muchos casos, no en un objetivo a promover y cumplir, sino en una necesidad. Nuestro instrumento, el EII-Control, ha alcanzado prácticamente la misma especificidad que el original para este fin, por lo que esta propiedad de detectar con seguridad a los pacientes quiescentes hace de él una herramienta idónea para este fin.
Recientemente, en programas de mejoría de la calidad en la EII en diversos ámbitos sanitarios, se ha resaltado el potencial de la medida rutinaria de los PRO para ayudar a mejorar los servicios centrados en el paciente29,30. En este contexto, y dado que las guías actuales para la EII no avalan/recomiendan el uso de ningún instrumento específico de PRO en la monitorización de la asistencia, quedando sobre todo como herramientas de investigación, creemos que la simplicidad del EII-Control junto con sus sólidas propiedades de medición lo hacen muy adecuado para este uso, además de su papel en estudios clínicos. Asimismo, el instrumento ofrece la posibilidad de captar datos seriados de resultados percibidos por el paciente, con una mínima carga para el usuario, y su contenido y formato reducido lo hacen especialmente adecuado para adaptarse a la captura electrónica a través de sistemas web y aplicaciones de dispositivos móviles.
Conflicto de interesesR.V.L. ha recibido asesoramiento científico, soporte para investigación y/o actividades formativas de Abbvie, Jannsen, MSD, Pfizer y Takeda. S.G.L. ha recibido soporte para asistencia a reuniones científicas desde Abbvie, MSD, FAES-FARMA, Ferring, Shire, Takeda, Pfizer y Janssen. También ha recibido honorarios por consultoría o apoyo a la investigación desde Abbvie, Janssen, MSD y Takeda.
F.G.G. ha recibido asesoramiento científico, soporte para investigación y/o actividades formativas de Abbvie, Jannsen, MSD, Pfizer, y Takeda.
El resto de los autores declaran no tener ningún conflicto de intereses.