Describir las características clínicas de pacientes pediátricos con aislamiento de Klebsiella productora de carbapenemasa.
Materiales y métodosEntre 2012 y 2015 se realizó un estudio descriptivo que incluyó a pacientes de 0-18 años (media 4,8 años), todos con aislamientos de Klebsiella productora de carbapenemasa.
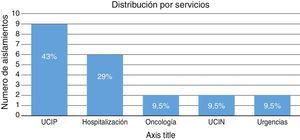
ResultadosSe documentó infección en 21 pacientes; el 81% tenía antecedente de hospitalización en los 6 meses previos y el 67% de antibioticoterapia. Los sitios de aislamiento fueron sangre (48%), orina (33%), líquido pleural (9%), líquido peritoneal y tráquea (5%). El 95% de los pacientes tenía comorbilidad asociada; el 81% de los aislamientos correspondió a infecciones nosocomiales. Los servicios de hospitalización fueron UCIP 43%, Pediatría General 29%, Oncología, Unidad Neonatal y Urgencias 9,5% cada uno. El 81% de los aislamientos presentó corresistencia a otros antimicrobianos. El tratamiento definitivo se realizó con monoterapia en un 19%, terapia doble en un 28,5% y terapia triple en un 23,8%. La mortalidad fue del 24%.
To describe the clinical characteristics of paediatric patients with carbapenemase-producing Klebsiella isolates.
Material and methodsBetween 2012 and 2015, we conducted a descriptive study that included patients aged 0-18 years (mean 4.8 years), all with Klebsiella carbapenemase-producing isolates.
ResultsThe infection was documented in 21 patients, 81% of the patients had a history of hospitalisation in the last 6 months and 67% had undergone antibiotic therapy. The isolation sites were blood (48%), urine (33%), pleural fluid (9%), peritoneal liquid and trachea (5). Ninety-five percent of the patients had associated comorbidity; 81% of the isolates corresponded to nosocomial infections. The hospital departments were the paediatric intensive care unit (43%), general paediatrics (29%), oncology, neonatal unit and emergency department (9.5% each). Eighty-one percent of the isolates had co-resistance to other antimicrobials. Definitive treatment was performed with monotherapy in 19% of the cases, double therapy in 28.5% and triple therapy in 23.8%. The mortality rate was 24%.
En las 2 últimas décadas se ha observado un problema creciente de resistencia antibiótica, generado en gran parte por el uso indiscriminado de los antimicrobianos, pero también por la colonización de pacientes con múltiples comorbilidades, que requieren estancias hospitalarias prolongadas, e invasiones de piel y mucosas como parte de su soporte vital. Las infecciones por bacilos gram negativos multirresistentes generan una enorme dificultad para la terapéutica y una morbimortalidad muy superior a la observada en infecciones causadas por gérmenes sensibles1,2.
El objetivo de este estudio fue realizar una descripción de las características clínicas de pacientes entre 0 y 18 años de edad con aislamiento de Klebsiella productora de carbapenemasa hospitalizados en la Fundación Hospital de La Misericordia de Bogotá (Colombia), centro de referencia de tercer nivel de atención pediátrica cuya principal población corresponde a pacientes con enfermedad oncohematológica.
Materiales y métodosEstudio tipo descriptivo retrospectivoSe revisaron en total 26 expedientes clínicos, de los cuales se obtuvieron los siguientes datos: edad, género, diagnóstico infeccioso, comorbilidades, tiempo total de estancia hospitalaria y estancia previa al aislamiento de carbapenemasa, servicio de hospitalización, días de invasión con catéter venoso central, ventilador, sonda vesical, procedimientos quirúrgicos, días de fiebre, recuento absoluto de leucocitos y neutrófilos, valor de proteína C reactiva y procalcitonina en el momento de la infección, antecedente de hospitalización en los 6 meses previos y esquemas antibióticos empleados, desenlace.
La selección de pacientes con aislamiento de Klebsiella spp. con patrón de resistencia de carbapenemasa se realizó a través del sistema Whonet. Se utilizaron como marcadores de carbapenemasa la resistencia a ertapenem o meropenem detectadas en el Laboratorio de Microbiología con el sistema VITEK con los puntos de corte CLSI 20123,4.
Se procedió a la confirmación del patrón de resistencia de todos los aislamientos de Klebsiella productora de carbapenemasa en la base de datos del Laboratorio de Microbiología del hospital (test de Hodge, test de Hodge modificado con LSD, ácido borónico, EDTA). Todos los patrones de resistencia fueron confirmados por la Secretaría de Salud de Bogotá con las mismas pruebas bioquímicas. Solo se realizó biología molecular a uno de los aislamientos.
Desde el punto de vista microbiológico se evaluó: Klebsiella spp., MIC para ertapenem, meropenem, corresistencia para amikacina, gentamicina, ciprofloxacina, tigeciclina y colistina, tratamiento antibiótico empírico recibido previamente al aislamiento y tratamiento antibiótico una vez conocido el aislamiento de carbapenemasa, tiempo de negativización de los cultivos.
Se realizó el análisis epidemiológico de los datos obtenidos, con medidas de tendencia central. Debe tenerse en cuenta que por el tipo de estudio realizado no es posible establecer causalidad entre las variables encontradas, y que simplemente nos limitamos a su descripción en una población específica.
ResultadosSe revisaron las historias clínicas de pacientes entre 0 y 18 años de edad con aislamiento de Klebsiella spp. con patrón de resistencia de carbapenemasa, hospitalizados entre enero del 2012 y marzo del 2015 en la Fundación Hospital de La Misericordia de Bogotá (Colombia), centro de tercer nivel de atención pediátrica, cuya principal población corresponde a pacientes con enfermedad oncohematológica.
Utilizando el sistema Whonet se detectaron 36 aislamientos de Klebsiella spp. resistente a ertapenem y meropenem. Se procedió a confirmar el patrón de resistencia en la base de datos del Laboratorio de Microbiología, descartando la producción de carbapenemasa en 6 de estos aislamientos mediante pruebas bioquímicas confirmatorias.
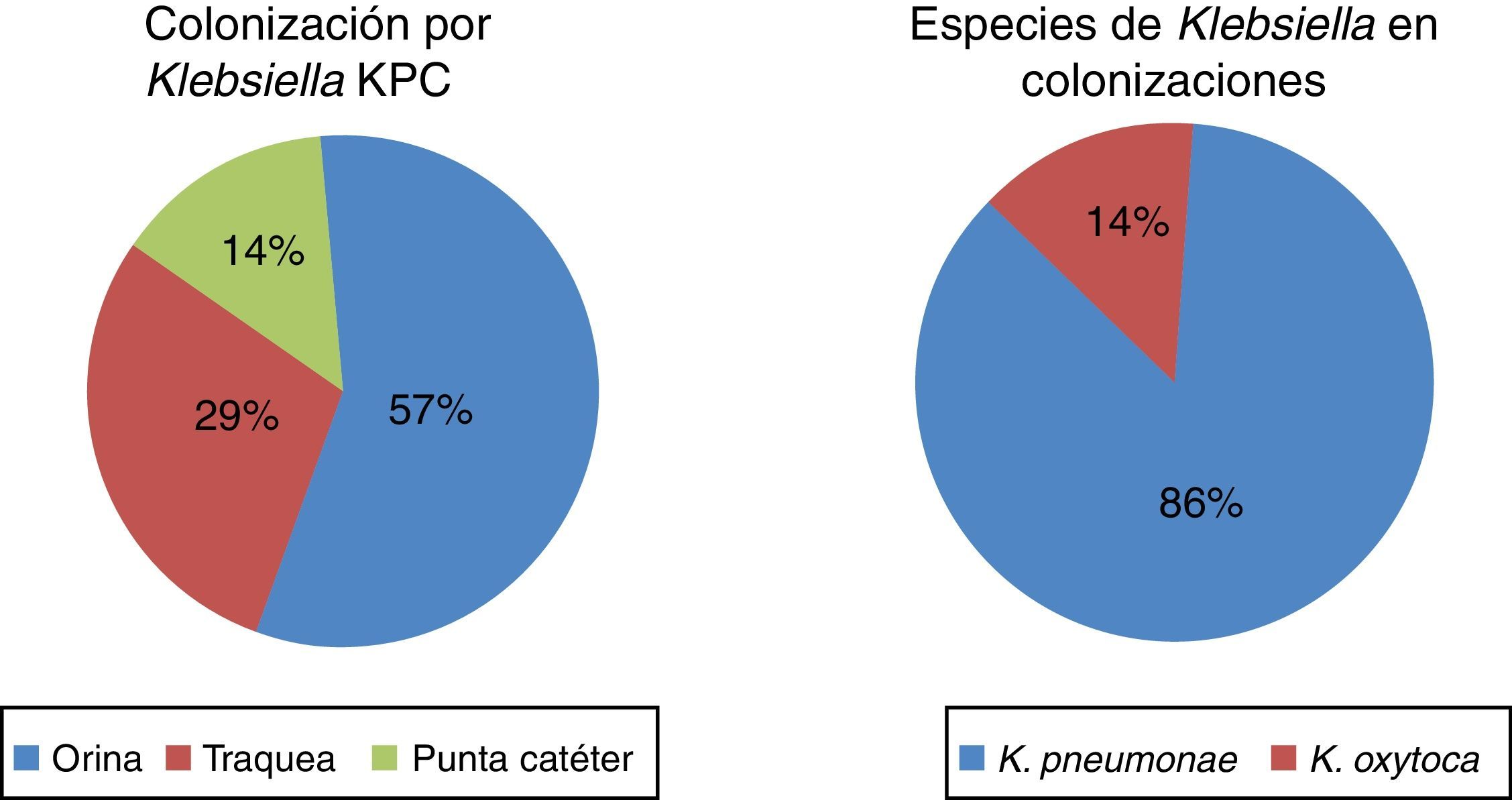
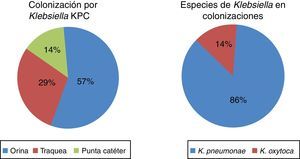
Se encontraron en total 28 pacientes con 30 aislamientos microbiológicos, 21 infecciones (75%) y 7 colonizaciones (25%) (fig. 1). De los 21 pacientes con infección por Klebsiella spp. productora de carbapenemasa, 8 (38%) fueron mujeres y 13 (62%) fueron hombres, con una media de edad de 4,8 años (0 a 16 años); 17 (81%) de ellos tenían el antecedente de hospitalización en los últimos 6 meses y 14 (67%) habían recibido tratamiento antibiótico (tabla 1).
En 3 (14,28%) de los 21 pacientes se había documentado colonización y en 5 pacientes (23,8%) se documentó un proceso infeccioso con aislamiento de germen en cultivos en los 6 meses previos (tabla 2).
Colonización e infección en los 6 meses previos al aislamiento de carbapenemasa
| Especie y patrón de resistencia | Sitio de aislamiento | |
|---|---|---|
| Colonización | K. oxytoca carbapenemasa | Orina |
| K. pneumoniae BLEE | Tráquea | |
| K. pneumoniae BLEE | Punta de catéter | |
| Infección | K. pneumoniae BLEE | Orina |
| K. pneumoniae BLEE | Tráquea | |
| K. pneumoniae fenotipo habitual (2 casos) | Sangre | |
| K. pneumoniae carbapenemasa | Orina | |
Con respecto al sitio de aislamiento, el más frecuente fue sangre en 10 casos (48%), seguido por orina en 7 pacientes (33%), líquido pleural en 2 (9%), uno en líquido peritoneal y uno en tráquea (5% cada uno). En 2 pacientes se obtuvo crecimiento del germen en 2 sitios diferentes: líquido pleural y tráquea en un caso, sangre y tráquea en el otro.
El 95% (20) de los pacientes tenía una comorbilidad previa que condicionó una estancia hospitalaria prolongada. Solo un caso (5%) no tenía una enfermedad de base: ingresó por una herida por proyectil de arma de fuego en región toracoabdominal y presentó una neumonía asociada al cuidado de la salud complicada con empiema, con aislamiento de Klebsiella productora de carbapenemasa en líquido pleural (tabla 3).
Comorbilidades de los pacientes con aislamiento de Klebsiella productora de carbapenemasa
| Comorbilidad. Porcentaje (número) | Descripción (número) |
|---|---|
| Oncohematológica 40 (8) | Tumor de Wilms (2) Leucemia linfoblástica aguda (2) Hepatoblastoma (1) Leucemia mieloide aguda (1) Linfoma de Burkitt (1) Talasemia (1) |
| Renal 25 (5) | Síndrome nefrótico congénito (1) Hidronefrosis (4) |
| Neurológica 20 (4) | Parálisis cerebral (1) Enfermedad de depósito (1) Toxoplasmosis (1) Epilepsia focal sintomática (1) |
| Otros 15 (3) | Lupus eritematoso sistémico (2) Atresia de vías biliares (1) |
| Sin comorbilidad 4,7 (1) |
Si se toman aparte las condiciones de los pacientes que contribuyen a un estado de inmunodeficiencia y en forma secundaria aumentan el riesgo de infección, 11 de ellos (52,4%) contaban con un factor predisponente. En orden de frecuencia, estos fueron: falla renal en 4 casos (36,3%), neutropenia en 3 casos (27,3%), hipogammaglobulinemia IgG, quimioterapia, corticoide a altas dosis y trasplante alogénico de cordón no emparentado, un caso cada uno (9,1% cada uno).
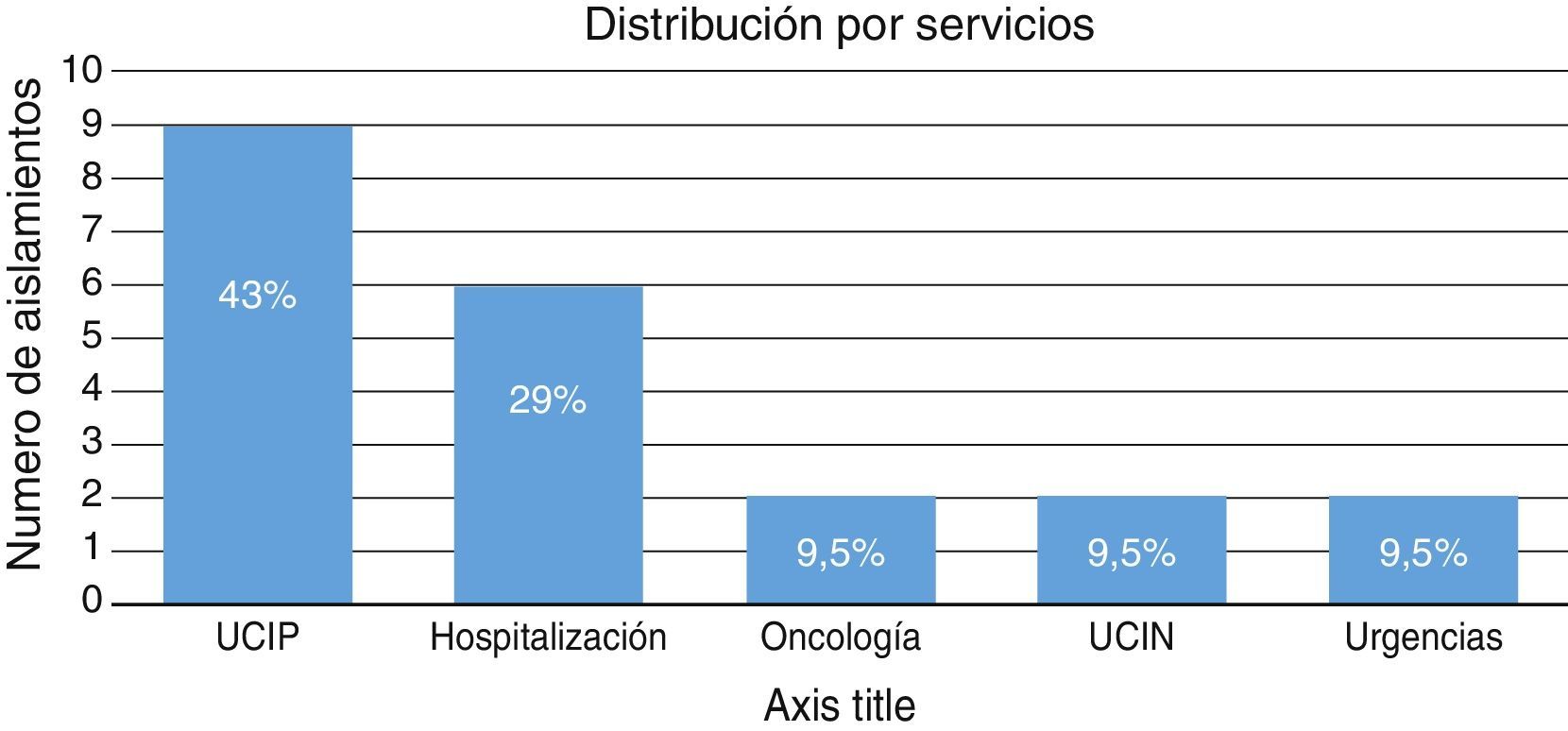
La distribución por servicios se muestra en la figura 2. El promedio de estancia hospitalaria en general fue de 53 días (rango 5-337 días) y de 20 días para UCIP (rango 3-48 días). El tiempo de hospitalización previo al aislamiento fue de 31 días en promedio (rango 0-169 días).
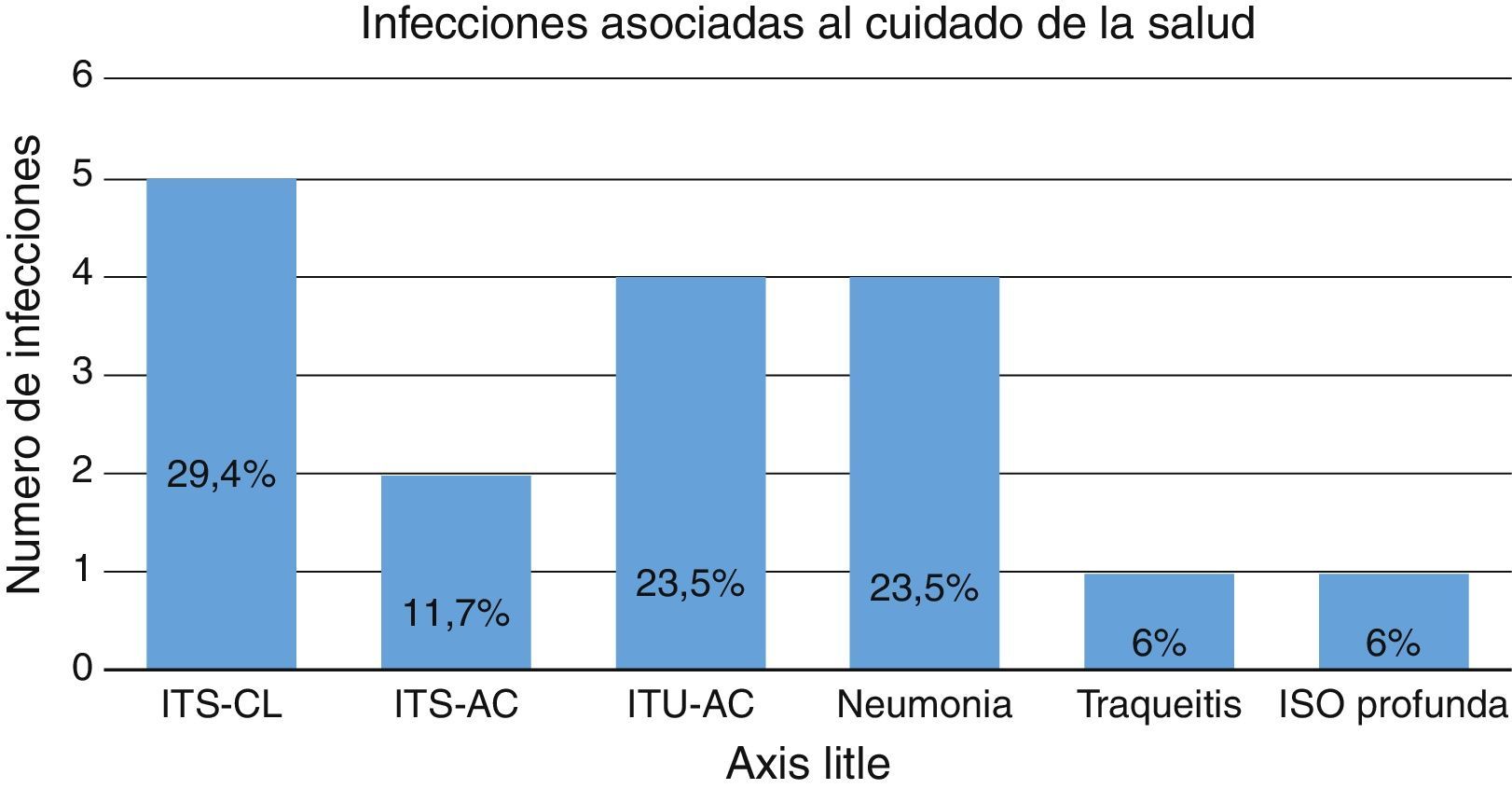
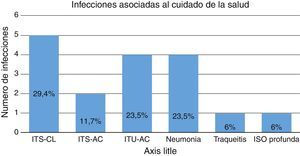
De los 21 aislamientos, 17 (81%) fueron infecciones asociadas al cuidado de la salud (IACS), 3 de ellas extrainstitucionales (17,6%), es decir que no fueron adquiridas en el Hospital de la Misericordia, sino que llegaron remitidos de otros hospitales de la ciudad. En la figura 3 se muestra la distribución de las IACS.
Distribución de infecciones asociadas al cuidado de la salud.
ISO: infección de sitio operatorio; ITS-AC: infección de torrente sanguíneo asociada a catéter; ITS-CL: infección de torrente sanguíneo confirmada por laboratorio; ITU-AC: infección del tracto urinario asociada a catéter vesical.
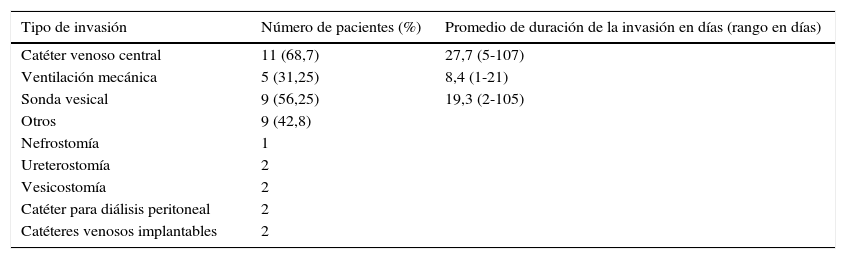
Los pacientes tuvieron dispositivos invasivos en el 76% de los casos (16); la distribución de las invasiones se muestra en la tabla 4. Cuatro pacientes del total (19%) requirieron cirugía abdominal.
Dispositivos invasivos en pacientes con aislamiento de carbapenemasa
| Tipo de invasión | Número de pacientes (%) | Promedio de duración de la invasión en días (rango en días) |
|---|---|---|
| Catéter venoso central | 11 (68,7) | 27,7 (5-107) |
| Ventilación mecánica | 5 (31,25) | 8,4 (1-21) |
| Sonda vesical | 9 (56,25) | 19,3 (2-105) |
| Otros | 9 (42,8) | |
| Nefrostomía | 1 | |
| Ureterostomía | 2 | |
| Vesicostomía | 2 | |
| Catéter para diálisis peritoneal | 2 | |
| Catéteres venosos implantables | 2 |
Con respecto al comportamiento clínico de los pacientes infectados por Klebsiella spp. productora de carbapenemasa, el promedio de duración de la fiebre fue de 1,5 días (rango 0-8 días); el conteo absoluto de leucocitos fue de 15.982/mm3 (rango 10-68.370/mm3), el número absoluto de neutrófilos de 11.292/mm3 (rango 0-59.940/mm3), la proteína C reactiva fue de 116mg/l (rango 1-384) y la procalcitonina de 30,7ng/ml (rango 0,05-284,7).
En el análisis microbiológico se encontró a K. pneumoniae como especie más frecuente en 16 casos (76%), seguida por K. oxytoca en 4 (19%) y K. ornithinolytica en uno (5%). La MIC más frecuentemente encontrada para ertapenem fue de 4 mcg/ml en 10 pacientes, seguida por 8 mcg/ml en 5 pacientes y para meropenem fue de 16 mcg/ml en 18 pacientes. Se realizó biología molecular en solo uno de los aislamientos, lo que permitió la identificación de una serina carbapenemasa.
Se encontró corresistencia en 17 (81%) de los pacientes, a aminoglucósidos en 10 pacientes (48%) (6 cepas resistentes a gentamicina y 4 a amikacina), ciprofloxacino en 6 (29%) y tigeciclina en uno (5%). No se llevó a cabo susceptibilidad antimicrobiana a colistina ni a fosfomicina.
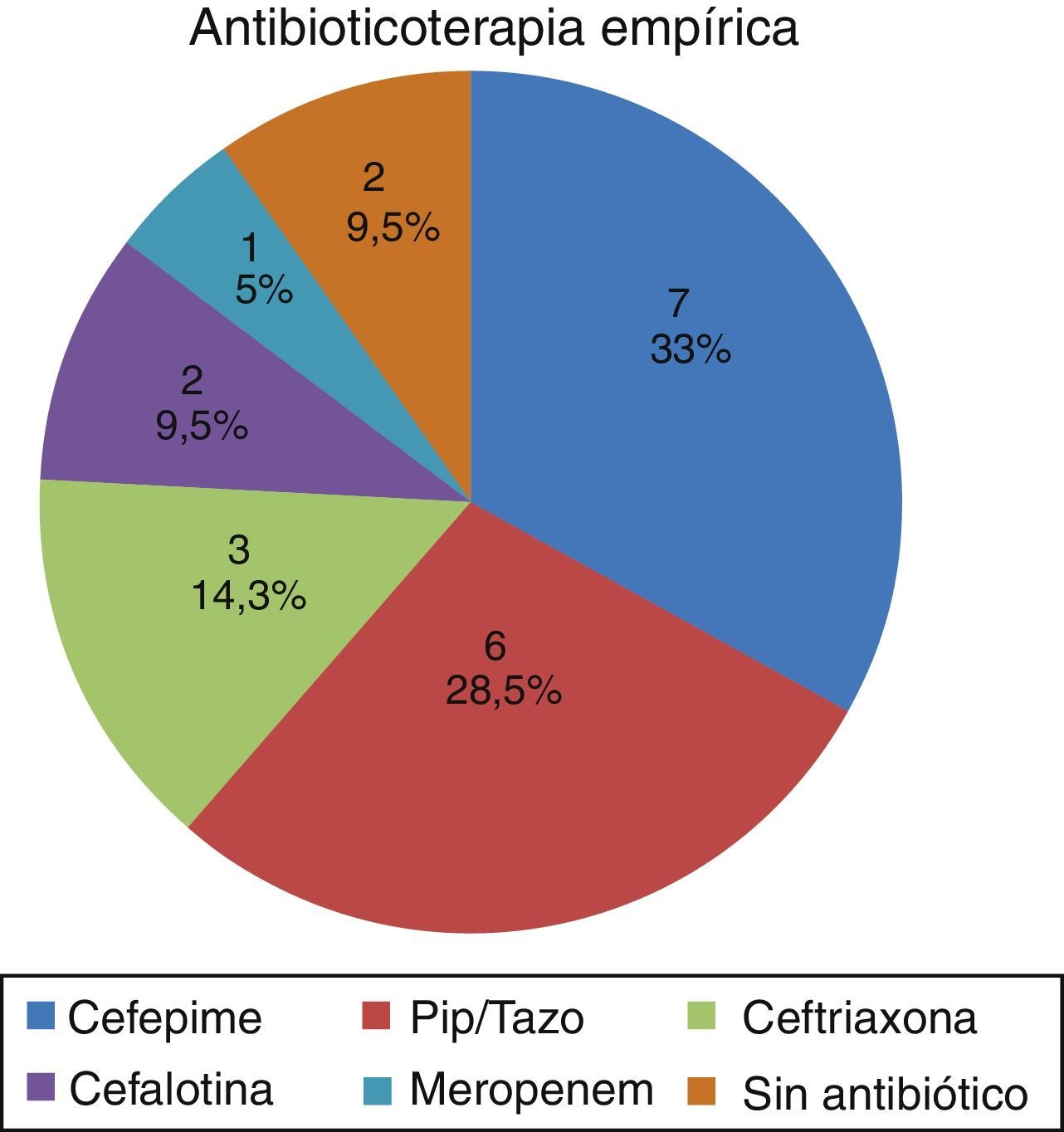
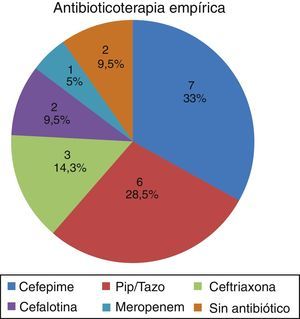
Los tratamientos antibióticos empíricos utilizados antes de conocer el aislamiento de Klebsiella productora de carbapenemasa se describen en la figura 4. Una vez conocido el aislamiento se utilizó terapia combinada en el 52% de los casos (11 pacientes); el tiempo promedio de antibioticoterapia empírica recibida previamente al aislamiento fue de 3,75 días (rango 1-14 días).
Cinco pacientes (23,8%) presentaron mejoría clínica y negativización de los cultivos a pesar de que no recibieron un tratamiento antibiótico dirigido contra carbapenemasa (3 recibieron cefepime con un aislamiento en hemocultivo y 2 aislamientos en urocultivo; uno recibió piperacilina/tazobactam con aislamiento en secreción traqueal y uno recibió ceftriaxona con aislamiento en urocultivo), razón por la que no fue necesario modificar el esquema antibiótico.
En 3 pacientes (14,2%), se presentó un desenlace fatal antes de conocerse el patrón de resistencia del germen. De ellos, uno tenía piperacilina/tazobactam y en 2 se había cambiado el esquema a meropenem por deterioro clínico.
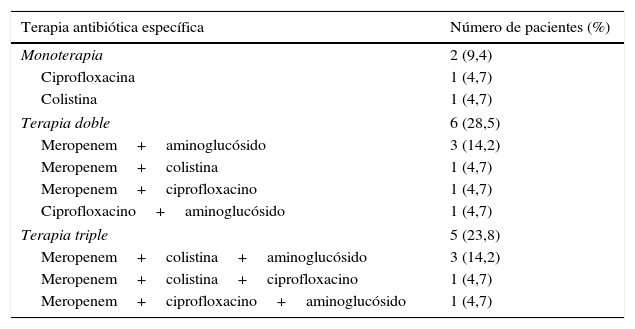
Se agrupó la terapia antibiótica específica que se les brindó a los 13 pacientes restantes luego de conocer el resultado de cultivo en 3 grupos: monoterapia, terapia doble y terapia triple, los cuales se resumen en la tabla 5.
Terapia antibiótica específica en 13 pacientes que requirieron modificación del esquema empírico
| Terapia antibiótica específica | Número de pacientes (%) |
|---|---|
| Monoterapia | 2 (9,4) |
| Ciprofloxacina | 1 (4,7) |
| Colistina | 1 (4,7) |
| Terapia doble | 6 (28,5) |
| Meropenem+aminoglucósido | 3 (14,2) |
| Meropenem+colistina | 1 (4,7) |
| Meropenem+ciprofloxacino | 1 (4,7) |
| Ciprofloxacino+aminoglucósido | 1 (4,7) |
| Terapia triple | 5 (23,8) |
| Meropenem+colistina+aminoglucósido | 3 (14,2) |
| Meropenem+colistina+ciprofloxacino | 1 (4,7) |
| Meropenem+ciprofloxacino+aminoglucósido | 1 (4,7) |
En promedio, el tiempo de tratamiento específico una vez conocido el aislamiento de la carbapenemasa fue de 11,9 días (rango 2-28 días). Los cultivos de control, tomados para verificar la negativización del aislamiento de carbapenemasa, fueron negativos a los 6,5 días (1-17 días) de iniciada la antibioticoterapia específica. La mortalidad reportada fue de 24% (5 pacientes), de los 5 pacientes fallecidos, 4 (80%) tuvieron el aislamiento de Klebsiella productora de carbapenemasa en sangre y uno (20%) en líquido peritoneal.
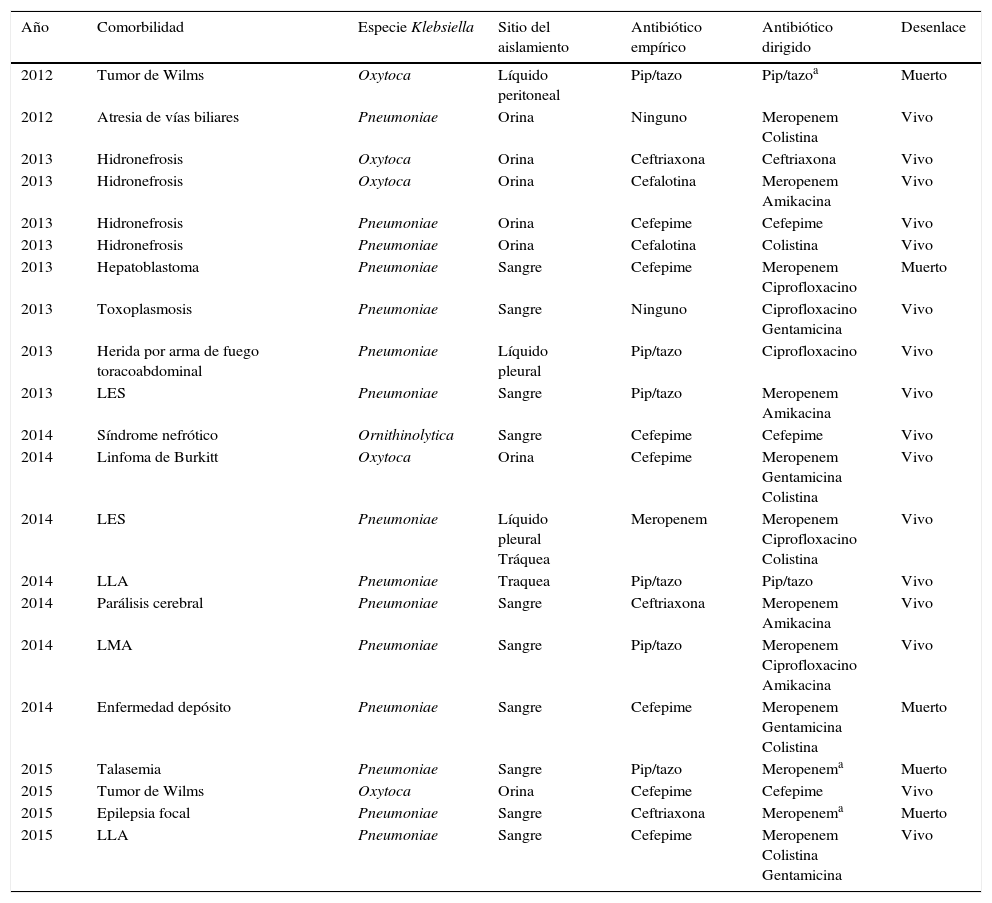
En la tabla 6, se resumen las características principales de los 21 pacientes con aislamiento de Klebsiella resistente a carbapenémicos, comorbilidad, especie y sitio de aislamiento, antibiótico empírico y dirigido, y desenlace.
Caracterización de pacientes pediátricos con aislamiento de Klebsiella productora de carbapenemasa en la Fundación Hospital de La Misericordia, Bogotá (Colombia)
| Año | Comorbilidad | Especie Klebsiella | Sitio del aislamiento | Antibiótico empírico | Antibiótico dirigido | Desenlace |
|---|---|---|---|---|---|---|
| 2012 | Tumor de Wilms | Oxytoca | Líquido peritoneal | Pip/tazo | Pip/tazoa | Muerto |
| 2012 | Atresia de vías biliares | Pneumoniae | Orina | Ninguno | Meropenem Colistina | Vivo |
| 2013 | Hidronefrosis | Oxytoca | Orina | Ceftriaxona | Ceftriaxona | Vivo |
| 2013 | Hidronefrosis | Oxytoca | Orina | Cefalotina | Meropenem Amikacina | Vivo |
| 2013 | Hidronefrosis | Pneumoniae | Orina | Cefepime | Cefepime | Vivo |
| 2013 | Hidronefrosis | Pneumoniae | Orina | Cefalotina | Colistina | Vivo |
| 2013 | Hepatoblastoma | Pneumoniae | Sangre | Cefepime | Meropenem Ciprofloxacino | Muerto |
| 2013 | Toxoplasmosis | Pneumoniae | Sangre | Ninguno | Ciprofloxacino Gentamicina | Vivo |
| 2013 | Herida por arma de fuego toracoabdominal | Pneumoniae | Líquido pleural | Pip/tazo | Ciprofloxacino | Vivo |
| 2013 | LES | Pneumoniae | Sangre | Pip/tazo | Meropenem Amikacina | Vivo |
| 2014 | Síndrome nefrótico | Ornithinolytica | Sangre | Cefepime | Cefepime | Vivo |
| 2014 | Linfoma de Burkitt | Oxytoca | Orina | Cefepime | Meropenem Gentamicina Colistina | Vivo |
| 2014 | LES | Pneumoniae | Líquido pleural Tráquea | Meropenem | Meropenem Ciprofloxacino Colistina | Vivo |
| 2014 | LLA | Pneumoniae | Traquea | Pip/tazo | Pip/tazo | Vivo |
| 2014 | Parálisis cerebral | Pneumoniae | Sangre | Ceftriaxona | Meropenem Amikacina | Vivo |
| 2014 | LMA | Pneumoniae | Sangre | Pip/tazo | Meropenem Ciprofloxacino Amikacina | Vivo |
| 2014 | Enfermedad depósito | Pneumoniae | Sangre | Cefepime | Meropenem Gentamicina Colistina | Muerto |
| 2015 | Talasemia | Pneumoniae | Sangre | Pip/tazo | Meropenema | Muerto |
| 2015 | Tumor de Wilms | Oxytoca | Orina | Cefepime | Cefepime | Vivo |
| 2015 | Epilepsia focal | Pneumoniae | Sangre | Ceftriaxona | Meropenema | Muerto |
| 2015 | LLA | Pneumoniae | Sangre | Cefepime | Meropenem Colistina Gentamicina | Vivo |
La mayoría de los datos encontrados en la literatura reportan infección por enterobacterias productoras de carbapenemasas en adultos. Hay pocos estudios al respecto en Pediatría1.
El presente estudio caracterizó a pacientes entre 0 y 18 años de edad, con infecciones por Klebsiella spp. resistente a carbapenémicos, atendidos en un hospital pediátrico de la ciudad de Bogotá.
Este estudio encontró el antecedente de hospitalización previa en el 81% de los pacientes y de uso de antibiótico en los 6 meses anteriores en el 67% de los pacientes: el meropenem fue el antimicrobiano más frecuentemente usado, en el 43% de los casos. Estos datos concuerdan con lo descrito en la literatura, donde se ha observado una relación directa entre el uso de antibióticos, principalmente carbapenémicos, piperacilinas y ceftriaxona, y la emergencia de gérmenes resistentes a carbapenémicos5–7.
Estudios previos en Pediatría muestran como hasta el 97% de los pacientes habían recibido esquemas antibióticos en los meses anteriores a la documentación del germen productor de carbapenemasa (Klebsiella y otras enterobacterias): en ninguno se especifica el tipo de antibiótico recibido.
No se encontraron datos reportados respecto la colonización previa de los pacientes por gérmenes resistentes en la literatura revisada. El presente trabajo evidenció la colonización e infección previa por Klebsiella de fenotipo usual, BLEE y productora de carbapenemasa en 3 y 5 de los 21 pacientes, respectivamente.
El 95% de los pacientes en esta serie tenían una comorbilidad asociada. La más frecuente fue la enfermedad oncohematológica en el 40%, la renal en el 25% y la neurológica en el 20%. Los resultados del presente trabajo no pueden extrapolarse a otros tipos de poblaciones, puesto que el Hospital de La Misericordia es un centro de tercer nivel de atención, con predominio de pacientes con enfermedades oncohematológicas y neurológicas.
En otros estudios, se reporta comorbilidad asociada en el 92% de los niños. Las enfermedades más comunes fueron: enfermedad pulmonar (30%), prematuridad (27%), leucemia o tumor sólido (19%), cardiopatía (19%), enterocolitis necrosante o síndrome de intestino corto en 5 (14%) y trasplante de órgano sólido o células hematopoyéticas (11%)1.
El tiempo promedio de estancia hospitalaria fue de 53 días; el servicio con mayor número de aislamientos fue la Unidad de Cuidados Intensivos Pediátricos con el 43% de los casos, seguido por Hospitalización General con el 29%. Está claramente descrita en la literatura la hospitalización prolongada como un factor de riesgo para infección por gérmenes resistentes, y en las diferentes series se sitúa la Unidad de Cuidados Intensivos como el servicio con mayor incidencia de gérmenes resistentes en relación con los múltiples dispositivos que requieren los pacientes allí hospitalizados para su soporte vital.
Otros estudios muestran una estancia hospitalaria promedio de 16 días (rango 1-385 días) antes de la infección por enterobacteria productora de carbapenemasa. Los servicios de hospitalización en su orden de frecuencia fueron: UCI Pediátrica o Neonatal (53%), salas de pediatría (18%), servicios quirúrgicos (15%), Hematooncología (7%) y otras salas (5%). Se encontró un niño infectado en el Servicio de Urgencias1.
De los 21 pacientes infectados por Klebsiella productora de carbapenemasa, el 81% adquirió el germen como IACS. La localización más frecuente son las infecciones del torrente sanguíneo con el 41,1% de los casos y con promedio de duración del catéter de 27,7 días. Estudios previos han descrito claramente la asociación del catéter venoso central y la prolongación de su uso con la adquisición de gérmenes resistentes (OR: 1,07), así como su relación con la necesidad de ventilación mecánica (HR: 3,8); sin embargo, en nuestro estudio el tiempo promedio de ventilación mecánica fue de 8,4 días y solo se documentó una neumonía asociada al ventilador5–7.
Con respecto al tratamiento antibiótico específico, una vez conocido el aislamiento microbiológico, el 52% de nuestros pacientes recibió terapia combinada, el 28,5% terapia doble y el 23,5% terapia triple.
El 19% (4 casos) recibió monoterapia, un aislamiento en orina tratado con colistina con evolución favorable, un caso de empiema tratado con ciprofloxacino con adecuada respuesta y 2 bacteriemias con esquema previo de ceftriaxona y piperacilina/tazobactam en la que se hizo cambio a meropenem por deterioro clínico, pero el paciente falleció antes de conocerse el patrón de resistencia del germen.
En el 23,8% (5 casos) no fue necesario realizar ajustes en el esquema antibiótico, ya que a pesar de recibir un antibiótico con resistencia in vitro del germen aislado se logró negativización de los cultivos y la evolución clínica fue favorable. De estos 5 casos, 3 aislamientos correspondieron a orina, uno a tráquea y solamente uno a sangre. Se puede atribuir el éxito en el tratamiento a que el inóculo bacteriano estaba controlado y el antibiótico alcanzó adecuadas concentraciones.
En otros estudios, los tratamientos utilizados fueron: aminoglucósidos en 14 casos (58%), en 5 de estos casos el aminoglucósido se asoció a fluoroquinolona (4 casos) o trimetoprim-sulfametoxazol (un caso); se utilizó tigeciclina como monoterapia en un caso. Nueve niños (38%) no recibieron antibioticoterapia específica para el aislamiento; 6 de estos niños sobrevivieron a la infección y no presentaron recurrencia1.
Es necesario aclarar que los primeros aislamientos de gérmenes con patrón de resistencia de carbapenemasa en nuestra institución datan del año 2012: fueron estos aislamientos los que recibieron monoterapia; posteriormente, conforme los conocimientos en el tema han mostrado que la mortalidad se ve incrementada con la monoterapia (40-80%) y se reduce significativamente con el uso de terapia combinada (20-30%), se ha implementado el uso de terapia antibiótica doble y triple en nuestros pacientes8–11.
De forma similar al presente estudio, cohortes realizadas por diferentes autores muestran como a lo largo de la historia se han tratado enterobacterias productoras de carbapenemasa con monoterapia con carbapenémico, tigeciclina, colistina y amikacina, con tasas de sobrevida de hasta el 58% (del 20 al 60%). De la misma manera, muestran cómo, tras la implementación de terapia combinada (terapia doble o triple), las tasas de supervivencia alcanzan hasta el 100% (50-100%)8.
El presente trabajo mostró corresistencias en el 81% de los casos: 48% a aminoglucósidos, 29% a ciprofloxacino y 5% a tigeciclina; este es un dato preocupante, ya que, además de presentar resistencia a los carbapenémicos, los gérmenes empiezan a mostrar resistencia a las opciones terapéuticas de rescate, limitando las posibilidades de tratamiento. Actualmente, se inició la sistematización en el Laboratorio de Microbiología del Hospital de la Misericordia de la inclusión de pruebas de sensibilidad a tigeciclina y, próximamente, a fosfomicina.
La mortalidad en el grupo de pacientes evaluados fue del 24%, similar a la reportada en los diferentes estudios (24-70%). El 80% de los pacientes fallecidos tuvieron el aislamiento en sangre y uno de ellos en líquido peritoneal, lo que estaría en relación con una mayor carga bacteriana y un difícil control de esta carga como factor ensombrecedor del pronóstico.
La resistencia bacteriana es un problema de salud pública. La diseminación mundial de cepas de Klebsiella spp. resistentes a carbapenémicos dificulta el manejo de los pacientes y empeora su pronóstico. Caracterizar a los pacientes que se han infectado por estos microrganismos permite conocer un poco este fenómeno y establecer las bases para el diseño de estudios experimentales que lleven a definir los factores de riesgo y a evaluar diferentes alternativas de prevención y tratamiento.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.