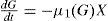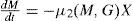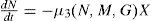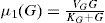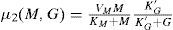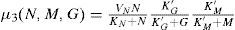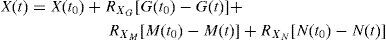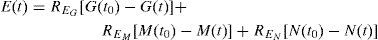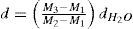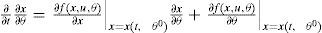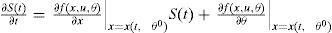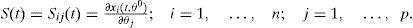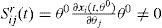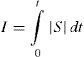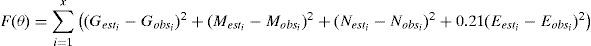El objetivo de la presente investigación fue estudiar el comportamiento del proceso de fermentación de cerveza artesanal mediante un modelo matemático dinámico. El modelo contiene las tasas de cambio de las variables de estado concentración de glucosa, maltosa y maltotriosa. La variable de salida es la concentración de etanol y como variable auxiliar contempla la concentración de biomasa (levaduras). Este modelo fue programado en el ambiente Matlab-Simulink y para su integración numérica se utilizó el método de Dormand-Prince de cuarto grado con tamaño de paso de integración variable y una tolerancia relativa de 10−8. Para conocer sus parámetros más importantes se realizó un análisis de sensibilidad local. Además se llevó a cabo un experimento para producir cerveza artesanal a una temperatura constante (21°C). Se implementaron 14 unidades experimentales (fermentadores) con las mismas condiciones iniciales. De cada fermentador, se midieron las concentraciones de las variables de estado incluidas en el modelo matemático. Usando los resultados experimentales el modelo se calibró mediante los algoritmos de optimización mínimos cuadrados no lineales y evolución diferencial. De acuerdo con las estadísticas sesgo (BIAS), coeficiente de correlación (r), raíz cuadrada del cuadrado medio (RMSE), error medio absoluto (MAE) y eficiencia de modelación (EF) se encontró un buen ajuste entre las predicciones del modelo y las mediciones de las variables de estado después de la estimación de los parámetros.
The goal of the current research was to study the behavior of the fermentation process of home-made beer using a mathematical dynamic model. The model contains the rates of change of the concentration state variables of glucose, maltose and maltotriose. An output variable is the ethanol concentration and an auxiliary variable is the biomass (yeast) concentration. The model was programmed in the Matlab-Simulink environment, and for its numerical integration Dormand-Prince method of fourth order with a variable integration step size and a relative tolerance of 10−8 was used. In order to know which model parameters are more important, a local sensitivity analysis was carried out. Furthermore, an experiment was performed to produce home-made beer at constant temperature (21°C). Fourteen experimental units (fermenters) with the same initial conditions were implemented. Using the experimental results the model was calibrated by nonlinear least squares and differential evolution algorithms. According to the statistics bias (BIAS), correlation coefficient (r), squared root of mean squared error (RMSE), mean absolute error (MAE) and the efficiency of modeling (EF), a good fit between the model predictions and measurements were found after the model parameters estimation.
La fermentación es el proceso más importante de la elaboración de cerveza. Según se realice, producirá resultados diferentes (López, 2007). En la práctica, esto significa que los tiempos de fermentación pueden variar considerablemente entre lotes de cerveza de la misma calidad (Defernez et al, 2007; Bamforth et al., 2009).
La temperatura de fermentación, así como el tipo de levaduras utilizado, son de gran relevancia al reproducir un estilo de cerveza determinado, por lo cual, en la producción es común usar refrigeración para controlar la temperatura en el proceso de fermentación (Ramirez y Maciejowski, 2007).
Actualmente existen diversos modelos matemáticos que permiten simular la dinámica de fermentación de cerveza, estos pueden usarse para predecir algunas variables durante la fermentación, como concentración de etanol, sustratos y ésteres (Hepworth et al., 2003). Un buen modelo debe incluir los componentes más importantes en la fermentación, entre ellos: azúcares, biomasa y etanol. Algunos modelos más complejos incluyen el sabor y aroma, los cuales distinguen una cerveza de otra. Estos modelos proveen de bases sólidas para realizar la optimización del proceso (Ramirez y Maciejowski, 2007).
Dentro de las investigaciones realizadas para simular el proceso de fermentación se encuentra la de Trelea et al. (2001), donde se proponen y validan tres modelos dinámicos de fermentación de cerveza a escala de laboratorio: un modelo basado en el conocimiento biológico de la fermentación, un modelo empírico basado en la forma de curvas experimentales y un modelo de caja negra basado en una red neural artificial. Los modelos toman en cuenta la temperatura de fermentación, la presión en la parte superior del fermentador y la concentración inicial de levadura, y predicen la densidad del mosto, la concentración de azúcar residual, la concentración de etanol y el dióxido de carbono (CO2) liberado. Dichos modelos fueron comparados en términos de precisión de la predicción, robustez y capacidad de generalización (interpolación y extrapolación), llegando a la conclusión de que debido a los pocos datos obtenidos durante el proceso de medición, los modelos que incluyen más conocimiento del proceso parecen igualmente precisos, pero más fiables que la red neuronal.
Por otra parte, Xiao et al. (2004) desarrollaron una investigación en la cual durante un periodo fijo de tiempo de fermentación, se construyeron una serie de perfiles de temperatura diferentes, del cual se eligió el perfil óptimo de temperatura con el que se maximiza la producción de etanol y se reduce al mínimo la concentración de subproductos y el riesgo de deterioro. Para la optimización de la cinética del modelo se utilizó un algoritmo de optimización de colonia de hormigas.
Madar et al. (2005) plantearon un problema de optimización del proceso de fermentación en su trabajo, utilizaron computación evolutiva interactiva (IEC). Los resultados que obtuvieron muestran que IEC es un método eficiente y cómodo para incorporar el conocimiento del usuario en la optimización del modelo basado en procesos por lotes.
Otro experimento importante relacionado con este tema, es el desarrollado por Oonsivilai y Oonsivilai (2009), quienes realizaron estudios controlando un perfil de temperatura para impulsar el proceso, a fin de obedecer ciertas restricciones durante la fermentación de la cerveza. El diseño de este perfil de temperatura también es un problema de optimización, donde el objetivo es reducir al mínimo el tiempo de operación y optimizar la calidad de la cerveza, dicho problema fue resuelto mediante un algoritmo evolutivo llamado evolución diferencial. Los resultados mostraron que este algoritmo es un método fácil y competente para incorporar el conocimiento previo del usuario en la optimización del perfil de temperatura de los procesos por lotes.
Otro modelo importante es el desarrollado por Engasser et al. (1981) para controlar el proceso de fermentación, el cual toma en consideración el metabolismo de la levadura y ecuaciones de cinética relativamente simples para la asimilación de diferentes azúcares. Este modelo fue modificado por Gee y Ramirez (1988) para incluir los efectos de la temperatura en dicho proceso, donde se supone que el medio de fermentación contiene tres azúcares, maltosa, glucosa y maltotriosa. En investigaciones más recientes, Gee y Ramirez (1994) desarrollaron un nuevo modelo de fermentación de cerveza, el cual se puede subdividir en un modelo de crecimiento, un modelo de aminoácidos y un modelo de sabor-aroma. Los resultados evidenciaron la capacidad de describir con precisión la dinámica de fermentación de cerveza por lotes.
Los diferentes modelos encontrados en la literatura para simular el proceso de fermentación, se han enfocado en la cerveza producida a gran escala en la industria, por lo que intentan duplicar en laboratorio las condiciones industriales reales. Por lo anterior, en el presente trabajo se plantearon los siguientes objetivos: i) simular el proceso de fermentación de cerveza artesanal mediante un modelo dinámico mecanicista utilizado para el proceso de producción de cerveza industrial, ii) realizar un análisis de sensibilidad local del modelo, iii) estimar los parámetros más importantes del modelo usando mediciones de las variables de estado provenientes de un experimento.
Desarrollo. Modelo matemático para la fermentaciónEl modelo matemático de fermentación de cerveza utilizado en este trabajo, fue propuesto Gee y Ramirez (1988). Sin embargo, en esta investigación no se consideró la variable de estado temperatura debido a que el proceso se llevó a cabo a temperatura constante. En este modelo se supone que el medio de fermentación contiene tres azúcares, maltosa, glucosa y maltotriosa. Las tasas de cambio de los tres azúcares (variables de estado) se calculan mediante tres ecuaciones diferenciales:
Glucosa:
Maltosa: Maltotriosa: donde y G (mol m−3) es la concentración de glucosa, M (mol m−3) es la concentración de maltosa, N (mol m−3) es la concentración de maltotriosa, X (mol m−3) es la concentración de biomasa, μi(h−1) es la tasa específica de absorción de azúcar, Vi (h−1)es la velocidad de reacción máxima para el azúcar (i=G, M, o N), Ki (mol m −3) es la constante de Michaelis para el azúcar (i=G, M, o N) y K'i es la constante de inhibición para el azúcar (i=G o M).Ecuaciones algebraicas para concentraciones de biomasa y etanol, respectivamente:
donde E (mol m −3) es la concentración de etanol, Rxi es el rendimiento estequiométrico de la biomasa por mol de azúcar reaccionado (i = G, M, o N) y REi es el rendimiento estequiométrico de etanol por mol de azúcar reaccionado i=G,M,o N,Rxi y REi se suponen constantes.Descripción del experimentoPara la obtención de datos experimentales se produjo cerveza artesanal en pequeña escala, comenzando con la elaboración de mosto, donde se utilizó extracto de malta en polvo con la finalidad de evitar todo el proceso anterior en la producción de cerveza. Para esto, se calentaron 10L de agua hasta llegar al punto de ebullición, en ese momento se agregaron 2kg de malta en polvo y 10L más de agua, para obtener una relación de un 1kg de malta por cada litro de agua. Después, se llevó la mezcla al punto de ebullición de nuevo y se mantuvo a esta temperatura durante los siguientes 55minutos. Durante este tiempo se agregó lúpulo (Humulus lupulus, var. cascade) en dos ocasiones, la primera a los 15 minutos después de haber alcanzado la temperatura de ebullición y la segunda 25minutos después de la primera aplicación. Finalmente se filtró el lúpulo y las impurezas para iniciar la puesta en marcha del experimento.
Condiciones de operaciónDado que la cerveza artesanal lleva a cabo su fermentación en un rango de 17–24°C (López, 2007) y el experimento se realizó a temperatura constante, se decidió trabajar a 21°C. Para esto, se acondicionaron 14 unidades experimentales (fermentadores) de 0.5L, a los cuales se les agregaron 0.4L de mosto.
En el proceso de fermentación se utilizó una levadura seca tipo ale (Saccharomyces cerevisiae), de la cual se agregó 0.2g (19.3 mol/m3) a cada unidad experimental. La levadura se sembró directamente en cada uno de los fermentadores y se verificó que la temperatura del mosto estuviera a 21°C. Los fermentadores se dejaron en reposo por 30 min y luego se mezclaron agitándolos lentamente con el fin de distribuir la levadura y airear el mosto. Después, cada fermentador se acondicionó con un tapón de goma y un airlock que permitiera la salida de gases durante la fermentación (figura 1).
Debido a que el proceso se realizó a temperatura constante fue necesario utilizar una incubadora acondicionada un día antes de iniciar el experimento para que se mantuviera a la temperatura requerida de 21°C. Finalmente, se acomodaron todos los fermentadores dentro de la incubadora.
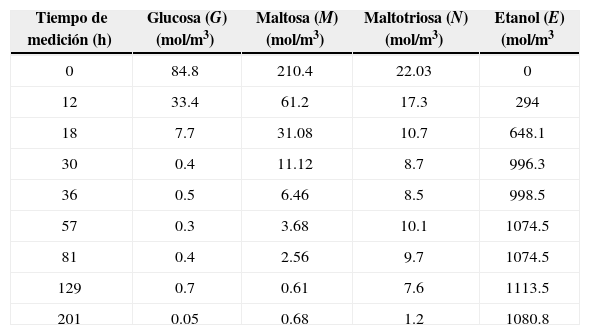
Adquisición de datosLas variables medidas durante la fermentación fueron: concentración de glucosa, maltosa, maltotriosa y etanol. Los tiempos de medición se determinaron de acuerdo con la dinámica del proceso de fermentación, la cual presenta una mayor variación durante los primeros días. En cada medición realizada se tomó una unidad experimental para su análisis, esta se agitaba para homogenizar la muestra. De cada fermentador se guardaron 40 mL de muestra en un tubo de ensayo para colocarlo en congelación. De las muestras congeladas se eligieron las más representativas, con base en el comportamiento de la dinámica del proceso de fermentación para una temperatura de 16°C. Las muestras seleccionadas se analizaron mediante cromatografía de gases para determinar las concentraciones de glucosa, maltosa y maltotriosa (tabla 1 más adelante).
Mediciones de concentración de glucosa, maltosa, maltotriosa y etanol
| Tiempo de medición (h) | Glucosa (G) (mol/m3) | Maltosa (M) (mol/m3) | Maltotriosa (N) (mol/m3) | Etanol (E) (mol/m3 |
|---|---|---|---|---|
| 0 | 84.8 | 210.4 | 22.03 | 0 |
| 12 | 33.4 | 61.2 | 17.3 | 294 |
| 18 | 7.7 | 31.08 | 10.7 | 648.1 |
| 30 | 0.4 | 11.12 | 8.7 | 996.3 |
| 36 | 0.5 | 6.46 | 8.5 | 998.5 |
| 57 | 0.3 | 3.68 | 10.1 | 1074.5 |
| 81 | 0.4 | 2.56 | 9.7 | 1074.5 |
| 129 | 0.7 | 0.61 | 7.6 | 1113.5 |
| 201 | 0.05 | 0.68 | 1.2 | 1080.8 |
Para obtener la concentración de etanol (tabla 1), se extrajeron 100mL de muestra, los cuales se montaron en un equipo de destilación (figura 2). La muestra se calentó hasta que se evaporó aproximadamente 60% de la cantidad contenida en el matraz, posteriormente el producto evaporado se mezcló con agua destilada hasta alcanzar nuevamente una muestra de 100mL. A partir del producto destilado se llevó a cabo el procedimiento de determinación de alcohol mediante diferencia de densidad con la ayuda de un picnómetro y una balanza de precisión.
Para determinar el contenido de etanol mediante el uso del picnómetro y la balanza de precisión, se utilizó la ecuación 9:
donde d es la densidad de la muestra destilada a 20°C (g mL−1), M1 es la masa del picnómetro vacío (perfectamente seco) (g), M2 es la masa del picnómetro lleno de agua destilada (g), M3 es la masa del picnómetro lleno con la muestra destilada (g) y dH2O es la densidad del agua a 20°C. Debido a que la ecuación 9 da como resultado la densidad de la muestra destilada, se utilizaron valores tabulados por Vogt (1972), para poder transformar las unidades en gramos de alcohol por litro (g/L). Sin embargo, el modelo matemático considera la concentración de etanol en mol m−3, por lo que la concentración se multiplicó por un factor de (1000/peso molecular del etanol) donde el peso molecular del etanol es 46.069g/mol (Doran, 2003) y de esta forma se obtuvo la concentración de etanol en las unidades deseadas.Implementación del modelo matemáticoLa implementación del modelo se llevó a cabo en el ambiente MATLAB-SIMULINK y consta de un programa principal (home_beer.m) donde se definen las condiciones iniciales, el tiempo de simulación y los parámetros del modelo para una temperatura de 16°C. Adicionalmente, se cuenta con una subrutina en SIMULINK donde se implementa el modelo dinámico (homebeer.mdl), en el cual se definen las variables de estado (glucosa, maltosa y maltotriosa), la ecuación auxiliar (biomasa) y la ecuación de salida (etanol). El programa principal llama al modelo simulink (archivo .mdl) que contiene el modelo matemático. Para integrar el modelo se utilizó el algoritmo de Dormand-Prince, el cual está programado en la función ode45.m de Matlab. Este método utiliza un tamaño de paso de integración (Δt) variable.
Se utilizó una tolerancia relativa de 1×10−8. Las estadísticas de ajuste utilizadas para evaluar el desempeño del modelo con los parámetros estimados en la calibración fueron: el error cuadrático medio (RMSE), el error absoluto (MAE), el sesgo (BIAS), la eficiencia (EF) y el coeficiente de correlación (r).
Análisis de sensibilidad del modeloPara determinar los parámetros que más influyen en el comportamiento de un modelo y, por consiguiente, candidatos para ser estimados, se realizó un análisis de sensibilidad local (Saltelli et al., 2000; López et al., 2004), para lo cual, diferenciando las ecuaciones de estado respecto al vector de parámetros θ y suponiendo que el vector de las variables de entrada no depende de θ, se tiene que:
De donde resultan las ecuaciones de sensibilidad:
donde S(t) se define como:En donde el número de ecuaciones de sensibilidad resultante es de nxp
Con fines de comparación entre parámetros, se calcularon las sensibilidades relativas mediante la ecuación:
Dado que las sensibilidades son funciones variantes en el tiempo, se calculó la integral del valor absoluto de las sensibilidades relativas S(t) en el periodo de fermentación:
Donde t es el tiempo final y 0 el tiempo inicial. La integral permite comparar de forma numérica los parámetros y determinar cuáles afectan en mayor medida el comportamiento del modelo.Calibración del modeloEn la calibración del modelo se tomaron en cuenta las mediciones obtenidas de las variables de estado (glucosa, maltosa y maltotriosa) y la variable de salida (etanol). Para llevar a cabo la calibración del modelo se planteó un problema de optimización, usando el procedimiento de mínimos cuadrados no lineales para estimar los valores de los parámetros de mayor importancia, los cuales fueron seleccionados previamente mediante el análisis de sensibilidad. El algoritmo de optimización utilizado permitió aproximar lo más posible las predicciones del modelo a las mediciones. La función a minimizar fue:
donde θ es un vector que contiene los parámetros a estimar, X es el número de mediciones de glucosa (G), maltosa (M), maltotriosa (N) y etanol (E), 0.21 es un factor de escala, el subíndice est indica el valor estimado y el subíndice obs, el valor observado. El problema de optimización se resolvió mediante la rutina lsqnonlin del optimization toolbox de Matlab, utilizando el algoritmo de Levenberg-Marquardt.Con la finalidad de verificar la calidad de la estimación de los parámetros del modelo, el problema de optimización anterior también se resolvió mediante el algoritmo de evolución diferencial, en donde se utilizó la estrategia clásica “DE/rand/1/bin” (Price et al., 2005), con una probabilidad de cruzamiento CR=0.2, factor de variación diferencial F=0.9, tamaño de la población igual NP=10×n donde n es el número de parámetros a estimar, con una precisión de convergencia de la población 1×10−8 y 50 como número máximo de generaciones.
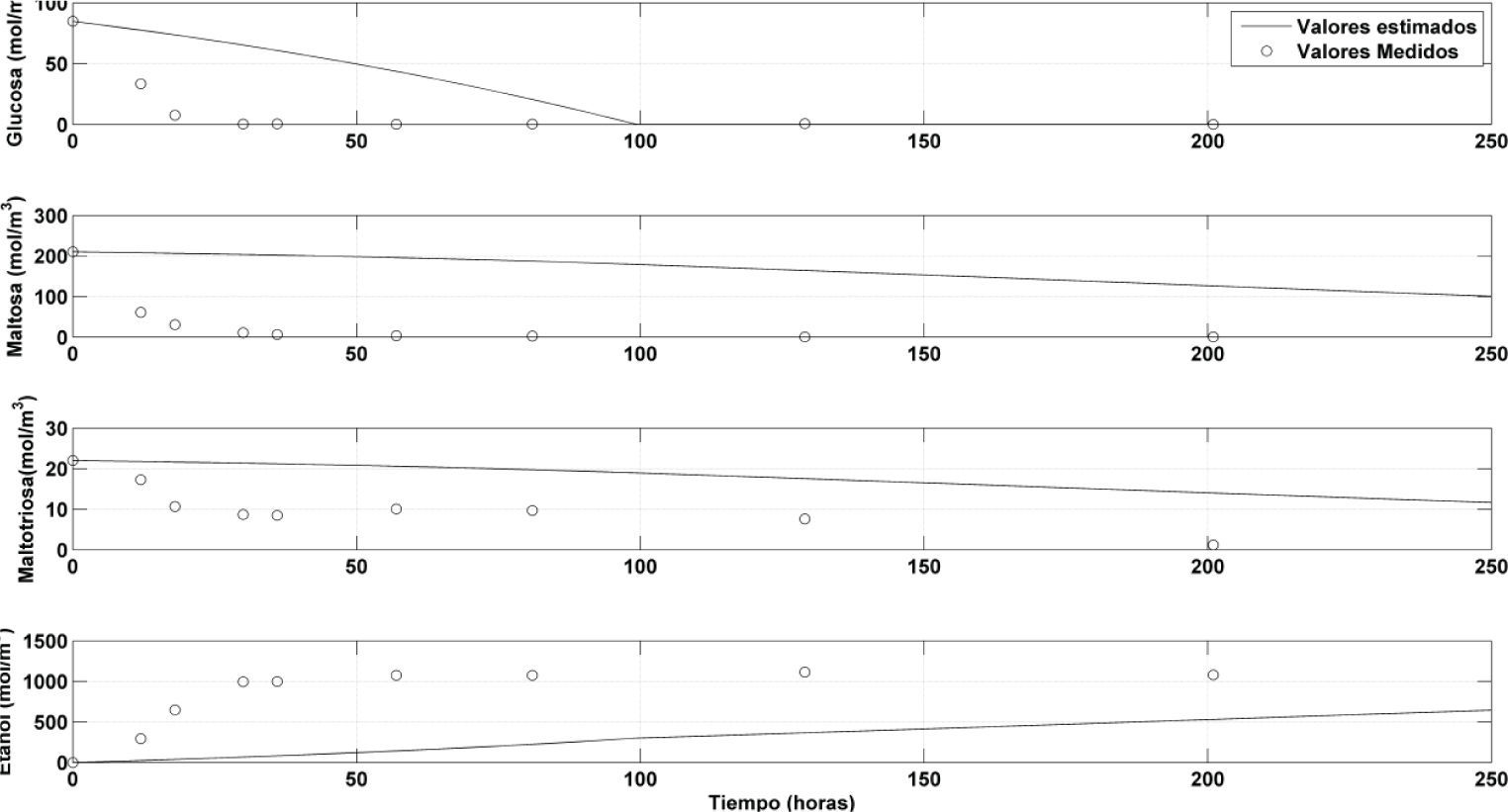
Discusión y análisis de resultadosLa figura 3 muestra la comparación entre los valores medidos (tabla 1) y los valores simulados para la concentración de las variables de estado (G, M y N) y la variable de salida (E) con respecto al tiempo de fermentación. Las condiciones iniciales utilizadas para la simulación fueron las del experimento (tabla 1), tomando en cuenta que para la biomasa la condición inicial fue 19.3 mol m−3. Debido a que el proceso de fermentación se realizó a una temperatura de 21°C, se utilizaron los valores de los parámetros cinéticos correspondientes a la temperatura de 16°C (Gee y Ramirez, 1988), esto con la finalidad de tener una mayor semejanza entre los valores simulados y los medidos.
Como puede observarse en la figura 3, las predicciones del modelo con los valores de los parámetros para una temperatura de 16°C, reproducen la dinámica del comportamiento de las variables modeladas; sin embargo, los valores medidos y los simulados difieren en gran escala, por lo que fue necesario realizar la estimación de los parámetros (calibración del modelo) seleccionados mediante el análisis de sensibilidad descrito.
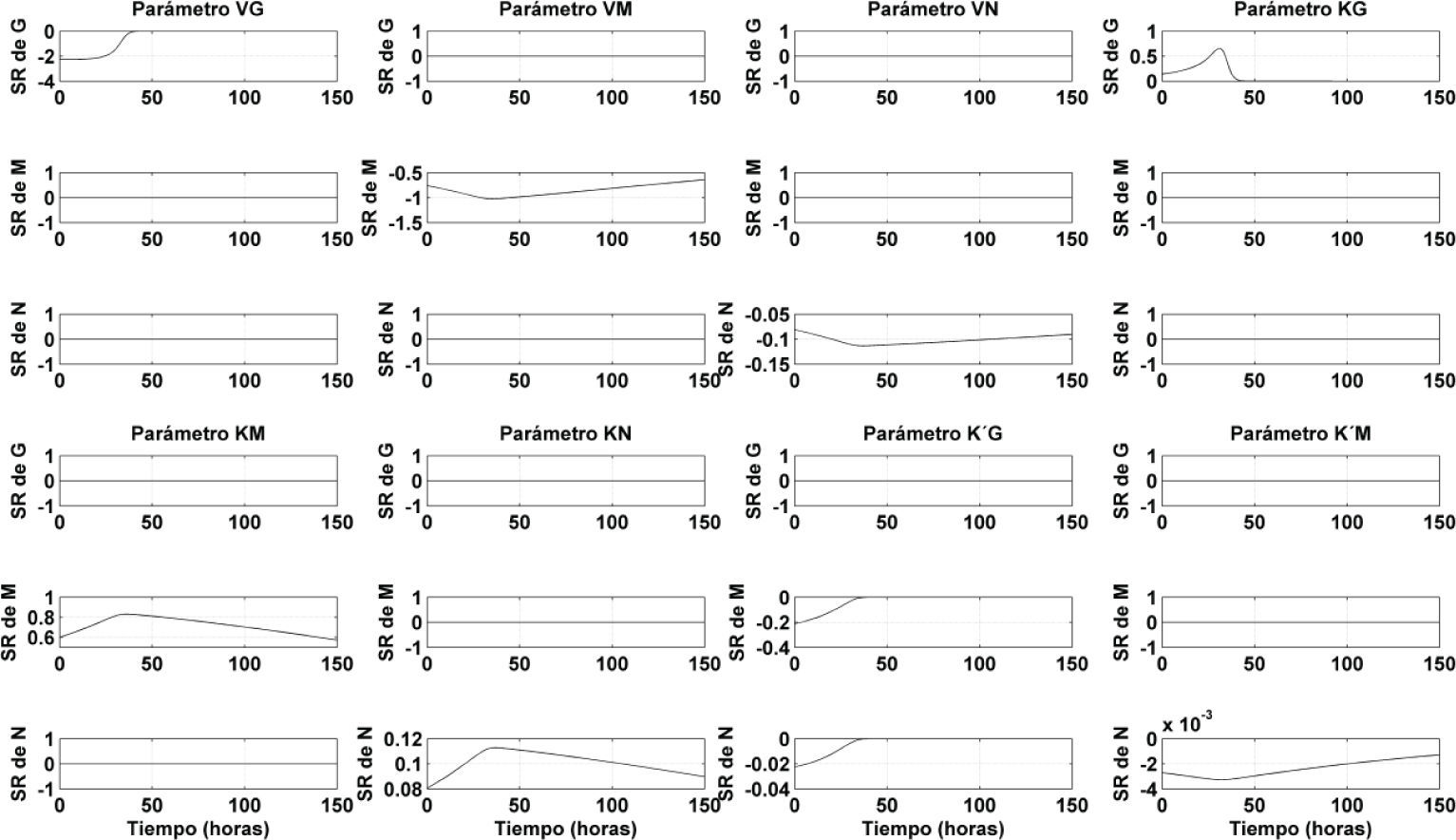
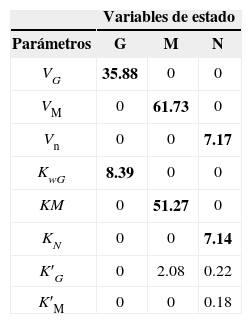
Análisis de sensibilidadEn la figura 4 se muestran las sensibilidades relativas de los estados glucosa (G), maltosa (M) y maltotriosa (N), con respecto a cada uno de los parámetros. Un valor absoluto de la sensibilidad relativa mayor que cero indica que el modelo es sensible a un cambio pequeño del parámetro respectivo. Las sensibilidades relativas de los parámetros se muestran en la tabla 2, donde G, M y N son las variables de estado y VG, VM, VN, KG, KM, KN, K′G, y K′M los parámetros cinéticos del modelo. En la misma tabla se observa que la variable de estado G es sensible al cambio en los parámetros VG y KG, la variable de estado M es sensible al cambio en los parámetros VM y KM, mientras que la variable de estado N es sensible al cambio en los parámetros VN y KN ; por lo cual, todos estos parámetros de gran importancia, fueron tomados en cuenta durante la calibración del modelo. Por otro lado, los parámetros K′G, y K′M, al ser poco relevantes debido a que su variación no afecta en gran medida al modelo, no fueron considerados para la calibración. Los valores de los parámetros no relevantes para el modelo se tomaron del trabajo de Gee y Ramirez (1988), para una temperatura de 16°C.
Una vez seleccionados los parámetros que afectan el comportamiento del modelo de manera importante, se llevó a cabo la calibración. Los valores de los parámetros nominales se aproximaron de forma manual siguiendo su tendencia al aumentar la temperatura de fermentación (Gee y Ramirez, 1988) en el momento en que se logró cierta proximidad entre los valores simulados y los valores medidos de las variables de estado, estos valores de los parámetros se consideraron como nominales; en la calibración se les dio un rango de variación para encontrar los valores que minimizaran la función objetivo (ecuación 15).
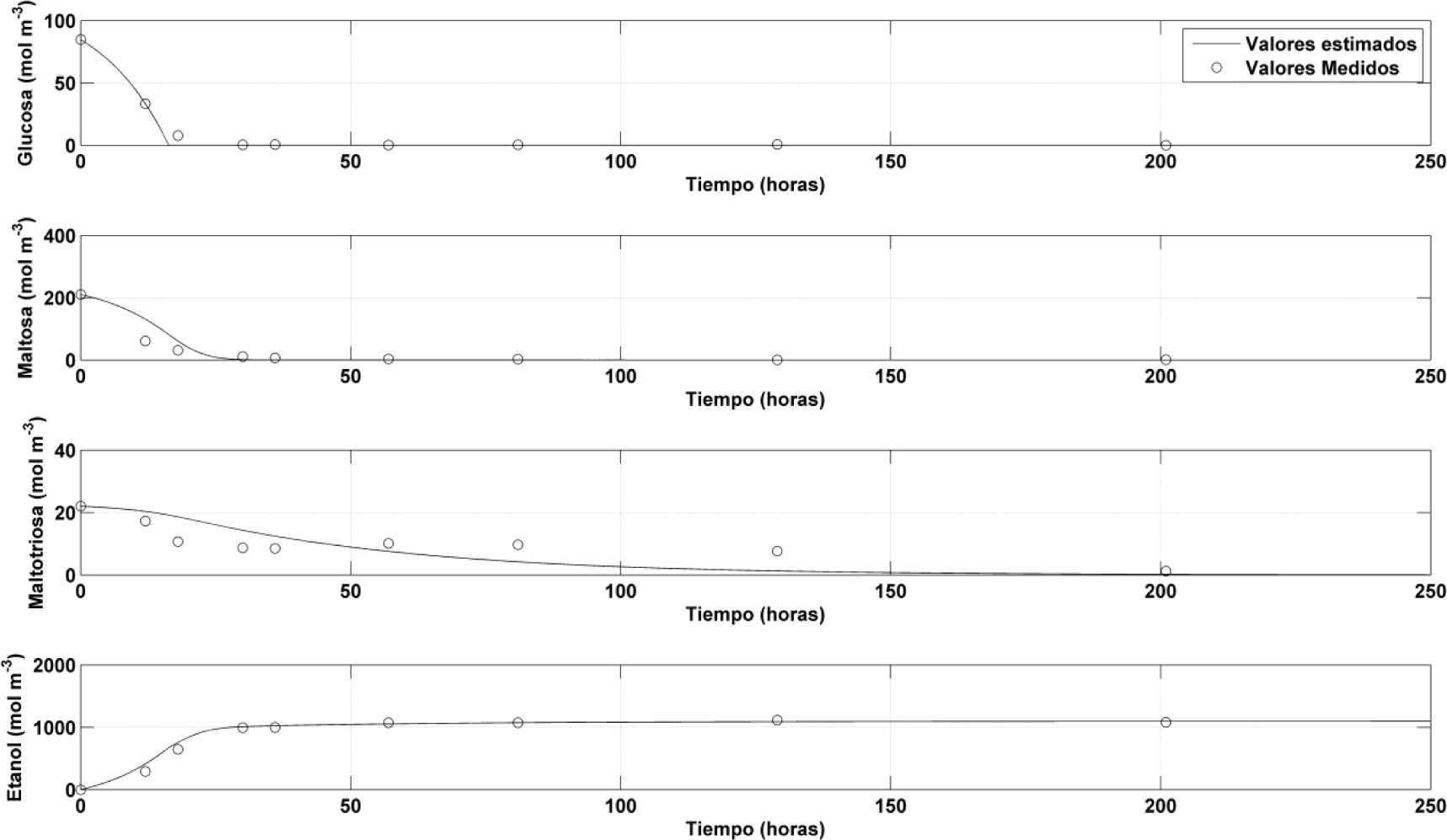
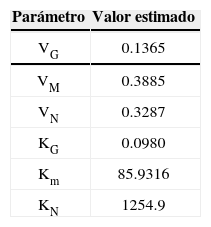
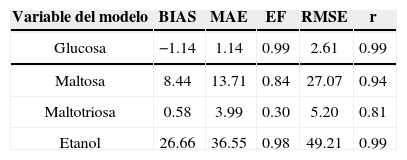
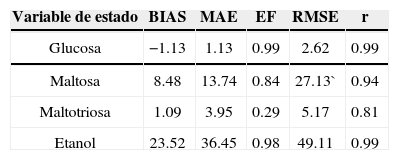
Calibración y simulación del modeloEn la figura 5 se muestra la comparación entre los valores de las concentraciones de las variables del modelo medidas y simuladas con respecto al tiempo de fermentación, en donde la simulación se realizó con los parámetros cinéticos estimados mediante el método de mínimos cuadrados no lineales para una temperatura de 21°C. En la tabla 3 se muestran los valores estimados para cada uno de los parámetros cinéticos del modelo mediante la rutina Isqnonlin del Optimization toolbox de Matlab. En la tabla 4 se encuentran las estadísticas de ajuste entre el modelo ya calibrado y los datos medidos para cada una de las variables de estado y la variable de salida. De acuerdo con la estadística sesgo (BIAS) el modelo sobreestima la cantidad de glucosa aunque esto difícilmente puede apreciarse en la figura 5 ya que el ajuste entre predicciones y mediciones es muy preciso. Esto puede apreciarse tanto en la figura 5 como en la estadística índice de eficiencia (EF) y en el coeficiente de correlación (r). De acuerdo con las estadísticas RMSE y MAE la variable glucosa puede predecirse con mayor precisión. En contraste, la maltosa, maltotriosa y etanol son subestimadas por el modelo tomando en cuenta la estadística sesgo. Esto, sin embargo, es válido sólo para la maltotriosa como puede notarse en la figura 5 y en el bajo valor del índice de eficiencia (EF) y coeficiente de correlación obtenido para esta variable. El ajuste entre predicciones y mediciones en el caso de maltosa y etanol fue bastante preciso como puede verificarse en los valores obtenidos para las estadísticas índices de eficiencia y coeficiente de correlación.
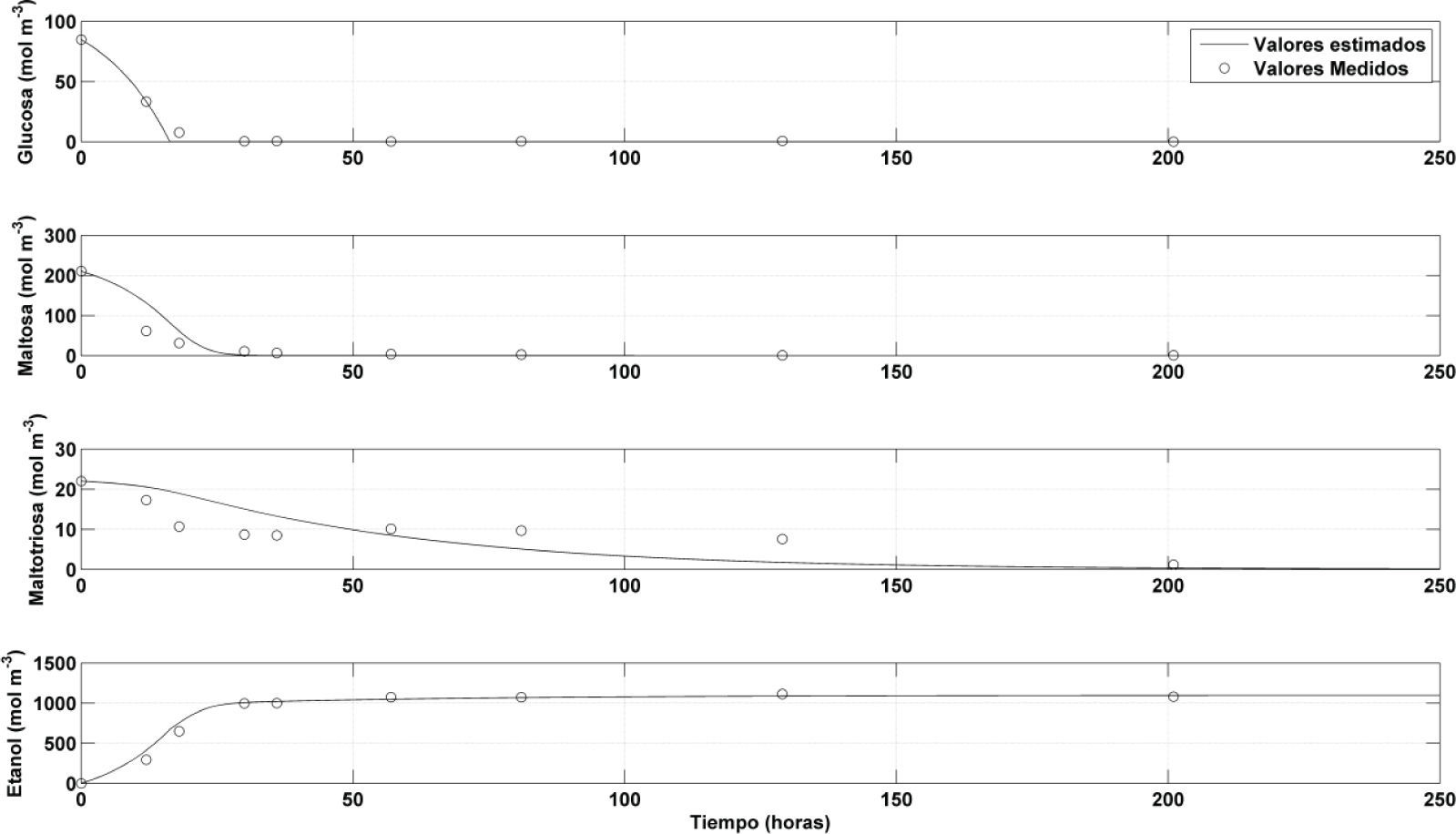
En la figura 6 se muestra la comparación entre los valores de las variables del modelo medidas y simuladas con respecto al tiempo de fermentación, en donde la simulación se realizó con los parámetros cinéticos estimados mediante el algoritmo de evolución diferencial para una temperatura de 21°C.
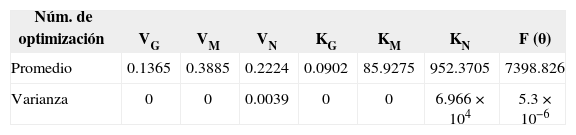
En la tabla 5 se muestran los valores estimados de los parámetros y de la función minimizada F(θ) de la ecuación 15 en cada una de las optimizaciones realizadas mediante evolución diferencial.
En la tabla 6 se encuentran las estadísticas de ajuste entre el modelo ya calibrado con evolución diferencial y los datos medidos para cada una de las variables de estado y la variable de salida.
El rango de la temperatura de fermentación dentro del cual se desarrolló el modelo de Gee y Ramirez (1988) tiene una variación importante con respecto al rango de temperatura de fermentación de cerveza artesanal; en consecuencia, cuando se realizaron las simulaciones previas utilizando los valores de los parámetros correspondientes a una temperatura de 16°C, se esperaba encontrar una diferencia significativa entre los valores simulados y los valores medidos de las concentraciones de las variables de estado del modelo (figura 6), de esta manera surgió la necesidad de realizar una estimación de los parámetros del modelo. En las figuras 5 y 6 puede observarse que la calibración del modelo en general es aceptable debido a que los resultados fueron similares usando un algoritmo de optimización local y un método de optimización global (rutinas lsqnonlin y evolución diferencial), ya que en los dos casos al comparar las simulaciones con las mediciones de las variables, puede observarse que se reproduce de manera general la tendencia de cada variable durante el proceso de fermentación.
En general, de acuerdo con las estadísticas de ajuste del modelo calibrado, en las tablas 4 y 6 se observa que es un buen predictor de la variable de estado glucosa, ya que en ambos casos de calibración se tiene un coeficiente de correlación (r) cercano a 1 y un sesgo cercano a cero, así como una alta eficiencia (EF).
De la misma forma, en las tablas 4 y 6, de acuerdo con el coeficiente de correlación (r) y la eficiencia (EF), el modelo es un buen predictor de la variable etanol, ya que ambos tienen un valor cercano a 1, sin embargo, también puede observarse que esta variable tiene valores relativamente grandes para el resto de las estadísticas (BIAS, MAE y MSE), lo cual es probable que se deba a la diferencia entre las concentraciones medidas y estimadas alrededor de las 35 y 50 h en el proceso de fermentación (figuras 5 y 6) que fueron posiblemente causadas por un error en la medición de la variable. Lo anterior se puede mejorar con un mayor número de mediciones de la variable etanol en el rango de tiempo mencionado, ya que es aquí donde el proceso de fermentación comenzó a estabilizarse. A pesar de que surgieron valores elevados en algunas estadísticas de ajuste para el etanol, debe tomarse en cuenta que las concentraciones de esta variable superan las 1 000 unidades, por lo que en forma porcentual el error es poco significativo.
Para el caso de la maltosa, el modelo calibrado por ambos métodos tiene estadísticas de ajuste aceptables, sin embargo, con el fin de obtener una mayor precisión en la predicción del modelo para esta variable, es necesario tomar un mayor número de mediciones entre las 10 y 25 h del tiempo de fermentación, ya que en este rango la concentración de maltotriosa presenta una mayor variación.
Al observar las tablas 4 y 6, puede decirse que el modelo calibrado por ambos métodos es un buen predictor de la variable de estado maltotriosa, debido a que tiene un coeficiente de correlación cercano a uno y un sesgo cercano a cero. Sin embargo, en este caso la EF presenta un valor aparentemente bajo, lo cual se debe a que las mediciones de maltotriosa son un poco irregulares entre las 20 y 40h del tiempo de fermentación. Lo anterior pudo haber sucedido, debido a que, a pesar de que la muestra se encontraba congelada, la fermentación siguió en una escala mucho más pequeña, sin embargo, esto se vio reflejado de forma más importante en la concentración de maltotriosa. Este mismo fenómeno fue observado por Gee y Ramirez (1988) para la variable maltosa.
ConclusionesEn la presente investigación se encontró que es posible estudiar el proceso de fermentación de cerveza artesanal usando modelos matemáticos dinámicos. Se mostró que se puede entender el comportamiento del proceso aplicando la metodología de modelado de sistemas. En particular, se encontró que un modelo matemático que simula la dinámica del proceso de fermentación de cerveza industrial, mediante las variables de estado concentración de glucosa, maltosa y maltotriosa, puede ser útil para predecir el comportamiento de las variables que influyen en el proceso de fermentación de cerveza artesanal, realizando previamente la estimación de los parámetros del modelo.
La metodología del análisis de sensibilidad local permitió determinar los parámetros que más influyen en el comportamiento del modelo, los cuales resultaron candidatos a ser estimados. Una vez calibrado el modelo matemático, puede utilizarse para el estudio de estrategias de manejo, que hagan más eficiente el proceso de fermentación de la cerveza artesanal. De la misma manera, dado que la concentración de etanol es una variable de gran importancia en la producción de cerveza, el modelo puede emplearse para controlar la cantidad de etanol final en el producto u optimizar el proceso de fermentación.
En esta investigación, se trabajó con una temperatura constante, por lo que el modelo se limita a simular el proceso de fermentación con esta condición, sin embargo, el trabajo realizado puede ser una referencia y base para futuras investigaciones, en las cuales se tomen en cuenta los efectos de la introducción de cambios en la temperatura ambiental.
Otro resultado obtenido, es la dinámica del comportamiento de cada una de las variables durante el tiempo de fermentación, la importancia de esto radica en el hecho de que en futuras investigaciones, se tendrá una referencia más exacta para determinar los tiempos y el número de mediciones en los intervalos donde suceden cambios significativos en el comportamiento de esas variables. Lo anterior incluye modelos más complejos que contengan un mayor número de variables de estado y modelos más simples como los de caja negra, ya que de igual manera, al conocer la dinámica del proceso de fermentación, también pueden elegirse de forma más eficiente los tiempos de muestreo en los cuales se realizará la medición de las variables.
Como comentario final, para trabajos posteriores es recomendable determinar la concentración de biomasa mediante el peso seco de las levaduras, para obtener directamente las unidades en masa por unidad de volumen.
Citación estilo Chicago Garduño-García, Angel, Irineo Lorenzo López-Cruz, Salvador Matínez-Romero, Agustín Ruíz-García. Simulación del proceso de fermentación de cerveza artesanal. Ingeniería Investigación y Tecnología, XV, 02 (2014): 221–232.
Citación estilo ISO 690 Garduño-García A., López-Cruz I.L., Matínez-Romero S., Ruíz-García A. Simulación del proceso de fermentación de cerveza artesanal. Ingeniería Investigación y Tecnología, volumen XV (número 2), abril-junio 2014: 221–232.
Graduado de la carrera de ingeniería mecánica agrícola en la Universidad Autónoma Chapingo (UACh) en 2010. Realizó una estancia preprofesional en Espaúa en el mismo año en la Universidad de Almería con el grupo de investigación: Automática, Electrónica y Robótica, (AER, código TEP197 del Plan Andaluz de Investigación). En el 2012 culminó sus estudios de maestría en ingeniería agrícola y uso integral del agua con especialización en ingeniería de biosistemas en la UACh.
Culminó estudios de doctorado en ingeniería agrícola en la Universidad de Wageningen, Países Bajos en 2002. Es profesorinvestigador del posgrado en ingeniería agrícola y uso integral del agua en la Universidad Autónoma Chapingo. Pertenece al Sistema Nacional de Investigadores (nivel I). Ha publicado 47 artículos en revistas arbitradas o indizadas, 40 ponencias en extenso y 45 presentaciones en congresos nacionales e internacionales y 4 capítulos en libros. Ha impartido 49 cursos a nivel de posgrado. Ha dirigido una tesis de doctorado, 12 de maestría y 5 de licenciatura. Sus publicaciones tienen más de 50 citas.
Graduado de la maestría en ingeniería agrícola en la Universidad Autónoma Chapingo (UACh) en 2009. Realizó estudios de maestría en ciencias en control automático en el CINVESTAV del Instituto Politécnico Nacional en 2006. Actualmente es estudiante de doctorado en ingeniería agrícola en la UACh. Sus líneas de investigación se enfocan al estudio de la dinámica de variables ambientales de invernaderos para fines de optimización y control.
Egresado de la Escuela Nacional de Ciencias Biológicas del Instituto Politécnico Nacional en el año de 1969, obtuvo el título de químico bacteriólogo parasitólogo. En el 2002 obtuvo el título de maestro en ciencias de la educación en la Universidad del Valle de México campus San Miguel. Ha dirigido y asesorado más de 50 tesis de licenciatura y una de maestría. Ha participado en varios congresos en el área de alimentos y fermentaciones. Actualmente es profesorinvestigador del Departamento de Ingeniería Agroindustrial de la Universidad Autónoma Chapingo, en donde ha impartido más de 60 cursos.