El objetivo principal del estudio fue determinar la prevalencia actual de insuficiencia renal crónica (IRC) en pacientes ambulatorios con diabetes mellitus tipo 2 (DM2), en seguimiento en los servicios de Endocrinología a nivel nacional.
Pacientes y métodoEstudio con diseño observacional, transversal, multicéntrico y con recogida de datos retrospectiva. De cada participante se registraron datos demográficos y antropométricos, de función renal, de la diabetes, de factores de riesgo cardiovascular, comorbilidades y tratamientos. La presencia de IRC fue definida con un filtrado glomerular inferior a 60ml/min/1,73m2, y se utilizó el método Modification in Diet of Renal Disease abreviado.
ResultadosSe incluyeron 541 pacientes con DM2 de ambos sexos (el 53% eran varones), con una edad media (DE) de 63 años (7,9) y una hemoglobina glucosilada media del 7,6% (1,3). La prevalencia (intervalo de confianza [IC] del 95%) de IRC fue del 22,9% (IC del 95%: 19,4–26,7), superior a la estimada previamente, que fue del 5,7% (IC del 95%: 3,9–8,0) (p<0,0001). Como factores de riesgo de tener IRC se identificaron la edad (odds ratio [OR]: 2,07 [IC del 95%: 1,47–2,91] por cada 10 años de aumento), el sexo femenino (OR: 2,25 [IC del 95%: 1,36–3,71]) y la hiperuricemia (OR: 3,15 [IC del 95%: 1,56–6,37]). No hubo diferencias en el control metabólico entre los pacientes con IRC frente a sin IRC objetiva.
ConclusiónUn 22,9% de los pacientes con DM2 seguidos de manera ambulatoria por endocrinólogos presenta IRC y de esta población sólo está diagnosticada una cuarta parte. La determinación automatizada del aclaramiento de creatinina podría incrementar el porcentaje de diagnóstico y facilitar un mejor control metabólico en estos pacientes.
The aim of this study was to estimate the current prevalence of Chronic Renal Insufficiency (RI) in ambulatory patients with type 2 Diabetes (T2DM) assisted in Endocrinology Departments all over Spain.
Patients and methodsThis was an observational, cross sectional, multicenter study. From each participant the following data were retrospective collected: demographic, anthropometric, renal function, diabetes, cardiovascular risk factors, comorbidities and treatment. RI was defined by a glomerular filtration rate lower than 60ml/min/1.73m2, using the shortened MDRD method.
Results541 patients with T2DM were included, 53% were men, the mean age (DS) was 63 years old (7.9) and the HbA1c was 7.6 % (1.3). The prevalence (CI95%) of RI was 22.9% (19.4–26.7), higher than the previous estimate, witch was 5,7% (3.9–8.0, p<0,0001). The associated risk factor for RI were age (OR 2.07; 95%CI: 1.47–2.91 per each ten year period of increase), female gender (OR 2.25; 95%CI: 1.36–3.71) and hyperuricemia (OR 3.15; 95% CI: 1.56–6.37). There were no differences in the metabolic control between patients with RI vs those without RI.
Conclusions22.9% of T2DM ambulatory patients followed by endocrinologist had RI, but just a quarter of them had previously been diagnosed. The automated determination of creatinine clearance could increase the proportion of diagnosis and facilitate the improvement of the metabolic control in these patients.
La nefropatía diabética (ND) es una enfermedad crónica y progresiva que se asocia a una elevada tasa de morbimortalidad de origen cardiovascular. En los pacientes con diabetes mellitus tipo 2 (DM2), un porcentaje significativo de los pacientes con ND progresan hasta la insuficiencia renal (IR)1.
En la práctica clínica, la excreción urinaria de albúmina y el cálculo del aclaramiento de creatinina son las determinaciones analíticas básicas en el seguimiento de la ND. La detección precoz de descensos significativos del filtrado glomerular (FG) es relevante clínicamente, ya que obliga a intensificar el control metabólico y el de los factores de riesgo2–4 para frenar, o al menos enlentecer, la progresión de la enfermedad. Además, condiciona la selección del tratamiento farmacológico, en especial el tratamiento hipoglucemiante, y obliga también a considerar posibles interacciones farmacológicas con efecto deletéreo sobre la función renal.
En nuestro país, la mayoría de los estudios epidemiológicos que han estudiado la prevalencia de nefropatía, en fases iniciales, tienen un carácter local5,6 o están basados en la excreción urinaria de albúmina7. Otros estudios han valorado la prevalencia de diabetes en pacientes que entran en programas de tratamiento renal sustitutivo. Pero hay pocos estudios de pacientes en fases intermedias de la enfermedad8,9 y ninguno en el que se valore la prevalencia de IR junto al porcentaje de diagnóstico previo y las implicaciones clínicas que de esto se derivan en la población con DM2.
El objetivo del presente estudio fue estimar la prevalencia de IR en pacientes con DM2 atendidos en consultas externas de servicios o unidades hospitalarias de Endocrinología a nivel nacional, y utilizar un criterio objetivo de evaluación de la función renal, como la estimación del FG (eFG) inferior a 60ml/min/1,73m210,11 mediante la Modification in Diet of Renal Disease (MDRD, ‘modificación de la dieta en la enfermedad renal’) abreviada12. Los objetivos secundarios fueron identificar los posibles factores asociados a la IR objetiva, comparar el porcentaje de IR objetiva con el de la previamente diagnosticada y comparar el control metabólico y el tratamiento de la DM2 en pacientes con y sin IR objetiva.
Pacientes y métodoDiseño del estudioSe llevó a cabo un estudio observacional, de corte transversal, multicéntrico, con recogida de datos retrospectiva, y se invitó a 50 endocrinólogos de todo el ámbito nacional a participar en éste como investigadores. Los investigadores interesados se inscribieron en una dirección web preparada para tal efecto. Tras el proceso de inscripción, en el que se registraron los datos sociodemográficos y de las tareas clínicas habituales del investigador (edad, sexo, años de praxis, entorno asistencial y número de pacientes diabéticos atendidos por día), éste recibía un código de usuario y clave de acceso únicos que le permitían acceder a una aplicación web para registrar los datos requeridos de los pacientes seleccionados. Para evitar posibles sesgos de selección, cada investigador debía seleccionar los últimos 12 pacientes con DM2, que cumplieran los criterios de selección (véase Participantes), que hubiera visitado en su consulta a partir del momento en que se incorporaba al estudio. Los datos de los pacientes se obtuvieron por revisión de la historia clínica y se utilizaron siempre los más recientes que estuvieran disponibles. No se realizó ningún tipo de seguimiento prospectivo de los pacientes. El estudio fue monitorizado on-line para asegurar la correcta selección de los pacientes y el registro de los datos solicitados.
ParticipantesSe seleccionaron pacientes atendidos en consultas de Endocrinología, de 45 a 75 años de edad, con diagnóstico clínico de DM2 establecido después de los 30 años, que no hubieran precisado insulina en los 2 primeros años del diagnóstico de la diabetes, con una duración de la diabetes superior a los 2 años, y con disponibilidad de los parámetros analíticos requeridos en su historia clínica. Dado que todos los datos de los pacientes debían obtenerse por revisión de la historia clínica, no se consideró necesaria la revisión del protocolo por parte de un comité de ensayos clínicos. No obstante, este estudio se diseñó y se completó siguiendo las normas de buena práctica clínica. Aun así, se tuvieron en cuenta en todo momento todos los postulados éticos orientados a garantizar la salvaguarda escrupulosa de los derechos del paciente, incluyendo la no interferencia con los hábitos de prescripción del médico y la preservación de la confidencialidad de los datos del paciente. La Sociedad Española de Diabetes avaló este estudio.
Variables registradasPara evaluar el objetivo principal se registró la última creatinina sérica, la edad, el sexo y la raza. Posteriormente, se calculó el FG mediante la fórmula de la MDRD abreviada de Levey et al11, y se consideró IR objetiva si la eFG era inferior a 60ml/min/1,73m210,11. Para los objetivos secundarios se registraron adicionalmente el peso; la talla; la existencia de un diagnóstico clínico previo de IR (criterio subjetivo del médico); la última hemoglobina glucosilada (HbA1c) como medida del control metabólico de la DM (se consideró buen control metabólico si la HbA1c era inferior al 7%4); la hipertensión arterial (HTA), definida como cifras de presión arterial (PA) superior a 130u 80mmHg comprobadas o en tratamiento antihipertensivo; las últimas PA sistólicas (PAS) y PA diastólicas (PAD) para evaluar el control de la PA actual (PAS/PAD menores o iguales a 130/80mmHg), la dislipidemia, definida como colesterol unido a lipoproteínas de baja densidad superior a 100mg/dl o colesterol unido a lipoproteínas de alta densidad inferior a 40mg/dl en varones e inferior a 48mg/dl en mujeres o tratamiento hipolipemiante, las comorbilidades de especial interés, como la insuficiencia cardíaca, la anemia (hemoglobina inferior a 12g/dl)5 y la hiperuricemia (ácido úrico superior a 7mg/dl)5, el tabaquismo, los tratamientos farmacológicos actuales, si se realizaba seguimiento por un nefrólogo, así como la procedencia (España o fuera de España) y el nivel de estudios finalizados (ninguno, primarios, secundarios o universitarios).
A partir de los tratamientos farmacológicos se identificaron las posibles asociaciones medicamentosas con efectos potenciales sobre la función renal (riesgo de nefrotoxicidad u otros tipos de afectación renal) según el British National Formulary (BNF, ‘formulario nacional británico’)13.
Análisis estadísticoEl tamaño muestral se determinó para poder estimar la prevalencia de IR con una imprecisión máxima del 8% (±4%). El protocolo del estudio previó realizar el análisis con todos los pacientes que cumplieran con los criterios de selección y tuvieran la información necesaria para evaluar el objetivo principal. En ningún caso se utilizaron estrategias de imputación de datos ausentes y todos los análisis realizados se basaron en los datos disponibles.
La estimación de la prevalencia de la IR se realizó calculando el intervalo de confianza (IC) del 95% mediante la aproximación normal. La identificación de factores asociados a la IR objetiva se realizó mediante modelos de regresión logística, y se consideraron inicialmente los siguientes factores: edad, sexo, procedencia, nivel de estudios finalizados, índice de masa corporal (IMC), seguimiento por un nefrólogo, tabaquismo, HTA, dislipidemia, buen control metabólico de la DM2, buen control de la PA, insuficiencia cardíaca, anemia, hiperuricemia e interacciones medicamentosas con algún efecto sobre la función renal según el BNF13.
La comparación de la IR objetiva con el establecimiento del diagnóstico clínico de IR (IR subjetiva) se realizó mediante la prueba de McNemar. La diferencia constatada entre el criterio objetivo y subjetivo (véase Resultados) motivó un análisis de regresión logística, no previsto inicialmente, para identificar factores determinantes del establecimiento del diagnóstico de IR en los pacientes con IR objetiva, y considerar factores del médico (edad, sexo y número de pacientes visitados al día) o del paciente (edad, sexo, IMC, perímetro de cintura, nivel de estudios, tabaquismo, HTA, dislipidemia e hiperuricemia).
Asimismo, los resultados descriptivos de control metabólico y de tratamiento de la DM2 motivaron 2 análisis inferenciales no previstos inicialmente, como el estudio de la relación entre la IR objetiva y el uso de metformina (mediante regresión logística), y la relación entre el control metabólico y la función renal (eFG inferior a 30, entre 30 y 60 o más de 60ml/min/1,73m2), que se evaluó mediante una prueba de tendencia de Cochrane-Armitage. En todos los análisis se utilizó un nivel de significación bilateral del 5%. No se realizaron análisis intermedios. Todos los análisis se realizaron mediante el paquete estadístico SAS® para Windows versión 9.1.
ResultadosCaracterísticas de los pacientesDurante los meses de mayo a julio de 2008, 49 médicos reclutaron un total de 543 pacientes, de los que 2 se consideraron inválidos a causa de incumplir algún criterio de selección y se retiraron del análisis. Todos los análisis se realizaron a partir de los 541 pacientes considerados válidos (99,6%).
Las características de la muestra estudiada se describen en la tabla 1. La edad media (DE) fue de 63 años (7,9), 290 pacientes (53,6%) fueron varones, 12 pacientes (2,2%) habían nacido fuera de España y 338 pacientes (62,4%) no habían completado los estudios primarios. Un 13,4% eran fumadores activos. Entre los datos clínicos más relevantes destacaron los valores de HbA1c, con una media del 7,6% (1,3), la PAS media de 139 (18)mmHg y la PAD media de 77 (10)mmHg.
Datos de los pacientes
| Panel | Ítem | Valores | Casos válidos (n=541) |
| Datos antropométricos | Edad (años) | Media (DE) | 63,0 (7,9) |
| Sexo (varones) | n (%) | 290 (53,6) | |
| Raza (caucásica) | n (%) | 540 (99,8) | |
| IMC (kg/m2) | Media (DE) | 30,2 (5,2) | |
| Perímetro de cintura (cm) | Media (DE) | 100,1 (13,6) | |
| Nacido fuera de España (sí) | n (%) | 521 (96,3) | |
| Nivel de estudios finalizado (primaria) | n (%) | 237 (43,8) | |
| Seguimiento por nefrólogo (sí) | n (%) | 48 (8,8) | |
| Función renal | Creatinina sérica (mg/dl) | Media (DE) | 1,0 (0,4) |
| Albúmina en orina (mg/dl) | Media (DE) | 75,5 (338,8) | |
| Cociente de albúmina/creatinina en orina (muestra matutina) | Media (DE) | 72,7 (292,3) | |
| eFG¿ ml/min/1,73m2 | Media (DE) | 78,1 (25,7) | |
| IR objetiva¿ | n (%) | 124 (22,9) | |
| IR según criterio del investigador | n (%) | 31 (5,7) | |
| Medición de la glucosa | Glucemia basal (mg/dl) | Media (DE) | 153,3 (48,9) |
| HbA1c (%) | Media (DE) | 7,5 (1,3) | |
| Buen control metabólico de DM¿ | n (%) | 197 (36,4) | |
| Tiempo medio de evolución de la DM | Media (DE) | 12,5 (7,3) | |
| Factores de riesgo cardiovascular | HTA¿ | n (%) | 392 (72,4) |
| PAS (mmHg) | Media (DE) | 139,0 (18,3) | |
| PAD (mmHg) | Media (DE) | 77,6 (10,3) | |
| Buen control de la PA (130/80 mmHg) | n (%) | 201 (37,1) | |
| Frecuencia cardíaca (ppm) | Media (DE) | 75,9 (9,8) | |
| Dislipidemia¿ | n (%) | 391 (72,2) | |
| Tabaquismo (fumador actual) | n (%) | 73 (13,4) | |
| Enolismo actual (habitual) | n (%) | 23 (69,3) | |
| Comorbilidades | Insuficiencia cardíaca | n (%) | 27 (4,9) |
| Anemia¿ | n (%) | 33 (6,0) | |
| Hiperuricemia¿ | n (%) | 59 (10,9) |
DE: desviación estándar; DM: diabetes mellitus; eFG: filtrado glomerular estimado; FG: filtrado glomerular; HbA1c: hemoglobina glucosilada; HTA: hipertensión arterial; IMC: índice de masa corporal; IR: insuficiencia renal; PA: presión arterial; PAD: presión arterial diastólica; PAS: presión arterial sistólica.
Se diagnosticaron un total de 124 pacientes con IR objetiva (eFG inferior a 60ml/min/1,73m2), lo que corresponde a una prevalencia del 22,9% (IC del 95%: 19,4–26,7).
En el estudio de las interacciones farmacológicas con potencial afectación de la función renal según el BNF (6) se detectaron un total de 22 interacciones en 14 de los 535 pacientes tratados que recibían al menos 2 fármacos simultáneamente, lo que representa una prevalencia del 2,6% (IC del 95%: 1,6–4,3). En todos los casos, estas interacciones involucraban un antiinflamatorio no esteroideo (AINE) asociado a un inhibidor de la enzima conversiva de la angiotensina (4 pacientes), a un antagonista de los receptores de la angiotensina II (9 pacientes) o a un diurético (9 pacientes). En los 2 primeros casos (AINE+enzima conversiva de la angiotensina, AINE+antagonista de los receptores de la angiotensina II), el BNF describe la consecuencia de la interacción como «antagonismo del efecto hipotensor y aumento del riesgo de empeoramiento renal» y, en el último, (AINE+diurético) como «riesgo de nefrotoxicidad de AINE aumentado y antagonismo del efecto diurético».
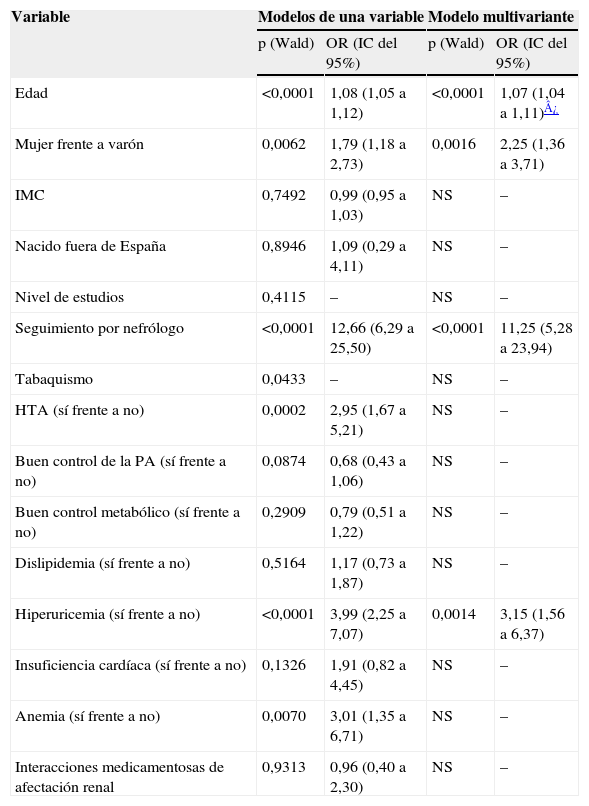
Los resultados de la regresión logística utilizada para intentar identificar factores asociados a la IR objetiva se muestran en la tabla 2. Los modelos de una sola variable mostraron una asociación estadísticamente significativa entre la IR objetiva y la edad, el sexo, el tabaquismo, la HTA, el buen control de la PA, la anemia y la hiperuricemia. Sin embargo, en el análisis multivariante, solamente la edad, el sexo, el seguimiento por un nefrólogo y la hiperuricemia se mantuvieron significativamente asociados a la IR objetiva. La asociación entre estos factores y la IR objetiva, medida mediante la odds ratio (OR), fue muy similar en los modelos univariantes y en el modelo multivariante, con la única excepción de la edad.
Regresión logística de insuficiencia renal objetiva (filtrado glomerular estimado inferior a 60ml/min/1,73m2)
| Variable | Modelos de una variable | Modelo multivariante | ||
| p (Wald) | OR (IC del 95%) | p (Wald) | OR (IC del 95%) | |
| Edad | <0,0001 | 1,08 (1,05 a 1,12) | <0,0001 | 1,07 (1,04 a 1,11)¿ |
| Mujer frente a varón | 0,0062 | 1,79 (1,18 a 2,73) | 0,0016 | 2,25 (1,36 a 3,71) |
| IMC | 0,7492 | 0,99 (0,95 a 1,03) | NS | – |
| Nacido fuera de España | 0,8946 | 1,09 (0,29 a 4,11) | NS | – |
| Nivel de estudios | 0,4115 | – | NS | – |
| Seguimiento por nefrólogo | <0,0001 | 12,66 (6,29 a 25,50) | <0,0001 | 11,25 (5,28 a 23,94) |
| Tabaquismo | 0,0433 | – | NS | – |
| HTA (sí frente a no) | 0,0002 | 2,95 (1,67 a 5,21) | NS | – |
| Buen control de la PA (sí frente a no) | 0,0874 | 0,68 (0,43 a 1,06) | NS | – |
| Buen control metabólico (sí frente a no) | 0,2909 | 0,79 (0,51 a 1,22) | NS | – |
| Dislipidemia (sí frente a no) | 0,5164 | 1,17 (0,73 a 1,87) | NS | – |
| Hiperuricemia (sí frente a no) | <0,0001 | 3,99 (2,25 a 7,07) | 0,0014 | 3,15 (1,56 a 6,37) |
| Insuficiencia cardíaca (sí frente a no) | 0,1326 | 1,91 (0,82 a 4,45) | NS | – |
| Anemia (sí frente a no) | 0,0070 | 3,01 (1,35 a 6,71) | NS | – |
| Interacciones medicamentosas de afectación renal | 0,9313 | 0,96 (0,40 a 2,30) | NS | – |
eFG: filtrado glomerular estimado; HTA: hipertensión arterial; IC: intervalo de confianza; IMC: índice de masa corporal; NS: no significativa; OR: odds ratio; PA: presión arterial.
El diagnóstico clínico de IR, según el criterio subjetivo del médico, se estableció en 31 pacientes, lo que corresponde a una prevalencia del 5,7% (IC del 95%: 3,9–8,0). Esta prevalencia fue muy inferior a la prevalencia estimada al utilizar el criterio objetivo de IR. La diferencia entre ambas prevalencias, IR objetiva y subjetiva, fue estadísticamente significativa (ji al cuadrado de McNemar=91,042; grados de libertad [GDL]=1; p<0,0001).
Cuando se intentó identificar los factores de los que podía depender que se estableciera el diagnóstico clínico de IR en los 124 pacientes que presentaban IR objetiva no se detectó ninguna relación con el género del médico encargado ni con su carga asistencial. Sin embargo, sí pudo constatarse una asociación marginal, aunque no significativa, con la edad del médico (p=0,0716), con una OR correspondiente a un incremento de 10 años de 0,58 (IC del 95%: 0,32–1,05). Esta relación podría indicar una posible reducción en la probabilidad de establecer el diagnóstico a mayor edad del médico.
La única característica del paciente que se asoció al establecimiento del diagnóstico clínico de IR fue la hiperuricemia (p=0,0002), con una OR de 7,31 (IC del 95%: 2,55–20,97). Ninguna de las restantes características del paciente consideradas, como edad, sexo, IMC, perímetro de cintura, nivel de estudios, tabaquismo, HTA o dislipidemia, se asoció significativamente al establecimiento del diagnóstico de IR.
Relación entre la insuficiencia renal objetiva y el control metabólico y tratamiento de la diabetes mellitusEl buen control metabólico (HbA1c inferior al 7%) fue ligeramente menos frecuente en los pacientes con IR objetiva (31,4%) que en los pacientes sin IR objetiva (37,9%), pero esta diferencia no alcanzó la significación estadística (ji al cuadrado=1,711; GDL=1; p=0,1909). Tampoco hubo diferencias significativas entre las medias de la HbA1c entre pacientes con y sin IR objetiva (test de la t de Student=−0,49; GDL = 539; p = 0,6256).
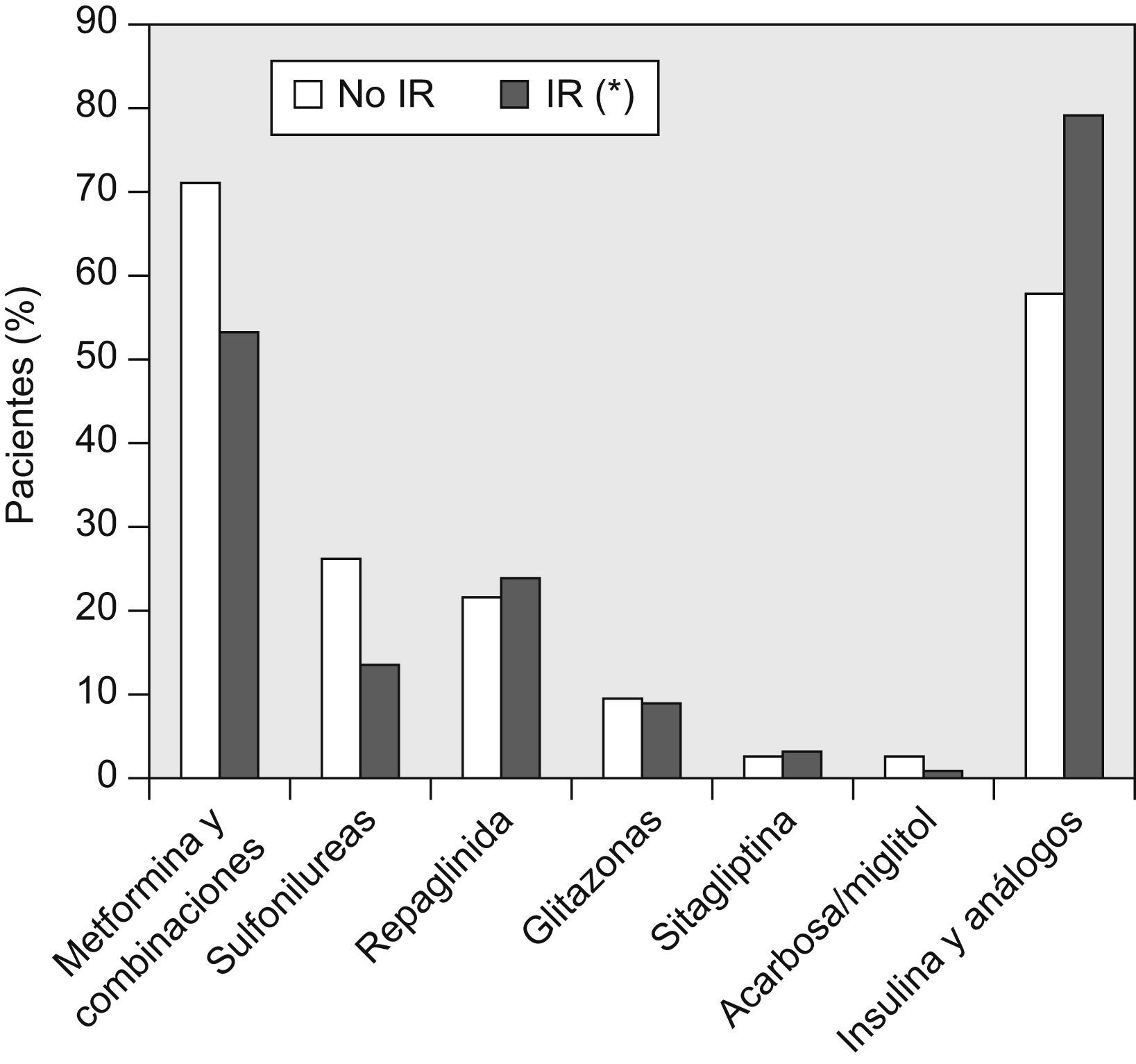
La figura 1 muestra los tratamientos hipoglucemiantes utilizados en pacientes con y sin IR objetiva. El tratamiento con metformina, sola o en asociación, fue más frecuente en pacientes con valores elevados de eFG (p<0,0001) con una OR de 1,16 (IC de 95%: 1,08–1,25), correspondiente a un aumento de 10 unidades en el valor de eFG (ml/min/1,73m2). Asimismo, se constató un aumento en la frecuencia de tratamiento con insulina a medida que aumenta la afectación renal, que es del 44,6% en pacientes con eFG superior a 60ml/min/1,73m2, del 56,5% en pacientes con eFG entre 30 y 60ml/min/1,73m2 y del 88,9% en pacientes con eFG inferior a 30ml/min (p=0,0014 en la prueba de Cochrane-Armitage).
Solamente 3 de los 9 pacientes que presentaron un eFG inferior a 30ml/min/m2 se trataron con un antidiabético oral (glibenclamida, pioglitazona o repaglinida).
DiscusiónLos principales hallazgos de este trabajo son que la prevalencia de IR es del 22,9% (IC del 95%: 19,4–26,7), aproximadamente 4 veces superior a la previamente diagnosticada (5,7% [IC del 95%: 3,9–8,0]). A pesar de que la IR se infradiagnosticó, el grado de control metabólico entre la población con IR frente a sin IR fue similar, el porcentaje de interacciones farmacológicas de potencial afectación sobre la función renal fue pequeño y el tratamiento hipoglucemiante fue adecuado al estatus renal. Los factores asociados a la presencia de IR fueron la edad, el sexo, el seguimiento por un nefrólogo y la hiperuricemia.
La prevalencia de IR en nuestra serie es concordante con lo anteriormente descrito en otros países europeos14. Sin embargo, 2 estudios con 2.59815 y con 934 pacientes16 realizados en nuestro país con una metodología similar muestran una prevalencia de IR más elevada, el 51,8 y el 42%, respectivamente. Una posible explicación a esta diferencia podría ser que se trata de poblaciones de pacientes con diferente tiempo de evolución, dado que la duración de la enfermedad es un factor determinante en la prevalencia de la ND. Desafortunadamente, este dato no figura en los trabajos mencionados.
No conocemos ningún trabajo en nuestro país que haya descrito la prevalencia de IR no diagnosticada en la población con DM2. Sin embargo, un estudio con una muestra de 1.059 pacientes con diferentes factores de riesgo mostró un resultado muy similar al nuestro (el 17,2 frente al 17,8% en el presente estudio)17. Todo esto indica que el infradiagnóstico de la IR es una situación desafortunadamente frecuente, incluso en pacientes con factores de riesgo para IR.
Las razones de este infradiagnóstico pueden ser diversas. De una parte, la recogida de orina durante 24 h es una tarea difícil para muchos pacientes. Por otro lado, la solución alternativa, como es el cálculo del aclaramiento sobre la base de la MDRD, con frecuencia no se lleva a cabo por el poco tiempo que con frecuencia dispone el clínico. Una solución ya adoptada en algunos hospitales es que el cálculo del aclaramiento se haga de manera automatizada y sistemática sobre la base de la creatinina plasmática y de los datos que previamente el clínico les ha proporcionado en la hoja de petición de análisis.
La ausencia de una diferencia significativa en el grado de control metabólico entre la población con IR frente a sin IR puede ser una de las consecuencias de la no identificación de la IR. Numerosos estudios2–4 han demostrado que la detención en la progresión de la nefropatía pasa por la intensificación en el registro del control glucémico y de los factores de riesgo. Esto tiene especial trascendencia entre aquellos que progresan a IR. Lógicamente, el primer paso para la prevención secundaria es la identificación de los pacientes que presentan disminución en su aclaramiento de creatinina.
Nuestra interpretación de que el porcentaje de utilización de insulina y de metformina fuese concordante con la función renal, a pesar de que había un porcentaje significativo de IR «oculta», puede deberse a que en la mayoría de los casos la decisión de insulinizar se tomó más en función del control metabólico que del status renal. No hay que olvidar que tanto el fracaso de la célula β como la progresión de las complicaciones microvasculares suelen ir paralelas y están relacionadas con la duración de la enfermedad.
Pese al infradiagnóstico de IR, se constata que la prevalencia de interacciones medicamentosas con algún grado de afectación renal fue pequeña y no pudo en ningún caso asociarse al diagnóstico de IR. Los pacientes del estudio son pacientes que presentan una DM2 avanzada y por definición están en riesgo de presentar daño renal. Nuestra interpretación de la ausencia de asociación entre diagnóstico objetivo de IR y presencia de interacciones lesivas a nivel renal pasaría porque existió una tendencia a la evitación, ya no sólo de asociaciones medicamentosas potencialmente peligrosas, sino, más específicamente, de fármacos o grupos de fármacos que por sí solos afectan la función renal. Más específicamente, son bien conocidos los efectos que a este nivel producen los AINE, y observamos que en todos los casos de interacciones lesivas a nivel renal detectados en el estudio estaba involucrado un AINE. Más aún, en todos los casos en los que un paciente tenía prescrito un AINE se registró interacción «de riesgo». Nuestra hipótesis a este respecto pasa, por tanto, porque el uso de AINE en la población del estudio se redujo, quizás como una medida preventiva dirigida para evitar la inducción de lesiones renales, lo que contribuyó a no hallar asociación entre diagnóstico objetivo de IR y presencia de interacciones con afectación renal. Los factores de riesgo asociados a la IR en nuestro trabajo son similares a los previamente descritos1. En relación con los factores que se asocian al diagnóstico de IR, queremos señalar que solo se identificó la hiperuricemia como factor relacionado con la probabilidad de realizar el diagnóstico de IR. Este hecho refuerza la idea de que la determinación automatizada del aclaramiento favorecería el diagnóstico de IR en fases más precoces.
El presente estudio tiene diversas limitaciones que se deben especificar. Primero, existe la limitación inherente a los estudios de corte. Segundo, la selección de los médicos investigadores no se hizo de manera aleatorizada, sino que realizaron el estudio aquellos que aceptaron participar. Esta circunstancia podría haber introducido un cierto sesgo, ya que los médicos que participan en los estudios epidemiológicos suelen tener una mayor motivación profesional, con lo que es posible que el porcentaje real de infradiagnóstico sea aún mayor al descrito en nuestro trabajo, si bien el hecho de que nuestro resultado es similar al de otro estudio en el que la selección de la muestra se hizo de manera aleatorizada indicaría que el sesgo es poco importante17. Tercero, a la hora de identificar factores del médico relacionados con el diagnóstico hay que tener en cuenta que en algunas circunstancias es posible que el seguimiento del paciente con DM2 no sea exclusivo del medico investigador, por lo que creemos que será necesario que se lleven a cabo investigaciones adicionales en este sentido.
En conclusión, este trabajo demuestra que casi una cuarta parte de los pacientes con DM2 seguidos de manera ambulatoria por especialistas de Endocrinología, presentan IR, aunque este diagnóstico era previamente conocido en tan sólo un 26% de los casos. La determinación sistemática del aclaramiento estimado de creatinina puede ser una buena herramienta para realizar un diagnóstico más precoz de la IR, lo que facilita un mayor control de los factores de riesgo y evita potenciales interacciones medicamentosas entre los fármacos prescritos.
Conflicto de interesesPedro Luis de Pablos Velasco y Francisco Javier Ampudia Blascono no tienen conflicto de intereses. Albert Cobos y Salvador Bergoñón trabajan en SAALIG CLINICAL, S. L., que fue la CRO que gestionó el estudio.
Laboratorios Menarini patrocinó el estudio.
A la Sociedad Española de Diabetes por conceder el aval científico y a laboratorios Menarini por financiar el proyecto.
CAP Montnegre, Barcelona: M Victoria Guasch; Centro Hospitalario de Jaén, Jaén: Alberto Moreno; Centro Médico de Asturias, Asturias: Soledad Paz García del Real; Complejo Asistencial Burgos, Burgos: Victor García-Hierro; Complejo Asistencial de Ávila, Ávila: Antonio López-Guzmán; Complejo Asistencial Zamora, Salamanca: Carmen Muñoz; Complexo Hospitalario Ourense, Ourense: Iria Pinal; Granada: María Jose Salas; Tarragona: José María Manzanares; Consultorio Monforte-Vaguada, Madrid: Luis Serrano; Hospital Arnau de Vilanova, Valencia: Juan Adrián Girbés; Hospital Cabueñes, Asturias: Emilio Suarez-Lledo; Hospital Clínic I Provincial, Barcelona: María Esther Batista; Hospital Clínico, Zaragoza: Fernando L. Calvo; Hospital Clínico, Valencia: Miguel Civera; Hospital de Cruces, Vizcaya: Ignacio Goicolea; Hospital de Mollet, Barcelona: Jesús Murillo; Hospital de Móstoles, Madrid: Mª Ángeles Tapia; Hospital de Navarra, Navarra: Javier Lafita; Hospital de Valme, Sevilla: Margarita Rivas; Hospital D’Igualada, Barcelona: Jesús Mayos; Hospital General de Ciudad Real, Ciudad Real: Miguel Aguirre; Hospital General Universitario de Alicante, Valencia: Paula Revert; Hospital Insular de Gran Canaria, Las Palmas: Antonio Ojeda; Hospital Juan Ramón Jiménez, Sevilla: Eloisa Roldán; Hospital Marina Baixa de Villajoyosa, Valencia: Rosa Casañ; Hospital Morales Messeguer, Murcia: Mª Soledad Alcaraz; Hospital Morales Messeguer, Murcia: Fátima Illan; Hospital Ramón y Cajal, Madrid: Francisco Álvarez; Hospital San Pedro de Alcántara, Badajoz: José Antonio Lucas; Hospital Sant Joan, Tarragona: Antoni Rabassa; Hospital Santa Teresa, A Coruña: Lazaro Bokser; Hospital Txagorritxu, Álava: Gonzalo Maldonado; Hospital Universitario de La Princesa, Madrid: José Alfonso Arranz;, Hospital Universitario Doctor Negrín, Las Palmas: Ignacio García; Hospital Universitario Doctor Negrín, Las Palmas: Pedro de Pablos; Hospital Universitario Doctor Peset, Valencia: Eva Solá; Hospital Universitario Doctor Peset, Valencia: Marcelino Gómez; Hospital Universitario Puerta de Hierro, Madrid: Miguel Brito; Hospital Universitario Puerto Real, Cádiz: María del Carmen Ayala; Hospital Universitario Reina Sofía, Córdoba: Rafael Palomares; Hospital Universitario Santa Cruz de Tenerife, Santa Cruz de Tenerife: Ángela Luisa Brito; Hospital Universitario Son Dureta, Baleares: Santiago Tofe; Hospital Universitario Virgen de La Victoria, Málaga: José Luis Pinzón; Hospital Universitario Virgen del Rocío, Sevilla: Miguel Ángel Mangas; Hospital Virgen de La Macarena, Sevilla: Cristina Hernández; Hospital Virgen de la Salud, Madrid: Mª Almudena Vicente; Hospital Xeral, A Coruña: Manuel Penin; Hospital Carlos Haya, Málaga: Juan Antonio García.