El síndrome de hipersensibilidad a anticonvulsivantes (SHA) es una entidad rara (incidencia aproximada entre 1/1.000 a 1/10.000 pacientes expuestos a anticonvulsivantes), pero potencialmente grave (tasa de mortalidad aproximada: 10%). Se presenta el caso de un paciente con epilepsia focal secundaria a leucoencefalopatía posradioterapia con varios episodios de exantema generalizado tras la introducción de tratamiento antiepiléptico. Tras varios episodios, el paciente es diagnosticado de síndrome de Drug Rash with Eosinophilia and Systemic Symptoms (DRESS), decidiéndose inicio de tratamiento con una benzodiacepina para control de las crisis hasta resolución del rash y eosinofilia.
El SHA debe sospecharse en todo paciente en tratamiento antiepiléptico que presente: fiebre, rash, linfadenopatías y aumento de transaminasas. Es importante el reconocimiento precoz con la retirada del fármaco antiepiléptico causante para evitar complicaciones y desenlaces fatales.
Anticonvulsant hypersensitivity syndrome (AHS) is a rare (incidence: 1 in 1,000 to 1 in 10,000 patients exposed to anticonvulsants), but potentially serious (approximate mortality rate: 10%) entity. We present the case of a patient diagnosed with left focal epilepsy due to post-radiotherapy leukoencephalopathy with several episodes of generalised rash after the introduction of antiepileptic treatment. After several episodes, the patient is diagnosed with Drug Rash with Eosinophilia and Systemic Symptoms (DRESS) syndrome. He was then treated with a benzodiazepine to control the seizures until resolution of rash and eosinophilia.
AHS should be suspected in all patients under antiepileptic treatment who present: fever, rash, lymphadenopathies and increased transaminases. In this situation, the drug should be suspended. Knowledge of this entity can avoid fatal outcomes.
El síndrome de hipersensibilidad a anticonvulsivantes (SHA) es un síndrome raro (incidencia aproximada entre 1/1.000 a 1/10.000 pacientes expuestos a anticonvulsivantes1), sin predilección por sexo o edad.
Los pacientes infectados con el virus de la inmunodeficiencia humana (VIH) y los pacientes oncológicos tienen un mayor riesgo de desarrollar esta reacción adversa medicamentosa.
Las manifestaciones clínicas, generalmente aparecen entre una y ocho semanas tras el inicio del tratamiento antiepiléptico. Sin embargo, en los casos de reexposición las manifestaciones clínicas pueden aparecer en horas o días.
La tasa de mortalidad aproximada es del 10%.
Es importante detectar de manera precoz esta entidad puesto que sus consecuencias pueden ser potencialmente graves. Se presenta el caso de un paciente con epilepsia focal secundaria a leucoencefalopatía posradioterapia con varios episodios de exantema generalizado tras la introducción de tratamiento antiepiléptico.
Caso clínicoVarón de 50 años diagnosticado de linfoma no-Hodgkin cerebral primario en 2006, y tratado mediante quimioterapia y radioterapia holocraneal, con desarrollo posterior de una leucoencefalopatía posradioterapia. En febrero de 2017 es diagnosticado de epilepsia focal frontotemporal izquierda sintomática, por lo que se inicia tratamiento antiepiléptico con levetiracetam. Tras 2 dosis de carga intravenosas de 1g, desarrolla fiebre y un exantema facio-tóraco-abdominal. En la analítica únicamente llama la atención la presencia de eosinofilia (12,6%). Se suspende levetiracetam y se instaura tratamiento con corticoides y antihistamínicos orales. Se decide entonces inicio de tratamiento con lacosamida vía oral a dosis de 100mg/12h. Tras unos meses, debido a la aparición de diplopía, se reduce la dosis a 50mg/12h.
Tras dicho cambio en la dosificación, en enero de 2018, el paciente acude a urgencias por nueva crisis comicial. Se suspende lacosamida y se inicia tratamiento con ácido valproico a dosis de 1.500mg/día. Tras 24h, presenta un rash generalizado, por lo que se suspende dicho fármaco y se reintroduce lacosamida.
Dos meses más tarde vuelve a presentar otra crisis epiléptica, decidiéndose en ese momento iniciar tratamiento con fenitoína (dosis de carga intravenosa de 1g, con dosis de mantenimiento vía oral de 250mg/24h). Pasados 4 días, presenta fiebre y un rash generalizado, en la analítica llama la atención la presencia de leucopenia y eosinofilia (las pruebas de función hepática no se encontraban alteradas). El paciente es tratado con dexclorfeniramina y metilprednisolona. Se suspende fenitoína, sustituyéndola por clobazam 10mg/12h.
Tras este último episodio, el servicio de alergología diagnostica al paciente de síndrome de DRESS y recomienda posponer la introducción de un nuevo antiepiléptico hasta resolución del rash y la eosinofilia.
La alta tasa de reactividad cruzada entre anticonvulsivantes, como se explicará más adelante, sugiere la existencia de relación entre todos los episodios que presentó este paciente.
DiscusiónEl SHA fue descrito por primera vez por Chaiken et al.2 en 1950.
Bocquet et al.3 utilizaron en 1996 el acrónimo DRESS (Drug Rash with Eosinophilia and Systemic Symptoms) para redefinir el término síndrome de hipersensibilidad a medicamentos.
Los fármacos más frecuentemente relacionados con el síndrome de DRESS son: antibióticos (41%), sobre todo derivados penicilínicos y sulfonamidas; AINE (11%) y anticonvulsivantes (10%).
Entre los anticonvulsivantes (tabla 1), los aromáticos son los más comúnmente involucrados en estas reacciones.
Clasificación de los anticonvulsivantes
| Aromáticos | 1.ª generación | Fenobarbital, fenitoína, etosuximida, primidona |
| 2.ª generación | Carbamazepina, oxcarbazepina, benzodiazepinas | |
| Nuevos aromáticos | Lamotrigina, topiramato, felbamato | |
| No aromáticos | Clásicos | Ácido valproico |
| Nuevos no-aromáticos | Gabapentina, vigabatrina |
La tasa de reactividad cruzada entre fármacos antiepilépticos es mayor del 75%4.
Es importante destacar que el desarrollo de este síndrome no está relacionado con la dosis de fármaco antiepiléptico (se trata de una reacción idiosincrásica).
El ácido valproico, en general, se considera una buena alternativa terapéutica en pacientes con SHA, aunque también existen algunos casos descritos en los que se relaciona con la producción de este síndrome5, como ocurrió en el caso del paciente descrito.
Características clínicas del síndrome de hipersensibilidad a anticonvulsivantesSe caracteriza principalmente por fiebre (presente entre el 90-100% de los pacientes), que suele ser el signo inicial y preceder en varios días a la erupción cutánea, linfadenopatías y compromiso de órganos internos.
La afectación cutánea se encuentra en aproximadamente el 90% de los casos. Habitualmente aparece como una erupción eritematosa, maculopapular confluente y pruriginosa que afecta la cara y el tronco para extenderse posteriormente a las extremidades. Aunque es poco habitual, las pústulas son una posible forma de manifestación, al igual que el síndrome de Stevens-Johnson (SSJ) y la necrólisis epidérmica tóxica (NET). En el 25% de los casos se observa edema facial y periorbitario, que puede llegar a ser muy deformante y ayuda a diferenciar este síndrome de las otras reacciones alérgicas medicamentosas en donde el edema respeta el rostro6.
Con relación al compromiso sistémico, el órgano interno más frecuentemente afectado es el hígado (50-60%). La afectación hepática puede ir desde elevaciones asintomáticas de las enzimas hepáticas hasta la necrosis hepática fulminante.
El siguiente órgano más comúnmente involucrado es el riñón (p. ej., nefritis intersticial, vasculitis).
Siguen al hígado y al riñón, en orden de frecuencia, las alteraciones a nivel del corazón, pulmón o sistema nervioso central. La afectación del tiroides puede aparecer como hipotiroidismo 3 meses después del inicio de la reacción, pero puede ser transitoria y la desaparición es esperable en la mayoría de los pacientes en un plazo de 12 a 18 meses.
Alteraciones analíticas del síndrome de hipersensibilidad a anticonvulsivantesSuele haber leucocitosis con eosinofilia y linfocitosis atípica. Otras anomalías descritas son: agranulocitosis, anemia aplásica, anemia hemolítica, trombocitopenia e hipogammaglobulinemia.
Criterios diagnósticos del síndrome de hipersensibilidad a anticonvulsivantesDeben estar presentes al menos 3 de los propuestos en 1996 por Bocquet et al. Actualmente existen métodos para calcular la probabilidad de manera online, empleando el denominado RegiSCAR score (tabla 2).
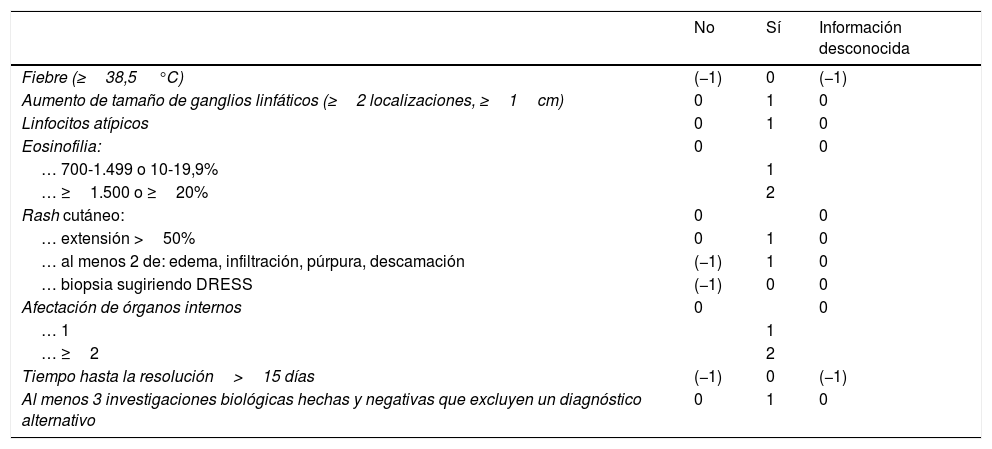
RegiSCAR score. Información y datos que valora para cálculo de la probabilidad de síndrome de DRESS
| No | Sí | Información desconocida | |
|---|---|---|---|
| Fiebre (≥38,5°C) | (−1) | 0 | (−1) |
| Aumento de tamaño de ganglios linfáticos (≥2 localizaciones, ≥1cm) | 0 | 1 | 0 |
| Linfocitos atípicos | 0 | 1 | 0 |
| Eosinofilia: | 0 | 0 | |
| … 700-1.499 o 10-19,9% | 1 | ||
| … ≥1.500 o ≥20% | 2 | ||
| Rash cutáneo: | 0 | 0 | |
| … extensión >50% | 0 | 1 | 0 |
| … al menos 2 de: edema, infiltración, púrpura, descamación | (−1) | 1 | 0 |
| … biopsia sugiriendo DRESS | (−1) | 0 | 0 |
| Afectación de órganos internos | 0 | 0 | |
| … 1 | 1 | ||
| … ≥2 | 2 | ||
| Tiempo hasta la resolución>15 días | (−1) | 0 | (−1) |
| Al menos 3 investigaciones biológicas hechas y negativas que excluyen un diagnóstico alternativo | 0 | 1 | 0 |
En función del resultado obtenido: <2 No DRESS; 2-3 posible; 4-5 probable; ≥6 definitivo.
Fuente: tabla extraída de: Roujeau JC et al.10.
Al aplicar este último método al paciente descrito se obtiene un total de 4 puntos, lo cual equivale a un probable síndrome de DRESS.
Etiopatogenia del síndrome de hipersensibilidad a anticonvulsivantesSe han postulado múltiples teorías para explicar esta reacción adversa medicamentosa. Algunas apuntan a mecanismos tóxicos de hipersensibilidad alérgica, así como a mecanismos relacionados con la inmunidad de tipo de injerto contra huésped. Sin embargo, ninguna de las teorías presentadas hasta la fecha ha sido completamente comprobada.
La mayoría de los casos de SHA se han asociado a fenitoína, fenobarbital y carbamazepina.
El SHA causado por los anticonvulsivantes aromáticos fenitoína, fenobarbital y carbamazepina muestra características comunes a los 3 fármacos implicados (tabla 3).
Características más comunes del SHA y tasa de incidencia
| Manifestaciones clínicas: |
| Fiebre (90-100%) |
| Erupción cutánea (90%) |
| Linfadenopatías (70%) |
| Hepatomegalia/hepatitis (50-60%) |
| Edema facial o periorbitario (25%) |
| Conjuntivitis/faringitis (10%) |
| Esplenomegalia |
| Resolución espontánea tras la interrupción del medicamento; reaparición con la reintroducción |
| Alteraciones analíticas: |
| Alteraciones hematológicas leucocitosis con eosinofilia (50%) |
| Puede haber alteración de las pruebas de función hepática |
Estos 3 fármacos siguen una ruta metabólica común: son metabolizados por el citocromo P-450. Los metabolitos intermedios de esta reacción se llaman «óxidos de areno» y son tóxicos. Normalmente son detoxificados por la enzima epóxido hidrolasa, por conjugación7. Una deficiencia hereditaria en la función de esta enzima podría predisponer a ciertos individuos a presentar un SHA.
ConclusionesExisten unos signos de alarma que pueden sugerir un SHA en pacientes en tratamiento con antiepilépticos: fiebre, aparición de rash, linfadenopatías y aumento de transaminasas. En estos casos debe suspenderse inmediatamente el fármaco.
En los pacientes con antecedente de SHA que precisan tratamiento antiepiléptico, se recomienda el uso de benzodiacepinas durante la fase aguda y, posteriormente (tras resolución de la posible alteración hepática) podría valorarse el empleo de ácido valproico.
Por el momento, no se han descrito casos de SHA con los antiepilépticos de comercialización más reciente (como gabapentina, vigabatrina, topiramato y tiagabina).
El conocimiento de esta entidad podría evitar desenlaces fatales.
Conflicto de interesesEl autor declara no tener ningún conflicto de intereses.