INTRODUCCIÓN. ANTECEDENTES HISTÓRICOS
El síndrome de piernas inquietas (SPI) o acromelalgia (sus siglas en inglés son RLS [restless legs syndrome]1) es un trastorno de tipo neurológico que afecta muy especialmente a la calidad del sueño. El SPI es conocido desde el siglo XVII, cuando Thomas Willis, famoso médico inglés, describió el primer caso. Sin embargo, la descripción de Willis quedó olvidada durante casi 300 años. A finales del siglo XIX, Wittmaak2 lo designó como anxietas tibianum. En 1945, el médico-neurólogo sueco Karl-Axel Ekbom3 publicó la descripción de una serie de casos, y acuñó el término restless legs con el que se conoce al síndrome, lo que ha motivado que este trastorno reciba también el nombre de síndrome de Ekbom. Otro médico sueco, Nils Brage Nordlander, contemporáneo de Ekbom, apreció la relación entre SPI y ferropenia, demostró que algunos pacientes podían mejorar de sus síntomas aportando hierro. Pero nuevamente el síndrome cayó en el olvido prácticamente hasta 1995, cuando el establecimiento de los criterios diagnósticos actuales y la posibilidad de un tratamiento eficaz con fármacos dopaminérgicos han provocado un resurgimiento del interés por este cuadro.
Definido en el Código CIE-10: G25.8 (otros trastornos extrapiramidales y del movimiento) y en la Publicación-catálogo de Enfermedades Raras4,5.
DEFINICIÓN
El SPI1,2,6-12 es un trastorno neurológico caracterizado por sensaciones desagradables de las piernas y un impulso incontrolable de moverse cuando se está descansando, en un esfuerzo para aliviar estas sensaciones. Las personas a menudo describen las sensaciones del SPI11 como quemantes, como si algo se les deslizara, o como si insectos treparan por el interior de sus piernas. Estas sensaciones2 llamadas parestesias o disestesias varían en gravedad de desagradable a irritantes, o dolorosas. Estos síntomas son acentuados por el hecho de acostarse y tratar de relajarse. Los síntomas predominan a últimas horas de la tarde y por la noche. Como consecuencia, la mayoría de los pacientes tiene dificultad para conciliar y mantener el sueño.
En los casos más graves los pacientes pueden experimentar discinesias13 cuando están despiertos, y algunos tienen síntomas en uno o ambos brazos y piernas. Un importante porcentaje de pacientes refieren perturbaciones del sueño7,14,15 como insomnio de conciliación e insomnio de mantenimiento y somnolencia diurna. Los pacientes aquejan un aumento de la latencia del sueño y una disminución de la eficacia del mismo con despertares frecuentes. Esto conlleva un agotamiento y una fatiga excesiva posteriores durante las horas del día.
Los pacientes en ocasiones describen los síntomas10,16 refiriendo sensaciones muy molestas de hormigueos, picor, ardor, dolor, burbujeo, sensación de que tiene gusanos en las piernas o de agua corriendo. Tales sensaciones desagradables les obligan a mover las piernas para aliviar temporalmente las molestias. Ese alivio se mantendrá mientras el paciente esté moviendo los pies, pero los síntomas reaparecen al volver a relajarse. Aparecen sólo en reposo, cuando están sentados o tumbados y no tiene relación con ninguna actividad ni situación previa.
Lo que define al síndrome es la sensación subjetiva de malestar. Alrededor de un 80% de los pacientes tiene asociado un trastorno de tipo motor.
En 1995, el Grupo Internacional de Estudio sobre el Síndrome de las Piernas Inquietas identificó los cuatro criterios básicos2,7,10-12,16-19 para diagnosticar el SPI (tabla 1). La presencia de estos criterios simultáneamente es suficiente para hacer el diagnóstico, apoyado quizás por la presencia de movimientos periódicos de piernas, además de si el trastorno responde a fármacos dopaminérgicos y si existe una historia familiar asociada.
Los movimientos periódicos de las piernas16 aparecen en un porcentaje muy alto en pacientes con SPI, las llamadas mioclonías nocturnas que se caracterizan por movimientos de flexión de las extremidades inferiores a la altura de la rodilla y el tobillo, con extensión del dedo grueso y relajación lenta. El movimiento tiene una duración de 0,5 a 5 segundos, apareciendo a intervalos de 20 a 40 segundos. Los movimientos son organizados, repetitivos. Aparecen predominantemente durante el sueño no REM (rapid eye movement) ligero y disminuyen durante el sueño no REM profundo. Desaparecen durante el sueño REM.
PREVALENCIA
El SPI es una patología extraordinariamente frecuente18,20. Varios estudios poblacionales realizados en Europa y EE.UU. encuentran cifras de prevalencia que normalmente oscilan entre el 5 y el 15%10,11,19-23 de la población. La frecuencia del SPI aumenta con la edad. Es más frecuente en mujeres con una relación 2:1 con respecto al varón. Sólo 1 de cada 4 pacientes que presenta SPI es bien diagnosticado por el clínico. El resto recibe diagnósticos diversos, como insuficiencia venosa periférica, polineuropatía, lumbalgia o radiculopatía lumbar, síndrome ansiosodepresivo, etc. En muchas de esas ocasiones suele pasar desapercibido o se confunde con otros diagnósticos6,24. Se presenta a cualquier edad.
En niños25 su diagnóstico puede ser difícil y diagnosticarse erróneamente de síndrome de hiperactividad26.
ETIOLOGÍA-FISIOPATOLOGÍA1,11,21
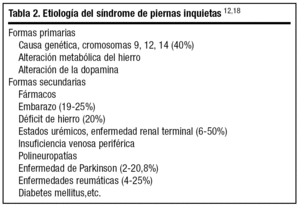
Es desconocida17,27. Se pueden distinguir formas idiopáticas23, sin identificar un trastorno subyacente, y formas sintomáticas, secundarias a otras patologías (una neuropatía incipiente, por ejemplo), lo que obligará a su estudio y tratamiento (tabla 2). En muchos casos es familiar, lo que sugiere un trasfondo genético con una herencia autosómica dominante28-30; entre un 30 y un 63% de las formas idiopáticas31,32 tienen antecedentes familiares. Además, el origen puede estar en el sistema nervioso central o en las vías periféricas. Habitualmente el SPI no se asocia a una causa clara. Sólo un pequeño porcentaje es secundario a otros trastornos como el déficit de hierro; la artritis reumatoide y la insuficiencia renal crónica presentan una asociación consistente con este síndrome. Determinados fármacos, como los antidepresivos tricíclicos (ATD) de todas las familias, los inhibidores de la recaptación de serotonina (ISRS), el litio o los fármacos antagonistas dopaminérgicos, pueden inducir o agravar el cuadro. La cafeína y los excitantes agravan los síntomas. El SPI afecta a las mujeres embarazadas33 en un porcentaje variable del 19%, desapareciendo en el puerperio. Se han identificado tres loci ligados a este síndrome18, situados en los cromosomas 12p, 14q y 9p, pero no se ha identificado ningún gen. El hierro34 es un componente de los receptores dopaminérgicos (D2) que pueblan densamente los ganglios basales. Su carencia7 podría interferir con la función de los receptores dopaminérgicos y provocar el trastorno del movimiento35 que conocemos como SPI. Esta hipótesis viene apoyada por la observación clínica de que el SPI mejora con la administración de dopamina y de agonistas dopaminérgicos. Aproximadamente un 20% de pacientes con SPI tiene anemia ferropénica. Las concentraciones inferiores a 45 µg/l pueden incrementar los síntomas. El hecho de que el SPI pueda ser inducido por la ferropenia16 y los fármacos antidopaminérgicos y que mejore casi siempre con fármacos dopaminérgicos hace pensar que tanto el hierro como la dopamina están implicados en la aparición del cuadro y que se relacione con una hipofunción dopaminérgica. Ambos factores están vinculados, pues el hierro actúa como coenzima de la tirosina-hidroxilasa, que es la enzima limitante de la síntesis de dopamina. Además esta enzima sigue un ritmo circadiano, es menos activa en las últimas horas del día, lo que explicaría el ritmo circadiano que sigue el síndrome.
Se ha comunicado su asociación con lesiones medulares, tanto por compresión extrínseca como por lesiones intrínsecas, como las provocadas por la esclerosis múltiple.
Los estados de hipoglucemia, hipotiroidismo, la enfermedad de Parkinson y el síndrome de apnea/hipoapnea pueden asociarse también.
Las vías de investigación se centran actualmente en que el SPI parece implicar alteraciones en el sistema dopaminérgico central, en el metabolismo del hierro y en la neurotransmisión opiácea, pero los detalles de estas alteraciones tienen que ser más y mejor explorados.
DIAGNÓSTICO DIFERENCIAL15,16,21,24,35-37
Es importante que el profesional establezca un protocolo de diagnóstico diferencial con varias patologías como:
1) Los calambres nocturnos de piernas (muy típicos en la edad avanzada y que se caracterizan por contracciones dolorosas involuntarias de las piernas).
2) La acatisia (necesidad imperiosa de movimiento, no limitado a las piernas y muy relacionada con determinados fármacos como los neurolépticos o sustancias antidopaminérgicas, sin que haya sensación desagradable acompañante y sin variaciones a lo largo del día).
3) Neuropatía periférica: hay disestesias pero no ceden al mover las piernas o con la actividad motora, no empeoran tampoco al anochecer o al acostarse.
4) Otras: afectación vascular, las polineuropatías (con síntomas sensitivos como hormigueos o quemazón38, siendo frecuente la alodinia, de modo que un estímulo sensitivo no doloroso se puede convertir y percibir como un dolor importante tan sólo por el roce simple de una sábana; en la exploración hay un déficit sensitivo distal y arreflexia) y la insuficiencia venosa en miembros inferiores. Se debe establecer un diagnóstico diferencial con los síndromes dolorosos de las piernas (por artropatía o neuropatía), pero la presencia del ritmo circadiano y el alivio inmediato de los síntomas al mover las piernas permiten distinguir el cuadro con facilidad. No debe confundirse con los movimientos periódicos de las piernas que se producen en la narcolepsia o el síndrome de Parkinson. También hay que diferenciarlo de otros trastornos del sueño en los que no está presente la necesidad de mover las piernas continuamente y de otros tipos de trastornos del sueño (parasomnias, sobresaltos de sueño, movimientos rítmicos durante el sueño), distonías paroxísticas y nocturnas y otros movimientos anormales.
DIAGNÓSTICO1,2,7,10-12,15,16,18,21
Es claramente clínico. No existe una prueba que sea diagnóstica para el SPI. Se evalúa analizando el historial clínico del paciente y su sintomatología10,24.
Se detalla en tabla 3.
TRATAMIENTO
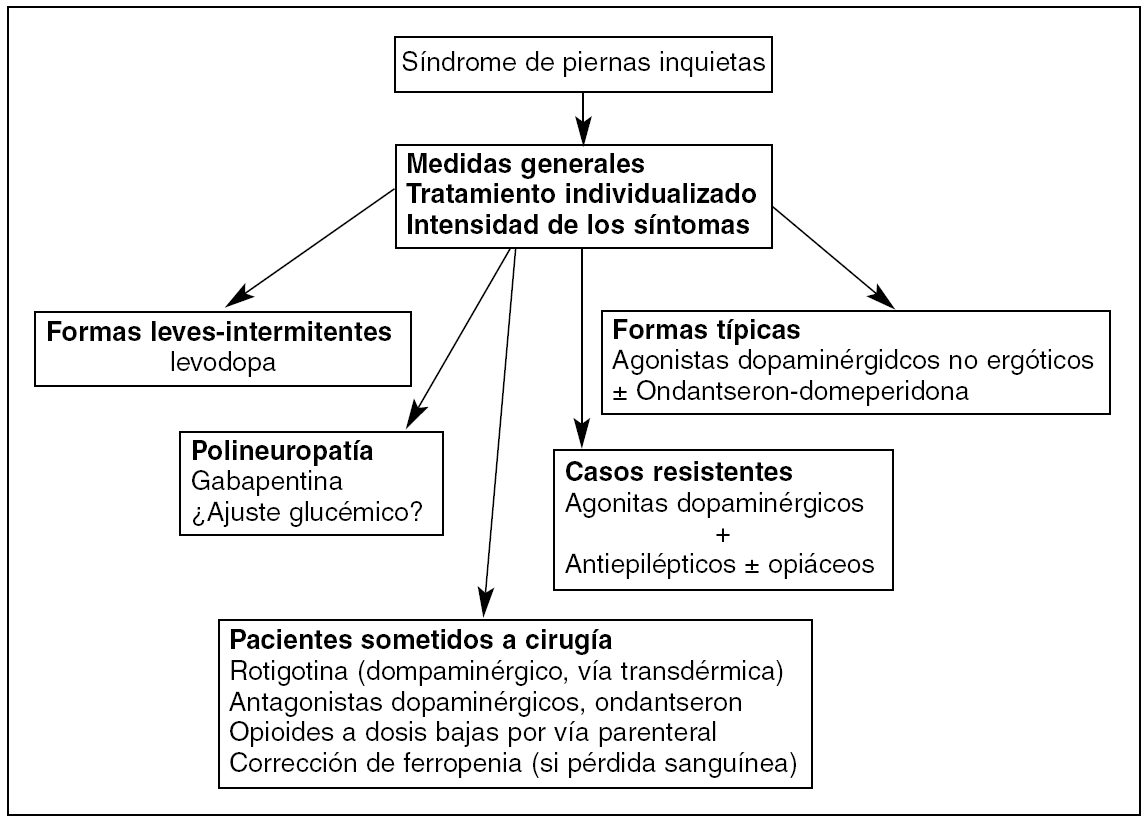
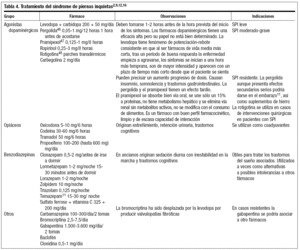
EL tratamiento10,11,7,15,17,18,21,35,44,45 del SIP debe ajustarse a la intensidad de los síntomas y al perfil del paciente en cada momento (tabla 4 y fig. 149).
Figura 1. Algoritmo terapéutico del síndrome de piernas inquietas18,49.
Tratamiento no farmacológico
El tratamiento no farmacológico del SPI podríamos dividirlo en dos partes: una serie de medidas específicas y las medidas no farmacológicas generales para el manejo del insomnio y otros trastornos del sueño.
1) Medidas específicas6: para los pacientes que presentan síntomas leves a moderados es posible utilizar medidas preventivas y sugerir cambios en el estilo de vida y las actividades que se realizan para reducir o eliminar los síntomas.
2) Los cambios y consejos o medidas generales podrían ser:
Medidas iniciales:
Buena higiene de sueño15,44.
La realización de actividad física aeróbica durante el día disminuye la tendencia a presentar síntomas. Se debe realizar durante el día, evitando realizar ejercicio vespertino.
En muchos pacientes7 los síntomas se alivian con el frío. El mojarse las piernas con agua fría antes de acostarse resulta eficaz.
Evitar11 la cafeína, el alcohol y el tabaco entre otros excitantes. Retirar los posibles fármacos inductores del síndrome.
En los pacientes con un nivel de ferritina inferior a 45-50 µg/l se realizará una búsqueda de causas de pérdida crónica de hierro, e iniciar una terapia de reemplazamiento.
Las técnicas de relajación progresiva o de biofeedback son beneficiosas, así como actividades mentales11 con crucigramas, puzles y técnicas de relajación para reducir el estrés.
Tratamiento farmacológico1,18
Fármacos dopaminérgicos10,49,50
Son los más eficaces para el tratamiento del SPI y deben ser considerados como el primer paso terapéutico. La indicación inicial es para el SPI leve o en los casos intermitentes. La levodopa51 es la referencia. La dosis media empleada de carbidopa/levodopa ha sido 25/100 mg, habitualmente en toma única. El riesgo asociado al tratamiento de la levodopa es el rebote de los síntomas.
Fármacos agonistas dopaminérgicos50,52
Son fármacos que estimulan directamente los receptores postsinápticos de la dopamina. Se pueden dividir según su estructura química en ergóticos y no ergóticos. Los ergóticos, entre los que se encuentran:
1) La bromocriptina: como dopaminérgico ergótico puede dar complicaciones fibróticas como valvulopatías fibróticas. Es peor tolerada que la levodopa. Dosis diaria 2,5-7,5 mg.
2) La pergolida46 (la principal limitación a su uso son los efectos secundarios): la dosis de pergolida53 oscila entre 0,25 y 1 mg/día.
3) La cabergolina54 (la dosis media eficaz es de 2 mg/día): la larga vida media del fármaco lo convierte en un buen candidato para tratar pacientes con síntomas diurnos; fue el primero en comercializarse.
Pero por inducir efectos secundarios potencialmente graves, como la fibrosis valvular cardíaca o los trastornos circulatorios en piernas, han sido desplazados a una segunda línea por los agonistas no ergóticos:
1) Pramipexol10,11,47,55. Es el primer fármaco aprobado para el tratamiento del SPI en Europa. Es agonista de receptores D2 y D3, con una vida media de 8 a 12 horas. Su absorción por vía oral es rápida. Existen pruebas concluyentes de que mejora todos los aspectos del SPI, lo que incluye las alteraciones del sueño, los síntomas diurnos y las alteraciones del estado de ánimo. Es el agonista dopaminérgico no ergótico con la pauta de dosificación más rápida y sencilla. El período de ajuste de dosis del pramipexol (hasta 4 semanas) es mucho menor que el del ropinirol (7 semanas), lo que es más cómodo tanto para los pacientes como para los médicos. El tratamiento se inicia con una dosis vespertina de 0,125 mg, administrada una vez al día, 2-3 horas antes de acostarse. En los pacientes que requieran un alivio sintomático adicional la dosis puede incrementarse progresivamente cada 4-7 días a 0,25 mg/día, 0,50 mg/día y hasta 0,75 mg/día Los pacientes más graves pueden necesitar dosis más elevadas, y en estos casos es recomendable repartirla en dos tomas, a mediodía y al anochecer.
2) Ropinirol44,52,56. Es un agonista de receptores D2 y D3 con una vida media intermedia, en torno a las 6 horas. Los efectos secundarios son similares a los indicados para otros fármacos dopaminérgicos, aunque la incidencia de náuseas es superior al pramipexol. El tratamiento se inicia con una dosis vespertina de 0,25 mg y se va aumentando progresivamente cada 3-7 días hasta controlar los síntomas. La dosis media eficaz oscila entre 2 y 4 mg al día. Al igual que con el pramipexol, en los casos en que se precisan dosis más elevadas es recomendable repartirlas en dos tomas, a mediodía y al anochecer.
Otros fármacos
1) Benzodiazepinas43. Fueron de los primeros fármacos en probarse en el SPI. El que más se usó fue el diazepam11. Sin embargo, no son un tratamiento adecuado para el SPI por su riesgo a crear adicción y por su efecto pasajero. El que ha demostrado efectividad es el clonazepam45 a dosis de 0,5-2 mg/día para la indicación del SIP moderado o intermitente. La última tendencia es utilizar fármacos de acción algo más corta como el lormetazepam o el lorazepam. Para el control del insomnio de conciliación se utilizan triazolam 0,25-0,5 mg/día, zolpidem57 5-10 mg/día y zaleplón 5-10 mg/noche. En el insomnio de mantenimiento el temazepan11 15-30 mg/día es el más empleado.
2) Fármacos antiepilépticos:
Carbamazepina. La carbamazepina58 fue el primer fármaco antiepiléptico en demostrar eficacia en este campo. La dosis media empleada es de 236 mg/diarios. Actualmente no se utiliza por haber sido desplazada por los dopaminérgicos.
Gabapentina59. Es un fármaco modulador de la subunidad a2d de un canal de calcio que ha demostrado su eficacia en el tratamiento del dolor neuropático y también del SPI. La dosis media eficaz osciló entre 1.300 y 1.800 mg/día, por lo que conviene repartirla en dos o tres tomas. Es útil en pacientes con síntomas menos intensos y en los que presentan neuropatía periférica dolorosa asociada, así como en patologías degenerativas como el Parkinson o la demencia. El tratamiento se iniciaría con una dosis vespertina de 300 mg que se iría aumentando progresivamente cada 3-7 días hasta conseguir el control adecuado de los síntomas. Los efectos secundarios más frecuentes asociados al tratamiento con este fármaco son somnolencia e inestabilidad, pero habitualmente son efectos secundarios leves.
Pregabalina. Similar a la gabapentina. Tiene una vida media más larga y una mayor tendencia a producir somnolencia que la gabapentina, lo que puede resultar beneficioso para tratar pacientes con este síndrome con importante alteración del sueño.
Opioides1,11,13. Su uso está limitado por los efectos secundarios que provocan como el estreñimiento y el riesgo de adicción. Los utilizados se emplean para los casos resistentes a otros tratamientos. Los que se utilizan en el SPI refractario son la metadona 5-10 mg, el tramadol 50-100 mg y la oxicodona60 5-15 mg, todos ellos en tres tomas diarias. En el SPI intermitente se emplean antes de acostarse la codeína 30-60 mg, el tramadol 50-100 mg y el propoxifeno51 100-200 mg.
Otros. En pacientes que vayan a ser sometidos a cirugía puede existir un empeoramiento de los síntomas. La propia cirugía conlleva una inmovilidad que acentuará la sintomatología. Dependiendo de los síntomas se emplean la rotigotina48, fármaco dopaminérgico en parche transdérmico, ondantseron, metroclopramida, para aliviar las náuseas y vómitos, los neurolépticos alivian el dolor ocasionado por los movimientos, sulfato ferroso + vitamina C (325 + 250 mg/día), etc. La pérdida sanguínea inducida en la cirugía conduce a estados de ferropenia que agravarán la sintomatología, lo que puede revertirse con transfusión sanguínea. El propanolol a dosis de 40-120 mg diarios, la clonidina61a 0,05 mg/día y la amantadina a dosis de 300 mg/día son otras opciones para aliviar los síntomas. El nicardipino5 a dosis de 20 mg/día se está utilizando como ensayo terapéutico desde el año 2003 sin evidencias previas y con resultados aún pobres. Algunos autores, sin embargo, señalan como precipitantes de los síntomas de piernas inquietas a los antagonistas del calcio.
PUNTOS CLAVE
EL SPI se define como la sensación desagradable en las extremidades inferiores que provoca la necesidad de mover las piernas y por esto se puede considerar como un trastorno del movimiento.
El SPI es una enfermedad neurológica motora caracterizada por parestesias (sensaciones anormales) y disestesias (sensaciones molestas o dolorosas) en las piernas que ocurren típicamente durante el sueño, el descanso o el reposo.
Actualmente se definen cuatro criterios para su diagnóstico recogidos por la Internacional Restless Legs Síndrome Group.
En muchos casos de enfermedad primaria las personas afectadas tienen antecedentes familiares, lo que puede sugerir una forma de herencia autosómica dominante.
EL SPI es un trastorno mucho más frecuente de lo que habitualmente se diagnostica.
Muy frecuente en ancianos y en el género femenino.
En la mayor parte de los casos el SPI es un trastorno primario (idiopático) sin que se encuentre otro problema de salud.
La patogenia relacionada podría deberse a una deficiencia de dopamina cerebral junto con niveles bajos de ferritina o de hierro.
EL SPI se ha relacionado con algunas enfermedades: el déficit de hierro-ferritina, la uremia elevada de la enfermedad renal terminal y la polineuropatía diabética.
Uno de los factores implicados en su infradiagnóstico es la dificultad de los pacientes para describir los síntomas.
La historia clínica con una detallada anamnesis es la base para llegar al diagnóstico.
Los síntomas predominan y empeoran al acostarse y originan insomnio al paciente con agotamiento y somnolencia diurnos.
El tratamiento se basa en medidas no farmacológicas como masaje, acupuntura, medidas higiénicos-dietéticas, y en fármacos como los agonistas dopaminérgicos entre otros.
Los fármacos agonistas dopaminérgicos no ergóticos pramipexol y ropirinol una hora antes de la aparición de los síntomas son eficaces y bien tolerados por los pacientes, siendo alternativa la levodopa y como coadyuvantes el clonazepam, la gabapentina y los opioides.
Las benzodiazepinas se utilizan para el control del insomnio asociado.
Correspondencia: M. Martínez García.
C/ Trovero Marín n.o 5 1.o F.
30730 San Javier. Murcia.
Correo electrónico: bagamontse@terra.es
Recibido el 02-10-06; aceptado para su publicación el 06-07-07.