La retinopatía diabética (RD) está considerada como la causa más frecuente de ceguera en la población activa en países industrializados. El edema macular diabético es la causa más frecuente de disminución de la agudeza visual en los diabéticos. De acuerdo con los resultados de los grandes estudios multicéntricos, la prevención de la ceguera por RD pasa por la realización de revisiones periódicas del fondo de ojo de los pacientes diabéticos de manera que puedan ser tratadas a tiempo. El uso de cámaras no midriáticas y la telemedicina han demostrado ser útiles para este fin (sensibilidad>80% y especificidad>90%). Si se sigue este método, la primera retinografía debería realizarse a los 5 años del diagnóstico en los diabéticos tipo 1 y en el momento del diagnóstico en los diabéticos tipo 2.
Por tanto, el papel del médico de atención primaria es fundamental para la detección precoz de esta enfermedad.
Diabetic retinopathy (DR) is considered the most common cause of blindness in the working-age population in industrialised countries, with diabetic macular oedema being the most common reason of decreased visual acuity in diabetics. According to the results of large multicentre studies, blindness prevention for RD involves conducting periodic check-ups, which include examinations of the back of the eye, so they can be treated in time. The use of non-mydriatic cameras and telemedicine have been shown to be useful in this regard (sensitivity>80% and specificity>90%). If this procedure is followed, the first retinography should be performed 5 years from diagnosis in type 1 diabetics and immediately after diagnosis in type 2 diabetics.
Therefore the role of the Primary Care physician is crucial to enable early diagnosis of this disease.
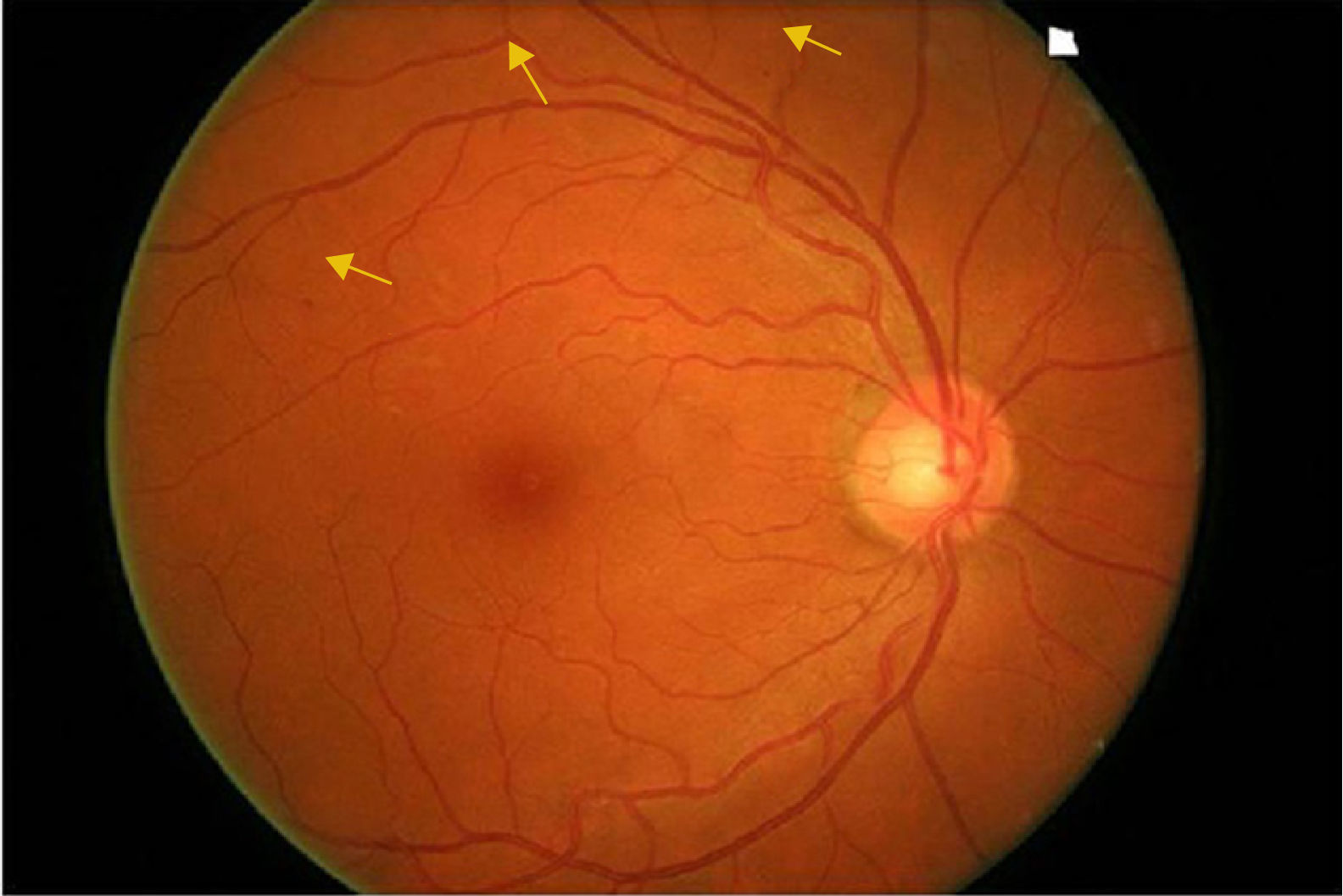
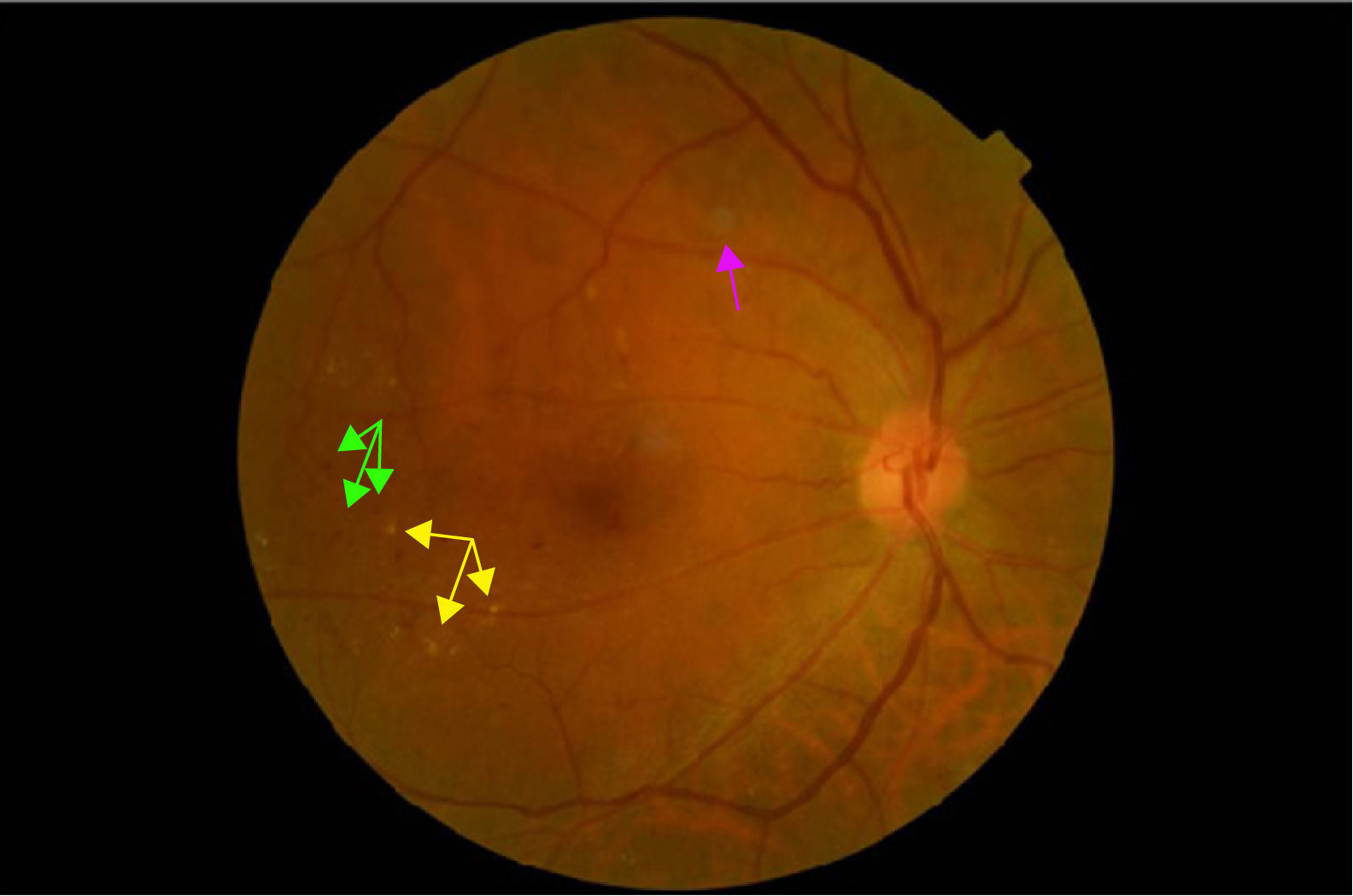
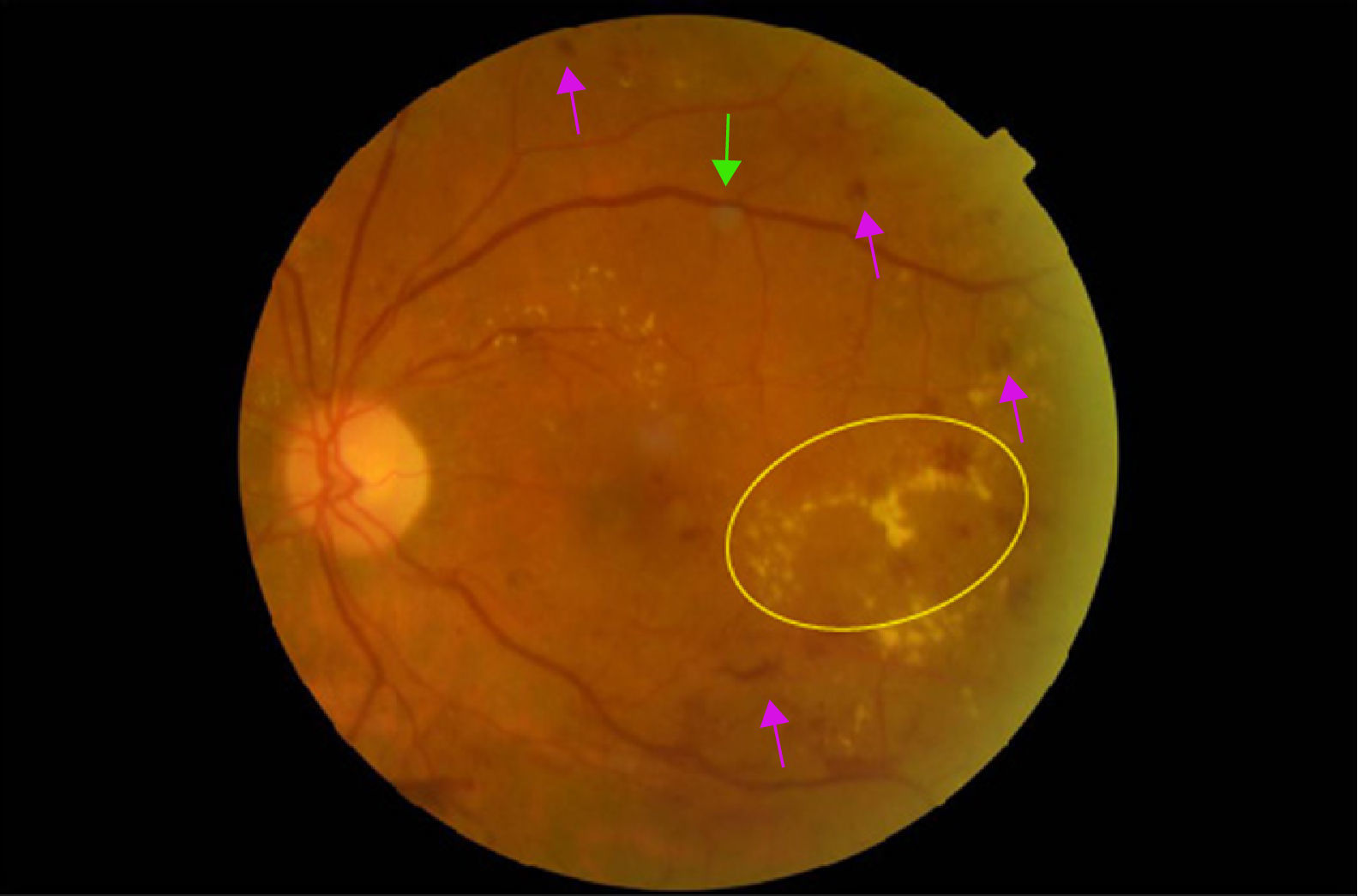
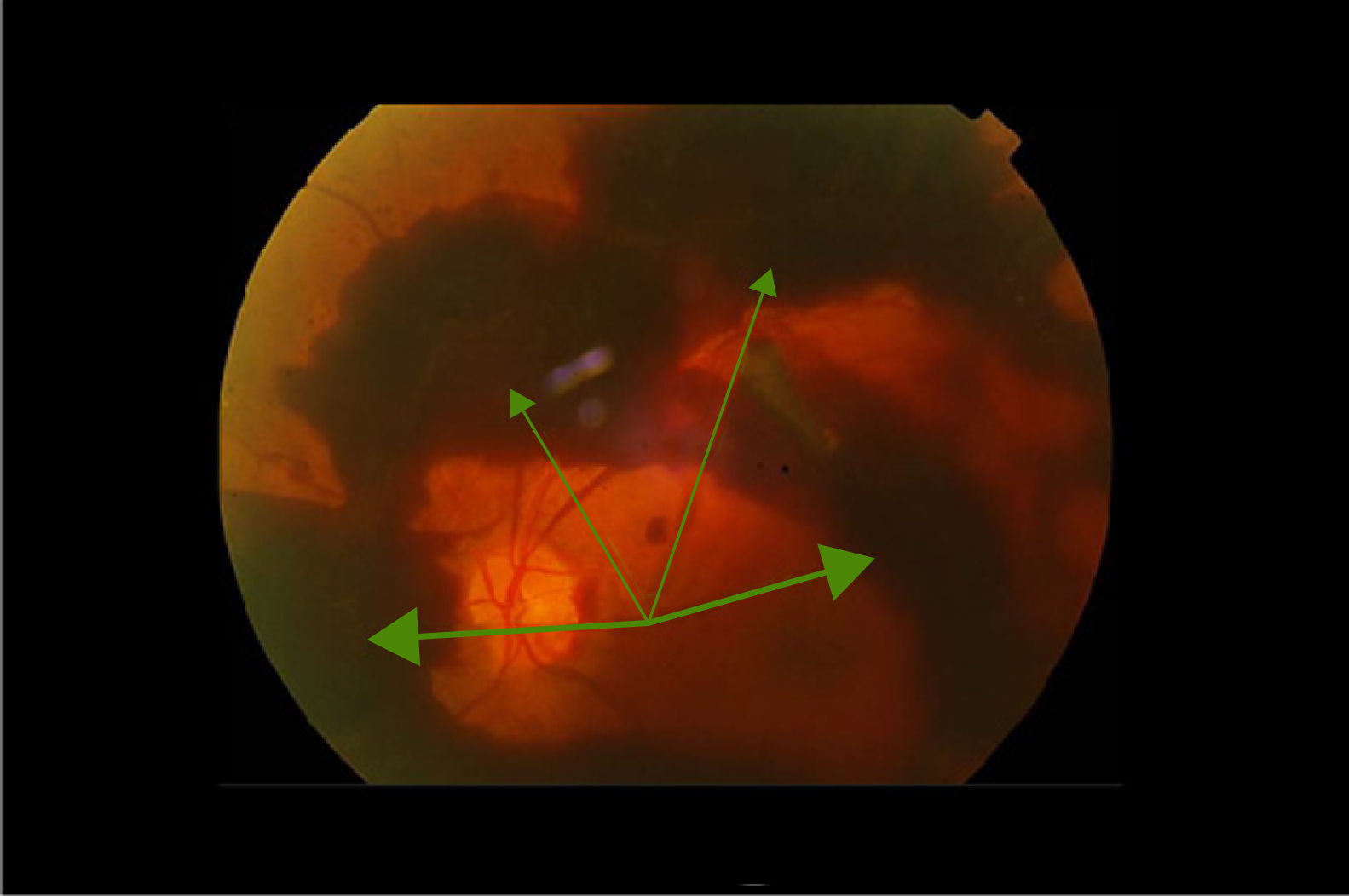
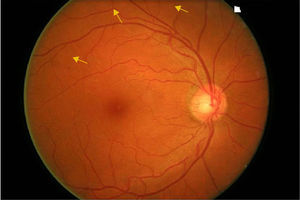
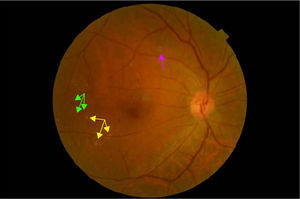
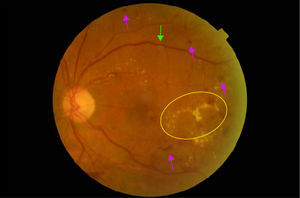
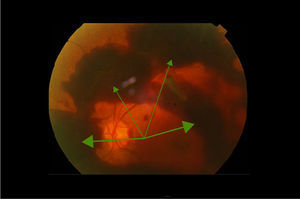
La retinopatía diabética (RD) está considerada como la causa más frecuente de ceguera en la población activa en países industrializados. El edema macular diabético (EMD) es la causa más frecuente de disminución de la agudeza visual en los diabéticos y la RD proliferativa la responsable de los déficits visuales más severos1,2 (figs. 1–4).
Aproximadamente el 25% de las personas afectadas de diabetes mellitus (DM) tienen algún grado de RD y entre el 2 y el 10% de los diabéticos presentan edema macular clínicamente significativo (EMCS). Incluso, entre los diabéticos con DM tipo 2, un 20% presentará algún grado de RD a los 2 años del diagnóstico. La incidencia del problema aumenta con la duración de la enfermedad, de forma que a los 15 años de evolución el 15% de los diabéticos tienen EMCS y a los 20 años más del 90% presentará algún grado de RD2,3.
FisiopatologíaLa RD es una microangiopatía que afecta a arteriolas, precapilares, capilares y vénulas de la retina. Hay que tener en cuenta que a veces pueden ser afectados también los vasos de mayor tamaño. Se caracteriza por presentar oclusión microvascular, hemorragias y alteración de la permeabilidad microvascular por la pérdida progresiva de pericitos. Las oclusiones microvasculares dan lugar a isquemia retiniana, cuyas consecuencias principales son la formación de shunts arteriovenosos y la neovascularización4. El aumento de la permeabilidad da lugar a extravasación, exudación y edema. Los procesos neovasculares pueden producir hemorragias vítreas, glaucoma neovascular y desprendimiento de retina traccional. La exudación produce edema macular. Ambos mecanismos (los procesos neovasculares y el edema) son causa de una importante pérdida progresiva de visión, e incluso de ceguera.
ClasificaciónDe acuerdo con los resultados de los grandes estudios multicéntricos, la prevención de la ceguera por RD pasa por la realización de revisiones periódicas del fondo de ojo de los pacientes diabéticos de manera que puedan ser tratadas a tiempo. Esto exige el empleo de criterios homogéneos de clasificación y tratamiento de la RD. La clasificación propuesta por el Early Treatment Diabetic Retinopaty Study (ETDRS) perseguía este fin, sin embargo, no se utiliza habitualmente en la práctica clínica debido a su complejidad y a los numerosos niveles o estadios. Por ello, la clasificación más utilizada en la práctica clínica diaria es la propuesta por un grupo de expertos del Global Diabetic Retinopathy Proyect Group (GDRPG)5, que está basada en los resultados del ETDRS y, por lo tanto, se apoya en la evidencia científica, y proporciona una base de manejo sencilla y adecuada (ver tabla 1).
Clasificación clínica internacional de la retinopatía diabética (GDRPG)
| Sin RD aparente | Ausencia de μA |
| RDNP leve | Solo μA |
| RDNP moderada | μA asociado a menos de 20 hemorragias intrarretinianas en cada uno de los 4 cuadrantes, exudados duros, exudados algodonosos, arrosariamiento venoso en un solo cuadrante. |
| RDNP severa | μA junto a uno de los siguientes hallazgos: |
| – B26 hemorragias intrarretinianas severas (¿20) en cada uno de los 4 cuadrantes | |
| – Arrosariamiento venoso ≥2 cuadrantes | |
| – Anomalías microvasculares intrarretinianas en ≥ 1 cuadrante | |
| RDP | Neovasos o hemorragia prerretiniana o hemovítreo |
RD: retinopatía diabética; RDNP: retinopatía diabética no proliferativa; RDP: retinopatía diabética proliferativa; μA: microaneurismas.
Un buen manejo de la RD implica, en primer lugar, la identificación de aquellos pacientes con riesgo de padecer pérdida visual por la diabetes antes de que ocurra un daño irreversible. Por ello, todos los pacientes diabéticos deberían ser explorados, bajo midriasis, por un oftalmólogo de forma periódica. El problema es la consiguiente sobrecarga asistencial para los oftalmólogos. El uso de cámaras no midriáticas (CNM) y la telemedicina ha demostrado ser útil para este fin (sensibilidad >80% y especificidad>90%)6–8. Si se sigue este método, la primera retinografía debería realizarse a los 5 años del diagnóstico en los diabéticos tipo 1 y en el momento del diagnóstico en los diabéticos tipo 2.
En todos los estadios de la RD es esencial el control metabólico y en concreto de la glucemia, hemoglobina glucosilada (HbA1c), la dislipidemia, la anemia, la hipertensión arterial (HTA), el sobrepeso y el estado renal (microalbuminuria en orina)9.
Una vez realizada la primera evaluación oftalmológica, el modo de actuación sería el siguiente:
Sin retinopatía diabética aparente- -
Examen oftálmico o CNM bienal si existe buen control metabólico (HbA1c<7%) y ausencia de factores de riesgo asociados (HTA, dislipidemia, etc.).
- -
Exploración oftalmológica o CNM anual si existen factores de riesgo asociados o el control metabólico es dudoso o deficiente.
Control oftalmológico o CNM anual. Adelantar en caso de mal control metabólico, gran número de lesiones cercanas a la fóvea y pacientes embarazadas (se hará un control cada trimestre y luego cada 6 meses durante el primer año tras el parto).
En este estadio es fundamental insistir y concienciar al paciente sobre la importancia del control metabólico, ya que este influirá en la progresión de la RD.
Con retinopatía diabética no proliferativa moderadaControl oftalmológico semestral. No precisa tratamiento con láser (panfotocoagulación [PFC] retiniana), dado que el riesgo de progresión a RD proliferativa (RDP) al año oscila entre un 5,4 y un 26,3%.
Con retinopatía diabética no proliferativa severaEn estos casos hay una alta probabilidad de progresión a RDP en un año, en torno al 50,2%, por lo que se realizará control hospitalario cada 3-4 meses, pudiendo ser incluso más próximo en algunos casos, según el criterio del oftalmólogo.
En este estadio se puede considerar PFC retiniana temprana en aquellos pacientes con mayor riesgo de progresar: DM2 con mal control metabólico, pacientes que no cumplen las revisiones de forma habitual, RDP en el otro ojo, evidencia de progresión de la retinopatía, pacientes con cataratas que puedan limitar en un futuro próximo la PFC, de modo previo a la cirugía de catarata, embarazo o intento de lograrlo y áreas de isquemia angiográficas generalizadas.
Retinopatía diabética proliferativaAnte este grado de RD debemos realizar PFC retiniana en el plazo de un mes o mes y medio. Esto disminuye al 50% el riesgo de pérdida visual severa en estos pacientes. Además también se puede asociar el uso de antifactores del crecimiento del endotelio vascular (anti-VEGF) intravítreos como el bevacizumab o ranibizumab que, aunque usados fuera de indicación para este fin (en los próximos meses dispondremos de la aprobación del uso de ranibizumab para RDP), han demostrado beneficios con respecto a la PFC aislada10.
Láser en la retinopatía diabéticaNo se trata de un tratamiento inocuo, por lo que su uso se realizará en los casos de RD no proliferativa (RDNP) severa señalados anteriormente y en la RDP. No mejora la visión y deja secuelas sobre el campo visual periférico, la sensibilidad al contraste y la visión nocturna. Sin embargo, disminuye ampliamente el riesgo de complicaciones severas derivadas de la RD11.
Se aplican entre 1.000 y 3.000 impactos en varias sesiones, de forma ambulante.
Cirugía vitreorretinianaSe realizará cirugía vitreorretiniana en los casos de hemovítreo persistente o desprendimiento de retina traccional.
En la tabla 2 se expone el resumen de las principales recomendaciones terapéuticas en el tratamiento de la RD.
Tabla resumen del manejo de la retinopatía diabética
| Control endocrinológico: es especialmente importante el control de glucemia (HbA1c<7%), HTA<130/80, lípidos; TG<150mg/dl; LDL colesterol<100 mg/dl salvo en pacientes con alto riesgo cardiovascular que debe ser<70 mg/dl. Estado cardíaco y renal. Evitar sobrepeso. Ejercicio físico. Dejar de fumar |
| 1. SIN RD APARENTE Control oftalmológico anual o bienal |
| 2. RDNP LEVE Control oftalmológico anual Adelantar en caso de mal control metabólico, gran número de lesiones cercanas a la fóvea y pacientes embarazadas |
| 3. RDNP MODERADA Control oftalmológico semestral |
| 4. RDNP SEVERA Revisión cada 3-4 meses Considerar PFC temprana en caso de: DM2 con mal control metabólico, pacientes que no cumplen las revisiones de forma habitual, RDP en el otro ojo, evidencia de progresión de la retinopatía, pacientes con cataratas que pueda limitar en un futuro próximo la PFC, previo a la cirugía de catarata, embarazo o intento de lograrlo y áreas de isquemia angiográficas generalizadas |
| 5. RDP PFC±anti-VEGF intravítreo en un mes o mes y medio Cirugía vitreorretiniana: en casos de hemovítreo persistente o desprendimiento de retina traccional |
anti-VEGF: antifactor del crecimiento del endotelio vascular; PFC: panfotocoagulación; RD: retinopatía diabética; RDNP: retinopatía diabética no proliferativa; RDP: retinopatía diabética proliferativa.
El glaucoma neovascular es un glaucoma secundario resultante de la obstrucción de la red trabecular por elementos fibrovaculares o sinequias asociadas.
Suele cursar con dolor ocular, disminución severa de la agudeza visual, presión intraocular muy alta, hiperemia conjuntival, edema corneal, tyndall, hipema, rubeosis de iris, corectopia (descentralización pupilar), ectropión uveal (eversión del epitelio pigmentario en borde pupilar, justo en la cara anterior del iris) y goniosinequias (sinequias en el ángulo iridocorneal) importantes.
Es imprescindible realizar un diagnóstico y tratamiento precoces, ya que esta entidad tiene muy mal pronóstico en los casos tardíos y puede llevar a la pérdida completa de visión o, incluso, a la pérdida del globo ocular.
El tratamiento consiste en tratar la causa, que es la isquemia retiniana producida por la RD, mediante PFC acompañada del uso de anti-VEGF intravítreos, así como usar hipotensores oculares. En casos no respondedores será necesario realizar cirugía.
Edema macular diabéticoLa clasificación utilizada es la del ETDRS y se planteará tratamiento siempre que exista un EMCS.
Si en la RD el control sistémico es indiscutible, en el edema macular esto resulta aún más evidente. El abordaje de esta complicación debe ser multidisciplinar. Es preciso insistir en el control de la glucemia (HbA1c), presión arterial, sobrepeso y lípidos. Un mal control metabólico puede justificar posponer el tratamiento hasta que este mejore, ya que la respuesta al tratamiento será mucho peor e incluso nula en los pacientes mal controlados sistémicamente.
Para el diagnóstico y tratamiento del edema macular será crítico el resultado de la tomografía de coherencia óptica12 y de la angiofluoresceingrafía (AFG). La tomografía de coherencia óptica macular es una técnica de imagen que se lleva empleando desde 1995, aunque ha evolucionado mucho desde entonces, y que permite el diagnóstico, control y seguimiento de los problemas de la mácula. Mediante emisión de luz y su reflexión en los tejidos del ojo, nos proporciona una imagen de las diferentes estructuras y sus capas a modo de escáner en una resolución de micras, pudiendo valorar la existencia de alteraciones por muy pequeñas que estas sean.
Manejo del edema macular diabético- -
Edema macular focal o multifocal: área bien definida (focal) o varias áreas bien definidas (multifocal) de difusión de contraste en la AFG. Se trata con láser focal dirigido mediante AFG, cuando no hay afectación central, en cuyo caso se utilizará tratamiento con anti-VEGF intravítreos. Si existe tracción vitreorretiniana hay que recurrir a la cirugía.
- -
Edema macular difuso: de primera elección se utilizan los anti-VEGF intravítreos si no existe tracción vitreorretiniana (en estos casos es preciso realizar cirugía, como se ha comentado anteriormente). En caso de no respuesta o edemas maculares de gran tamaño se puede recurrir al empleo de corticoides intravítreos, Ozurdex®, que es un dispositivo biodegradable de polilaticoglicólico que libera dexametasona durante 4-6 meses. Este dispositivo viene a abordar el componente inflamatorio que sin duda tiene el EMD, con buenos resultados.
- -
Edema macular quístico: englobado dentro del edema macular difuso, se aborda de la misma manera.
- -
Anti-VEGF en EMD: la expresión del VEGF juega un papel central en la patogénesis de la RD. La disregulación del VEGF en los ojos de los pacientes con diabetes se asocia a la rotura de la barrera hematorretiniana con aumento de la permeabilidad vascular, dando lugar a las distintas manifestaciones clínicas de la RD4. Por eso, el tratamiento con anti-VEGF se ha convertido en el gold standard en el manejo del EMD. Los agentes utilizados son: bevacizumab, ranibizumab y aflibercept, siendo estos 2 últimos los aprobados para uso intraocular. Además de la terapia antiangiogénica, las inyecciones intravítreas de corticoides también obtienen buenos resultados en los estudios, debido al componente inflamatorio que está presente en el EMD13, como se comentó anteriormente.
Ha habido muchos avances en el abordaje y tratamiento de la RD y sus complicaciones. Los pacientes con RD necesitan una atención de por vida con enfoques versátiles en su tratamiento. Los recientes avances en imagen y diagnóstico de la RD y EMD y el uso de terapia intravítrea (anti-VEGF y corticoides) ha mejorado el manejo de este gran problema de salud pública. Sin embargo, sigue siendo de máxima importancia realizar un diagnóstico precoz y un abordaje multidisciplinar para conseguir buenos resultados y, en este aspecto, el médico de atención primaria tiene un papel crucial debido a su participación activa en los procesos de telemedicina. Por otro lado, el control metabólico se convierte en imprescindible y ayuda de forma significativa a reducir el riesgo de pérdida de visión en los pacientes con RD.
Conflicto de interesesLos autores declaran la inexistencia de conflicto de intereses de cada uno de los autores.