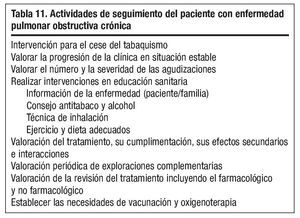
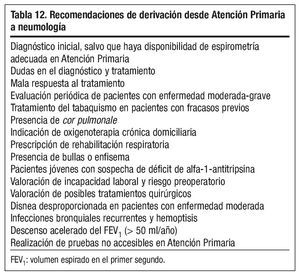
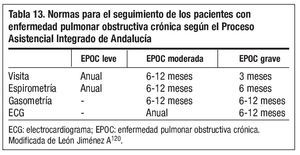
PRÓLOGO
La enfermedad pulmonar obstructiva crónica (EPOC) es una patología crónica muy prevalente, que conlleva una gran repercusión social y económica. El impacto real sobre la población está infravalorado dado que su diagnóstico es generalmente tardío, realizándose, en la mayoría de los casos, cuando la enfermedad está ya bastante evolucionada.
El estudio IBERPOC permitió conocer la prevalencia de la EPOC en España, situándose en el 9,1% en la población entre 40 y 69 años, aportando como dato preocupante que el 78,2% de los pacientes no estaba previamente diagnosticado.
Como es conocido, para el diagnóstico de esta enfermedad es condición imprescindible la realización de espirometrías fiables, siendo el criterio funcional la puerta de entrada recogida en el Proceso Asistencial Integrado EPOC. Persisten aún importantes problemas para poder efectuar esta exploración con todos los criterios de calidad exigidos.
Estos factores han motivado que las tres sociedades científicas NEUMOSUR, SAMFyC y SEMERGEN nos sintiéramos en la obligación de trabajar juntos y aportar la experiencia y conocimientos de nuestros Grupos de Trabajo para compartirlos con todos los profesionales que cuidan a los pacientes con EPOC.
Como indica la evidencia científica, un diagnóstico precoz y un correcto abordaje terapéutico pueden mejorar el curso de la enfermedad, por lo que nosotros, como médicos, tenemos una responsabilidad fundamental en conseguir este objetivo.
En este sentido consideramos que nuestras sociedades científicas tienen un papel destacado en aportar, desde una visión independiente y profesional, las recomendaciones basadas en la mejor evidencia científica existente hasta el momento.
Fruto de este trabajo conjunto, tras muchas horas de estudio individual de sus autores y de trabajo colectivo en arduas reuniones, es este Documento de Consenso que recoge de una forma resumida, pero sin dejar nada importante, todo lo que el médico no debe olvidar para realizar un abordaje integral de los pacientes con EPOC.
Es necesario recalcar el ambiente de cordialidad, compañerismo y colaboración que ha existido en todas las reuniones, que en todo momento tenían como objetivo fundamental conseguir conjugar la mayor evidencia científica en cada tema, con la experiencia clínica de los participantes. Creemos que el resultado ha sido altamente satisfactorio, aunque está abierto a las críticas y aportaciones de todos nuestros socios y de la comunidad científica.
Esperamos y deseamos continuar en esta línea de colaboración que pueda contribuir de una forma real y tangible a la continuidad asistencial deseada por todos y, en definitiva, a la mejor asistencia a nuestros pacientes.
F.J. Álvarez Gutiérrez (NEUMOSUR),
J.A. Quintano Jiménez (SEMERGEN),
M. Lubián López (SAMFyC).
INTRODUCCIÓN
La enfermedad pulmonar obstructiva crónica (EPOC) se caracteriza por la presencia de obstrucción crónica, progresiva y no totalmente reversible al flujo aéreo, causada fundamentalmente por una reacción inflamatoria anormal frente al humo del tabaco. Es una enfermedad prevenible y tratable, con algunos efectos extrapulmonares significativos que pueden contribuir a la gravedad de los pacientes1. La exposición a otros tóxicos inhalados también puede producir EPOC, pero esta causa es muy poco frecuente en nuestro medio. Por consiguiente, el diagnóstico de la enfermedad se establece sobre la base del antecedente de consumo de tabaco y la demostración de una obstrucción no reversible mediante una espirometría forzada2.
El conocimiento de la enfermedad ha evolucionado considerablemente en los últimos años y hoy en día se considera una enfermedad multicomponente en la que conceptos clásicos, como bronquitis crónica y enfisema, y otros más novedosos, como afectación sistémica o hipertensión pulmonar, constituyen distintas manifestaciones de la enfermedad.
La EPOC es una enfermedad directamente ligada al consumo de tabaco. En Europa, aproximadamente un 35% de la población adulta es fumadora. En España, según los datos de la última Encuesta Nacional de Salud de 2006, la prevalencia del consumo de tabaco en la población de 16 y más años es del 30% (diaria el 27%) y hay un 21% de exfumadores. El estudio epidemiológico de la EPOC en España (IBERPOC)3 demostró que en la población con edad comprendida entre 40 y 70 años la prevalencia global de EPOC es del 9,1%, con una relación varón/mujer de 4:1. En fumadores de más de 30 paquetes/año y edad superior a 60 años, la prevalencia incluso puede superar el 40%. En nuestro país esta enfermedad está infradiagnosticada, ya que sólo el 22% de los pacientes identificados en el estudio IBERPOC había sido diagnosticado previamente. Por otra parte, la EPOC representa la cuarta causa de mortalidad, con una tasa global de 33 por 100.000 habitantes, que se eleva a 176 por 100.000 habitantes en los individuos mayores de 75 años. Es causante del 10-15% del total de visitas de Atención Primaria, el 30-35% de las consultas externas de neumología y supone el 7-8% de los ingresos hospitalarios. Junto a los trastornos cerebrovasculares, la EPOC es el proceso no quirúrgico cuya atención hospitalaria genera más costes. Tratar la EPOC cuesta 3.000 millones €/año a la sanidad española (2,5% del presupuesto de Sanidad y 0,2% del PIB), por lo que supone una carga muy importante para el sistema sanitario. En Andalucía, se ha estimado que los ingresos por EPOC producen un coste mínimo de 27 millones de euros al año4.
Todos los datos expresados con anterioridad indican la importancia de un diagnóstico precoz y correcto de la enfermedad, para lo cual es indispensable la realización de espirometrías de calidad. El apoyo para dejar el tabaco sigue siendo la actuación que más incide en la evolución de la enfermedad, por lo que debemos emplear todas las posibilidades terapéuticas actualmente disponibles (incluido el apoyo psicológico y tratamiento farmacológico en los casos necesarios) para conseguir la deshabituación. Además, con las estrategias actuales de terapia farmacológica5, como después se indicará, la enfermedad puede frenarse e incluso mostrar datos de mejoría funcional con un continuado y correcto tratamiento.
En definitiva, con un correcto diagnóstico, tratamiento y seguimiento el paciente puede mejorar de forma notable su calidad de vida, que debe ser el objetivo fundamental de todas nuestras actuaciones. Para ello es fundamental una buena coordinación de los distintos niveles asistenciales, que asegure una atención sanitaria adecuada y de calidad.
DIAGNÓSTICO
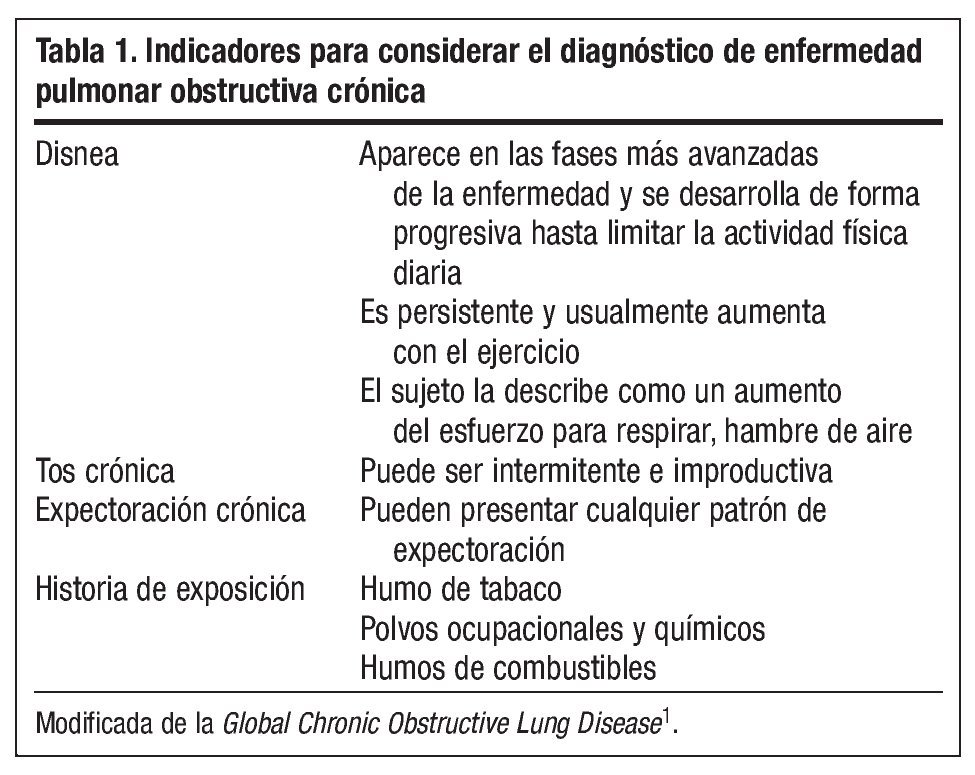
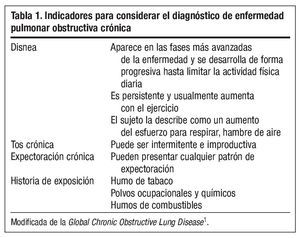
Las manifestaciones clínicas de esta enfermedad son inespecíficas. Los motivos más frecuentes para acudir a consulta son la disnea de esfuerzo o algún episodio de agudización. Por ello, el diagnóstico de EPOC se debe considerar en cualquier paciente que presente tos, aumento de la producción de esputo o disnea (tabla 1), y/o una historia de exposición a factores de riesgo de la enfermedad, principalmente el humo del tabaco6. El grado de exposición al tabaco deberá ser cuantificado mediante el cálculo del consumo acumulado medido en paquetes/año (el cálculo del consumo acumulado en paquetes/ año se realiza mediante la fórmula [cigarrillos-día/20] x años fumando). Estos síntomas por sí mismos no son diagnósticos de EPOC, pero la presencia de varios de ellos aumenta la probabilidad de padecer la enfermedad. Frecuentemente los pacientes con EPOC pueden estar asintomáticos durante mucho tiempo, incluso en la mayoría de ellos puede no haber síntomas hasta estadios avanzados de la enfermedad. Los síntomas, en cualquier caso, tienen una pobre correlación con el grado de obstrucción7,8.
La disnea es el síntoma principal y el que mayor pérdida de calidad de vida produce. En la EPOC responde a un origen multifactorial (aumento del trabajo respiratorio, hipoxemia, hipercapnia, desnutrición e hipertensión pulmonar, entre otros). La disnea es persistente, progresiva y empeora con el ejercicio, aunque es percibida de forma desigual por pacientes con igual grado de obstrucción. A medida que la función pulmonar se deteriora, la dificultad para la respiración se hace más evidente y ello hace que los sujetos soliciten atención médica. Es recomendable cuantificar el grado de disnea según la escala modificada del Medical Research Council (MRC; tabla 2)9.
La tos puede ser intermitente en el inicio, aunque más tarde aparece a diario y frecuentemente es matutina. No obstante, en algunos casos la tos y/o expectoración pueden no estar presentes, por lo que su ausencia no excluye el diagnóstico de EPOC. Las sibilancias y la opresión torácica son síntomas relativamente inespecíficos, que pueden variar en el curso de los días o incluso en el mismo día. Es importante hacer una adecuada valoración de esta opresión torácica y su diagnóstico diferencial con el dolor anginoso. En los estadios avanzados de la enfermedad son comunes la pérdida de peso, la anorexia y síntomas como depresión y ansiedad. En cuanto a la exploración física, indicar que aunque es de gran importancia en la evaluación del paciente, es de poca utilidad en el diagnóstico de la EPOC. En estadios iniciales la exploración física suele ser anodina y los signos de limitación del flujo aéreo pocas veces son patentes hasta estadios ya avanzados de la enfermedad, teniendo pues una sensibilidad y especificidad relativamente bajas7,8.
Una vez establecida la sospecha clínica, el diagnóstico debe ser confirmado mediante espirometría, que debe realizarse a todo paciente fumador con síntomas respiratorios crónicos o con un consumo acumulado de tabaco igual o superior a 20 paquetes/año. La espirometría es una prueba básica en el estudio de las enfermedades respiratorias, pero su utilidad puede verse mermada si no es realizada siguiendo unos criterios de calidad estandarizados, siendo causa de diagnósticos erróneos, visitas innecesarias al neumólogo, indicación incorrecta de otras pruebas complementarias y tratamientos mal indicados y/o innecesarios. La espirometría debe medir el volumen máximo de aire espirado de manera forzada partiendo de una inspiración máxima (capacidad vital forzada o FVC), el volumen espirado forzado durante el primer segundo de esta misma maniobra (FEV1) y debe calcularse el cociente entre estas dos variables (FEV1/FVC). Los valores espirométricos se comparan con los valores de referencia basados en la edad, la altura, el peso, el sexo y la raza.
El diagnóstico de EPOC se establece por una relación FEV1/FVC < 0,7 tras prueba broncodilatadora en un contexto clínico adecuado. Dicho diagnóstico debe realizarse en la fase estable de la enfermedad. Una prueba broncodilatadora se considera positiva si la mejora del FEV1 es superior al 12%, siempre que la diferencia sea mayor de 200 ml1,2. La prueba broncodilatadora se debe realizar con 400 μg de salbutamol o 1.000 μg de terbutalina. La espirometría es imprescindible para el diagnóstico, evaluación de la gravedad y seguimiento de la EPOC1,2.
En las fases iniciales de la enfermedad puede haber reducción leve del flujo aéreo con FEV1 dentro de los valores de referencia, reflejándose la obstrucción en la disminución de la relación FEV1/FVC. Por el contrario, en fases avanzadas puede disminuir la FVC por atrapamiento aéreo, por lo que esta relación no es un buen índice de gravedad ni es útil para el seguimiento1,2.
La EPOC debe diferenciarse de otras enfermedades que también cursan con obstrucción crónica al flujo aéreo pero que tienen una causa específica (tabla 3). La más importante a tener en cuenta es el asma crónica, no sólo por su prevalencia sino también porque en algunos pacientes ambas enfermedades pueden coexistir, no siendo posible establecer una distinción clara a partir de la clínica, las técnicas de imagen o las pruebas de función pulmonar.
Recomendaciones sobre el diagnóstico de la enfermedad:
El diagnóstico de EPOC se establece sobre la base del antecedente del consumo de tabaco y la demostración de una obstrucción al flujo aéreo no completamente reversible en fase de estabilidad clínica.
El diagnóstico de obstrucción al flujo aéreo no completamente reversible se establece con un cociente FEV1/FVC < 0,7 obtenido mediante una espirometría forzada tras prueba broncodilatadora y realizada en fase de estabilidad clínica.
Se recomienda cuantificar el consumo acumulado de tabaco en paquetes/año en todos los pacientes, siendo paquete/año = (cigarrillos-día/20) x años fumando.
Se recomienda cuantificar el grado de disnea según la escala modificada del Medical Research Council en todos los pacientes.
Recomendaciones sobre la espirometría en el diagnóstico de EPOC:
La espirometría es imprescindible para el diagnóstico de la enfermedad, la valoración del grado de gravedad y el seguimiento de los pacientes.
Debe realizarse una espirometría a todo paciente fumador con síntomas respiratorios crónicos o con un consumo acumulado de tabaco ≥ 20 paquetes/año.
Todos los centros que traten a estos pacientes deben disponer de espirómetro.
Es imprescindible que los espirómetros estén debidamente calibrados a diario.
Es imprescindible que los técnicos que realicen las espirometrías dispongan de una adecuada formación y experiencia y que dispongan del tiempo necesario para llevarla a cabo correctamente.
Se recomienda realizar una prueba broncodilatadora a todos los pacientes que estén siendo evaluados por EPOC, independientemente de los valores espirométricos basales obtenidos.
Se recomienda realizar la prueba broncodilatadora con 400 μg de salbutamol o 1.000 μg de terbutalina.
Se considera que la prueba broncodilatadora es positiva si el FEV1 experimenta un aumento relativo del 12% o superior, siempre que la diferencia sea mayor de 200 ml.
Valoración de la gravedad
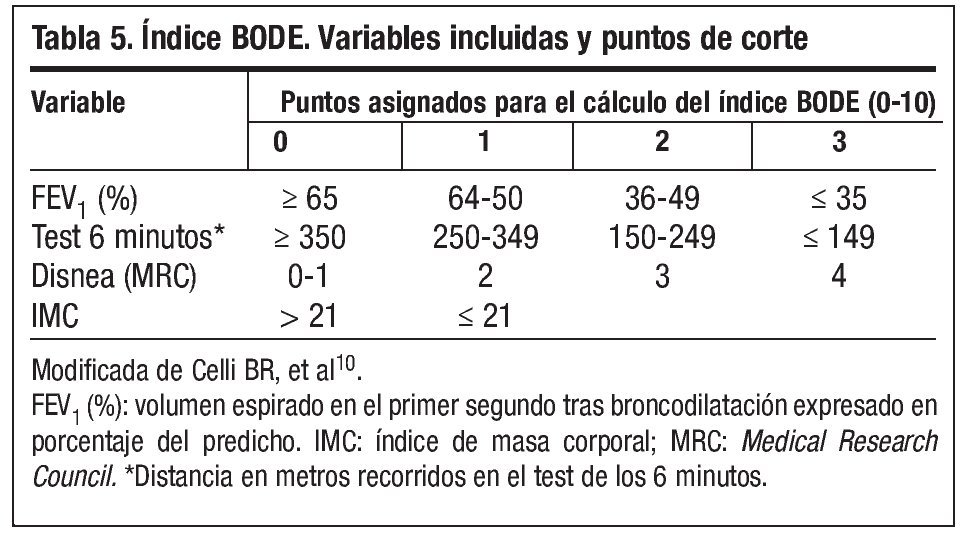
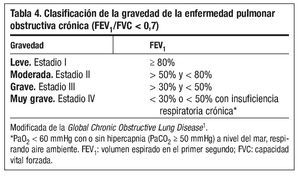
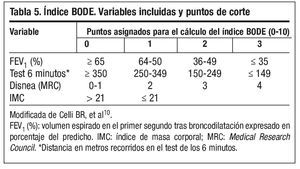
En el momento actual la gravedad de la EPOC se establece mediante la espirometría y se recomienda seguir la actual clasificación de la GOLD (Global Initiative for Chronic Obstructive Lung Disease)1 (tabla 4). Sin embargo, dado el carácter heterogéneo y sistémico de la EPOC, puede ser muy conveniente tener presentes también, además del FEV1, otras variables como el intercambio gaseoso, los volúmenes pulmonares, la percepción de los síntomas, la capacidad de ejercicio, la frecuencia de las agudizaciones, el índice de masa corporal o índices combinados como el BODE (tabla 5)10. Aunque el índice BODE ha demostrado ser un buen marcador pronóstico, por el momento no se ha incorporado en el algoritmo de toma de decisiones en el tratamiento de la EPOC, por lo que su uso está reservado para la valoración de los candidatos a trasplante y para investigación.
Recomendaciones sobre la valoración de la gravedad de la EPOC:
Se recomienda establecer el grado de gravedad de la enfermedad según el consenso GOLD 2007.
El índice BODE debe emplearse para la evaluación de los candidatos a trasplante pulmonar o en el ámbito de la investigación.
Exploraciones adicionales
Radiografía de tórax
Aunque la radiografía simple de tórax no es diagnóstica en la EPOC, es de gran valor para excluir diagnósticos alternativos, por lo que es imprescindible en la evaluación inicial.
Tomografía computarizada de tórax
No se recomienda el uso sistemático de esta técnica de imagen, excepto si se sospechan bronquiectasias o neoplasia broncopulmonar, en la valoración del enfisema y en la evaluación de pacientes subsidiarios de tratamientos quirúrgicos como la bullectomía o la cirugía de reducción de volumen pulmonar11,12.
Medición de los gases en sangre arterial
La gasometría es de gran importancia en pacientes con EPOC avanzada. Su objetivo es estadificar la gravedad de la enfermedad y establecer la indicación y control de la oxigenoterapia crónica domiciliaria. Por tanto, esta prueba debe realizarse en pacientes con un FEV1 < 50% del valor de referencia13, pacientes con síntomas o signos sugestivos de insuficiencia respiratoria o cardiaca derecha y en aquellos que presenten una saturación de oxígeno medida por pulsioximetría (SpO2) inferior al 92%2,5. Se recomienda que los centros de Atención Primaria dispongan de pulsioximetría para el control de los pacientes con EPOC.
Otras pruebas de función pulmonar
La determinación de los volúmenes pulmonares y de la difusión de monóxido de carbono es útil en el diagnóstico de enfisema y en la evaluación de pacientes en los que se ha indicado bullectomía, cirugía de reducción de volumen o trasplante pulmonar. La medida de la capacidad inspiratoria podría ser de utilidad en el futuro para la valoración y seguimiento del grado de hiperinsuflación estática del paciente con EPOC. Otras mediciones, como el flujo mesoespiratorio o el flujo pico, no tienen relevancia en la valoración funcional de la EPOC. En la evaluación rutinaria de los pacientes con EPOC tampoco se aconseja realizar estudios de la distensibilidad pulmonar ni de la función muscular respiratoria. En cuanto a las pruebas de esfuerzo, como el test de los 6 minutos, su realización estará indicada en el estudio de pacientes con disnea desproporcionada al grado de obstrucción espirométrica, para valorar la eficacia de nuevos tratamientos, en los programas de rehabilitación respiratoria, en la indicación de oxigenoterapia portátil, en la valoración del riesgo quirúrgico en la resección pulmonar, en la valoración de la capacidad laboral y en cualquier paciente con EPOC muy sintomática a pesar de tratamiento óptimo, o actividad física disminuida.
Cuestionarios de calidad de vida
La cuantificación del impacto de la enfermedad en la calidad de vida relacionada con la salud puede realizarse mediante cuestionarios genéricos o específicos. Se recomienda el uso de cuestionarios específicos, de los que existen dos en versión española14,15. Estos cuestionarios (St. George's Respiratory Questionnaire y Chronic Respiratory Disease Questionnaire) son útiles en trabajos de investigación, pero su aplicabilidad en la práctica clínica es limitada2,5.
Otras pruebas
Hemograma
Útil para la detección de anemia o poliglobulia. Se recomienda la realización de un hemograma en el diagnóstico de la enfermedad.
Alfa-1 antitripsina
Actualmente se recomienda que a todos los pacientes con EPOC se les realice, por lo menos una vez en la vida, una determinación de las concentraciones de alfa-1 antitripsina (AAT)16,17. En los casos en los que la AAT esté descendida se deberá investigar el fenotipo18.
Cultivo de esputo
Puede ser de utilidad en los pacientes con esputo purulento persistente en fase estable para caracterizar la flora bacteriana colonizante, o bien en aquellos que tengan frecuentes agudizaciones.
Electrocardiograma
Es poco sensible para valorar la presencia o gravedad de la hipertensión pulmonar, pero es útil para detectar comorbilidad cardiaca (arritmias, isquemia, etc.).
Ecocardiograma
Indicado si se sospecha hipertensión pulmonar significativa y para el estudio de comorbilidad cardiaca.
Estudios del sueño (poligrafía respiratoria/polisomnografía) Se deberá indicar su realización cuando se sospeche la coexistencia de síndrome de apnea-hipoapnea del sueño y si se evidencia poliglobulia y/o signos de insuficiencia cardiaca derecha no justificadas por el grado de afectación de la función pulmonar.
Pruebas de imagen:
La radiografía simple del tórax no es diagnóstica de EPOC en ningún caso.
A todos los pacientes en estudio por EPOC se les debe realizar una radiografía simple del tórax en proyección posteroanterior y lateral.
No se recomienda el uso de la tomografía computarizada del tórax de rutina en los pacientes con EPOC.
Se recomienda realizar una tomografía computarizada del tórax para el estudio de bronquiectasias, la valoración del enfisema, si se sospecha neoplasia broncopulmonar y en la evaluación de pacientes subsidiarios de tratamientos quirúrgicos.
Otras exploraciones funcionales:
El objetivo de la gasometría es estadificar la gravedad de la enfermedad y establecer la indicación y control de la oxigenoterapia crónica domiciliaria. Se recomienda su realización en pacientes con un FEV1 < 50%, pacientes con síntomas o signos sugestivos de insuficiencia respiratoria o cardiaca derecha y en aquellos que presenten una saturación de oxígeno medida por pulsioximetría inferior al 92%.
Todos los centros que traten a estos pacientes deben disponer de un pulsioxímetro.
Se recomienda la determinación de volúmenes pulmonares estáticos y de la capacidad de difusión del monóxido de carbono para valoración del grado de enfisema y en la evaluación de pacientes subsidiarios de tratamientos quirúrgicos.
Otras exploraciones funcionales como el flujo mesoespiratorio, el flujo pico, la medición de la distensibilidad o de la función muscular respiratoria no se recomiendan ni para el diagnóstico ni para la evaluación de la progresión de la enfermedad.
Se recomienda la realización de pruebas de esfuerzo para estudio de disnea desproporcionada al grado de obstrucción, en los programas de rehabilitación respiratoria, en la indicación de oxigenoterapia portátil, en la valoración del riesgo quirúrgico en la resección pulmonar, en la valoración de la capacidad laboral, en cualquier paciente con EPOC muy sintomática a pesar de tratamiento óptimo y en investigación.
Exploraciones adicionales:
Se recomienda el uso de cuestionarios de calidad de vida exclusivamente para investigación.
Se recomienda la realización de un hemograma a todos los pacientes que estén en evaluación de su EPOC.
Se recomienda que a todos los pacientes con EPOC se les realice, por lo menos una vez en la vida, una determinación de las concentraciones séricas de alfa1-antitripsina.
Se recomienda la realización de cultivos de esputo en aquellos pacientes que en fase estable tengan esputo purulento persistente o bien en aquellos que tengan frecuentes agudizaciones.
Se recomienda la realización de un electrocardiograma en la valoración inicial del paciente y en caso de eventos clínicos sugestivos de tener un origen cardiológico.
Se recomienda la realización de un ecocardiograma sólo en los casos en los que se sospeche hipertensión pulmonar.
Se recomienda la realización de un estudio de sueño (poligrafía respiratoria o polisomnografía) en los casos en que se sospeche un trastorno respiratorio durante el sueño.
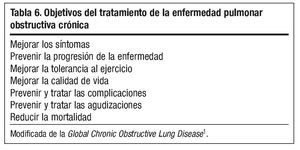
TRATAMIENTO EN FASE ESTABLE
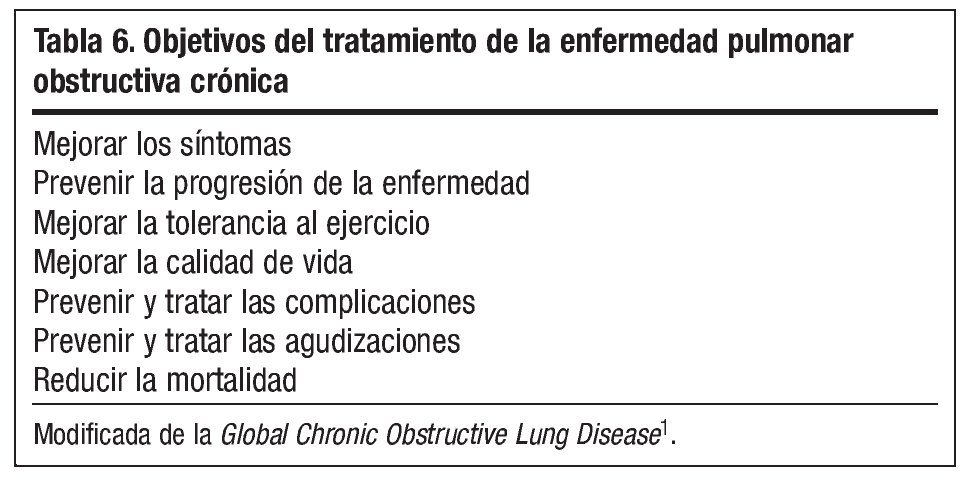
El tratamiento de la enfermedad durante los periodos de estabilidad clínica debe ser integral, progresivo y escalonado en función de los síntomas, el grado de obstrucción y la frecuencia de las agudizaciones. Los objetivos del tratamiento están resumidos en la tabla 6. Los medicamentos más útiles son los broncodilatadores, siendo la vía inhalada la de elección1. Es fundamental revisar la técnica de inhalación con todos los dispositivos que se utilicen y asegurar el uso de cámaras espaciadoras en caso de que se haya indicado tratamiento con cartuchos presurizados. El tratamiento integral de la enfermedad incluye aspectos farmacológicos y no farmacológicos, cuya importancia es equiparable con objeto de obtener beneficios en la mejoría de los síntomas, la calidad de vida y la supervivencia. Por tanto, además del tratamiento farmacológico, durante las próximas páginas se abordarán las principales recomendaciones en el tratamiento de la enfermedad, incluyendo aspectos como la deshabituación tabáquica, la rehabilitación respiratoria, la oxigenoterapia o la administración de vacunas.
Recomendaciones generales del tratamiento en fase estable:
El tratamiento debe ser integral, progresivo y escalonado en función de los síntomas, el grado de obstrucción y la frecuencia de las agudizaciones.
Los medicamentos más útiles son los broncodilatadores.
La vía inhalada es la de elección.
Es fundamental revisar la técnica de inhalación en todos los dispositivos y asegurar el uso de cámaras espaciadoras en caso de que se haya indicado tratamiento con cartuchos presurizados.
El tratamiento no farmacológico es tan importante como el farmacológico y se debe llevar a cabo en todos los pacientes.
Deshabituación tabáquica
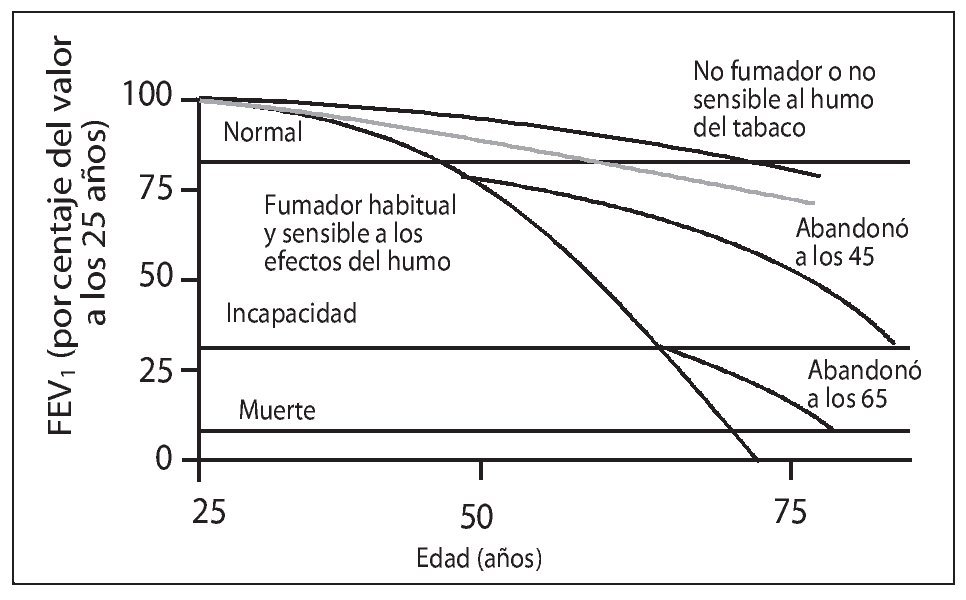
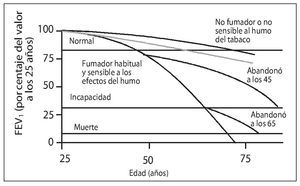
El humo del tabaco es, prácticamente, la única causa de EPOC en nuestro medio19. La deshabituación tabáquica es, en consecuencia, la medida más eficaz para evitar la aparición y la progresión de la EPOC (fig. 1)1,20-22.
Figura 1. Historia natural de la enfermedad pulmonar obstructiva crónica. FEV1: volumen espirado en el primer segundo. Modificada de Fletcher C y Peto R6.
En la actualidad no existen guías específicas para la deshabituación tabáquica en los pacientes con EPOC, por lo que se aplican las normas generales para el tratamiento del tabaquismo23,24. Aunque estas guías son aplicables a estos pacientes, es importante tener presente algunas particularidades.
En primer lugar, los pacientes diagnosticados de EPOC están más motivados para dejar de fumar25. El porcentaje de abstinencia en este grupo de fumadores es mayor que en los fumadores con espirometría normal. Por ello, es necesario plantear una estrategia de deshabituación a todos los pacientes con EPOC en el momento del diagnóstico26.
En segundo lugar, los pacientes fumadores con EPOC presentan una mayor dependencia manifestada por un mayor consumo y nivel de monóxido de carbono en el aire espirado27. Esto supone que en muchos casos sea necesaria la asociación de técnicas de abandono del tabaquismo tanto farmacológicas, como de psicoterapia, unidas a un seguimiento más estrecho.
En tercer lugar, en la EPOC se aprecia una mayor prevalencia de enfermedades psiquiátricas, sobre todo depresión, en la mayoría de los casos encubierta. Se ha demostrado que la nicotina ejerce también un efecto antidepresivo y por tanto estos enfermos con clínica depresiva asociada tienen un mayor reforzamiento del consumo, presentando un problema más en la deshabituación28. La terapia con bupropion puede ser una opción en este tipo de enfermos, siempre que no existan contraindicaciones, ya que esta molécula une a su capacidad de atenuación del síndrome de abstinencia un efecto antidepresivo.
En cuarto lugar, la comorbilidad es muy frecuente en esta patología: se observan a menudo otras enfermedades crónicas asociadas como hipertensión arterial, cardiopatía isquémica, diabetes mellitus, etc., lo que puede condicionar la elección del tratamiento de deshabituación29.
Por último, el ingreso en un hospital es un factor añadido que motiva al paciente a dejar de fumar. Los trabajos publicados sobre programas de deshabituación en pacientes ingresados demuestran un mayor porcentaje de éxito en comparación con grupos controles, siempre que se mantenga un seguimiento del paciente un mes después del alta hospitalaria30.
Métodos de deshabituación tabáquica
Las actuaciones de los médicos en este sentido tienen una gran repercusión sobre la sanidad pública. La intervención mínima es la realización de un consejo firme, serio, breve y personalizado. Con esta intervención mínima se consiguen tasas de abstinencia del 5-10%. Por este motivo, se recomienda que sea realizada en todos los pacientes con EPOC que fumen.
En una revisión sistemática publicada en la Cochrane Library se demostró la eficacia de la psicoterapia unida a medidas farmacológicas (terapia sustitutiva con nicotina) para la deshabituación de estos pacientes, siendo más eficaz la unión de psicoterapia y método farmacológico que la psicoterapia sola31. Por otra parte, Tashkin et al32 publicaron un trabajo donde se demuestra la eficacia de la terapia con bupropion en la deshabituación tabáquica de pacientes con EPOC. Recientemente ha sido aprobada la vareniclina como un nuevo medicamento para la deshabituación tabáquica. La vareniclina es un agonista parcial de los receptores nicotínicos centrales. Algunos estudios han demostrado su eficacia en la deshabituación tabáquica, con resultados incluso superiores a los conseguidos con bupropion33. Su uso en EPOC es prometedor, pero deberá estar avalado por experiencias aún no publicadas.
Recomendaciones generales para la deshabituación tabáquica:
En todos los pacientes fumadores, con EPOC, se debe hacer una intervención antitabaco mínima y ofertar además un programa de deshabituación que incluya tratamiento farmacológico.
Tratamiento farmacológico
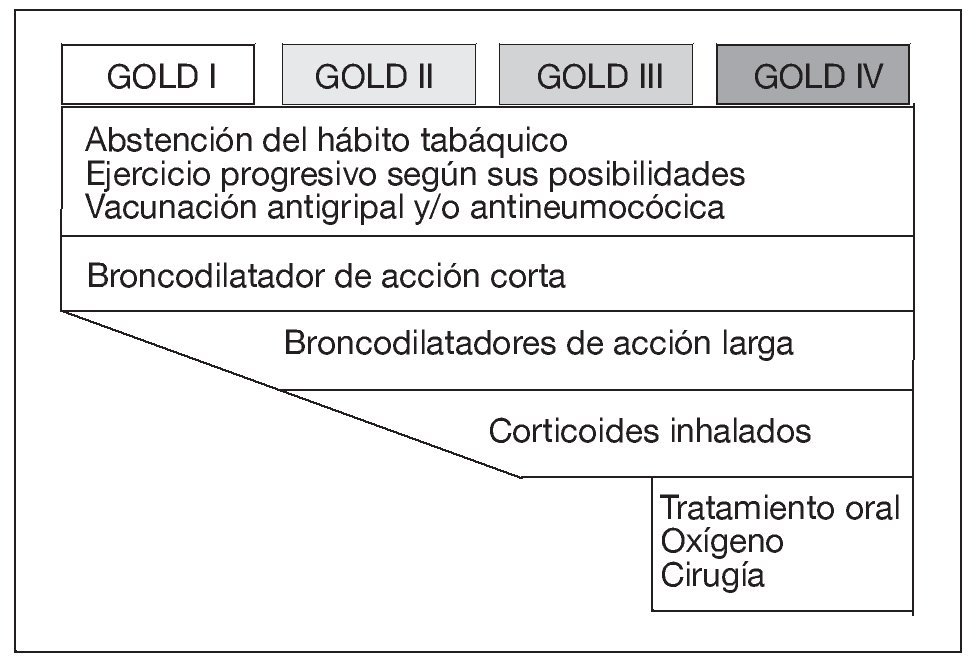
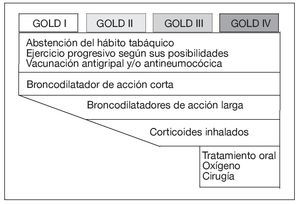
El tratamiento escalonado de la EPOC estable queda resumido en la figura 2.
Figura 2. Tratamiento escalonado de la enfermedad pulmonar obstructiva crónica estable. GOLD: Global Initiative for Obstructive Lung Disease.
Broncodilatadores de acción corta
Los broncodilatadores de acción corta han demostrado mejoría de la disnea, de la tolerancia al ejercicio y del FEV134. Son los de elección a demanda para pacientes poco sintomáticos. Los disponibles en nuestro país son salbutamol, terbutalina y bromuro de ipratropio. Los β2-agonistas tienen un inicio de acción más rápido que ipratropio, pero éste tiene un efecto más prolongado. Para la elección de cualquiera de ellos tendremos presente su pauta de administración, los efectos adversos de estos fármacos y las comorbilidades del paciente (antecedentes cardiovasculares, síntomas prostáticos avanzados). La dosis recomendada de salbutamol es 200-400 μg cada 4 a 6 horas, la de terbutalina 500 μg cada 8 horas y la de ipratropio 20-80 μg cada 6 a 8 horas.
Si no existe mejoría de los síntomas, algunas guías aconsejan realizar un ensayo de prueba con salbutamol más ipratropio35. No obstante, nuestra recomendación en este tipo de pacientes que no mejoran o con síntomas persistentes, es iniciar un tratamiento con broncodilatadores de acción prolongada.
Recomendaciones sobre broncodilatadores de acción corta:
Los broncodilatadores de acción corta (salbutamol, terbutalina y bromuro de ipratropio) están indicados en pacientes poco sintomáticos y como medicación de rescate en pacientes más graves.
Para la elección de cualquiera de ellos es necesario tener presente su pauta de administración, sus efectos adversos y las comorbilidades del paciente.
Si no existe mejoría de la clínica, se recomienda iniciar tratamiento con broncodilatadores de acción prolongada.
Broncodilatadores de acción prolongada
Los broncodilatadores de acción prolongada son más eficaces que los de acción corta36. Han demostrado que mejoran la función pulmonar, la disnea, la calidad de vida, la cumplimentación y la capacidad de ejercicio, y que disminuyen la frecuencia de agudizaciones37,38. Son de elección en pacientes con síntomas persistentes, que afectan a las actividades de su vida diaria y que no están controlados con broncodilatadores de acción corta, los cuales se deben emplear a demanda como medicación de rescate. Si el paciente está en tratamiento con tiotropio se aconseja usar β2-agonistas de acción corta como medicación de rescate39.
Algunos pacientes con obstrucción moderada-grave infravaloran sus síntomas. En estos pacientes paucisintomáticos se aconseja indicar un tratamiento con broncodilatadores de acción prolongada y realizar un seguimiento para evaluar su respuesta clínica y/o funcional antes de mantener un tratamiento a largo plazo.
Salmeterol y formoterol son β2-agonistas y el tiotropio un anticolinérgico. Tiotropio ha demostrado ser superior a ipratropio en cuanto a mejoría de función pulmonar, síntomas, calidad de vida y reducción de agudizaciones40. No hay estudios que demuestren diferencias entre los β2-agonistas de acción prolongada salmeterol y formoterol. Un reciente metaanálisis sobre ensayos clínicos que comparan salmeterol y tiotropio concluye que ambos fármacos son similares en sus efectos sobre agudizaciones, disnea y calidad de vida, aunque el beneficio en FEV1 es significativamente mayor para tiotropio41. No obstante, se requieren más estudios para confirmar esta diferencia. Por tanto, para la elección de cualquiera de ellos tendremos presente su diferente posología, sus efectos adversos y las comorbilidades del paciente.
En aquellos pacientes que persistan sintomáticos, con disnea o intolerancia al ejercicio, la asociación de ambos fármacos podría ser beneficiosa dado su diferente mecanismo de acción42, aunque los resultados de los ensayos clínicos son contradictorios. En un reciente ensayo clínico43 la asociación de tiotropio y salmeterol no demostró mejorías significativas ni en FEV1 ni en la tasa de hospitalizaciones comparada con tiotropio más placebo. Estos resultados contrastan, sin embargo, con los obtenidos en el ensayo de Van Noord et al44 en el que la adición de formoterol a tiotropio consiguió mejorías significativas, no sólo en el FEV1, sino también en la capacidad inspiratoria. Se necesitan, por tanto, nuevos ensayos clínicos para generalizar esta práctica.
Recomendaciones sobre broncodilatadores de acción prolongada:
Los broncodilatadores de acción prolongada están indicados en pacientes con síntomas persistentes, que afectan a las actividades de su vida diaria y que no están controlados con broncodilatadores de acción corta.
En los casos en los que se inicie tratamiento con broncodilatadores de acción prolongada, se deben mantener los de acción corta como medicación de rescate. Si el paciente está en tratamiento con tiotropio se aconseja usar β2-agonistas de acción corta como medicación de rescate.
En caso de pacientes paucisintomáticos con obstrucción moderada-grave se aconseja indicar un tratamiento con broncodilatadores de acción prolongada y realizar un seguimiento para evaluar su respuesta clínica y/o funcional antes de mantener un tratamiento a largo plazo.
No existen evidencias que indiquen una mayor eficacia de un grupo farmacológico frente a otro. Por tanto, para la elección de cualquiera de ellos se deben tener en cuenta su posología, sus efectos adversos y las comorbilidades del paciente.
Aunque no existen datos definitivos sobre el efecto aditivo de ambos grupos farmacológicos, en el caso de pacientes con un broncodilatador y persistencia o progresión de los síntomas, se recomienda hacer un ensayo terapéutico con dos broncodilatadores de acción prolongada de distinta familia.
Corticoides inhalados
El uso de corticoides inhalados (CI) reduce el número de agudizaciones y mejora la calidad de vida45. La evidencia obtenida de varios ensayos clínicos amplios de hasta 3 años de duración nos muestra que los CI no tienen un efecto en el declive del FEV1 en ninguno de los grados de gravedad de la enfermedad46-49. Están indicados en EPOC grave (FEV1 < 50%) con frecuentes agudizaciones (≥ 2 anuales) y en aquellos pacientes con síntomas persistentes a pesar del tratamiento combinado con broncodilatadores de acción prolongada. Tras los resultados del estudio Torch esta indicación se ampliará a EPOC con FEV1 < 60% para la combinación salmeterol-fluticasona. Actualmente no disponemos de evidencia científica para otras combinaciones de CI y broncodilatadores de acción prolongada.
Los CI nunca deben utilizarse como monoterapia en la EPOC y siempre serán añadidos al tratamiento broncodilador de base. La dosis apropiada de CI en la EPOC no ha sido definida, aunque la mayoría de los estudios se han realizado con dosis de 1.600 μg de budesonida o 1.000 μg de fluticasona al día. Actualmente no hay evidencia de que dosis menores sean eficaces. La respuesta a los CI inhalados no es uniforme y tampoco es predecible por la respuesta a glucocorticoides sistémicos o a la prueba broncodilatadora46,50. Por tanto, se recomienda emplear esas dosis, mientras no dispongamos de otros estudios.
Se ha descrito un aumento de las agudizaciones en algunos casos al retirar el tratamiento con CI51. Parece que factores como la edad, el tabaquismo activo, ser mujer o tener una prueba broncodilatadora positiva a pesar de dicho tratamiento con CI, son factores de riesgo para que aumenten las agudizaciones al retirar los CI52. Por tanto, habrá que tener especial cautela en estos casos53. Si al prescindir de ellos aumentaran las agudizaciones, se deben reintroducir de nuevo en el tratamiento.
Hoy en día existen numerosos ensayos clínicos que han demostrado que el uso de un CI combinado con un β2-agonista de acción prolongada en el mismo dispositivo de inhalación es más efectivo que administrar cada uno de los componentes de manera aislada54-58.
Aunque los CI son bastante seguros, es necesario recordar la presentación de efectos adversos locales (candidiasis y disfonía) que pueden ser reducidos mediante una correcta técnica inhalatoria y el uso de cámaras espaciadoras. Aunque los estudios sobre osteoporosis y riesgo de fracturas son discrepantes, la última revisión de la Cochrane indica que los pocos estudios que existen a largo plazo no muestran un aumento del riesgo de fractura, pero que se precisan más estudios45. En cuanto a otros efectos adversos, recientes estudios comunican una mayor frecuencia de infecciones del tracto respiratorio inferior, en especial neumonías de la comunidad59.
Recomendaciones sobre corticoides inhalados: Añadir un CI a un broncodilatador de acción prolongada está indicado en EPOC grave (FEV1 < 50%) con frecuentes agudizaciones (≥ 2 anuales) y en aquellos pacientes con síntomas persistentes. Tras los resultados del estudio Torch esta indicación se ampliará para la combinación salmeterol-fluticasona a EPOC con FEV1 < 60%. Los CI nunca deben utilizarse como monoterapia en la EPOC y siempre serán añadidos al tratamiento broncodilatador de base.
Se recomienda el empleo de CI con dosis de 1.600 μg de budesonida o 1.000 μg de fluticasona al día.
En caso de plantearse una retirada, se deben tener en cuenta factores de riesgo para una agudización como la edad, el ser fumador activo, ser mujer o tener una prueba broncodilatadora positiva a pesar del tratamiento con CI.
Otros tratamientos farmacológicos
Metilxantinas
La utilización de este grupo farmacológico ha disminuido paulatinamente desde la aparición de los broncodilatadores de acción prolongada. En general todas las recomendaciones y normativas proponen su utilización, cuando con otros broncodilatadores no se controlan los síntomas de forma adecuada1,2, siempre que al introducirlas se observe una mejoría clínica significativa sin la aparición de efectos secundarios destacables.
Mucolíticos
La utilización de fármacos mucolíticos continúa siendo bastante cuestionada, y aunque no existen evidencias concluyentes, pueden ser utilizados de forma continuada en aquellos pacientes con esputo viscoso difícil de expectorar si se constata una mejoría de dichos síntomas60,61.
Antioxidantes
La administración de N-acetil cisteína puede reducir el número de agudizaciones, sobre todo en pacientes no tratados con CI60, por lo que debe considerarse su uso en pacientes con EPOC moderada-grave en los que los CI no son prescritos por alguna razón.
Antitusígenos
Su uso de forma regular está contraindicado en la EPOC estable.
Estimulantes respiratorios
No hay evidencia de que bismesilato de almitrina y doxapran aporten ningún beneficio al tratamiento del paciente con EPOC en fase estable. Ambos fármacos pueden producir efectos secundarios neurológicos periféricos.
Recomendaciones sobre otros tratamientos farmacológicos:
El empleo de metilxantinas (teofilina, mepifilina o aminofilina) se valorará en pacientes con síntomas progresivos a pesar de un tratamiento adecuado, siempre que al introducirlas se observe una mejoría clínica significativa sin la aparición de efectos secundarios destacables.
Los mucolíticos pueden ser utilizados de forma continuada en aquellos pacientes con esputo viscoso difícil de expectorar si se constata una mejoría de dichos síntomas.
Debe considerarse el uso de N-acetil cisteína en pacientes con EPOC moderada-grave y agudizaciones frecuentes, en los que los CI no son prescritos por alguna razón.
Antitusígenos y estimulantes respiratorios no están indicados en el tratamiento de la EPOC estable.
Tratamiento de pacientes con déficit de alfa-1 antitripsina
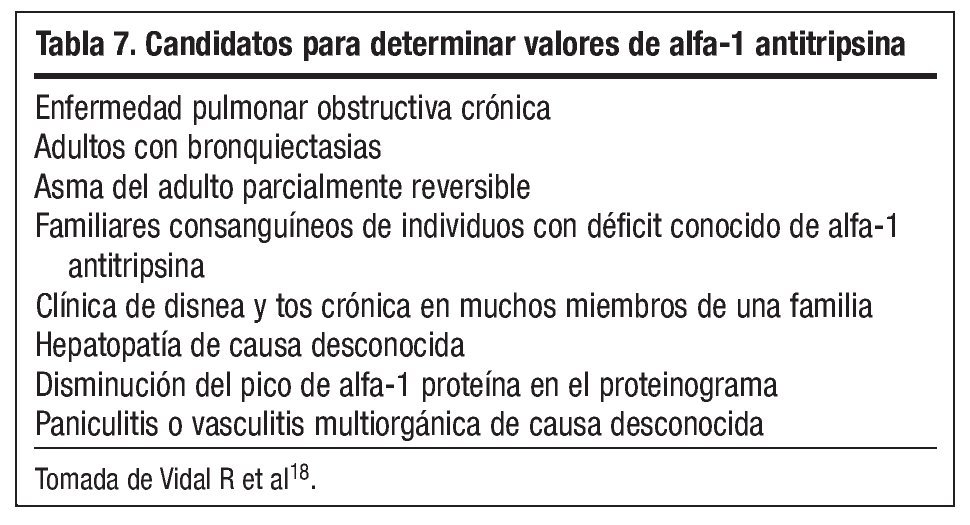
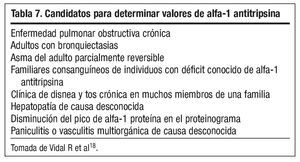
El déficit de AAT es responsable del 1-2% de todos los casos de enfisema18. Los enfermos suelen presentar síntomas habituales de la EPOC, pero de inicio más precoz, debiendo sospecharse por tanto en pacientes con una manifestación temprana de la enfermedad (tabla 7).
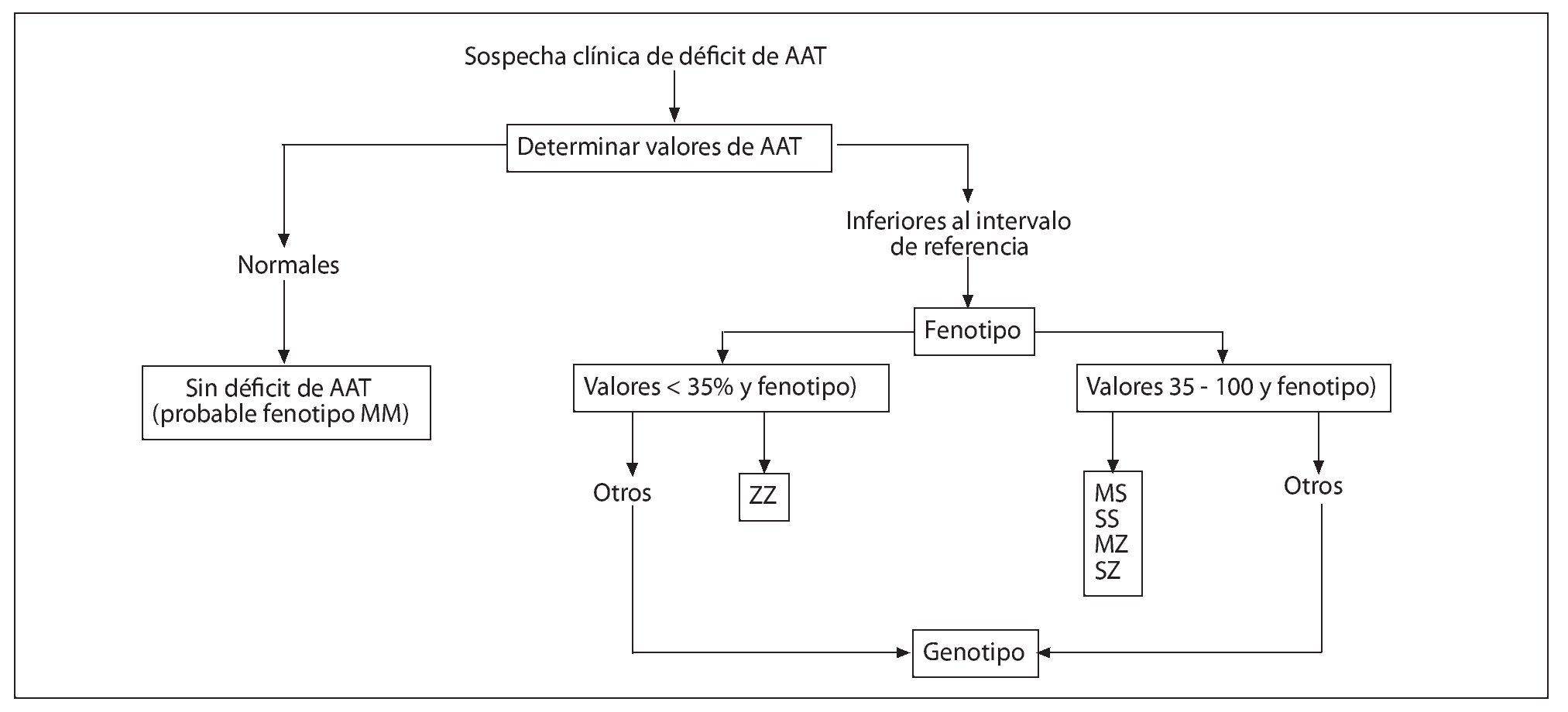
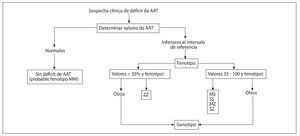
La Organización Mundial de la Salud (OMS) y las principales sociedades científicas de Neumología recomiendan la determinación del nivel sérico de AAT a todos los pacientes con EPOC al menos una vez en la vida17. En aquellos en los que estos niveles sean inferiores al intervalo de referencia se recomienda la investigación del fenotipo. El análisis molecular del gen de la AAT es el método de referencia para identificar las variantes alélicas poco frecuentes y para el estudio de los casos en los que no existe concordancia entre la concentración de AAT y el fenotipo (fig. 3).
Figura 3. Algoritmo diagnóstico en el déficit de alfa-1 antitripsina (AAT). Modificada de Vidal R et al18.
El tratamiento sustitutivo solamente está indicado en pacientes con enfisema pulmonar con déficit grave de AAT (fenotipo PiZZ o variantes raras deficitarias). En la actualidad disponemos en España de dos preparados de AAT procedente de plasma humano para su administración intravenosa: Prolastina® y Trypsone®. Aunque en la ficha técnica se recomienda el tratamiento con dosis de 60 mg/kg/semana, diversos estudios han demostrado la eficacia y seguridad de otras pautas18.
En cuanto a su efectividad, los datos que se conocen derivan de estudios comparativos de seguimiento. Estos estudios muestran una disminución significativa en la caída del FEV1 en pacientes con un FEV1 del 30-60%62,63, una reducción del 36% en la mortalidad64 y una reducción del número de agudizaciones65.
Recomendaciones sobre déficit de alfa-1 antitripsina:
Se recomienda la determinación del nivel sérico de AAT a todos los pacientes con EPOC al menos una vez en la vida y el estudio de la posible alteración genética subyacente en caso de estar disminuidos.
El tratamiento sustitutivo con AAT procedente de plasma humano está indicado sólo en pacientes con enfisema pulmonar con déficit grave de AAT (fenotipo PiZZ o variantes raras deficitarias).
Oxigenoterapia crónica domiciliaria
La oxigenoterapia crónica domiciliaria (OCD) es la única medida terapéutica, junto con la abstinencia tabáquica, que ha demostrado mejorar la supervivencia de los pacientes con EPOC. Dos estudios realizados en la década de los ochenta66,67, ratificados en una revisión Cochrane68, demostraron que la terapia con oxígeno mejoraba las expectativas de vida de los pacientes con hipoxemia crónica. Los resultados de estos estudios marcaron las directrices actuales de la oxigenoterapia como tratamiento de la EPOC.
Además de la evidencia de la supervivencia en la EPOC, la OCD ha demostrado otros efectos beneficiosos en pacientes con insuficiencia respiratoria crónica, como son la reducción de la poliglobulia y la disminución o estabilización de la hipertensión pulmonar69-71, la reducción del número y días de hospitalización72, así como efectos sobre la capacidad de ejercicio, el sueño y el rendimiento cognitivo73.
El objetivo de la oxigenoterapia es aumentar la presión parcial arterial de oxígeno (PaO2) hasta 60 mmHg en reposo, el sueño y el ejercicio, con objeto de asegurar un aporte de oxígeno adecuado a los tejidos42. Por tanto, no está indicada en pacientes con hipoxemia leve o moderada (PaO2 > 60 mmHg)74.
Las indicaciones de la OCD en la EPOC son pacientes con PaO2 < 55 mmHg o bien en aquellos con PaO2 entre 55 y 60 mmHg si existe evidencia de hipertensión pulmonar, insuficiencia cardíaca derecha o poliglobulia1,2,42.
Para conseguir los efectos clínicos deseados es necesario administrarla en dosis adecuada y durante el tiempo necesario (mínimo 15 horas al día), por lo que es esencial lograr una buena adherencia al tratamiento66,67. Las fuentes de administración de oxígeno, los dispositivos de aplicación y los riesgos de la terapia con oxígeno vienen recogidas en normativas específicas como las de la Sociedad Española de Neumología y Cirugía Torácica (SEPAR)75.
La gasometría arterial es el método de elección para establecer la indicación de OCD y debe realizarse según las normativas actuales76. La saturación arterial de oxígeno medida mediante pulsioximetría no sustituye a la gasometría a la hora de prescribir la OCD, pero puede ser un buen método para seleccionar a los pacientes candidatos a realizarse una gasometría arterial y para establecer la dosis de oxígeno necesaria, siempre y cuando se tengan en cuenta las relaciones que afectan a la curva de disociación de la hemoglobina y la relación entre saturación arterial y capilar77.
Existe controversia sobre la indicación de la OCD en situaciones de hipoxemia intermitente como la que aparece exclusivamente durante el sueño o durante el ejercicio78. Aunque en estos pacientes no se ha demostrado el efecto de la OCD sobre la supervivencia68,79, es posible que sea beneficiosa en el resto de parámetros clínicos descritos68,80. Por tanto, se recomienda iniciar OCD durante el sueño en pacientes con EPOC con más del 30% del tiempo de sueño con una SaO2 < 90% si se acompaña de hipertensión pulmonar, insuficiencia cardíaca derecha o poliglobulia, y siempre que se haya descartado un síndrome de apneashipopneas durante el sueño2. Durante la realización de ejercicio puede plantearse su indicación cuando exista desaturación menor al 92% en el test de marcha de 6 minutos, siempre y cuando se compruebe su normalización, mejoría sintomática y de la distancia recorrida en el test al repetirlo con mochila de oxígeno líquido2.
Recomendaciones sobre oxigenoterapia crónica domiciliaria:
Las indicaciones de la OCD en la EPOC son pacientes con PaO2 < 55 mmHg o bien en aquellos con PaO2 entre 55 y 60 mmHg si existe evidencia de hipertensión pulmonar, insuficiencia cardíaca derecha o poliglobulia.
Para conseguir los efectos clínicos deseados es necesario administrarla en dosis adecuada y durante el tiempo necesario (mínimo 15 horas al día), por lo que es esencial lograr una buena adherencia al tratamiento.
La gasometría arterial es el método de elección para establecer la indicación de OCD.
La pulsioximetría puede ser un buen método para seleccionar a los pacientes candidatos a realizarse una gasometría arterial y para establecer la dosis de oxígeno necesaria.
Se recomienda iniciar OCD durante el sueño en pacientes con EPOC con más del 30% del tiempo de sueño con una SaO2 < 90% si se acompaña de hipertensión pulmonar, insuficiencia cardíaca derecha o poliglobulia y siempre que se haya descartado un síndrome de apneas-hipopneas durante el sueño.
Se recomienda iniciar OCD durante el ejercicio cuando exista desaturación menor al 92% en el test de marcha de 6 minutos, siempre y cuando se compruebe su normalización, mejoría sintomática y de la distancia recorrida en el test al repetirlo con mochila de oxígeno líquido.
Ventilación mecánica no invasiva
Aunque actualmente no hay evidencias para recomendar su uso de manera generalizada en la EPOC estable81, es posible que algún grupo de pacientes se beneficie de la ventilación mecánica domiciliaria. Según el último consenso internacional disponible, la ventilación estaría indicada en los pacientes con hipercapnia diurna severa > 55 mmHg o en aquellos con hipercapnia entre 50 y 54 mmHg junto con desaturaciones nocturnas a pesar de tratamiento con oxígeno (a ≥ 2 lpm) o ≥ 2 hospitalizaciones anuales por insuficiencia respiratoria global82.
Recomendaciones sobre ventilación mecánica no invasiva en la EPOC estable:
Está indicada en los pacientes con hipercapnia diurna severa > 55 mmHg o en aquellos con hipercapnia entre 50 y 54 mmHg junto con desaturaciones nocturnas a pesar de tratamiento con oxígeno (flujo ≥ 2 lpm) o ≥ 2 hospitalizaciones anuales por insuficiencia respiratoria global.
Vacunaciones
Vacuna antigripal
La vacuna antigripal ha demostrado ser eficaz para reducir la morbilidad y mortalidad asociada a la epidemia por Influenza y los gastos sanitarios derivados de la misma. La administración anual de la vacuna antigripal reduce la mortalidad y el número de hospitalizaciones durante los periodos epidémicos, por lo que debe recomendarse a todos los pacientes con EPOC2.
La vacunación se realizará anualmente, con las cepas recomendadas por la OMS (dos cepas del tipo A y una del tipo B, detectadas el año anterior)83. La mejor época de vacunación es en octubre y noviembre, con dosis única.
Está contraindicada en caso de hipersensibilidad a proteínas del huevo o pollo, aminoglucósidos utilizados en su producción y excipientes incluidos en ella. Se recomienda aplazar la vacunación unos días si coexiste enfermedad febril o infección aguda.
Vacuna antineumocócica
La vacuna antineumocócica de 23 serotipos es eficaz en individuos inmunocompetentes para evitar la enfermedad neumocócica invasiva y la neumonía bacteriémica, recomendándose en pacientes mayores de 65 años83. En pacientes con EPOC menores de 65 años la vacuna antineumocócica ha demostrado, además, ser eficaz para prevenir las neumonías de la comunidad, sobre todo en pacientes con FEV1 < 40%84. Debe ofrecerse al paciente con EPOC de 65 o más años y a los menores de esta edad con obstrucción grave2.
La dosis es de 0,5 ml por vía intramuscular o subcutánea. Se recomienda su administración simultánea con la vacuna antigripal, pero con lugares de inoculación diferentes. El uso conjunto de ambas vacunas puede tener un efecto sinérgico y reducir las formas más graves de neumonía2.
En cuanto a la revacunación, sus indicaciones no están claras. A pesar de las restricciones que incluyen las recomendaciones de los Centers for Disease Control (CDC) en Estados Unidos, se debe recomendar tras 5 años a todos los vacunados previamente.
Otras vacunaciones
No existe suficiente evidencia para recomendar el uso de vacunas frente a Haemophilus influenzae ni de vacunas microbianas polivalentes2.
Recomendaciones sobre vacunaciones:
Se recomienda la vacunación antigripal en todos los pacientes con EPOC.
La vacuna antineumocócica debe ofrecerse al paciente con EPOC de 65 años o más y a los menores de esta edad con obstrucción grave. Se debe revacunar tras 5 años a todos los vacunados previamente.
Se recomienda la administración simultánea de las vacunas antineumocócica y antigripal, pero con lugares de inoculación diferentes.
Rehabilitación respiratoria
La disnea que padecen los pacientes con EPOC hace que los pacientes se hagan progresivamente más sedentarios. Esta falta de ejercicio, junto con otros factores, produce un decondicionamiento muscular con debilidad y pérdida de masa muscular que a su vez incrementa la sensación de disnea. Por ello, evitar el sedentarismo y estimular la actividad y el ejercicio físico cotidiano es beneficioso para romper este círculo vicioso1,2.
El entrenamiento al ejercicio mejora la disnea, la capacidad de resistencia al esfuerzo y la calidad de vida. Además, los programas de rehabilitación disminuyen la utilización de los servicios sanitarios85 y parece asociarse con una más lenta disminución de la función pulmonar y con un aumento de la supervivencia86,87. Estos efectos del entrenamiento al ejercicio han sido demostrados en numerosos ensayos clínicos recogidos en varios metaanálisis para todos los estadios de la enfermedad88-91. Por este motivo, el presente documento, junto con todas las sociedades científicas y guías de práctica clínica, recomiendan el entrenamiento de ejercicio como una parte fundamental de la rehabilitación respiratoria y del tratamiento de la enfermedad1,2,92. En concreto, la rehabilitación respiratoria debería ofertarse a todos los pacientes que tras un tratamiento farmacológico óptimo sigan limitados por síntomas.
En los programas de rehabilitación suelen distinguirse distintos componentes, que con frecuencia se utilizan combinados. Factores como el grupo muscular entrenado, la duración del programa, así como la frecuencia e intensidad de las sesiones, son determinantes para conseguir el efecto deseado.
El componente más validado es el entrenamiento muscular a resistencia que incluya ejercicio de extremidades inferiores, en general en bicicleta ergométrica o tapiz rodante91,92.
Las evidencias de la utilización aislada de la rehabilitación aeróbica de extremidades superiores son menos manifiestas, pero parece razonable incorporarla al programa de entrenamiento de miembros inferiores, realizándose en estos casos con bicicleta de brazos o pequeños pesos93.
Los programas basados en entrenamiento a fuerza pueden ser una alternativa válida en estos pacientes con buenos resultados y tolerancia94. Incluso programas mixtos, a fuerza y resistencia, pueden tener efectos más completos fisiológicamente y pueden ser la estrategia más adecuada para estos pacientes95. Aunque programas más prolongados consiguen mejores efectos, se recomienda que la duración mínima del programa sea entre 8 y 12 semanas. Los beneficios de un programa de rehabilitación se mantienen durante varios meses; sin embargo, se recomienda que estos pacientes mantengan una actividad física adecuada una vez concluido el mismo. La ubicación para la realización de estos programas puede ser variada. Actualmente se han desarrollado programas completos de rehabilitación respiratoria en el hospital, programas de ejercicio en el domicilio con visitas periódicas al hospital o exclusivamente en el domicilio. Los programas en el hospital ofrecen una supervisión directa y adaptación a cada caso. Los programas domiciliarios pueden ser una opción importante para mantener las mejorías conseguidas, haciendo que los pacientes integren el ejercicio en su vida cotidiana, y conseguir un mayor alcance de la rehabilitación respiratoria con costes mucho menores96,97.
La elección entre estas posibilidades dependerá de los recursos disponibles. Siempre que sea posible se remitirá al paciente a un centro con programas de rehabilitación completos. En caso contrario, cualquiera de las otras opciones es también válida. Si no es posible ninguna, al menos se le recomendará al paciente que haga ejercicio de manera regular y progresiva como forma sencilla de rehabilitación respiratoria con objeto de evitar el sedentarismo y favorecer el ejercicio físico cotidiano, o simplemente andar a diario puede ser beneficioso y debería recomendarse de forma general a todos los pacientes con EPOC98.
Recomendaciones sobre rehabilitación respiratoria:
La rehabilitación respiratoria debería ofertarse a todos los pacientes que tras un tratamiento farmacológico óptimo sigan limitados por síntomas.
La duración mínima debe ser de 8-12 semanas, con un entrenamiento que incluya, al menos, entrenamiento a resistencia de miembros inferiores añadiendo, si es posible, los miembros superiores y el entrenamiento a fuerza.
El tipo de programa (hospitalario, ambulatorio o mixto) debe ser el más completo posible, dentro de las posibilidades de cada centro.
Independientemente de las posibilidades de programas de rehabilitación existentes en cada centro, a todos los pacientes se les debe recomendar ejercicio diario y progresivo según sus posibilidades.
Educación del paciente con enfermedad pulmonar obstructiva crónica
La educación del paciente con EPOC constituye un elemento fundamental de la rehabilitación respiratoria y del tratamiento de la EPOC. El paciente debe conocer la enfermedad que padece, aprender las habilidades sobre el manejo del tratamiento y adoptar una actitud participativa para afrontar su enfermedad99. Los programas de educación tienen que ser individualizados y estar dirigidos al paciente y también a la familia, con unos contenidos que abarquen, al menos, los siguientes aspectos:
1) Aspectos relevantes sobre su enfermedad.
2) Medidas para aliviar sus síntomas.
3) Tabaquismo activo y pasivo y contaminación ambiental.
4) Actividad física y nutrición.
5) Reconocimiento precoz de las agudizaciones y medidas a realizar.
6) Conocimiento de los dispositivos y técnica inhalatoria.
7) Oxigenoterapia y ventilación domiciliaria.
8) Conocimientos de los recursos de la comunidad.
La intervención educacional corresponde a todos los profesionales implicados en la atención a estos pacientes. En este sentido recomendamos incluir la educación de pacientes con EPOC en las consultas de enfermería.
Recomendaciones sobre educación:
La educación del paciente con EPOC constituye un elemento fundamental de la rehabilitación respiratoria y del tratamiento de la EPOC.
Los programas de educación tienen que ser individualizados y estar dirigidos al paciente y también a la familia, incluyendo los contenidos definidos en el presente consenso.
La intervención educacional corresponde a todos los profesionales implicados en la atención a estos pacientes.
Nutrición
La pérdida de peso contribuye a una disminución de la tolerancia al esfuerzo y al empeoramiento de la calidad de vida, siendo un indicador pronóstico de morbimortalidad demostrado. Por el contrario, la obesidad aumenta la hipoventilación y disminuye la capacidad de ejercicio. Por estos motivos, es necesario mantener un peso y un estado nutricional dentro de unos límites razonables.
Es recomendable realizar una evaluación del estado nutricional en la EPOC al diagnóstico y durante su seguimiento. Se recomienda la medida del índice de masa corporal (IMC) como parámetro de mayor utilidad (rango normal entre 22 y 27).
En los casos de pérdida de peso no justificada, o si el IMC está por debajo de 22 kg/m2, será preciso evaluar de forma detallada la ingesta habitual de alimentos. Lo más racional es conseguir que los pacientes realicen una dieta equilibrada para mantener un peso adecuado. Si persiste la alteración, se debe remitir al especialista correspondiente.
Recomendaciones sobre nutrición:
Es recomendable realizar una evaluación del estado nutricional en la EPOC al diagnóstico y durante su seguimiento.
Se recomienda la medida del IMC como parámetro de mayor utilidad.
Tratamiento quirúrgico
En los pacientes con EPOC muy grave la cirugía (bullectomía, cirugía de reducción de volumen y trasplante pulmonar) puede mejorar la tolerancia al esfuerzo, la función pulmonar, la disnea y la calidad de vida relacionada con la salud. Ello requiere una adecuada selección de los pacientes.
Bullectomía
Está indicada en pacientes con FEV1 > 40%, FVC normal o ligeramente disminuido cuando las bullas ocupan más de un tercio del hemitórax correspondiente, comprimen el tejido pulmonar adyacente o el paciente tiene una disnea progresiva. Es preciso señalar que las recomendaciones están basadas en estudios no controlados100. Otras indicaciones son la abscesificación de la bulla, hemoptisis grave o neumotórax persistente.
Cirugía de reducción de volumen pulmonar
La cirugía de reducción de volumen pulmonar (CRVP) consiste en la resección de las regiones pulmonares con mayor destrucción de tejido pulmonar. Con ello se pretende facilitar que el resto del parénquima se expanda mejorando la fuerza de retracción elástica y el intercambio gaseoso. Puede ser una alternativa al trasplante pulmonar en pacientes muy seleccionados.
La CRVP se indica en pacientes con enfisema de distribución heterogénea y de predominio en lóbulos superiores que tienen baja tolerancia al esfuerzo y con FEV1 y capacidad de difusión del pulmón para el monóxido de carbono (DLCO) > 20%. En este grupo este proceder quirúrgico mejora la supervivencia a los 4 años, la tolerancia al ejercicio y la calidad de vida. La CRVP no aporta beneficio si el enfisema es homogéneo, no predomina en lóbulos superiores o presenta un FEV1 o DLCO < 20%101.
Trasplante pulmonar
El objetivo del trasplante es mejorar la supervivencia. Además, ha demostrado que puede mejorar la calidad de vida, la tolerancia al esfuerzo, la función pulmonar y el intercambio gaseoso.
El trasplante pulmonar debe ser considerado únicamente en pacientes con EPOC muy grave, con deterioro progresivo a pesar de un tratamiento médico óptimo que incluya el abandono del tabaco, tratamiento broncodilatador, oxigenoterapia y rehabilitación. La actual normativa de trasplante recomienda derivar a un paciente para trasplante cuando tenga un BODE > 5. La indicación de trasplante está establecida actualmente con índice BODE ≥ 7 o bien tener un BODE inferior con uno de los siguientes: una historia de hospitalizaciones por fracasos respiratorios hipercápnicos severos, hipertensión pulmonar, cor pulmonaleo ambos a pesar de OCD, una función pulmonar con FEV1 < 20% junto con difusión < 20% o bien una distribución homogénea del enfisema102.
Recomendaciones sobre tratamiento quirúrgico:
La bullectomía está indicada en pacientes con FEV1 > 40%, FVC normal o ligeramente disminuido cuando las bullas ocupan más de un tercio del hemitórax correspondiente, comprimen el tejido pulmonar adyacente o el paciente tiene una disnea progresiva.
La cirugía de reducción de volumen pulmonar se indica en pacientes con enfisema de distribución heterogénea y de predominio en lóbulos superiores que tienen baja tolerancia al esfuerzo y con FEV1 y DLCO > 20%.
La actual normativa de trasplante recomienda derivar a un paciente para trasplante cuando tenga un BODE > 5.
La indicación de trasplante está establecida actualmente con índice BODE ≥ 7 o bien tener un BODE inferior con uno de los siguientes: una historia de hospitalizaciones por fracasos respiratorios hipercápnicos severos, hipertensión pulmonar, cor pulmonale o ambos a pesar de OCD, una función pulmonar con FEV1 < 20% junto con difusión < 20% o bien una distribución homogénea del enfisema.
AGUDIZACIONES DE LA ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
Una agudización de la EPOC (AEPOC) es un evento en el desarrollo natural de la enfermedad, que conlleva un cambio agudo en la situación clínica basal del paciente más allá de la variabilidad diaria, que cursa con aumento de la disnea, de la expectoración, purulencia del esputo, o cualquier combinación de estos tres síntomas y que precisa un cambio en el tratamiento103.
Las AEPOC se han relacionado con un deterioro en la calidad de vida del paciente, y el número de agudizaciones sufridas influye en el pronóstico de la enfermedad104, por lo que su prevención y tratamiento constituyen uno de los objetivos del tratamiento de la EPOC (tabla 6).
Las causas más frecuentes de AEPOC son:
1) Infecciones (50-70%), de las que las bacterias constituyen alrededor del 60%. Fundamentalmente se aíslan Haemophilus influenzae, Streptococcus pneumoniae, Moraxella catarrhalis y Chlamydia pneumoniae. En pacientes con EPOC grave y frecuentes agudizaciones la infección puede estar causada por Pseudomona aeruginosa. Los virus constituyen el 40% restante.
2) Otras causas (30-50%) que se han relacionado son: factores ambientales, polución atmosférica, inadecuado tratamiento o incumplimiento del mismo, toma de sedantes, etc. Hasta en un tercio de los casos la causa no puede ser identificada.
Existen otros procesos patológicos que pueden simular una agudización pero que no deben ser definidos como tales, entre los que se incluyen: neumotórax, insuficiencia cardíaca, cardiopatía isquémica, tromboembolismo pulmonar, arritmias, anemia y neoplasia pulmonar, entre otros1,2.
Diagnóstico de la agudización de la enfermedad pulmonar obstructiva crónica
El diagnóstico de la AEPOC es clínico. El síntoma más importante es el aumento de la disnea, que puede ir acompañada de aumento de tos y expectoración o de cambios en la coloración del esputo. Dentro del proceso diagnóstico es importante valorar la gravedad de la AEPOC, sin embargo no existe una clasificación unánime para la gradación de la severidad de la misma. En la valoración de la severidad de la AEPOC lo más importante es decidir si su gravedad es de suficiente entidad como para derivarla a un centro de urgencias o si puede ser tratada de forma ambulatoria. Para tomar esta decisión se deben considerar los criterios de gravedad resumidos en la tabla 8. De esta manera, se puede considerar la gravedad de la agudización según el consenso ATSERS (American Thoracic Society-European Respiratory Society)42:
1) Leve, aquella que no presenta criterios de gravedad y que por tanto puede ser manejada ambulatoriamente.
2) Moderada-grave, la que presenta criterios de gravedad y por tanto precisa de atención por un Servicio de Urgencias.
3) Grave, la que precisa ingreso hospitalario.
4) Muy grave, la que precisa ingreso en Unidad de Cuidados Intensivos (UCI).
En la valoración de la gravedad es importante tener presente algunas circunstancias que deben hacernos estar alerta por ser factores de riesgo para presentar criterios de gravedad, como las resumidas en la tabla 9. Además de la presencia de criterios de gravedad, aquellas AEPOC que precisen descartar otras enfermedades responsables del empeoramiento o en las que haya una imposibilidad de tratar la enfermedad en el domicilio deberán ser remitidas a un centro hospitalario.
En las AEPOC leves sin criterios de gravedad habitualmente no es necesario realizar ninguna exploración complementaria. En aquellas que presenten algún criterio de gravedad y sean por tanto remitidas a un Servicio de Urgencias es necesario realizar los siguientes estudios complementarios:
1) Hemograma: existencia de poliglobulia, anemia o leucocitosis.
2) Bioquímica: alteraciones hidroelectrolíticas, de las enzimas hepáticas o cardiacas, hiperglucemia o dímero-D (sospecha de tromboembolismo pulmonar).
3) Radiografía de tórax: útil para descartar neumonía, neumotórax, etc.
4) Electrocardiograma: útil para evaluar signos de sobrecarga aguda o crónica de cavidades derechas, arritmias o isquemia.
5) Gasometría arterial: imprescindible en las agudizaciones graves y siempre que la SpO2 sea inferior a 92%.
6) Cultivo de esputo: indicado en pacientes con antecedentes de ingreso hospitalario previo, tratamiento antibiótico en los últimos tres meses o antecedentes de colonización o infección por microorganismos no habituales o con factores de riesgo para ello.
Recomendaciones sobre el diagnóstico de la AEPOC:
El diagnóstico de la AEPOC es clínico. Dentro del proceso diagnóstico es importante valorar los criterios de gravedad, con objeto de decidir si la AEPOC debe derivarse a un centro de urgencias o puede ser tratada de forma ambulatoria.
Las AEPOC leves sin criterios de gravedad habitualmente no precisan realizar ninguna exploración complementaria.
Dentro del hospital es necesario realizar al menos: analítica general, radiografía del tórax, electrocardiograma y gasometría arterial. Además, se debe realizar un cultivo de esputo en determinadas circunstancias resumidas en el texto.
Tratamiento de la agudización de la enfermedad pulmonar obstructiva crónica
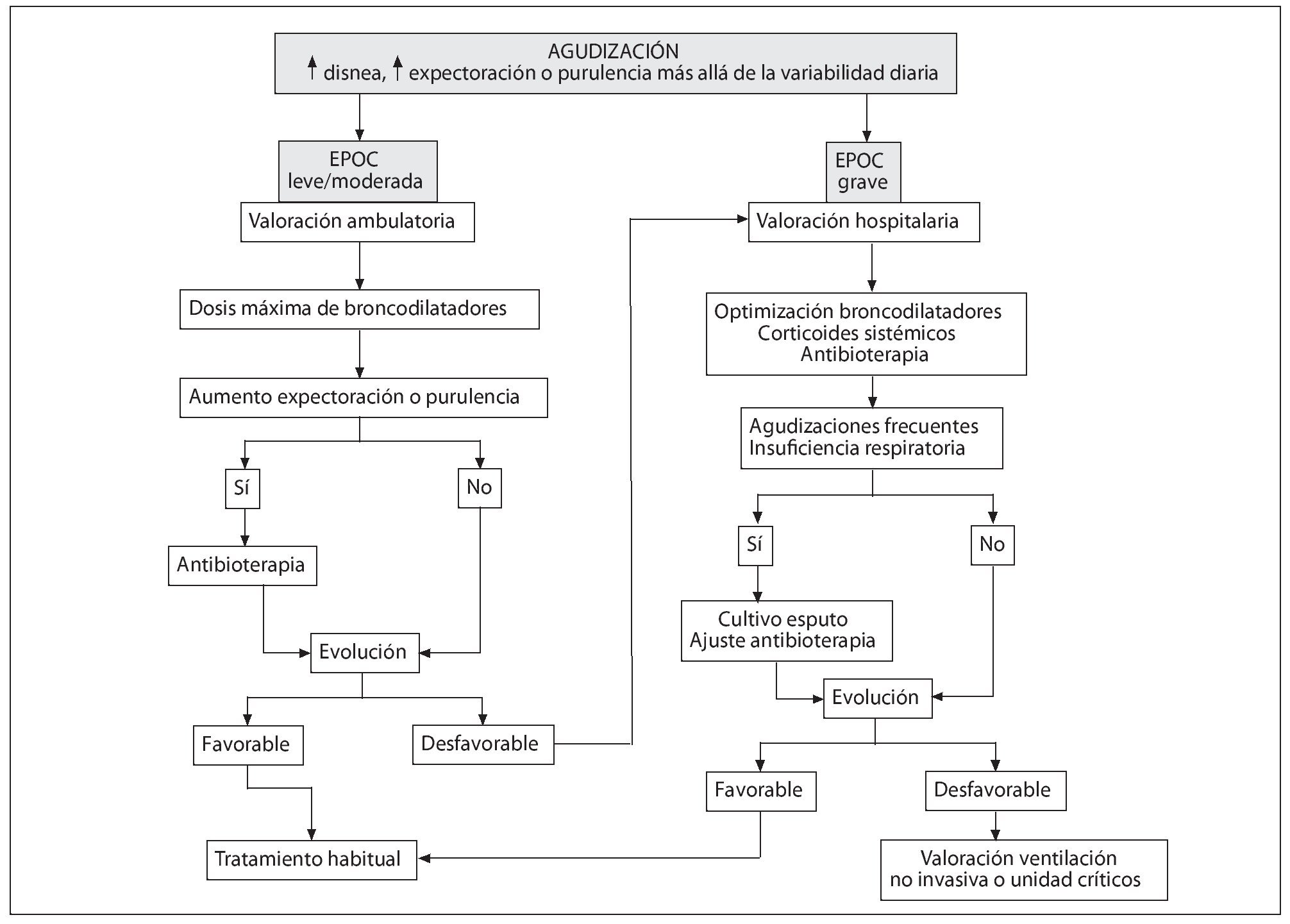
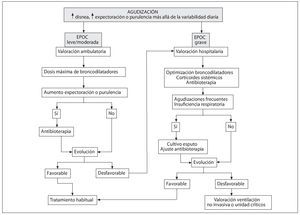
El algoritmo de tratamiento de la AEPOC queda resumido en la figura 42. En el caso de AEPOC leves o moderadas que se traten de forma ambulatoria deben ser reevaluados tras 48-72 horas para decidir si se debe o no remitir al paciente a un centro hospitalario o si precisa algún cambio en el tratamiento1,2.
Figura 4. Algoritmo de manejo de la agudización de la enfermedad pulmonar obstructiva crónica. Modificada de SEPAR-ALAT2.
Criterios de alta hospitalaria y propuesta de seguimiento
En caso de precisar ingreso hospitalario el alta se puede considerar siempre que el paciente presente estabilidad clínica, no necesite medicación intravenosa, sea capaz de manejar su enfermedad en el domicilio y tenga la mejor gasometría posible. Existen alternativas de altas precoces que se acompañan de programas de atención domiciliaria o consultas de atención rápida con resultados satisfactorios105. El paciente deberá realizar controles estrechos por su dispositivo de Atención Primaria que permitan, entre otros, el control del descenso de los corticoides sistémicos y las complicaciones asociadas como cambios en la glucemia y las cifras tensionales y el uso correcto del tratamiento de su enfermedad, con especial cuidado en la duración del tratamiento antibiótico, la cumplimentación y técnica del tratamiento inhalado y la oxigenoterapia. La primera revisión por el neumólogo se hará como máximo a los 15 días tras el alta en pacientes con EPOC grave-muy grave, con frecuentes agudizaciones y/o reingresadores. Cuando el paciente requiera oxigenoterapia domiciliaria al alta, la gasometría arterial deberá ser repetida en situación clínica estable, no antes de dos meses después del alta, para determinar si es candidato a oxigenoterapia crónica domiciliaria.
La hospitalización a domicilio en pacientes seleccionados (sin insuficiencia respiratoria, sin comorbilidades graves, con buen soporte familiar y con pH normal) puede disminuir las visitas a urgencias y los costes sanitarios. No obstante, la generalización de esta modalidad asistencial en estos pacientes requiere de más estudios y de una organización sanitaria específica y estructurada para ello106.
Tratamiento broncodilatador en la agudización de la enfermedad pulmonar obstructiva crónica
La primera opción farmacológica en la AEPOC debe ser la intensificación del tratamiento broncodilatador. Para esto se suelen emplear broncodilatadores de acción corta y se aumenta la dosis y la frecuencia de las inhalaciones. Por lo general, los β-2 agonistas de acción corta son los más usados por su rapidez de acción107. Sin embargo, no existe suficiente evidencia en cuanto a diferencias en la eficacia broncodilatadora entre éstos y los anticolinérgicos108. En cuanto a la asociación de ambos broncodilatadores, aunque no hay evidencias disponibles de sus beneficios adicionales108, es frecuente su asociación y se recomiendan especialmente en AEPOC con criterios de gravedad o con respuesta incompleta inicial, por sus efectos sinérgicos en cuanto a su acción broncodilatadora.
En lo referente a los sistemas de inhalación, se deben emplear cartuchos presurizados con cámara espaciadora, ya que la eficacia de éstos frente a la terapia nebulizada no ha demostrado ser diferente109. No obstante, en aquellos pacientes con criterios de gravedad, especialmente los pacientes muy taquipneicos, es preferible emplear terapia nebulizada durante las primeras horas para garantizar un adecuado depósito del fármaco.
La terapia nebulizada se suele administrar mediante nebulizadores neumáticos con oxígeno o con aire. El uso de uno u otro gas dependerá del estado del intercambio gaseoso del paciente. Aunque el breve espacio de tiempo que dura la nebulización no ha demostrado empeorar la situación clínica del paciente, algunos autores prefieren emplear aire o nebulizadores ultrasónicos en caso de insuficiencia respiratoria hipercápnica.
Corticoides
Los corticoides sistémicos han demostrado ser beneficiosos en el tratamiento de la AEPOC. Acortan el tiempo de recuperación, mejoran la función pulmonar, reducen el riesgo de recidiva y la estancia hospitalaria. Por esto, se deben administrar a todos los pacientes con criterios de gravedad o con FEV1 < 50%. En la AEPOC leve/moderada se recomienda su uso si existe hiperreactividad bronquial o cuando la evolución inicial no es favorable. La dosis recomendada es entre 30 y 40 mg/día de prednisona o equivalente durante 7-10 días1.
La vía de administración puede ser intravenosa u oral y no se han encontrado diferencias significativas en el pronóstico de la AEPOC entre ambas110. No obstante, en los pacientes ingresados suelen administrarse por vía intravenosa durante los primeros días por la comodidad de tener un acceso venoso garantizado.
Diversos estudios apuntan a que los corticoides inhalados pueden ser una alternativa en pacientes que no los estén tomando previamente y presenten agudizaciones leves-moderadas, sin acidosis respiratoria111. Sin embargo, son necesarios más estudios que evalúen esta opción terapéutica.
Antibioterapia
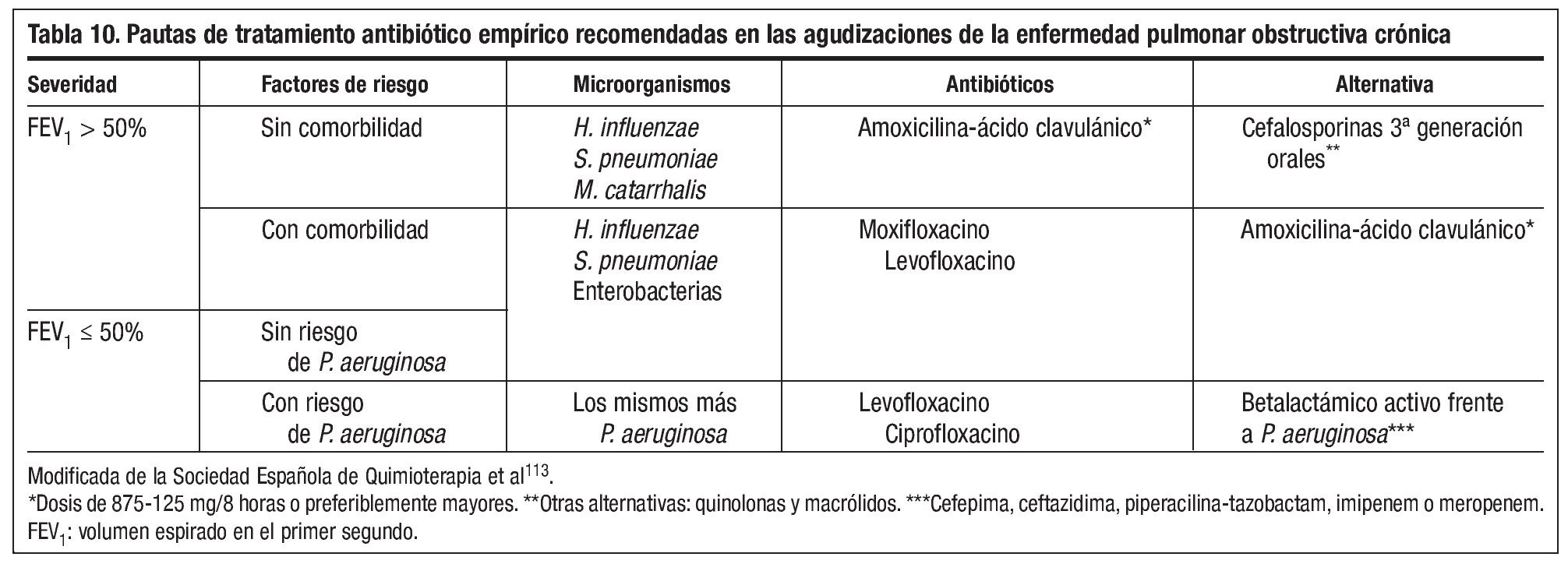
No todas las AEPOC son de causa bacteriana y por tanto no tienen necesariamente que ser tratadas con antibióticos112. Los antibióticos están indicados en aquellos pacientes que presenten la tríada de aumento de la disnea, aumento del volumen del esputo y purulencia del mismo, o bien en aquellos con dos de estos síntomas, siempre que uno sea la purulencia del esputo. Además, también se administra en aquellas AEPOC graves que requieran ventilación mecánica1.
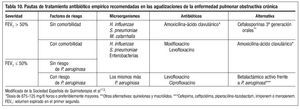
La elección del antibiótico se basará en la gravedad de la EPOC, la existencia de comorbilidades, los patrones de resistencia bacteriana de la zona, los efectos secundarios y el riesgo de participación de Pseudomona aeruginosa (hospitalización reciente, administración de antibióticos en los tres últimos meses o en más de cuatro ocasiones en el último año, colonización crónica por Pseudomona aeruginosao aislamiento en agudización previa). La elección del tratamiento antibiótico queda resumida en la tabla 10113. La duración y las dosis del tratamiento antibiótico dependerán del agente elegido, pero suele ser entre 7-10 días.
Metilxantinas
No se recomienda el uso sistemático de metilxantinas en las AEPOC ya que no ejercen mayor efecto broncodilatador que los broncodilatadores de acción corta y su uso conlleva riesgo de importantes efectos secundarios1,2. Pueden ser usados en pacientes que no han tenido una respuesta favorable al tratamiento con otros fármacos broncodilatadores y siempre en el medio hospitalario114.
Oxigenoterapia
El objetivo de esta terapia es garantizar una adecuada oxigenación a los tejidos, por lo que se debe administrar a pacientes en AEPOC moderadas-graves en situación de insuficiencia respiratoria.
Se recomienda su administración mediante mascarillas tipo Venturi ya que proporcionan una fracción inspiratoria de oxígeno estable. En general, se consigue con FiO2 entre el 24 y 28%, suficiente para alcanzar una PaO2 superior a 60 mmHg o SpO2 superior a 92%.
Se recomienda realizar una nueva gasometría a los 30-60 minutos de instaurado el tratamiento, para valorar la situación del intercambio gaseoso, especialmente el grado de retención de CO2 y acidosis respiratoria. Esta valoración tiene que ser realizada mediante gasometría arterial en todos los casos. En caso de presentar depresión respiratoria se deberá evaluar al paciente para ver si procede ajustar la dosis de oxígeno o instaurar ventilación mecánica no invasiva.
En caso de que el paciente ya presente insuficiencia respiratoria crónica en fase estable, la administración de oxigenoterapia seguirá las mismas pautas, prestando especial atención al pH durante la evaluación.
Una vez queel paciente esté más estable y el pH sea normal, la oxigenoterapia puede ser administrada con gafas nasales y controlarse mediante pulsioximetría.
Ventilación mecánica no invasiva
La ventilación mecánica no invasiva es una modalidad de soporte ventilatorio que ha demostrado mejorar la supervivencia, disminuir la estancia y reducir el número de intubaciones en los pacientes con AEPOC en situación de insuficiencia respiratoria global con acidosis respiratoria. Estos beneficios los ha demostrado al aplicarse tanto en la UCI como en la planta de hospitalización convencional115.
Está indicada en pacientes con AEPOC grave que presenten insuficiencia respiratoria global con acidosis respiratoria a pesar de un tratamiento correcto de la AEPOC116.
La ventilación mecánica no invasiva no es un sustituto de la ventilación invasiva, por lo que está contraindicada si el paciente requiere esta última, salvo que se hayan desestimado maniobras de resucitación invasivas.
La modalidad más empleada es la ventilación a presión positiva limitada por dos niveles de presión (BIPAP)117. Para su aplicación es necesario contar con los recursos materiales y humanos necesarios, siendo indispensable un personal con el conocimiento, el tiempo y la experiencia suficientes para garantizar su éxito y evitar sus complicaciones118.
Recomendaciones sobre el tratamiento de la AEPOC:
En el caso de AEPOC leves sin criterios de gravedad deben ser tratadas de forma ambulatoria como primera opción y reevaluadas tras 48-72 horas.
En caso de ser ingresado por una AEPOC, el alta se puede considerar siempre que el paciente presente estabilidad clínica, sea capaz de manejar su enfermedad en el domicilio y tenga la mejor gasometría posible.
Tras el alta el paciente deberá realizar controles estrechos por su dispositivo de Atención Primaria.
La primera revisión por el neumólogo se hará como máximo a los 15 días tras el alta en pacientes con EPOC grave-muy grave, con frecuentes agudizaciones y/o reingresadores.
Recomendaciones sobre el tratamiento farmacológico de la AEPOC:
La primera opción farmacológica en la AEPOC debe ser la intensificación del tratamiento broncodilatador.
Aunque no existe evidencia sobre la distinta eficacia de los fármacos broncodilatadores, por lo general los β2-agonistas de acción corta son los más usados por su rapidez de acción.
Se recomienda asociar distintos broncodilatadores de acción corta en AEPOC con criterios de gravedad o con respuesta incompleta inicial.
Los cartuchos presurizados con cámara espaciadora han demostrado ser igual de eficaces que la terapia nebulizada. Ésta se recomienda en pacientes con criterios de gravedad, especialmente en aquellos muy taquipneicos.
Los corticoides sistémicos se deben administrar a todos los pacientes con criterios de gravedad o con FEV1 < 50%. En la AEPOC leve/moderada se recomienda su uso si existe hiperreactividad bronquial o cuando la evolución inicial no es favorable. La dosis recomendada es 30-40 mg/día de prednisona o equivalente durante 7-10 días.
No se recomienda el uso sistemático de metilxantinas en las AEPOC.
No todas las AEPOC son de causa bacteriana y por tanto no tienen necesariamente que ser tratadas con antibióticos.
Los antibióticos están indicados en aquellos pacientes que presenten la tríada de aumento de la disnea, aumento del volumen del esputo y purulencia del mismo, o bien en aquellos con dos de estos síntomas, siempre que uno sea la purulencia del esputo. Además, también se administra en aquellas AEPOC graves que requieran ventilación mecánica.
La elección del antibiótico se basará en la gravedad de la EPOC, la existencia de comorbilidades, los patrones de resistencia bacteriana de la zona, los efectos secundarios y el riesgo de participación de Pseudomonas aeruginosa.
Recomendaciones sobre oxigenoterapia y ventilación no invasiva en la agudización de la EPOC:
La oxigenoterapia se debe administrar en pacientes en AEPOC moderada-grave en situación de insuficiencia respiratoria.
En la fase aguda, se recomienda su administración mediante mascarillas tipo Venturi ya que proporcionan una fracción inspiratoria de oxígeno estable.
Una vez instaurada, se recomienda realizar una nueva gasometría a los 30-60 minutos de instaurado el tratamiento, para valorar la situación del intercambio gaseoso.
La ventilación mecánica no invasiva está indicada en pacientes con AEPOC grave que presenten insuficiencia respiratoria global con acidosis respiratoria a pesar de un tratamiento correcto y que no presenten ninguna contraindicación.
Para su aplicación es necesario contar con los recursos materiales y humanos necesarios, siendo indispensable un personal con el conocimiento, tiempo y experiencia suficientes para garantizar su éxito y evitar sus complicaciones.
Es necesario establecer una adecuada monitorización que sea constante durante las primeras horas y hacer un control gasométrico tras las primeras horas de ventilación.
Uno de los indicadores pronósticos más importantes es la respuesta a la misma durante las primeras horas119, por lo que es necesario establecer una adecuada monitorización que sea constante inicialmente y hacer un control gasométrico tras las primeras horas de ventilación.
SEGUIMIENTO DEL PACIENTE CON ENFERMEDAD PULMONAR OBSTRUCTIVA CRÓNICA
La atención y seguimiento de estos pacientes es una responsabilidad compartida entre Atención Primaria y neumología, siendo fundamental la comunicación y coordinación entre ambos niveles asistenciales (fig. 5). Para ello sería conveniente la utilización de protocolos consensuados, en donde además del médico, esté implicado el personal de enfermería, y se recojan los objetivos de seguimiento de la EPOC1 (tabla 6).
Figura 5. Relación entre neumología y Atención Primaria en el seguimiento de la enfermedad pulmonar obstructiva crónica (EPOC). Modificada de SEPAR-ALAT2
Las actividades en el seguimiento del paciente con EPOC quedan recogidas en la tabla 11. El seguimiento clínico del paciente con EPOC leve puede efectuarse correctamente en Atención Primaria, siendo recomendable consultar con el neumólogo para excluir otras patologías, reforzar el cese del hábito tabáquico, tratar las complicaciones, optimizar el tratamiento o para indicar tratamientos más complejos en pacientes con EPOC grave (tabla 12)2.
No existen datos que nos permitan establecer un orden cronológico de pruebas complementarias y controles1. Se recomienda realizar al menos una valoración clínica y funcional anual a todos los pacientes con EPOC con objeto de evaluar la progresión de la enfermedad y valorar posibles cambios de tratamiento. Estos controles deberán ser más estrechos conforme la enfermedad vaya avanzando y aparezca mayor limitación por síntomas, más agudizaciones y deterioro de la función pulmonar. En Andalucía, el Proceso Asistencial Integrado sobre EPOC ha establecido unas normas sobre la periodicidad del seguimiento que se recogen en la tabla 13120.
Recomendaciones sobre el seguimiento de los pacientes:
La atención y seguimiento de estos pacientes es una responsabilidad compartida entre Atención Primaria y Neumología, siendo fundamental la comunicación y coordinación entre ambos niveles asistenciales.
Se recomienda realizar al menos una valoración clínica y funcional anual a todos los pacientes con EPOC con objeto de evaluar la progresión de la enfermedad y valorar posibles cambios de tratamiento.
Este Documento de Consenso ha sido publicado en NEUMOSUR. 2008;20(3):146-74.
*Documento elaborado por la Asociación de Neumólogos del Sur (NEUMOSUR), Sociedad Andaluza de Medicina Familiar y Comunitaria (SAMFyC) y Sociedad Española de Médicos de Atención Primaria en Andalucía (SEMERGEN-Andalucía). Con la colaboración de Boehringer.