La enfermedad de Mondor es una vasculopatía benigna, poco conocida, que fue descrita como tal por el cirujano Henri Mondor en 19931. Su incidencia oscila entre el 0,5-0,8%, incluyendo solo pacientes sintomáticos1,2, desde el primer caso diagnosticado por Fagge en 1869 se han descrito unos 500 casos en el mundo3,4. Afecta predominantemente a mujeres entre 21-55 años3,5, presentando un 5% de recurrencia.
En la actualidad, la etiología aún es desconocida. Los factores predisponentes se han relacionado con traumatismos locales (p. ej., procedimientos quirúrgicos en la mama, radiación, electrocución o golpes)4,6,7; fármacos intravenosos (p. ej., vasoconstrictores), esfuerzos físicos intensos, sexo vigoroso después de un periodo de abstinencia, procesos febriles, compresión de vasos sanguíneos (p. ej., uso de ropa ajustada o vendajes constrictivos), cáncer de mama (12,7%), enfermedades sistémicas (p. ej., sepsis por Rickettsias o estafilococos coagulasa positivos, linfangitis, polimialgia reumática, arteritis de células gigantes, hepatitis C, estados de hipercoagulabilidad, neoplasias y otras condiciones fisiológicas como embarazo y puerperio)4,5.
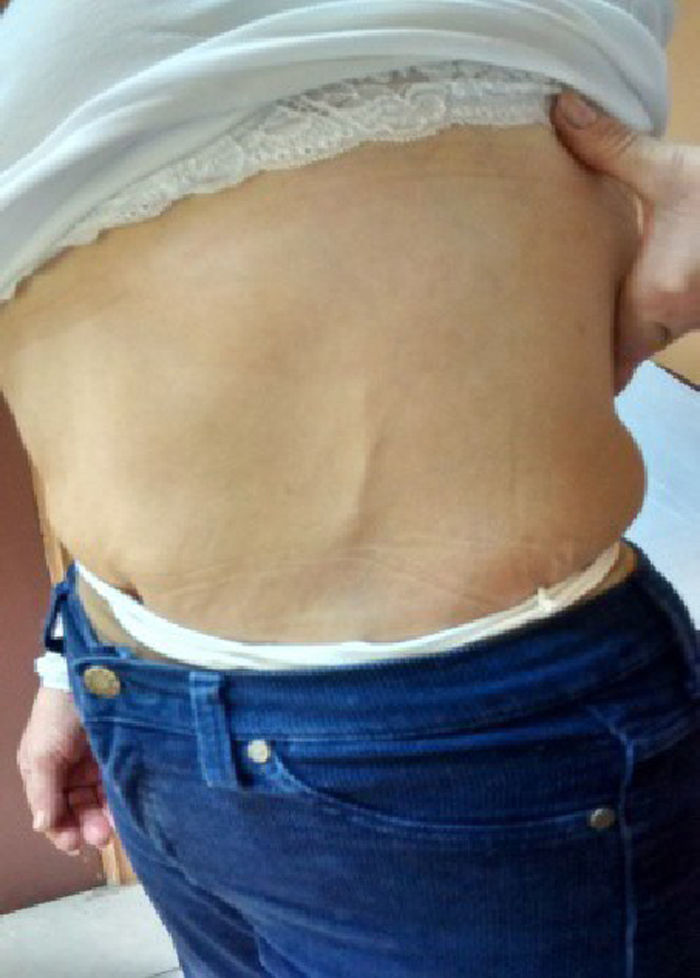
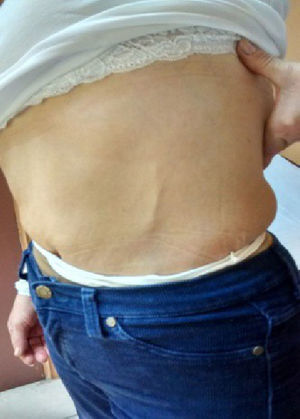
El cuadro clínico se caracteriza por la aparición brusca de dolor en la mama, en la pared antero-lateral del tórax o en ambas zonas, en relación con la aparición de un cordón subcutáneo que corresponde a la vena afectada, habitualmente la torácica lateral o toracoepigástrica, que puede extenderse hacia la pared abdominal en la región epigástrica4. Este cordón (fig. 1), visible y doloroso al tacto, puede ser acompañado de eritema, edema o retracción. Raras veces la palpación puede ser indolora. Se han descrito otras áreas afectadas como la región cervical posterior, axilar, fosa antecubital, región inguinal y región peneana (por compromiso de la vena dorsal)6.
Habitualmente evoluciona de forma espontánea a la curación entre 2-4 semanas. Durante este tiempo pasa por etapas histológicas consecutivas: a) formación del trombo, sin obliteración de la luz, con células inflamatorias y fibrina; b) organización del trombo, con fibroblastos elongados y fibrina; c) generación de múltiples áreas pequeñas de recanalización del trombo y, finalmente, d) vena recanalizada, con pared fibrosada. En un pequeño porcentaje la evolución es hacia la cronicidad, apareciendo pequeñas necrosis cutáneas sobre la zona de la vena trombosada5-8.
DiagnósticoEl diagnóstico se realiza principalmente mediante el interrogatorio clínico y el examen físico, en el cual se observa un cordón lineal en la región afectada2.
Se puede corroborar mediante los siguientes exámenes de imágenes:
- 1.
Mamografía: permite evaluar la masa palpable. El principal hallazgo es el aumento en la densidad tubular, que puede ser confundida con una dilatación ductal y que corresponde a la vena trombosada2,5.
- 2.
Ecografía simple: el vaso con trombosis aparece como una estructura larga, anecoica, localizada superficialmente, con una apariencia «rosariada»2.
- 3.
Ecografía Doppler: mediante este examen se observan vasos subcutáneos dilatados, con disminución o ausencia del flujo sanguíneo venoso y, en casos agudos, puede aparecer un trombo6,7.
A nivel histopatológico se observa en la pared del vaso un infiltrado inflamatorio y la formación de un trombo que lo ocluye, generándose un cordón duro. La inmunohistoquímica permite confirmar el origen venoso, con presencia de anticuerpos monoclonales CD31 y CD348.
Diagnóstico diferencialDebido a que el diagnóstico se lleva a cabo principalmente mediante la anamnesis del paciente, es importante descartar otras enfermedades con signos o síntomas parecidos5,7,8. Se deben excluir cuadros de hipercoagulabilidad, como antitrombina III, déficit de proteína S o C, y la presencia de anticuerpos anticardiolipinas. También se debe descartar la existencia de enfermedades linfáticas mediante inmunohistoquímica, la que informa resultados negativos para el marcador policlonal LYVE1 y el monoclonal D2408.
Otros diagnósticos diferenciales son: rotura de fibras musculares, angeítis subaguda o debido al uso de drogas, poliarteritis nodosa, infección por larva migrans y enfermedad de Ackerman, caracterizada por artritis y lesiones cutáneas con placas infiltradas y cordones eritematosos que constituyen el signo de la cuerda8,9.
TratamientoLa enfermedad de Mondor es una enfermedad autolimitada y su tratamiento es sintomático5,7. Dentro de las medidas generales está indicado el uso de calor local en la zona afectada10. En la mayoría de los casos, la enfermedad evoluciona espontáneamente hacia la curación en un periodo de hasta 6 semanas, sin requerir tratamiento10. Pero en otros casos puede evolucionar a la cronicidad, con pequeñas necrosis cutáneas sobre la vena trombosada7,8, en estos casos se indican analgésicos y antiinflamatorios no esteroideos entre 5-7 días, asociados a un corticoide de depósito, la mezcla más usada es dipropionato de betametasona 5mg y betametasona, como fosfato de sodio 2mg. Se espera la respuesta terapéutica entre 4-6 semanas7.
Se puede considerar una intervención quirúrgica, como es una trombectomía o una resección venosa superficial en el caso de que el paciente presente alguna malignidad, dolor severo, retracción o persistencia de la enfermedad posterior al tratamiento9.
Finalmente, es importante recordar que los antibióticos y anticoagulantes no están indicados2,9.
Caso clínicoPaciente mujer de 58 años, con antecedentes de varices en ambas extremidades inferiores, artritis reumatoide en etapa I inactiva, hipertensión arterial crónica en tratamiento con losartán 50mg/día. Consultó por un cuadro de 3 días de evolución, caracterizado por la aparición de un cordón solevantado vertical de 5cm de largo en la zona anterolateral izquierda del abdomen. Al examen físico era doloroso a la palpación superficial, sin signos de infección, ni inflamación, ni adenopatías adyacentes. Se observaban, además, 3 cordones de iguales características localizados en la cara anterior de la pierna derecha de un largo no superior a los 3cm. La paciente no presentaba conflicto hemodinámico, ni compromiso sistémico. Se realizaron exámenes generales que incluyeron hemograma, perfil bioquímico, perfil hepático, función renal y pruebas de coagulación que incluían protrombina y tiempo parcial de tromboplastina, las cuales no evidenciaron alteraciones. Además, se realizaron marcadores reumatológicos, anticuerpos antinucleares (ANA), antígenos extractables nucleares (ENA), anticoagulante lúpico y anticardiolipinas que también fueron negativos, a excepción de ANA 1/80 patrón moteado.
Fue la ecografía de partes blandas, la que demostró la existencia de una tromboflebitis superficial de la rama tributaria de la vena tóraco-epigástrica izquierda, en la interfase dermo-hipodérmica. Consistente en una estructura tubular hipoecogénica de aproximadamente 1,5mm de diámetro, no compresible y sin flujo vascular detectable al estudio Doppler, rodeado por un tenue halo hiperecogénico en las partes blandas adyacentes. El examen fue realizado con un transductor lineal de alta resolución. Se inició tratamiento sintomático con meloxicam 15mg/vía oral, por el periodo de un mes. Se efectuó control a los 15 días de tratamiento, evidenciando disminución del grosor de los cordones y ausencia del dolor. Al mes del tratamiento fue dada de alta.
DiscusiónEn nuestro caso hubo un factor que podría ser decisivo en la expresión clínica del síndrome de Mondor, como es el uso habitual de ropa ajustada. De este modo se descartó que la causa fuera idiopática como ocurre en el 50% de ellos y que coincide con lo planteado por Peña-Irún. Por otra parte, todos los estudios generales se informaron en rango de normalidad, lo que permitió excluir estados de hipercoagulabilidad y neoplasias, hipótesis de trabajo que debieron ser consideradas por la edad de la paciente.
Resultó determinante el rol del estudio imagenológico para confirmar la sospecha diagnóstica.
Finalmente, la paciente era portadora de artritis reumatoide, cuadro sistémico que la literatura ha asociado a síndrome de Mondor. Es esta condición la que permite relacionar el resultado de los ANA positivo, patrón moteado, con la génesis de un síndrome de Sjögren en curso.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.