Valorar la interpretación de ApnealinkTM® (AL) por médicos de atención primaria (MAP), y la alcanzada mediante poligrafía respiratoria (PGR) en la Unidad de Sueño Hospitalaria (USH) en pacientes con alta probabilidad de síndrome de apnea e hipopnea del sueño (SAHS).
MétodosSe recogen aleatoriamente, durante tres meses, pacientes seleccionados en USH para estudio mediante PGR, con elevada probabilidad de SAHS que aceptaron repetir estudio mediante AL. La USH corregía la PGR según normativa SEPAR; el MAP corregía el AL y planteaba manejo. Se analizaron los pacientes con estudios válidos(tiempo registro ≥ 240 min) para ambos dispositivos, comparándose resultados. Se consideró el estudio AL automático y corregido, considerando un índice de desaturación de oxihemoglobina (ODI) al 4% (ODI 4%), (AL 4%) y al 3% (ODI 3%), (AL 3%). Cuando ODI 4% era ≥ 12/h, se estableció diagnóstico SAHS moderado/grave, suponiendo un IAH ≥ 15/h. Para interpretar AL con ODI 3% y tratamiento, se siguieron criterios SEPAR. Se compararon los resultados para las mismas variables del AL frente a PGR.
ResultadosSe incluyeron 43 pacientes válidos para AL, 45 para PGR y 41 válidos para ambos estudios. El estudio AL 4% mostró 27 (62,8%) positivos (OR 5,5, p < 0,05), que el AL 3% corroboró con IAH ≥ 15/h. La PGR detectó 19 (42,2%) con IAH ≥ 15/h; el AL 3% detectó 31 (72%). El análisis del AL 4% y AL 3% comparado con PGR no mostró diferencias de diagnóstico o manejo.
Se compararon los resultados para las mismas variables del AL frente a PGR.
ConclusionesExiste equivalencia entre las decisiones del MAP y la USH. El AL sería un buen método diagnóstico de SAHS en atención primaria, en pacientes seleccionados con alta probabilidad de SAHS.
To assess diagnosis and therapeutic decisions-making by General Practitioners (GP) using ApnealinkTM® (AL) in patients with high suspicion of obstructive sleep apnea (OSA), in comparison with conclusions of Hospital Sleep Unit (HSU) specialists based on home respiratory polygraphy (PGR) results.
MethodsThis study involved patients previously selected by HSU for sleep testing by PGR. After it, patients were offered to complete AL test. PGR was checked at HSU; AL was checked by hemoglobin desaturation index of 4% (4% ODI), (4% AL) and 3% (3% ODI) patients with positive test to proceed with CPAP; and those with negative test for further testing. Automatically adjusted 4% AL, was considered valid as it was demonstrated to be equivalent to manual AL. Results were compared by automatically adjusted 3%AL against PGR results.
Results48 patients were collected. 43 had AL valid test, 45 had PGR valid study, and 41 had both valid test. 27 patients (62,8%) had positive 4% AL (OR 5,51, p < 0,05), that showed AHI ≥ 15/h at 3% AL test; and 19 patients (42,2%) had a positive PGR test. 31 (72%) patients had a positive 3% AL. AL had shown to be a good screening method of SAHS.
ConclusionsThere is equivalence between the decisions of GP and HSU. AL is a good diagnostic tool and screening method for OSA in primary care when it is used in patients with high suspicion of moderate-severe OSA.
El síndrome de apneas e hipopneas durante el sueño (SAHS) se caracteriza por la presencia de episodios repetidos de obstrucción de la vía aérea superior (VAS), debido al colapso de las partes blandas durante el sueño, reduciendo la cantidad de oxígeno arterial y produciendo múltiples despertares inconscientes que ocasionan un sueño no reparador. Aparece un cuadro de hipersomnolencia, trastornos cognitivo-conductuales, neuropsiquiátricos, respiratorios, cardíacos, metabólicos o inflamatorios1. Es una enfermedad relevante, aunque infradiagnosticada, con consecuencias negativas sobre la salud, para la que existe tratamiento1. Comporta elevado riesgo de accidentabilidad, demostrado riesgo cardiovascular, conllevando un exceso de mortalidad y un elevado impacto económico en la población que representa un problema fundamental de salud pública1–5. Tiene alta prevalencia en población general. En España, la prevalencia en adultos es de 5-7 millones (4-6% en hombres; 2-4% en mujeres, aumentando en la menopausia1). Se estima que 1.200.000-2.150.000 sufren un grado severo, siendo subsidiarios de tratamiento. Solo están diagnosticados y tratados el 5-9%2.
La terapia incluye recomendaciones generales (cambio de hábitos, pérdida ponderal, evitar tóxicos), cirugía y dispositivos de estabilización que persiguen evitar el colapso de la VAS. La administración de presión positiva continua (CPAP) en la VAS es el tratamiento más eficaz para el SAHS. Mejora el control de comorbilidades cardiovasculares (hipertensión [HTA], insuficiencia cardíaca, arritmias, cardiopatía isquémica e ictus) y reduce el exceso de mortalidad secundaria2,6,7.
El diagnóstico requiere valoración clínica confirmada con la presencia de alteración del patrón respiratorio durante el sueño, mediante estudios diagnósticos. Existen cuatro tipos8 de estudios diagnósticos: tipo I, polisomnografía completa vigilada (PSGv), dispositivo de siete o más canales realizada bajo supervisión; tipo II, polisomnografía completa no vigilada (PSGnv); tipo III, dispositivos con cuatro a siete canales, como la poligrafía respiratoria (PGR); y tipo IV, dispositivos de diagnóstico simplificado con uno a tres canales, incluyendo pulsioximetría, como el dispositivo ApneaLink™Air® (AL).
Los criterios diagnósticos y gravedad del SAHS se basan en el número promedio de eventos respiratorios (apneas, hipopneas y esfuerzos respiratorios asociados a microdespertares [ERAM]) por hora de sueño. Se considera diagnóstico de SAHS cuando el índice de alteración respiratoria (IAR) es ≥ 5 eventos/h. Se considera leve (IAR 5-15/h), moderado (IAR 15-29/h) o grave (IAR ≥ 30/h)9. La prueba gold-standard es la PSGv, pero su menor disponibilidad, relativa complejidad y elevados costes condicionan su acceso. La alta prevalencia del SAHS y sus consecuencias clínicas, hacen necesario considerar otros métodos diagnósticos simplificados como alternativas a la PSG en pacientes seleccionados10,11 y la necesidad de colaboración entre la Unidad de Sueño Hospitalaria (USH) y médicos de atención primaria (MAP).
Los casos de SAHS moderado-grave tienen mayor grado de desorden respiratorio, mayor frecuencia, gravedad sintomatológica y mayor evidencia de asociación a patología cardiovascular, con una clara evidencia de respuesta favorable al tratamiento con CPAP2.
El objetivo fue comparar la interpretación diagnóstica y actitud terapéutica realizada por los MAP, a partir de los resultados obtenidos mediante el dispositivo AL y los obtenidos mediante PGR realizada por la USH en una muestra de pacientes con alta probabilidad de SAHS.
MétodosEl proyecto fue aprobado por el Comité de Ética e Investigación Clínica del centro hospitalario de referencia, conforme lo establecido en la Ley de Investigación Biomédica 14/2007 del 3 de julio. Se realizó un estudio descriptivo, transversal, desarrollado por un equipo formado por tres investigadores especialistas en medicina familiar y comunitaria pertenecientes al equipo de atención primaria (MAP), los neumólogos de la USH y el Servicio de Estadística y Epidemiología (SEE).
ParticipantesPoblación, tamaño muestral y selección de la muestra. Se estableció una muestra de conveniencia de hasta cincuenta pacientes reclutados aleatoriamente de la población de pacientes en estudio por USH, a los que se había indicado completar estudio de sueño mediante PGR domiciliaria.
Criterios de inclusión y exclusión. Se incluyen pacientes con edad ≥ 18 años con clínica moderada-alta de SAHS (Epworth ≥ 10 y/o roncopatía y/o apneas) e indicación de PGR por USH.
Se excluyeron pacientes con problemas cognitivos o dificultades en el aprendizaje del uso del dispositivo AL, pacientes con enfermedad obstructiva crónica (EPOC) grave (volumen espiratorio forzado en un segundo/capacidad vital forzada [FEV1/CVF] < 70% y FEV1 < 50% del valor predicho), embarazadas, pacientes ya diagnosticados de SAHS o en tratamiento con CPAP u oxigenoterapia, y aquellos que rehusasen participar.
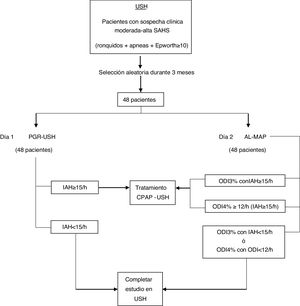
IntervenciónSe reclutaron entre marzo-junio 2018. Los investigadores MAP acudieron por turnos en días aleatorios y alternos a la consulta de enfermería de USH. Durante esta primera visita (día 1), enfermería adiestraba y entregaba el dispositivo PGR al paciente; seguidamente, el investigador MAP informaba sobre el presente estudio ofreciendo la realización del estudio AL al día siguiente. Si aceptaban, se entregaba un documento informativo (Apéndice A) y el consentimiento informado (Apéndice B).
Al día siguiente (día 2), cuando el paciente devolvía la PGR, los investigadores le entregaban el AL, lo adiestraban en su uso y entregaban un documento ilustrado de soporte, creado por los investigadores. Se les asignaba un código de anonimización (ID).
Al siguiente día (día 3), devolvían el AL a los investigadores. Los registros se repartieron de manera aleatoria entre los investigadores MAP para su interpretación. Los investigadores MAP recibieron adiestramiento básico para el uso del dispositivo e interpretación de los registros.
Los registros AL y PGR eran válidos cuando la duración era ≥ 240 min. Los investigadores MAP desconocían el manejo diagnóstico-terapéutico del SAHS propuestos por la USH y viceversa.
Dispositivos diagnósticosLa USH realizó el estudio de sueño domiciliario con dispositivo tipo III mediante PGR, modelo Embletta-GOLD-5.1® del programa Remlogic-E-2.0 de la compañía ResMed (San Diego, CA, Estados Unidos), que dispone de seis canales (flujo nasal por presión, esfuerzo torácico y abdominal, pulsioximetría con Nonin Medical Inc. (Plymouth, MN, Estados Unidos), frecuencia cardíaca, posición corporal y ronquido).
Los investigadores MAP realizaron estudio de sueño con dispositivo tipo IV, ApneaLink™Air®-versión 0.20 de la compañía ResMed y software basado en la AASM-2013-v2.0.112 con tres canales: flujo nasal por presión, pulsioximetría mediante dispositivo Nonin Medical Inc. y banda de esfuerzo torácico.
Análisis de los estudios ALLos AL fueron analizados por los investigadores MAP con lectura automática (ALA) y manual (ALM), mediante el software del equipo AL basado en la AASM-2013-v.2.0.112 y análisis de la pulsioximetría con desaturaciones al 4 y al 3%, que define: apnea: caída del flujo ≥ 90% durante ≥ 10 s que pueden ser obstructivas, mixtas o centrales. Hipopnea:1A: caída del flujo ≥ 30% y < 90% seguida de desaturación del 3% y duración ≥ 10 s; y 1B: caída del flujo ≥ 30% y < 90% seguida de desaturación al 4% y duración ≥ 10 s.
Análisis de los estudios PGRLas PGR fueron interpretadas por la USH, según normativa de la Sociedad Española de Neumología y Cirugía Torácica (SEPAR)9, que define la apnea como caída del flujo ≥ 90%; y la hipopnea como la caída del flujo ≥ 30% y < 90%, seguida de desaturación al 3% y duración ≥ 10 s. El análisis se realizó de manera automática con revisión posterior por el neumólogo.
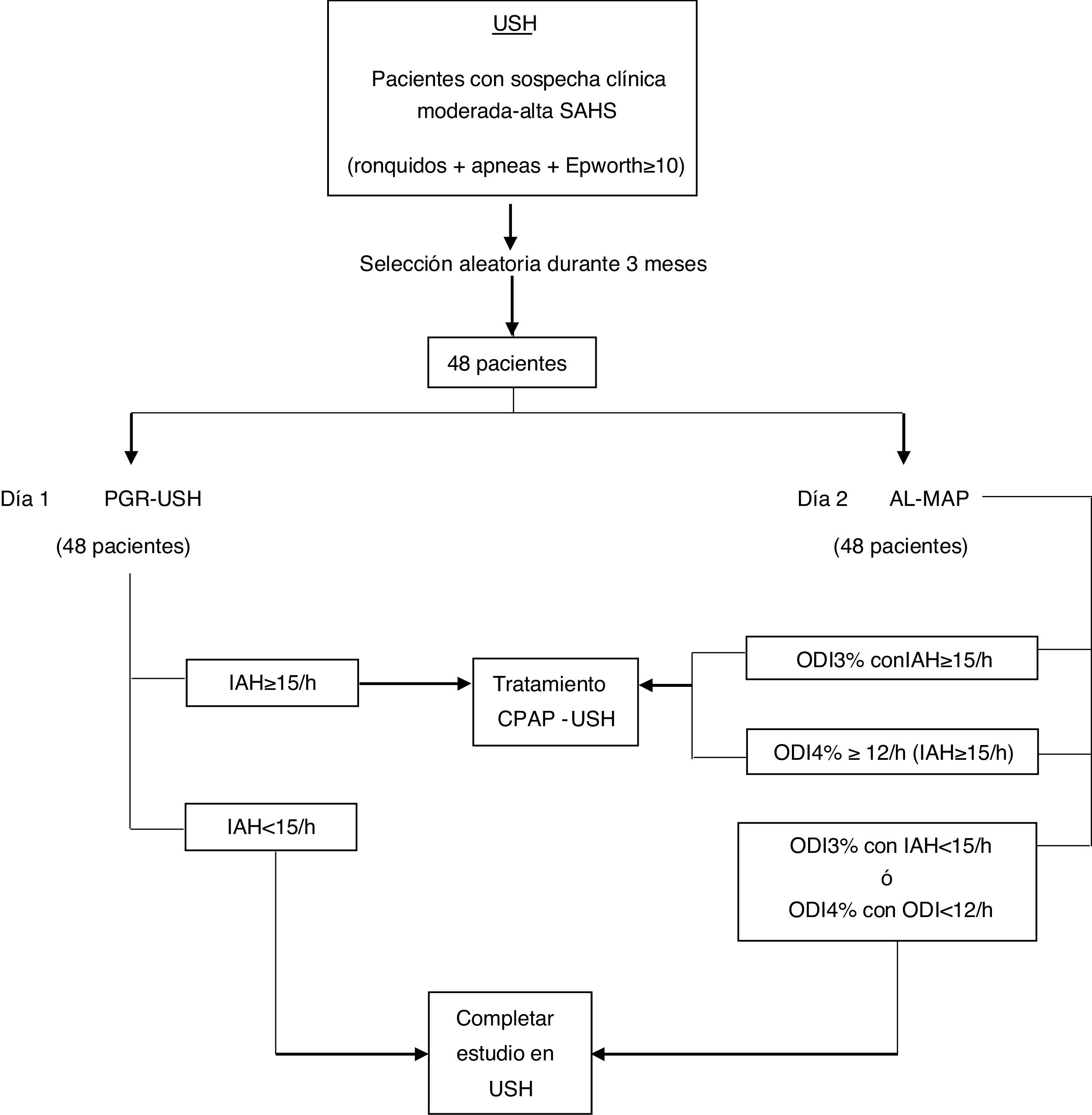
Manejo diagnóstico-terapéutico (figs. 1 y 2)A) Actuación realizada por USH con PGR: interpretó la PGR, según normativa SEPAR9. Consideró diagnóstico de SAHS cuando el índice de apneas e hiponeas del sueño (IAH) fuera ≥ 5/h; leve IAH = 5-15/h, moderado IAH = 15-29/ h y grave IAH ≥ 30 /h (figs. 1 y 2).
B) Actuación realizada por MAP con AL: interpretaron los AL y se consideraron diagnósticos cuando IAH ≥ 5/h; leve cuando IAH = 5-15/h, moderado IAH = 15-29/h y grave IAH ≥ 30/h, según normativa SEPAR9. La actuación terapéutica propuesta seguía el siguiente protocolo: si el resultado era positivo (IAH ≥ 15/h), se consideró tratamiento con CPAP; si el resultado fuera IAH < 15/h, se derivaría a la USH para continuar estudio. Los resultados y actuaciones terapéuticas se compararon posteriormente con las realizadas por la USH.
En ambas actuaciones (MAP y USH), se agruparon a los que tenían IAH ≥ 15 y los que lo tenían inferior, proponiendo tratamiento con CPAP cuando IAH ≥ 15/h, según criterios SEPAR9.
Variables recogidas: se recogieron variables de filiación y antropométricas: código de identificación, género, edad, peso, talla, índice de masa corporal kg/m2 (IMC). En AL se obtuvieron: tiempo de registro, tiempo de evaluación, ODI 3% y ODI 4%, saturación mínima, porcentaje de tiempo de registro con saturación de oxihemoglobina < 90% (Tc < 90%), además, los eventos respiratorios (IAR, IAH). En la PGR: tiempo de registro, ODI 3%, saturación mínima y eventos respiratorios (IAH). También se recogieron variables sobre decisiones diagnóstico-terapéuticas tomadas por los investigadores (USH y MAP).
Estudios comparativos: estudio descriptivo de variables y análisis comparativo entre los resultados del ALA y ALM; tanto con criterio de desaturación al 4% (AL 4%) como al 3% (AL 3%), según AASM-201312, y se comparan con los resultados de PGR y la concordancia de las decisiones terapéuticas planteadas por MAP y USH.
Se agrupan los estudios con IAH ≥ 5/h con diagnóstico de SAHS y los que tienen IAH ≥ 15/h (SAHS moderado-grave), que serían candidatos a tratamiento con CPAP.
Además, en un intento por simplificar la toma de decisión terapéutica, se consideró, tal como indican estudios previos13,14, que un ODI 4% ≥ 12/h en AL 4% suponía un IAH ≥ 15 al realizar la corrección al 3% mediante PSG, que representa un SAHS moderado-grave e indicaría el tratamiento con CPAP. Se analizará la concordancia con las correcciones de AL 4%, AL 3% y PGR.
Análisis estadísticoMediante el programa de análisis estadístico IBM-SPSS.v27 (IBNM Corp., Armonk, NY), se obtuvieron los estadísticos de resumen para variables cuantitativas, valores absolutos y sus porcentajes para variables cualitativas en relación con el análisis univariado. Los contrastes bivariados se realizaron con las pruebas estadísticas correspondientes a la naturaleza de las variables contrastadas. Se consideró que los resultados de PGR obtenidos en USH representaban el gold standard y los obtenidos mediante AL se compararon en los términos propios de las pruebas diagnósticas y, por ello, se obtuvo la sensibilidad (S) y la especificidad (E) de los resultados diagnósticos de AL y sus cocientes de probabilidad (CP), que no dependen de la prevalencia de la enfermedad. Se calcularon los intervalos de confianza (IC) al 95%, fijando el nivel de error alfa en 5% para aceptar las hipótesis alternas.
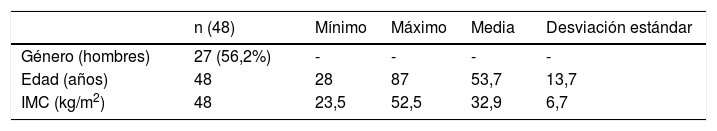
ResultadosEstudio descriptivoSe recogieron 48 pacientes y los datos de las variables se muestran en la tabla 1 (1.1-1.4).
Datos estadísticos descriptivos de toda la muestra
| n (48) | Mínimo | Máximo | Media | Desviación estándar | |
|---|---|---|---|---|---|
| Género (hombres) | 27 (56,2%) | - | - | - | - |
| Edad (años) | 48 | 28 | 87 | 53,7 | 13,7 |
| IMC (kg/m2) | 48 | 23,5 | 52,5 | 32,9 | 6,7 |
| Poligrafía | n | Mínimo | Máximo | Media | Desviación estándar |
|---|---|---|---|---|---|
| Tiempos de registro | 46 | 139 | 744 | 426,4 | 103,7 |
| Índice de apnea e hipopnea | 46 | 0,9 | 66,6 | 18,1 | 14,9 |
| Índice de desaturación de O2 (3%) | 44 | 0,1 | 59,1 | 17,9 | 16,5 |
| Saturación de O2 más baja | 41 | 54 | 96,3 | 81,1 | 10 |
| ApneaLink® ODI al 3% | n | Mínimo | Máximo | Media | Desviación estándar | |
|---|---|---|---|---|---|---|
| Corrección automática | Tiempos de registro | 48 | 0 | 720 | 401,1 | 127,1 |
| Índice de apnea e hipopnea | 47 | 0,6 | 58,6 | 20 | 14,5 | |
| Índice respiratorio | 47 | 1,5 | 61,7 | 22,9 | 14,3 | |
| Índice de desaturación de O2 (3%) | 47 | 1,4 | 78,0 | 27,9 | 17,9 | |
| Saturación de O2 más baja | 47 | 50 | 92 | 77,7 | 9,2 | |
| Tiempo de saturación de O2 < 90% | 47 | 0 | 98 | 34,1 | 31 | |
| Corrección manual | Tiempos de registro | 48 | 0 | 720 | 401,8 | 127,5 |
| Índice de apnea e hipopnea | 47 | 0,6 | 62,5 | 23,8 | 15,5 | |
| Índice respiratorio | 47 | 1,5 | 65,6 | 26,7 | 15,3 | |
| Índice de desaturación de O2 (3%) | 47 | 1,4 | 78,4 | 27,9 | 17.947 | |
| Saturación de O2 más baja | 47 | 50 | 92 | 77,7 | 9,2 | |
| Tiempo de saturación de O2 < 90% | 47 | 0 | 98 | 34,1 | 31,0 |
| ApneaLink® ODI al 4% | n | Mínimo | Máximo | Media | Desviación estándar | |
|---|---|---|---|---|---|---|
| Corrección automática | Tiempos de registro | 48 | 0 | 720 | 401,8 | 127,5 |
| Índice de apnea e hipopnea | 47 | 0,3 | 118 | 18,9 | 20,3 | |
| Índice respiratorio | 47 | 1,3 | 161 | 22,7 | 24,8 | |
| Índice de desaturación de O2 (3%) | 47 | 0,6 | 54,4 | 18,8 | 14,5 | |
| Saturación de O2 más baja | 47 | 50 | 92 | 77,7 | 9,2 | |
| Tiempo de saturación de O2 < 90% | 47 | 0 | 98 | 34,1 | 31 | |
| Corrección manual | Tiempos de registro | 48 | 0 | 720 | 401,8 | 127,5 |
| Índice de apnea e hipopnea | 47 | 0,4 | 60,1 | 18,9 | 14,5 | |
| Índice respiratorio | 47 | 1,4 | 63,3 | 21,7 | 14,4 | |
| Índice de desaturación de O2(3%) | 47 | 0,6 | 54,4 | 18,9 | 14,5 | |
| Saturación de O2 más baja | 47 | 50 | 92 | 77,7 | 9,2 | |
| Tiempo de saturación de O2 < 90% | 47 | 0 | 98 | 34,1 | 31 |
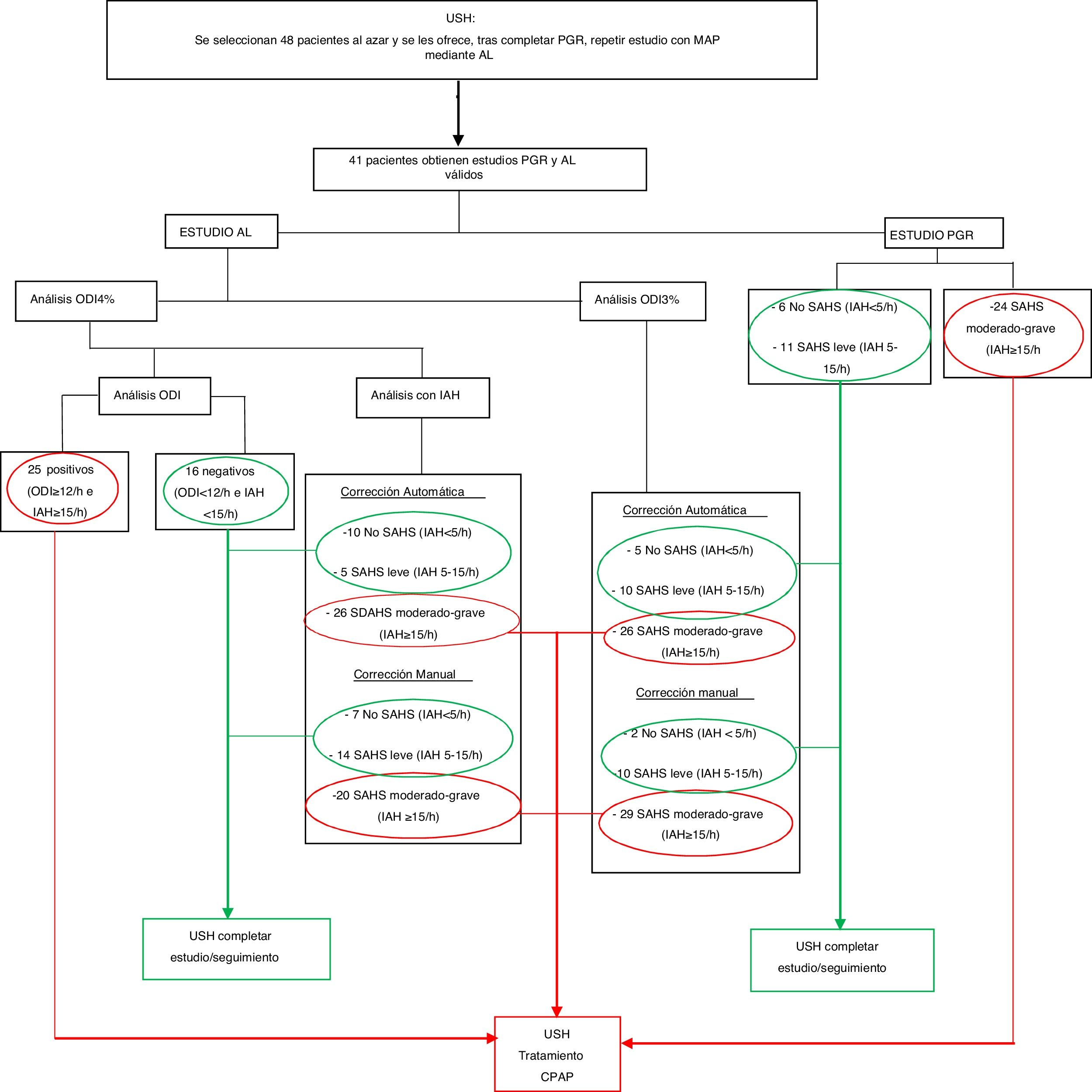
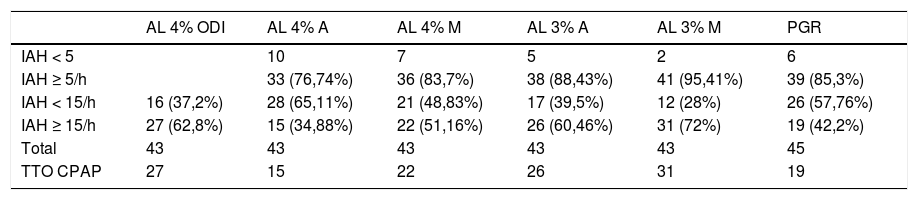
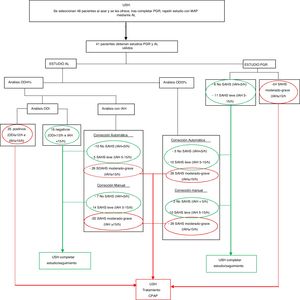
Había 45 registros válidos (figs. 1 y 3.1, tabla 2.1). Se diagnosticó de SAHS al 85,3% de los pacientes; el 42,22% presentaba SAHS moderado-grave y recibieron tratamiento con CPAP.
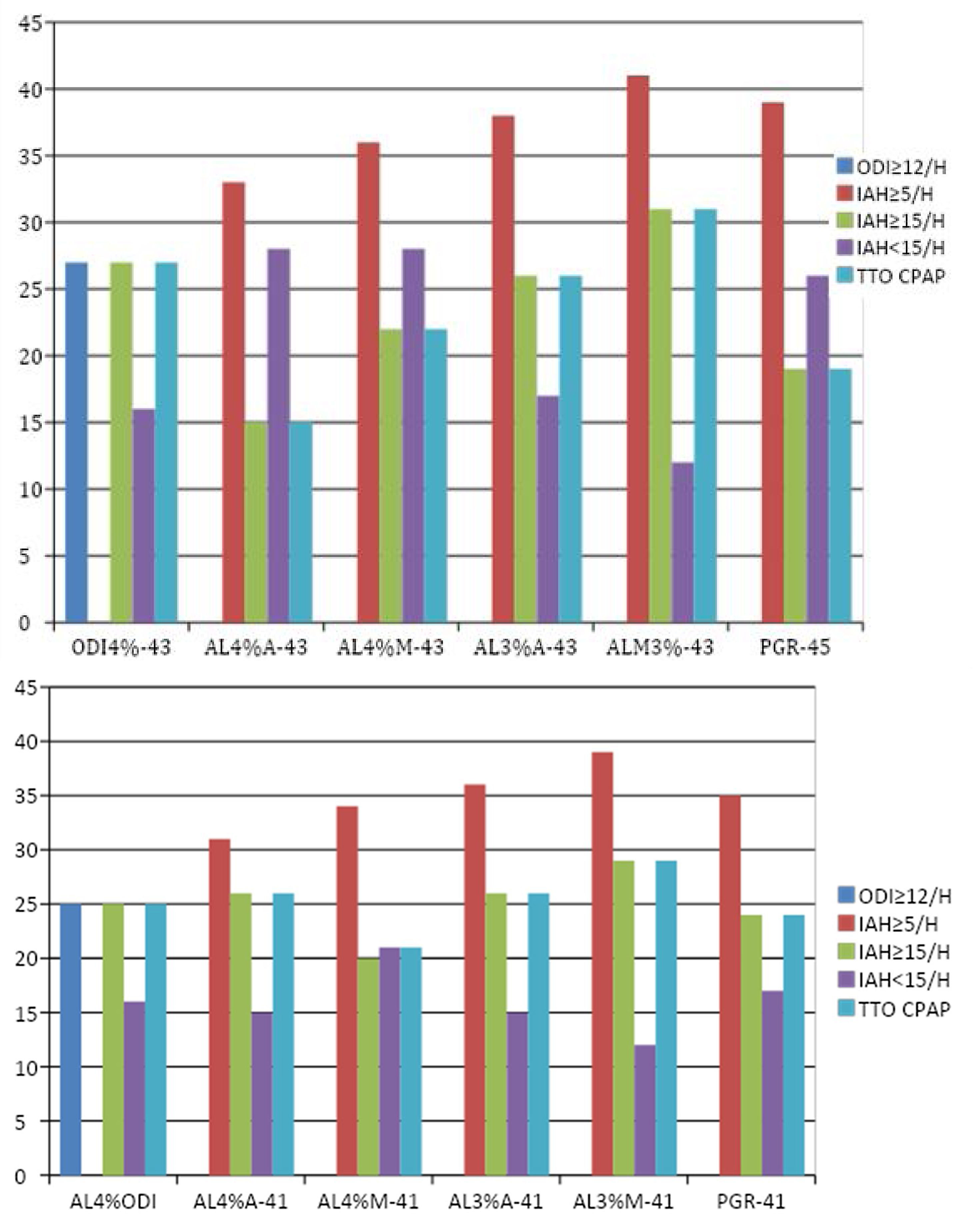
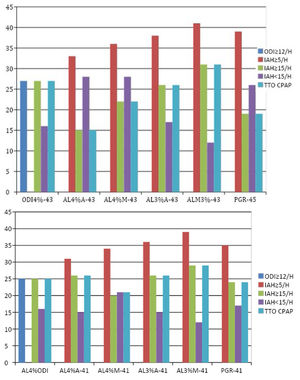
Figura 3.1. Representación gráfica de los resultados de los estudios AL (n = 43) y PGR (n = 41) incluidos en el estudio.
Figura 3.2. Representación gráfica de los resultados de los estudios incluidos con ambas pruebas (PGR y AL) válidas (n = 41).
Leyenda figura 3:
- ODI 4%. Resultados de estudios AL del ODI automático al 4% ≥ 12/h (que implicaría un IAH ≥ 15/h) o < 12/h (que implicaría un IAH < 15/h).
- AL 4% A. Resultados del IAH de estudios AL automático al 4%.
- AL 4% M. Resultados del IAH de estudios AL corregidos manualmente al 4%.
- AL 3% A. Resultados del IAH de estudios AL automático al 3%.
- AL 3% M. Resultados del IAH de estudio AL corregidos manualmente al 3%.
- PGR. Resultados del IAH de los estudios PGR.
- ODI ≥ 12. Indica los estudios que tienen el ODI al 4% ≥ 12 en el AL automático.
- IAH ≥ 5/H. Indica los estudios que tenían IAH ≥ 5/h en los estudios AL o PGR.
- IAH ≥ 15. Indica los estudios que tenían IAH ≥ 15/h en el AL o en la PGR.
- IAH ≤ 15. Indica los estudios que tenían IAH ≤ 15/h.
- TTO CPAP. Indica los pacientes a los que se pautó el tratamiento con CPAP.
Resultados de los estudios incluidos con AL y PGR válidos (tiempo de registro ≥ 240 min)
| AL 4% ODI | AL 4% A | AL 4% M | AL 3% A | AL 3% M | PGR | |
|---|---|---|---|---|---|---|
| IAH < 5 | 10 | 7 | 5 | 2 | 6 | |
| IAH ≥ 5/h | 33 (76,74%) | 36 (83,7%) | 38 (88,43%) | 41 (95,41%) | 39 (85,3%) | |
| IAH < 15/h | 16 (37,2%) | 28 (65,11%) | 21 (48,83%) | 17 (39,5%) | 12 (28%) | 26 (57,76%) |
| IAH ≥ 15/h | 27 (62,8%) | 15 (34,88%) | 22 (51,16%) | 26 (60,46%) | 31 (72%) | 19 (42,2%) |
| Total | 43 | 43 | 43 | 43 | 43 | 45 |
| TTO CPAP | 27 | 15 | 22 | 26 | 31 | 19 |
- AL 4% ODI. Resultados de estudios AL del ODI automático al 4% ≥ 12/h (que implicaría un IAH ≥ 15/h) O < 12/h (que implicaría un IAH < 15/h).
- AL 4% A. Resultados del IAH de estudios AL 4% automático al 4%.
- AL 4% M. Resultados del IAH de estudios AL corregidos manualmente al 4%.
- AL 3% A. Resultados del IAH de estudios AL automático al 3%.
- AL 3% M. Resultados del IAH de estudio AL corregidos manualmente al 3%.
- PGR. Resultados del IAH de los estudios PGR.
- ODI ≥ 12. Indica los estudios que tienen el ODI al 4% ≥ 12/h en el AL automático.
- IAH < 5. Indica los estudios que tenían IAH< 5/h en los estudios AL o PGR.
- IAH ≥ 5. Indica los estudios que tenían IAH ≥ 5/h en los estudios AL o PGR.
- IAH ≥ 15. Indica los estudios que tenían IAH ≥ 15/h en el AL o en la PGR.
- IAH ≤ 15. Indica los estudios que tenían IAH ≤ 15/h
- Total. Número de estudios válidos con AL o PGR.
- TTO CPAP. Indica los pacientes a los que se pautó tratamiento con CPAP.
Había 43 registros válidos como se muestra en figura 3.1 y tabla 2.1.
Análisis con ODI 4% (AL 4%): se realizó atendiendo al valor de ODI ≥ 12/h y al valor de IAH en modo automático (AL 4% A) y manual (AL 4% M).
Según los valores de ODI: el 62,8% fueron positivos (ODI ≥ 12/h) y considerados SAHS moderado-grave. El 37,2% fueron negativos siendo devueltos a la USH para completar estudio.
Observando valores de IAH: AL 4% A detectó que el 76,74% presentaba SAHS (IAH ≥ 5/h) y el 34,88% de ellos tenían SAHS moderado-grave.
El AL 4% M detectó SAHS en el 83,7%, el 51,16% con grado moderado-grave (entre ellos los 15 pacientes que ya habían sido positivos con ODI ≥ 12 en AL 4% A).
Análisis con ODI 3% (AL 3%): el IAH con corrección automática de AL 3% (AL 3% A), detectó como SAHS al 88,43%, el 60,46% con grado moderado-grave.
El análisis manual del AL 3% (AL 3% M) mostraba que el 95,41% tenía un IAH ≥ 5/h, y el 72% presentaba SAHS moderado-grave.
Los diagnosticados como SAHS moderado-grave (IAH ≥ 15/h) se devolvían a USH con propuesta de tratamiento con CPAP, y el resto se derivarían a USH para completar estudio.
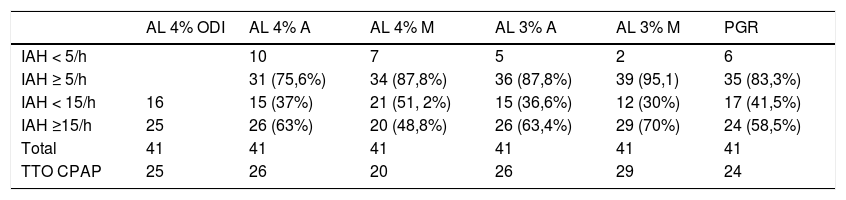
Resultados de estudios incluidos con AL y PGR válidosTenían AL y PGR válidas 41 (fig. 2). Sus resultados se resumen en la fig. 3.2 y tabla 2.2, agrupados según valor de IAH. La tabla 2.3 recoge los datos de los estudios AL y PGR, en relación con el valor de ODI 4% ≥ 12/h del AL 4%.
Resultados de los estudios incluidos con ambas pruebas (PGR y AL) válidas
| AL 4% ODI | AL 4% A | AL 4% M | AL 3% A | AL 3% M | PGR | |
|---|---|---|---|---|---|---|
| IAH < 5/h | 10 | 7 | 5 | 2 | 6 | |
| IAH ≥ 5/h | 31 (75,6%) | 34 (87,8%) | 36 (87,8%) | 39 (95,1) | 35 (83,3%) | |
| IAH < 15/h | 16 | 15 (37%) | 21 (51, 2%) | 15 (36,6%) | 12 (30%) | 17 (41,5%) |
| IAH ≥15/h | 25 | 26 (63%) | 20 (48,8%) | 26 (63,4%) | 29 (70%) | 24 (58,5%) |
| Total | 41 | 41 | 41 | 41 | 41 | 41 |
| TTO CPAP | 25 | 26 | 20 | 26 | 29 | 24 |
- AL 4% ODI. Resultados de estudios AL del ODI automático al 4% ≥ 12/h (que implicaría un IAH ≥ 15/h) o < 12/h (que implicaría un IAH < 15/h).
- AL 4% A. Resultados del IAH de estudios AL automático al 4%.
- AL 4% M. Resultados del IAH de estudios AL corregidos manualmente al 4%.
- AL 3% A. Resultados del IAH de estudios AL automático al 3%.
- AL 3% M. Resultados del IAH de estudio AL corregidos manualmente al 3%.
- PGR. Resultados del IAH de los estudios PGR.
- ODI ≥ 12. Indica los estudios que tienen el ODI al 4% ≥ 12/h en el AL automático.
- IAH < 5. Indica los estudios que tenían IAH < 5/h en los estudios AL o PGR.
- IAH ≥ 5. Indica los estudios que tenían IAH ≥ 5/h en los estudios AL o PGR.
- IAH ≥ 15. Indica los estudios que tenían IAH ≥ 15/h en el AL o en la PGR.
- IAH ≤ 15. Indica los estudios que tenían IAH ≤ 15/h.
- Total. Número de estudios que tienen válidos el AL y la PGR.
- TTO CPAP. Indica los pacientes a los que se pautó tratamiento con CPAP.
Resultados del AL con ODI 4% ≥ 12/h que han obtenido un IAH ≥ 15 en los estudios AL automático y manual al 3%; y PGR, en los 41 pacientes con ambos estudios válidos (AL y PGR)
| Tipo de estudio | AL 4% con ODI ≥ 12/h | PGR (IAH ≥ 15/H) | AL 3% automático (IAH ≥ 15/H) | AL 3% manual(IAH ≥ 15/H) |
|---|---|---|---|---|
| Total pacientes con ODI ≥ 12/h | 25 | 18 (72%) | 23 (92%) | 25 (100%) |
- AL 4% con ODI ≥ 12/h (que implicaría un IAH ≥ 15/h).
- PGR con IAH ≥ 15/h.
- AL automático al 3% con IAH ≥ 15/h.
- AL corregido manualmente con ODI al 3%.
En el estudio AL 4% había 25 pacientes con ODI 4% ≥ 12/h, que supondría un IAH ≥ 15/h13,14; de ellos, atendiendo al IAH del AL 3% A, el 92% tenían IAH ≥ 15/h; y en AL 3% M, los 25 presentaron también IAH ≥ 15/h. En la PGR solo el 72% tenían IAH ≥ 15/h (tabla 2.3).
Con AL 3% M se diagnostican de SAHS (IAH ≥ 5/h), el 95%, y con PGR, el 85%.
Estudio analíticoSe realizó un estudio comparativo de los resultados obtenidos entre las diferentes pruebas.
Estudios AL 4%El análisis del AL4% no mostró diferencias estadísticamente significativas en cuanto a las decisiones diagnósticas y terapéuticas, entre los resultados del AL 4% A y AL 4% M. Por ello, al realizar el estudio analítico comparativo entre AL y PGR, se consideraron únicamente los resultados obtenidos mediante AL 4% A.
La comparación de los registros realizados con AL 4%, considerando el ODI 4% y el IAH, muestra la tendencia que a mayor ODI, existe mayor IAH sin alcanzar significación estadística.
Estudios AL3%La comparación de AL 3% A y AL 3% M, no alcanzó conclusiones estadísticamente significativas, probablemente por el limitado tamaño muestral, pero sí una clara tendencia que en AL 3% M aumentaba el valor de IAH y, por tanto, la detección de casos de SAHS (IAH ≥ 5) y SAHS moderado-grave (IAH ≥ 15).
Estudio comparativo entre resultados de AL 4% vs. AL 3%Se comparó el IAH obtenido del estudio AL 4% A con el IAH obtenido del análisis de AL 3% M; mostraba una clara tendencia de que a mayor IAH en AL 4% A, hay mayor IAH en AL 3% M; pero sin demostrarse significancia estadística por el limitado tamaño muestral. Lo mismo sucedía al comparar el valor de ODI 4% con el IAH del AL 3% M. Y por ello, este fue el resultado del AL que se comparará con la PGR.
Estudio comparativo entre resultados de AL 4% vs. PGREl AL 4% A, según su valor de ODI 4%, presentó S = 82,4% y E = 54,2%, con valor predictivo negativo (VPN) del 81,3%. Indicando elevada probabilidad de que un paciente con AL 4% A negativo para SAHS no tenga la enfermedad. El CP del resultado positivo fue 1,80 (IC 95%:1,10-2,93), que conlleva una estimación puntual estadísticamente significativa de casi doblar la probabilidad de tener una PGR diagnóstica para SAHS cuando AL 4% A es positiva. El CP del resultado negativo fue 0,33 (IC 95%: 0,11-0,97), indicando que la negatividad de la prueba AL 4% A reduce la probabilidad de que una prueba PGR sea diagnóstica a la tercera parte (13%).
Si se utiliza el AL 4% A según la positividad a IAH, comparando con la PGR se obtiene S = 52,9% y E = 75,0%. El CP del resultado positivo fue 2,12 (IC 95%: 0,93-4,83), que no tiene significación estadística (p > 0,05). Tampoco tiene significación estadística el CP del resultado negativo, que fue 0,63 (IC 95%: 0,11-0,97). Por tanto, no se puede decir que, con AL 4% A con base en IAH, un resultado negativo indique una reducción de la probabilidad de que una PGR sea diagnóstica para SAHS.
Estudio comparativo entre resultados de AL 3% vs. PGREl AL 3%, atendiendo su valor ODI, presentó S = 94,1%, E = 45,8% y VPN = 91,7%, que indica elevada probabilidad de que no tenga la enfermedad un paciente con AL 3% negativo para SAHS. El CP del resultado positivo fue 1,74 (IC 95%: 1,18-2,56), que conlleva una estimación puntual estadísticamente significativa de casi doblar la probabilidad de tener una PGR diagnóstica para SAHS cuando AL 3% es positiva. De manera complementaria, el CP del resultado negativo fue 0,13 (IC 95%: 0,02-0,90) indicando que la negatividad de la prueba AL 3% reduce (p < 0,05) la probabilidad de que una prueba PGR sea diagnóstica a una décima parte (al 13%).
DiscusiónUn reciente metaanálisis internacional4 corrobora una prevalencia de SAHS (IAH 5/h) en población adulta de 9-38% (hombres: 13-33% y mujeres: 6-19%), presentando gravedad moderada-severa (IAH ≥ 15/h) un 6-17%; con mayor prevalencia en hombres, personas con IMC elevado y edad avanzada. Esta elevada prevalencia en población general justifica la búsqueda de métodos diagnósticos más sencillos y económicos que la PSG en pacientes seleccionados, y la implicación de personal menos especializado para agilizar el diagnóstico y tratamiento.
Se incluyeron pacientes con moderada-alta probabilidad de SAHS, ya seleccionados por la USH para estudio PGR domiciliario y, por ello, candidatos a realizar estudio mediante métodos simplificados como el AL. Siguiendo a otros autores15,16, se planteó realizar estudio con AL por MAP y comparar los resultados con la PGR realizada por la USH y comparar la actitud terapéutica planteada por los MAP y la USH.
Los resultados del AL son similares a los de la PGR realizada con el dispositivo Embletta, incluso el AL 3% M tiene mayor sensibilidad en el diagnóstico de SAHS con IAH ≥ 5/h, y mayor rendimiento en pacientes con IAH > 10, corroborando estudios similares17–19. Al utilizar AL 3% M siguiendo criterios SEPAR9 para el diagnóstico de SAHS (IAH ≥ 5/h), confirmó el 95 vs. el 85% de la PGR. Se diagnosticó SAHS moderado-grave en el 63% de pacientes mediante AL 4% A atendiendo a ODI 4% ≥ 12/h y se inició CPAP. Todos los AL 4% A con ODI 4% ≥ 12/h mostraron IAH ≥ 15/h en AL 3% M, mostrando coherencia con otros autores20, aunque ellos comparaban con PSG. Esta lectura rápida podría ser útil para AP, para el diagnóstico de SAHS moderado-grave y poder tomar decisiones terapéuticas14. Las conclusiones diagnóstico-terapéuticas tomadas por los MAP fueron consistentes, y más del 90% fueron concluyentes, sin diferencias con la USH. Además, AL es sencillo en manejo e interpretación, con la ventaja que con AL 4% A conduce a las mismas decisiones que los especialistas de la USH, sin que su corrección manual aporte beneficios. Esto responde a las incógnitas planteadas por estudios previos18, basados en el uso de AL con análisis automático planteaban si la corrección manual habría aportado beneficio.
Otros investigadores han demostrado la fiabilidad de este método diagnóstico con resultados similares a este estudio15,16, mostrando una reducción económica importante por paciente. Sería recomendable que en una ampliación futura se incluyan las variables pertinentes y poder aportar más información socioeconómica dentro del ámbito sanitario. Mejorando el diseño epidemiológico y aumentando la muestra de pacientes, se aportarían importantes resultados para la implementación de nuevos protocolos ante el problema de salud pública que representa el SAHS, confirmando estudios previos14,17,18,21. Consensos científicos recientes apuntan la importancia de la colaboración entre MAP y la USH en el diagnóstico y tratamiento de esta patología22.
Entre las limitaciones está el reducido tamaño muestral. Los resultados obtenidos, que son favorables al uso de AL en AP, deben considerar esta circunstancia: su validez externa puede estar comprometida, pero su validez interna es robusta. Sería interesante ampliar el estudio con inicio desde AP con un protocolo ya establecido. Otra limitación sería la escasa experiencia de los investigadores MAP, mejorando este aspecto se obtendrían mejores resultados.
Considerar que PGR y AL están realizados en diferentes noches y algunos autores han demostrado una variabilidad del valor de RDI, de un mismo paciente, de hasta el 50% entre diferentes noches19, relacionado con diferencias de tiempo de sueño/registro o diferencias posturales, afectando así al valor de IAH en pacientes con SAHS posicional. Estas variaciones influyen en las decisiones diagnóstico-terapéuticas cuando están en el límite entre SAHS leve-moderado que requerirán completar estudio con PSG para confirmar si se beneficiarían de tratamiento. Serían aquellos pacientes con AL negativo, pero con clínica muy marcada19.
ConclusionesEl método simplificado AL es un buen método de detección de SAHS en población seleccionada con alta probabilidad de SAHS en AP. Es una técnica sencilla, fiable, de fácil implementación en AP; cuya lectura automática puede considerarse para el diagnóstico y manejo del SAHS moderado-grave.
Los resultados obtenidos demuestran que los resultados AL 4% y AL 3% aumentan la probabilidad DE que, ante la positividad de la prueba realizada por los MAP, se obtenga una PGR diagnóstica en la USH.
El establecimiento de protocolos de abordaje conjuntos entre MAP y USH serían recomendables para conseguir mejorar el diagnóstico de pacientes con SAHS en términos de eficacia y fiabilidad.
Conflicto de interesesComo conflictos de intereses declaramos que los dispositivos de diagnóstico simplificado modelo ApneaLink™Air®-Resmed-versión10.20 fueron cedidos por ResMed Ltd® para realizar este proyecto. Los investigadores no tienen otros conflictos de intereses a declarar.
Al personal de la USH del Hospital Universitario de Vic y del Centro de Salud de Manlleu.