La dislipidemia constituye uno de los principales factores de riesgo para el desarrollo de la aterosclerosis. Diversos estudios han demostrado que el colesterol LDL, cuanto más bajo, mejor. Las evidencias actuales muestran que los objetivos de colesterol LDL recomendados por las guías de práctica clínica son beneficiosos y seguros, si bien existen datos consistentes que muestran que reducciones mayores podrían aportar beneficios cardiovasculares adicionales, sin un aumento en el riesgo de los efectos adversos. Desafortunadamente, el control de la dislipidemia es muy pobre en la actualidad. Si bien las estatinas son el tratamiento de elección en la mayoría de los pacientes con dislipidemia, el arsenal terapéutico hipolipidemiante actual dispone de diferentes alternativas que reducen eficazmente el colesterol LDL y que, solas o en combinación, permitirían lograr los objetivos de control de colesterol LDL en la gran mayoría de los pacientes.
Dyslipidaemia is one of the main risk factors for the development of atherosclerosis. Different studies have demonstrated that the lower the LDL cholesterol, the better. Current evidence shows that the LDL cholesterol targets recommended by the clinical practice guidelines are beneficial and safe. However, consistent data show that higher reductions might provide additional cardiovascular beneficial effects, without an increase in side effects. Unfortunately, the current control of dyslipidaemia is very poor. Although statins are the treatment of choice in the majority of patients with dyslipidaemia, the current therapeutic armamentarium has different alternatives that effectively reduce LDL cholesterol levels, and that alone, or in combination, help to achieve LDL cholesterol targets in the majority of patients.
Las enfermedades cardiovasculares constituyen la principal causa de muerte en nuestro medio y el motivo que subyace en la mayoría de los casos1es la cardiopatía isquémica. La aterosclerosis constituye la base principal en la etiopatogenia de la cardiopatía isquémica y, en este contexto, el colesterol es el principal factor de riesgo cardiovascular2. De hecho, en los últimos años se ha observado en nuestro medio un descenso de la mortalidad de cardiopatía isquémica ajustada por edad, entre otros motivos, por el mejor control de los factores de riesgo cardiovascular, en particular la presión arterial y el colesterol3.
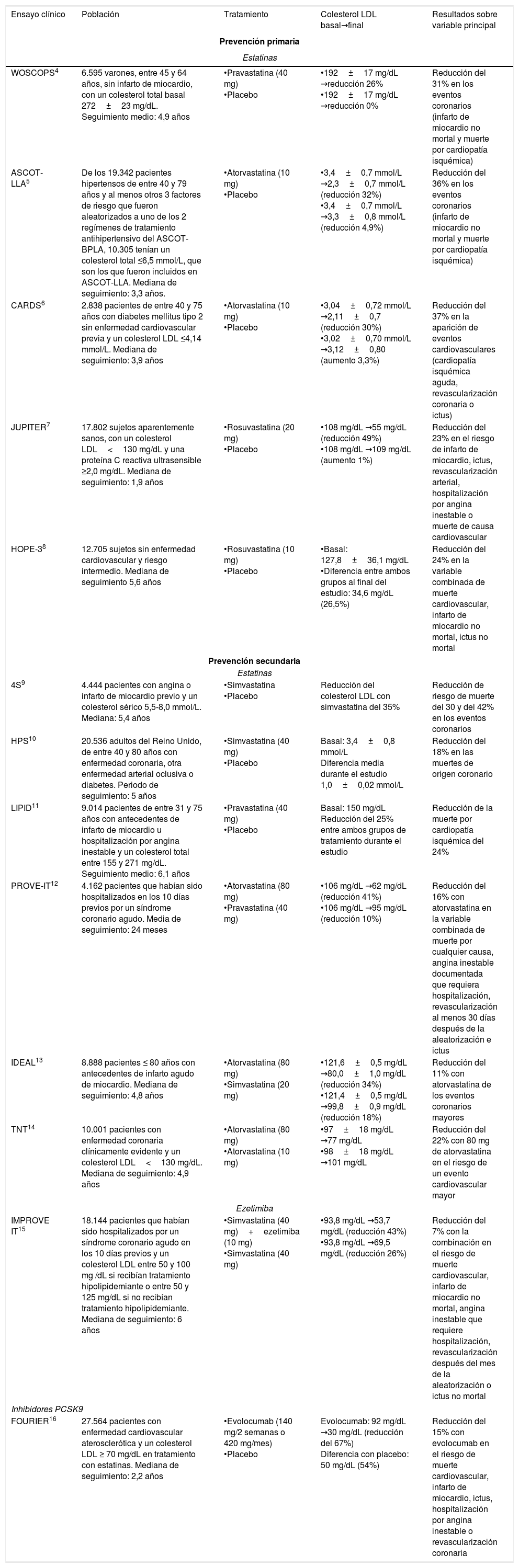
Hasta dónde bajar el colesterol LDLA raíz de las evidencias provenientes de los ensayos clínicos (tabla 1)4–16, las guías europeas establecen claramente que el objetivo principal del paciente con dislipidemia es reducir el colesterol LDL hasta las metas recomendadas2. Ahora bien, ¿en todos los pacientes el objetivo debería ser el mismo?; ¿existe un umbral de colesterol LDL por debajo del cual la reducción resulta excesiva y comienza a ser perjudicial?
Efectos de la reducción de colesterol LDL sobre los eventos cardiovasculares
| Ensayo clínico | Población | Tratamiento | Colesterol LDL basal→final | Resultados sobre variable principal |
|---|---|---|---|---|
| Prevención primaria | ||||
| Estatinas | ||||
| WOSCOPS4 | 6.595 varones, entre 45 y 64 años, sin infarto de miocardio, con un colesterol total basal 272±23 mg/dL. Seguimiento medio: 4,9 años | •Pravastatina (40 mg) •Placebo | •192±17 mg/dL →reducción 26% •192±17 mg/dL →reducción 0% | Reducción del 31% en los eventos coronarios (infarto de miocardio no mortal y muerte por cardiopatía isquémica) |
| ASCOT-LLA5 | De los 19.342 pacientes hipertensos de entre 40 y 79 años y al menos otros 3 factores de riesgo que fueron aleatorizados a uno de los 2 regímenes de tratamiento antihipertensivo del ASCOT-BPLA, 10.305 tenían un colesterol total ≤6,5 mmol/L, que son los que fueron incluidos en ASCOT-LLA. Mediana de seguimiento: 3,3 años. | •Atorvastatina (10 mg) •Placebo | •3,4±0,7 mmol/L →2,3±0,7 mmol/L (reducción 32%) •3,4±0,7 mmol/L →3,3±0,8 mmol/L (reducción 4,9%) | Reducción del 36% en los eventos coronarios (infarto de miocardio no mortal y muerte por cardiopatía isquémica) |
| CARDS6 | 2.838 pacientes de entre 40 y 75 años con diabetes mellitus tipo 2 sin enfermedad cardiovascular previa y un colesterol LDL ≤4,14 mmol/L. Mediana de seguimiento: 3,9 años | •Atorvastatina (10 mg) •Placebo | •3,04±0,72 mmol/L →2,11±0,7 (reducción 30%) •3,02±0,70 mmol/L →3,12±0,80 (aumento 3,3%) | Reducción del 37% en la aparición de eventos cardiovasculares (cardiopatía isquémica aguda, revascularización coronaria o ictus) |
| JUPITER7 | 17.802 sujetos aparentemente sanos, con un colesterol LDL<130 mg/dL y una proteína C reactiva ultrasensible ≥2,0 mg/dL. Mediana de seguimiento: 1,9 años | •Rosuvastatina (20 mg) •Placebo | •108 mg/dL →55 mg/dL (reducción 49%) •108 mg/dL →109 mg/dL (aumento 1%) | Reducción del 23% en el riesgo de infarto de miocardio, ictus, revascularización arterial, hospitalización por angina inestable o muerte de causa cardiovascular |
| HOPE-38 | 12.705 sujetos sin enfermedad cardiovascular y riesgo intermedio. Mediana de seguimiento 5,6 años | •Rosuvastatina (10 mg) •Placebo | •Basal: 127,8±36,1 mg/dL •Diferencia entre ambos grupos al final del estudio: 34,6 mg/dL (26,5%) | Reducción del 24% en la variable combinada de muerte cardiovascular, infarto de miocardio no mortal, ictus no mortal |
| Prevención secundaria | ||||
| Estatinas | ||||
| 4S9 | 4.444 pacientes con angina o infarto de miocardio previo y un colesterol sérico 5,5-8,0 mmol/L. Mediana: 5,4 años | •Simvastatina •Placebo | Reducción del colesterol LDL con simvastatina del 35% | Reducción de riesgo de muerte del 30 y del 42% en los eventos coronarios |
| HPS10 | 20.536 adultos del Reino Unido, de entre 40 y 80 años con enfermedad coronaria, otra enfermedad arterial oclusiva o diabetes. Periodo de seguimiento: 5 años | •Simvastatina (40 mg) •Placebo | Basal: 3,4±0,8 mmol/L Diferencia media durante el estudio 1,0±0,02 mmol/L | Reducción del 18% en las muertes de origen coronario |
| LIPID11 | 9.014 pacientes de entre 31 y 75 años con antecedentes de infarto de miocardio u hospitalización por angina inestable y un colesterol total entre 155 y 271 mg/dL. Seguimiento medio: 6,1 años | •Pravastatina (40 mg) •Placebo | Basal: 150 mg/dL Reducción del 25% entre ambos grupos de tratamiento durante el estudio | Reducción de la muerte por cardiopatía isquémica del 24% |
| PROVE-IT12 | 4.162 pacientes que habían sido hospitalizados en los 10 días previos por un síndrome coronario agudo. Media de seguimiento: 24 meses | •Atorvastatina (80 mg) •Pravastatina (40 mg) | •106 mg/dL →62 mg/dL (reducción 41%) •106 mg/dL →95 mg/dL (reducción 10%) | Reducción del 16% con atorvastatina en la variable combinada de muerte por cualquier causa, angina inestable documentada que requiera hospitalización, revascularización al menos 30 días después de la aleatorización e ictus |
| IDEAL13 | 8.888 pacientes ≤ 80 años con antecedentes de infarto agudo de miocardio. Mediana de seguimiento: 4,8 años | •Atorvastatina (80 mg) •Simvastatina (20 mg) | •121,6±0,5 mg/dL →80,0±1,0 mg/dL (reducción 34%) •121,4±0,5 mg/dL →99,8±0,9 mg/dL (reducción 18%) | Reducción del 11% con atorvastatina de los eventos coronarios mayores |
| TNT14 | 10.001 pacientes con enfermedad coronaria clínicamente evidente y un colesterol LDL<130 mg/dL. Mediana de seguimiento: 4,9 años | •Atorvastatina (80 mg) •Atorvastatina (10 mg) | •97±18 mg/dL →77 mg/dL •98±18 mg/dL →101 mg/dL | Reducción del 22% con 80 mg de atorvastatina en el riesgo de un evento cardiovascular mayor |
| Ezetimiba | ||||
| IMPROVE IT15 | 18.144 pacientes que habían sido hospitalizados por un síndrome coronario agudo en los 10 días previos y un colesterol LDL entre 50 y 100 mg /dL si recibían tratamiento hipolipidemiante o entre 50 y 125 mg/dL si no recibían tratamiento hipolipidemiante. Mediana de seguimiento: 6 años | •Simvastatina (40 mg)+ezetimiba (10 mg) •Simvastatina (40 mg) | •93,8 mg/dL →53,7 mg/dL (reducción 43%) •93,8 mg/dL →69,5 mg/dL (reducción 26%) | Reducción del 7% con la combinación en el riesgo de muerte cardiovascular, infarto de miocardio no mortal, angina inestable que requiere hospitalización, revascularización después del mes de la aleatorización o ictus no mortal |
| Inhibidores PCSK9 | ||||
| FOURIER16 | 27.564 pacientes con enfermedad cardiovascular aterosclerótica y un colesterol LDL ≥ 70 mg/dL en tratamiento con estatinas. Mediana de seguimiento: 2,2 años | •Evolocumab (140 mg/2 semanas o 420 mg/mes) •Placebo | Evolocumab: 92 mg/dL →30 mg/dL (reducción del 67%) Diferencia con placebo: 50 mg/dL (54%) | Reducción del 15% con evolocumab en el riesgo de muerte cardiovascular, infarto de miocardio, ictus, hospitalización por angina inestable o revascularización coronaria |
4S: Scandinavian Simvastatin Survival Study; ASCOT-LLA: Anglo-Scandinavian Cardiac Outcomes Trial-Lipid Lowering Arm; CARDS: Collaborative Atorvastatin Diabetes Study; FOURIER: Further Cardiovascular Outcomes Research with PCSK9 Inhibition in Subjects with Elevated Risk; HOPE-3: Heart Outcomes Prevention Evaluation; HPS: Heart Protection Study; IDEAL: Incremental Decrease in End Points Through Aggressive Lipid Lowering; IMPROVE-IT: Improved Reduction of Outcomes: Vytorin Efficacy International Trial; JUPITER: Justification for the Use of Statins in Prevention: an InterventionTrialEvaluating Rosuvastatin; LIPID: Long-Term Intervention with Pravastatin in Ischaemic Disease; PROVE-IT: Pravastatin or Atorvastatin Evaluation and Infection Therapy; TNT: Treating to New Targets; WOSCOPS: West of Scotland Prevention Study Group.
Fuente: Adaptado4–16.
Los diferentes ensayos clínicos realizados con hipolipidemiantes, sobre todo con estatinas, han demostrado que reducir el colesterol LDL es beneficioso a la hora de disminuir el riesgo de presentar complicaciones cardiovasculares. Y esto ocurre tanto en prevención primaria como en secundaria. Lógicamente, cuanto mayor sea el riesgo del paciente y más elevado sea el colesterol LDL basal, el beneficio de la reducción del colesterol LDL en términos absolutos será mayor2.
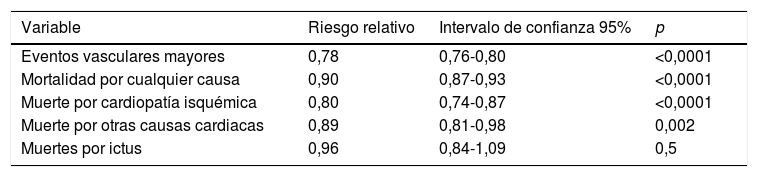
En el metaanálisis de Baigent et al. en el que se incluyó a 170.000 sujetos provenientes de 26 ensayos clínicos se objetivó que en los ensayos clínicos que comparaban el tratamiento intensivo con estatinas frente al tratamiento menos intensivo con estatinas, el tratamiento intensivo se asoció con una reducción al año del colesterol LDL de 0,51mmol/L y esto, con una reducción del 15% (IC 95%: 11-18; p<0,0001) en el riesgo de eventos cardiovasculares mayores, del 13% (IC 95%: 7-19; p<0,0001) en la muerte por cardiopatía isquémica o infarto de miocardio no mortal, del 19% (IC 95%: 15-24; p<0,0001) en la revascularización coronaria y del 16% (IC 95%: 5-26; p=0,005) en el ictus isquémico. En términos relativos, las reducciones de riesgo fueron similares cuando se comparaban las estatinas en su conjunto con los grupos control. De forma global, por cada mmol/L (39mg/dL) de descenso del colesterol LDL, se reducía el riesgo de eventos vasculares mayores en un 22% (IC 95%: 0,76-0,80; p<0,0001), independientemente del tipo de paciente estudiado (tabla 2)17.
Reducción de eventos por cada descenso en 1 mmol/L (39mg/dL) de colesterol LDL con el tratamiento hipolipidemiante
| Variable | Riesgo relativo | Intervalo de confianza 95% | p |
|---|---|---|---|
| Eventos vasculares mayores | 0,78 | 0,76-0,80 | <0,0001 |
| Mortalidad por cualquier causa | 0,90 | 0,87-0,93 | <0,0001 |
| Muerte por cardiopatía isquémica | 0,80 | 0,74-0,87 | <0,0001 |
| Muerte por otras causas cardiacas | 0,89 | 0,81-0,98 | 0,002 |
| Muertes por ictus | 0,96 | 0,84-1,09 | 0,5 |
Fuente: Adaptado17.
En un metaanálisis en el que se incluyeron 19 ensayos clínicos con 71.344 pacientes adultos sin enfermedad cardiovascular, el tratamiento con estatinas se asoció con un descenso en el riesgo de muerte por cualquier causa (RR: 0,86; IC 95%: 0,80-0,93), muerte de causa cardiovascular (RR: 0,69; IC 95%: 0,54-0,88), ictus (RR: 0,71; IC 95%: 0,62-0,82), infarto de miocardio (RR: 0,64; IC 95%: 0,57-0,71) y eventos cardiovasculares (RR: 0,70; IC 95%: 0,63-0,78). Si bien los beneficios relativos fueron consistentes en los diferentes subgrupos de pacientes, los beneficios absolutos fueron mayores en los subgrupos de mayor riesgo18.
En consecuencia, tanto en prevención primaria como en secundaria, la reducción del colesterol LDL con estatinas mejora el pronóstico cardiovascular.
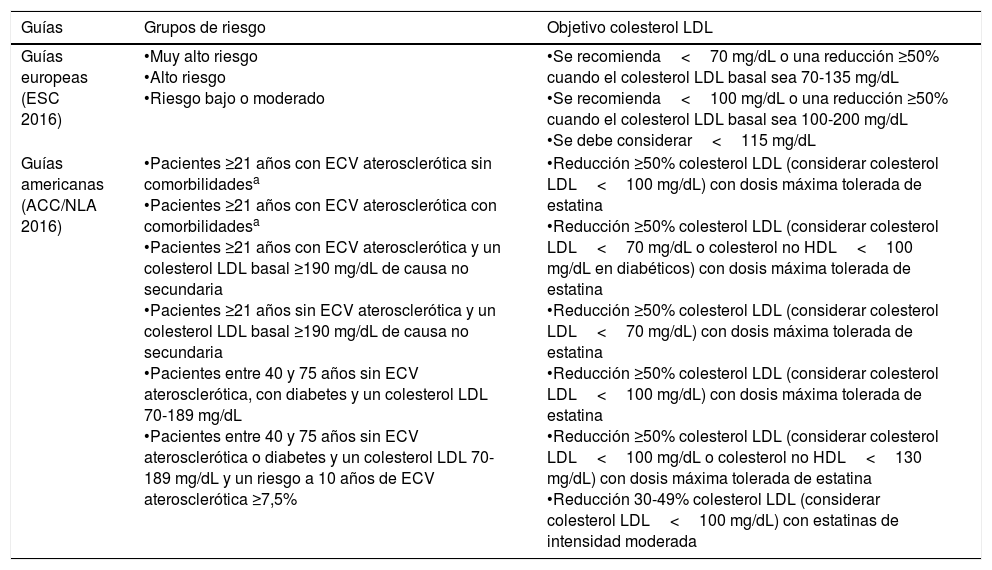
Aunque en las polémicas guías americanas de dislipidemia de 2013 se suprimieron los objetivos de colesterol LDL y prácticamente se limitaba el tratamiento hipolipidemiante al empleo de las estatinas, en la última actualización de estas guías, y como consecuencia de los nuevos datos publicados, se volvieron a establecer unos objetivos de colesterol LDL (con algunas diferencias con respecto a las guías europeas). Aunque las estatinas constituyen el tratamiento de elección en la mayoría de los pacientes, en determinados pacientes se pueden emplear otros tratamientos hipolipidemiantes para reducir el colesterol LDL19. En la tabla 3 se resumen las recomendaciones sobre la estratificación de riesgo propuesta por las guías europeas de dislipidemia de 2016 y en la tabla 4 las recomendaciones realizadas por la Sociedad Europea de Cardiología y por el Colegio Americano de Cardiología de 2016 sobre los objetivos terapéuticos, de acuerdo con los diferentes grupos de riesgo2,20.
Grupos de riesgo de acuerdo con las guías europeas de dislipidemia de 2016
| Categorías de riesgo | Características |
|---|---|
| Muy alto | •Enfermedad cardiovascular aterosclerótica (infarto de miocardio previo, síndrome coronario agudo, revascularización coronaria y otros procedimientos de revascularización arterial, ictus/ataque isquémico transitorio, aneurisma aórtico o enfermedad arterial periférica) •Diabetes mellitus con daño en órgano diana como proteinuria o con un factor de riesgo mayor •Enfermedad renal crónica grave (filtrado glomerular<30 ml/min/1,73 m2). •SCORE ≥10% a 10 años |
| Alto | •Factores de riesgo cardiovascular muy elevados •Resto de pacientes con diabetes mellitus (excepto jóvenes con diabetes tipo 1 sin factores de riesgo, que pueden tener un riesgo bajo o moderado) •Enfermedad renal crónica moderada (filtrado glomerular 30-59 ml/min/1,73 m2) •SCORE ≥5% y<10% a 10 años |
| Moderado | •SCORE ≥1% y<5% a 10 años |
| Bajo | •SCORE <1% a 10 años |
Fuente: Adaptado2.
Recomendaciones realizadas por las guías europeas y americanas de dislipidemia de 2016
| Guías | Grupos de riesgo | Objetivo colesterol LDL |
|---|---|---|
| Guías europeas (ESC 2016) | •Muy alto riesgo •Alto riesgo •Riesgo bajo o moderado | •Se recomienda<70 mg/dL o una reducción ≥50% cuando el colesterol LDL basal sea 70-135 mg/dL •Se recomienda<100 mg/dL o una reducción ≥50% cuando el colesterol LDL basal sea 100-200 mg/dL •Se debe considerar<115 mg/dL |
| Guías americanas (ACC/NLA 2016) | •Pacientes ≥21 años con ECV aterosclerótica sin comorbilidadesa •Pacientes ≥21 años con ECV aterosclerótica con comorbilidadesa •Pacientes ≥21 años con ECV aterosclerótica y un colesterol LDL basal ≥190 mg/dL de causa no secundaria •Pacientes ≥21 años sin ECV aterosclerótica y un colesterol LDL basal ≥190 mg/dL de causa no secundaria •Pacientes entre 40 y 75 años sin ECV aterosclerótica, con diabetes y un colesterol LDL 70-189 mg/dL •Pacientes entre 40 y 75 años sin ECV aterosclerótica o diabetes y un colesterol LDL 70-189 mg/dL y un riesgo a 10 años de ECV aterosclerótica ≥7,5% | •Reducción ≥50% colesterol LDL (considerar colesterol LDL<100 mg/dL) con dosis máxima tolerada de estatina •Reducción ≥50% colesterol LDL (considerar colesterol LDL<70 mg/dL o colesterol no HDL<100 mg/dL en diabéticos) con dosis máxima tolerada de estatina •Reducción ≥50% colesterol LDL (considerar colesterol LDL<70 mg/dL) con dosis máxima tolerada de estatina •Reducción ≥50% colesterol LDL (considerar colesterol LDL<100 mg/dL) con dosis máxima tolerada de estatina •Reducción ≥50% colesterol LDL (considerar colesterol LDL<100 mg/dL o colesterol no HDL<130 mg/dL) con dosis máxima tolerada de estatina •Reducción 30-49% colesterol LDL (considerar colesterol LDL<100 mg/dL) con estatinas de intensidad moderada |
ACC: American College of Cardiology; ECV: enfermedad cardiovascular; ESC: European Society of Cardiology; NLA: National Lipid Association.
Comorbilidades: diabetes, evento cardiovascular aterosclerótico agudo (<3 meses), ECV aterosclerótica mientras se está en tratamiento con estatinas, un colesterol LDL basal ≥190mg/dL no secundario a otras causas, pobre control de factores de riesgo CV, lipoproteína (a) elevada y enfermedad renal crónica.
Fuente: Adaptado2,20.
No solo es importante alcanzar los objetivos de control de colesterol LDL sino mantener este control a lo largo del tiempo. En un estudio en que se incluyó a 1.321 pacientes con síndrome coronario agudo tratados al alta con atorvastatina (80mg/día), al 42% de los pacientes o se les redujo la dosis de atorvastatina o se les cambió a otra estatina menos potente, en los 12 meses siguientes, bien por efectos secundarios o bien por miedo a que se presentaran. Esto se asoció con un aumento del colesterol LDL y, consecuentemente, con un incremento en los eventos adversos clínicos mayores21.
Ahora bien, aunque las evidencias actuales apuntan claramente a que el colesterol LDL, cuanto más bajo, mejor, la realidad es que todavía no se conoce si hay un umbral por debajo del cual reducir excesivamente el colesterol LDL podría ser perjudicial22,23. En el estudio JUPITER (rosuvastatina vs. placebo), aquellos pacientes que lograron un colesterol LDL<50mg/dL frente a aquellos que no lo lograron presentaron menos complicaciones cardiovasculares, sin un aumento en los efectos adversos24. En el estudio IMPROVE-IT, los pacientes con la combinación ezetimiba y simvastatina presentaron un colesterol LDL final de 53,7 frente al 69,5mg/dL en el grupo de monoterapia con simvastatina. Tras una mediana de seguimiento de 6 años, la terapia combinada se asoció con un descenso de los eventos cardiovasculares sin un aumento en el riesgo de efectos adversos15. Los inhibidores PCSK9 reducen de manera muy importante el colesterol LDL, incluso más del 60% en algunos casos16,25,26. En estos estudios, en el subgrupo de pacientes en los que se logró un colesterol LDL<30mg/dL, parece que no hubo un incremento el riesgo de efectos adversos. Sin embargo, hay que ser cautos, puesto que tanto el número de pacientes incluidos en estos subgrupos como el tiempo de seguimiento de estos pacientes fueron limitados. A la luz de estas evidencias, se puede afirmar que:
- •
El colesterol LDL, cuanto más bajo, mejor.
- •
Son seguros los objetivos actuales de control de colesterol LDL marcados por las guías de práctica clínica.
- •
Existen datos consistentes que muestran que reducir el colesterol LDL hasta 50mg/dL aporta beneficios cardiovasculares adicionales, sin un aumento en el riesgo de efectos adversos.
- •
A la espera de tener más datos (más estudios y, sobre todo, un tiempo de seguimiento mayor), reducciones por debajo de 50mg/dL de colesterol LDL se deberían reservar a pacientes de muy alto riesgo cardiovascular, como aquellos que siguen teniendo eventos cardiovasculares a pesar del tratamiento con estatinas a las dosis máximas toleradas.
- •
Finalmente, estudios que han analizado el seguimiento a largo plazo de los pacientes incluidos en los ensayos clínicos iniciales con estatinas han demostrado 2cosas: cuanto antes se trate al paciente y se logren los objetivos de control, mejor, y que el tratamiento hipolipidemiante se debe mantener a largo plazo para mantener los beneficios cardiovasculares a lo largo del tiempo27,28.
Las mayores evidencias acerca del beneficio pronóstico de reducir el colesterol LDL con el tratamiento hipolipidemiante provienen de los ensayos clínicos con las estatinas4–14. Por lo tanto, constituyen el tratamiento de elección para el manejo de la dislipidemia en la mayoría de los pacientes, como bien recomiendan las guías europeas y americanas2,20. Sin embargo, existe un porcentaje significativo de pacientes que o bien no logran los objetivos de colesterol LDL solo con las estatinas, o bien en ellos las estatinas no se pueden emplear (intolerancia, etc.). Aunque se dispone de otras posibilidades terapéuticas, además de la dieta y el ejercicio físico2,29, en los últimos años se han publicado 2 importantes ensayos clínicos (IMPROVE-IT, con ezetimiba y FOURIER, con evolocumab) que, por un lado, confirman la teoría lipídica de que el colesterol LDL cuanto más bajo, mejor y, por otro, que no solo con las estatinas se obtienen beneficios pronósticos15,16. En consecuencia, se dispone de 3 tratamientos (estatinas, ezetimiba e inhibidores PCSK9) que han demostrado disminuir los eventos cardiovasculares al reducir el colesterol LDL. El empleo de cada uno de ellos, solos o en combinación, dependerá del tipo de paciente y de sus características clínicas2,20.
Situación actual del control de la dislipidemiaEn el estudio EUROASPIRE IV, realizado en pacientes con cardiopatía isquémica crónica, el 86% de los varones y el 84% de las mujeres tomaban estatinas, y solo el 22% de los varones y el 17% de las mujeres lograron un colesterol LDL<70mg/dL30. En España, en pacientes con cardiopatía isquémica crónica, el control de colesterol LDL mejoró del 9,5% en 2006 al 27,2% en 2014. La prescripción de estatinas también aumentó del 69 al 96% (en la mayoría de los casos con estatinas de moderada a alta intensidad), así como la de ezetimiba (del 2,3 al 13,3%) (tabla 5)31. Otros estudios realizados en países de nuestro entorno muestran cifras similares tanto en prevención primaria como en secundaria32,33.
Control del colesterol LDL (<70mg/dL) en prevención secundaria
| Estudios | Proporción de pacientes con colesterol LDL<70 mg/dL | Tratamientos |
|---|---|---|
| EUROASPIRE IV | Varones: 22% Mujeres: 17% | Estatinas: •86% de los varones •84% de las mujeres |
| Cordero et al. | 2006: 9,5% 2014: 27,2% | Estatinas: •2006: 69% •2014: 96% Ezetimiba: •2006: 2,3% •2014:13,3% |
Fuente: Adaptado30,31.
En todo paciente con dislipidemia es imprescindible estratificar adecuadamente el riesgo cardiovascular y, de esta forma, conocer cuál debe ser su objetivo de colesterol LDL. Es imprescindible lograr los objetivos de colesterol LDL para mejorar el pronóstico de los pacientes con dislipidemia. Incluso reducciones mayores a las recomendadas de colesterol LDL parecen ser beneficiosas y seguras. El tratamiento con mayores evidencias actualmente disponible en cuanto a beneficio pronóstico son las estatinas y, por lo tanto, constituyen el tratamiento de elección en la mayoría de los pacientes. Sin embargo, en aquellos casos en los que no sea posible el empleo de las estatinas o en los que estas resulten insuficientes, existen otras alternativas terapéuticas que reducen el colesterol LDL y que también han demostrado ser beneficiosas. Por lo tanto, en la actualidad disponemos de un amplio abanico de tratamientos hipolipidemiantes que son eficaces y que, solos o en combinación, van a permitir alcanzar los objetivos de control en la mayoría de los pacientes.