La enfermedad tromboembólica venosa (ETEV), que comprende la trombosis venosa profunda y la tromboembolia pulmonar, constituye un problema de salud por su alta incidencia, morbimortalidad y costes sociosanitarios. El mejor tratamiento es la profilaxis de ésta. Aunque la clase sanitaria ha asumido mayoritariamente la instauración de la profilaxis en el paciente quirúrgico o traumatológico, no ha ocurrido lo mismo en el paciente con patología médica, tanto hospitalizado como ambulatorio. El paciente con patología médica presenta ETEV de forma más frecuente y más grave que el quirúrgico o el traumatológico cuando no se instaura la profilaxis adecuada. La correcta estratificación del riesgo que presenta este tipo de sujeto nos inducirá a instaurar la prevención más idónea para la ETEV. En la valoración de riesgo, la guía PRETEMED ha aportado la descripción de los factores de riesgo de ETEV relacionados con el paciente con patología médica, definiendo unas recomendaciones sobre la instauración de la profilaxis en este tipo de pacientes hospitalizados o ambulatorios.
Venous thromboembolic disease (VTED), that includes deep venous thrombosis and pulmonary thromboemolism, constitutes a health problem due to its high incidence, morbidity-mortality and socio-health care costs. The best treatment is its prophylaxis. Although the health care class has most assumed the establishment of prophylaxis in the surgical or trauma patient, the same has not occurred in the hospitalized patient or out-patient with a medical condition. The patient with a medical condition has VTED more frequently and more severely than the surgical or trauma patient when adequate prophylaxis is not established. Correct staging of the risk presented by this type of subject will lead us to establish the best prevention for VTED. In the evaluation of risk, the PRETEMED guide has provided the description of the risk factors of VTED related with the medical patient, defining some recommendations on the establishment of the prophylaxis in this type of hospitalized patient or out-patient.
La oclusión parcial o total de la luz venosa del sistema venoso profundo de las extremidades inferiores por un trombo de fibrina da lugar al cuadro conocido como trombosis venosa profunda (TVP). En la evolución de este trombo puede ocurrir el desprendimiento de un fragmento que, viajando por el sistema venoso profundo de las extremidades inferiores, se enclave en el árbol arterial pulmonar, dando lugar a la tromboembolia pulmonar (TEP). Ambos cuadros, íntimamente relacionados, constituyen la entidad patológica denominada enfermedad tromboembólica venosa (ETEV).
La ETEV, con una incidencia de 1–2 casos/1.000 habitantes/año y una prevalencia del 3–5%, se erige actualmente como la 3.a causa de muerte cardiovascular, tras la cardiopatía isquémica y el ictus. Actualmente supone la causa más frecuente de muerte evitable en hospitales. Se le atribuye una mortalidad del 14–17% a los 3 meses, siendo del 29% a los 7 días en el caso de la TEP o del 39% al año en el caso de los ancianos, y recurre en un 20–25% de los casos a los 5 años del diagnóstico; además, la TEP debuta en un 25% de las ocasiones como una muerte súbita. El coste sanitario de la enfermedad es muy alto, situándose alrededor de los 60.000€ en el año 2005, y viene acompañado de un coste social también elevado por la ocupación de camas, incapacidades laborales y la disminución de la calidad de vida del paciente debido a su alta morbilidad (síndrome postrombótico, hipertensión pulmonar, complicaciones hemorrágicas del tratamiento)1.
La reducción de la carga de la ETEV requiere una prevención primaria efectiva, un diagnóstico temprano, un tratamiento apropiado del proceso trombótico agudo y una prevención secundaria eficaz2.
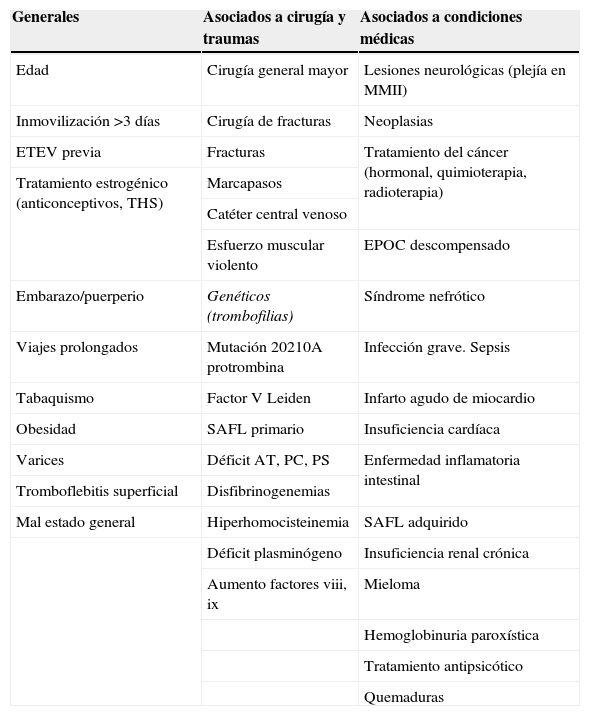
Se han identificado numerosos factores de riesgo (FR) para la ETEV; sin embargo, la magnitud del riesgo conferido varía de unos a otros y hay evidencia de que el riesgo de ETEV se incrementa proporcionalmente al número de FR predisponentes presentes, de forma que el 85% de los pacientes con TVP tenía al menos un FR, y más del 50% tenía al menos dos en el estudio de Samama et al3. Se han dividido en generales, relacionados con la cirugía y los traumatismos, hereditarios y los relacionados con circunstancias o patologías médicas (tabla 1)1.
Factores de riesgo para la enfermedad tromboembólica venosa
| Generales | Asociados a cirugía y traumas | Asociados a condiciones médicas |
| Edad | Cirugía general mayor | Lesiones neurológicas (plejía en MMII) |
| Inmovilización >3 días | Cirugía de fracturas | Neoplasias |
| ETEV previa | Fracturas | Tratamiento del cáncer (hormonal, quimioterapia, radioterapia) |
| Tratamiento estrogénico (anticonceptivos, THS) | Marcapasos | |
| Catéter central venoso | ||
| Esfuerzo muscular violento | EPOC descompensado | |
| Embarazo/puerperio | Genéticos (trombofilias) | Síndrome nefrótico |
| Viajes prolongados | Mutación 20210A protrombina | Infección grave. Sepsis |
| Tabaquismo | Factor V Leiden | Infarto agudo de miocardio |
| Obesidad | SAFL primario | Insuficiencia cardíaca |
| Varices | Déficit AT, PC, PS | Enfermedad inflamatoria intestinal |
| Tromboflebitis superficial | Disfibrinogenemias | |
| Mal estado general | Hiperhomocisteinemia | SAFL adquirido |
| Déficit plasminógeno | Insuficiencia renal crónica | |
| Aumento factores viii, ix | Mieloma | |
| Hemoglobinuria paroxística | ||
| Tratamiento antipsicótico | ||
| Quemaduras |
AT: antitrombina; EPOC: enfermedad pulmonar obstructiva crónica; ETEV: enfermedad tromboembólica venosa; MMII: miembros inferiores PC: proteína C, PS: proteína S; SAFL: síndrome antifosfolípido; THS: tratamiento hormonal sustitutivo.
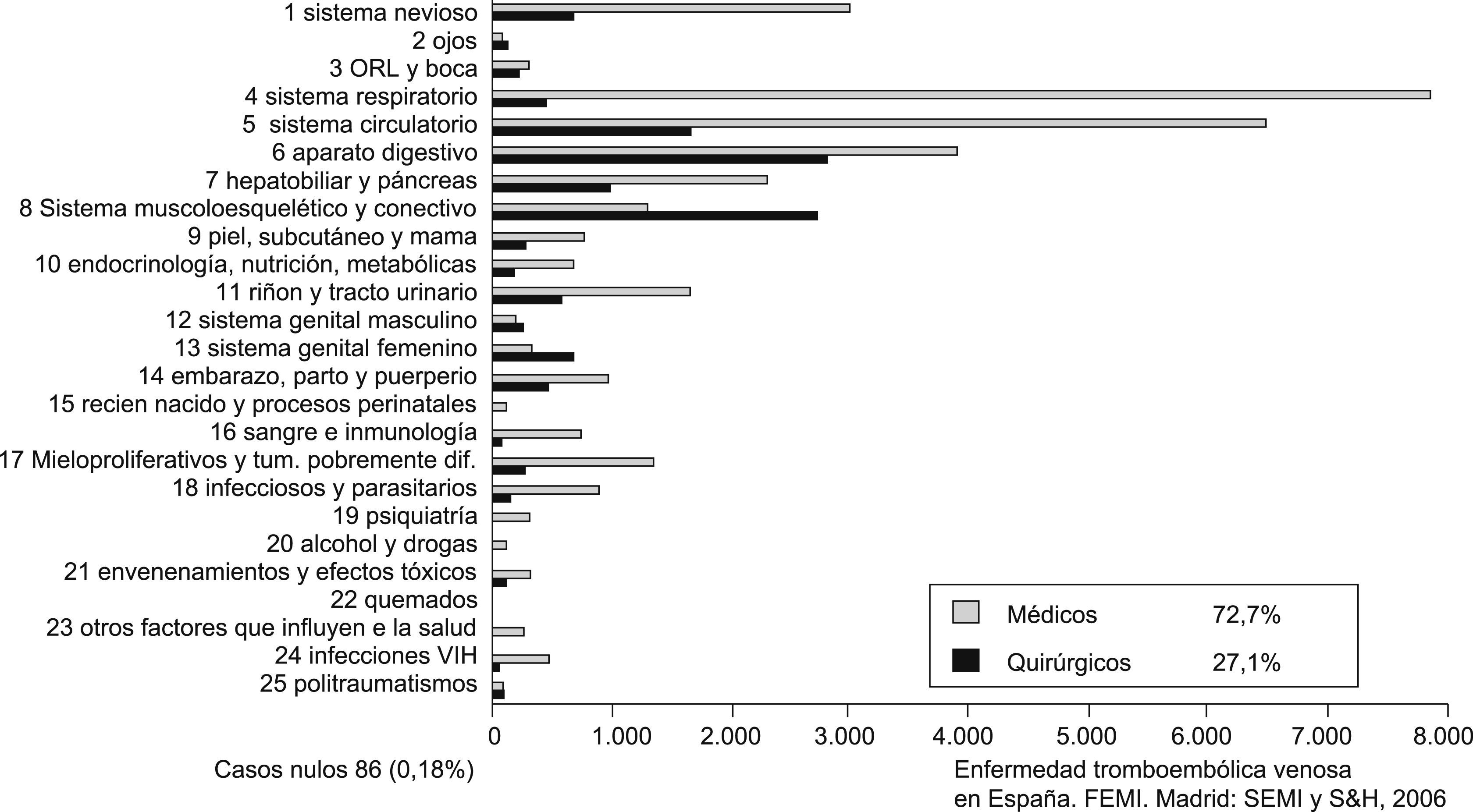
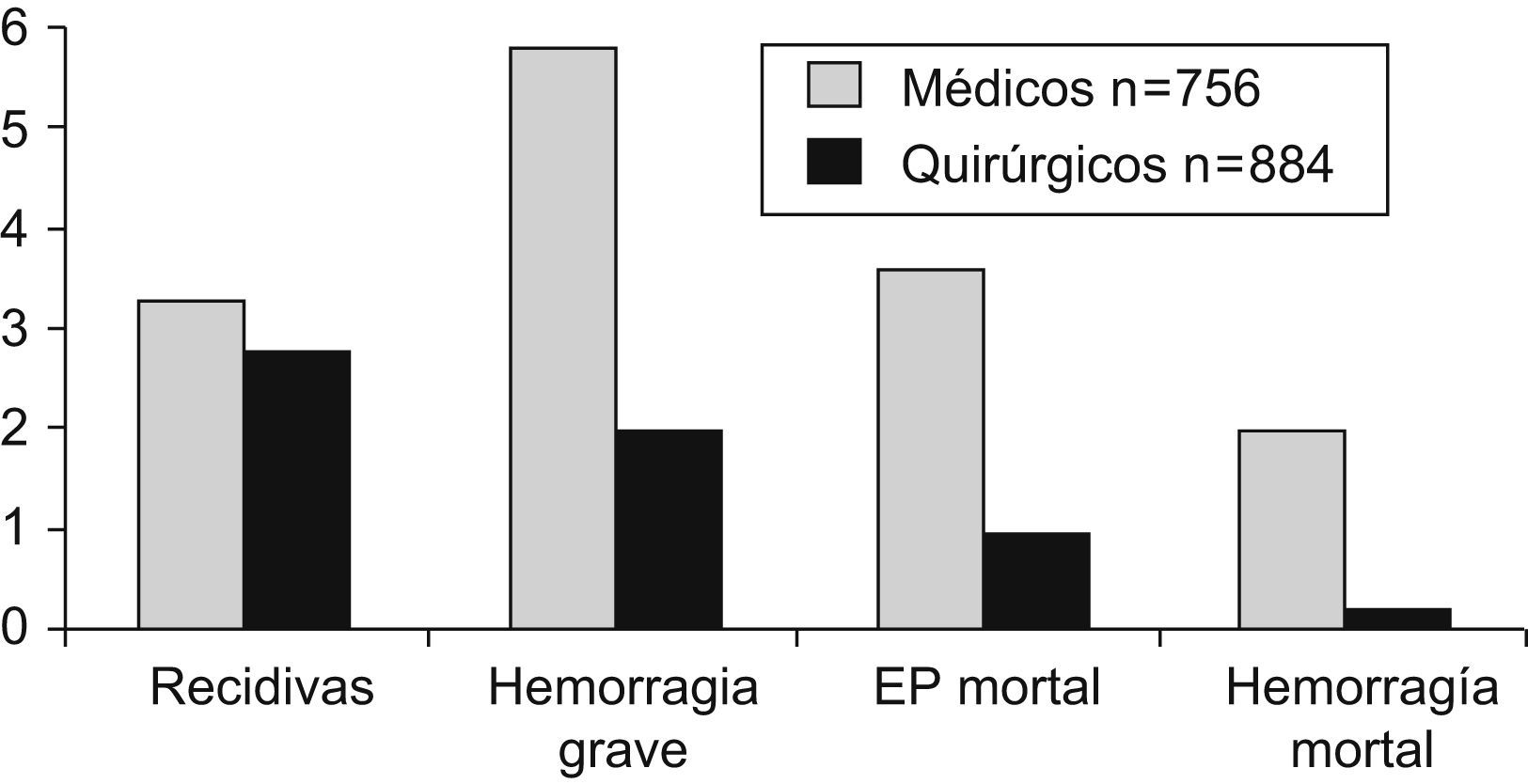
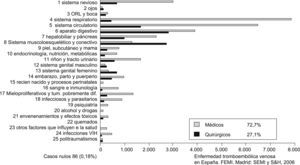
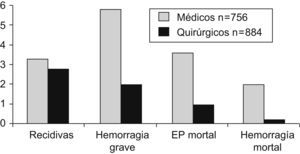
Aunque la frecuencia de la ETEV sea superior en pacientes sometidos a cirugía (15–60%) que en los ingresados por patología médica (10–20%), estos últimos constituyen la mayoría de los ingresos hospitalarios, por lo que la frecuencia de la ETEV es mayor en ellos4. Así, la hospitalización por una enfermedad médica aguda está independientemente asociada a un incremento de 8 veces el riesgo relativo de ETEV, de forma que el 50–70% de accidentes tromboembólicos sintomáticos y el 70–80% de TEP ocurren en estos pacientes no quirúrgicos4. Además, la ETEV en pacientes con un proceso médico es más grave que con uno quirúrgico porque presentan 4 veces más muertes por TEP, tienen 3 veces más tasa de hemorragias graves y 9 veces más de hemorragias mortales. Las principales patologías implicadas fueron insuficiencia cardíaca, enfermedades pulmonares, infecciones agudas y neoplasias5 (figs. 1 y 2).
De los pacientes ingresados en el hospital que desarrollaron una enfermedad tromboembólica venosa (ETEV), el 72,7%, es decir, 3 de cada 4, son enfermos cuyo motivo de ingreso en el hospital fue una enfermedad médica. Solamente el 27% de los pacientes que estando ingresados en el hospital desarrollan una ETEV, ésta es consecuencia de la intervención quirúrgica que se le ha practicado (datos del Ministerio de Sanidad).
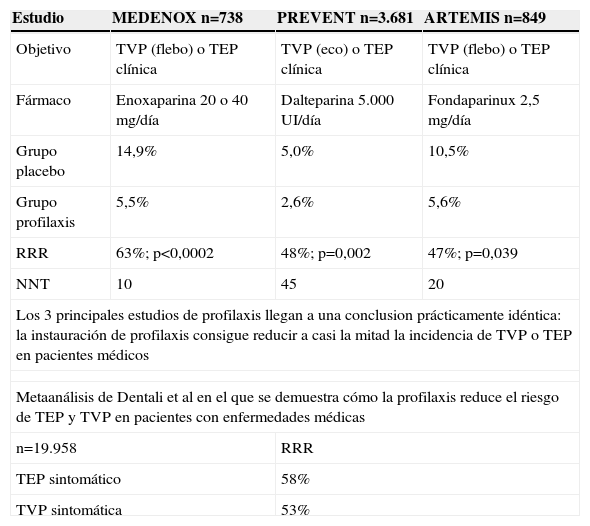
La necesidad de la tromboprofilaxis en pacientes con patología médica y otros FR se basa en el carácter silente de la ETEV, en las consecuencias deletéreas de no realizar profilaxis, en el alto coste sociosanitario de las complicaciones y en la probada eficacia de su indicación4,6–9 (tabla 2).
Estudios de prevención en pacientes con patología médica
| Estudio | MEDENOX n=738 | PREVENT n=3.681 | ARTEMIS n=849 |
| Objetivo | TVP (flebo) o TEP clínica | TVP (eco) o TEP clínica | TVP (flebo) o TEP clínica |
| Fármaco | Enoxaparina 20 o 40mg/día | Dalteparina 5.000UI/día | Fondaparinux 2,5mg/día |
| Grupo placebo | 14,9% | 5,0% | 10,5% |
| Grupo profilaxis | 5,5% | 2,6% | 5,6% |
| RRR | 63%; p<0,0002 | 48%; p=0,002 | 47%; p=0,039 |
| NNT | 10 | 45 | 20 |
| Los 3 principales estudios de profilaxis llegan a una conclusion prácticamente idéntica: la instauración de profilaxis consigue reducir a casi la mitad la incidencia de TVP o TEP en pacientes médicos | |||
| Metaanálisis de Dentali et al en el que se demuestra cómo la profilaxis reduce el riesgo de TEP y TVP en pacientes con enfermedades médicas | |||
| n=19.958 | RRR | ||
| TEP sintomático | 58% | ||
| TVP sintomática | 53% | ||
ARTEMIX: Arixtra for Thromboembolism Prevention in a Medical Indications Study; MEDENOX: Prophylaxis in Medical Patients with Enoxaparin Study Group; PREVENT: prevention of venous thromboembolism in acutely ill medical patients; Eco: ecografía; flebo: flebografía; NNT: número necesario de pacientes para tratar; TEP: tromboembolismo pulmonar; TVP: trombosis venosa profunda; RRR: reducción del riesgo relativo con profilaxis.
Si bien se le ha dado gran importancia a la prevención de la ETEV en pacientes quirúrgicos ortopédicos y traumatológicos, no ha ocurrido así con el grupo de pacientes sometidos a otro tipo de cirugía y mucho menos con pacientes que padecen una enfermedad médica, quizá porque la información disponible en pacientes con procesos médicos es cualitativa y cuantitativamente menor. En el marco extrahospitalario, la tromboprofilaxis de estos pacientes encamados o inmovilizados en su domicilio es un problema aún no resuelto. También, en algunas circunstancias, el riesgo de ETEV en pacientes hospitalizados no desaparece con el alta, y la profilaxis debe mantenerse en su domicilio hasta que desaparezca aquel; pero en otras ocasiones, el riesgo de ETEV aparece aun sin precisar el ingreso hospitalario y es aquí donde el médico de atención primaria (AP) juega un papel destacado en la profilaxis de la enfermedad.
Situaciones de riesgo de enfermedad tromboembólica venosa en el paciente con patología médica de ámbito extrahospitalarioAunque la mayoría de los estudios se realizan en el ámbito hospitalario y la información sobre pacientes con patología médica es cualitativa y cuantitativamente menor que en pacientes quirúrgicos, las situaciones de riesgo de ETEV no son exclusivas del hospital, ya que los perfiles de pacientes con riesgo de ETEV en AP no difieren mucho con respecto a la población hospitalaria3,10–14. Del mismo modo, las circunstancias de riesgo no acaban con el alta hospitalaria, prolongándose éstas en el tiempo, y, junto con la aparición de situaciones que aumentan el riesgo de ETEV sin necesidad de ingreso hospitalario, implican al médico de familia en el manejo de la tromboprofilaxis de estos pacientes.
Los FR de la ETEV y las situaciones asociadas a la patología médica han sido descritos recientemente en la guía para la prevención de la ETEV en pacientes con patología médica (prevención de la enfermedad tromboembólica venosa en paciente médico [PRETEMED])15. Esta guía describe y pondera los diferentes FR relacionados con la ETEV en un intento de calcular el riesgo ajustado que presenta el enfermo con patología no quirúrgica para establecer unas recomendaciones a la hora de facilitar la toma de decisiones en la práctica diaria.
Enumera los factores relacionados sobre la base de aquellos que son de bajo, moderado o alto riesgo y los clasifica por pesos, según la incidencia de la ETEV (tabla 3).
Peso de los distintos factores de riesgo de enfermedad tromboembólica venosa en pacientes no quirúrgicos ni con traumatismos mayores según la guía PRETEMED 2007
| Factores de riesgo para la enfermedad tromboembólica venosa en pacientes con patología médica | |||||
| Sin riesgo | Riesgo bajo | Riesgo medio | Alto riesgo | ||
| Peso 0 | Peso 1 (incidencia de ETEV <0,99%) | Peso 2 (incidencia de ETEV 1–9,9%) | Peso 3 (incidencia de ETEV 10–19,9%) | Peso 4 (incidencia de ETEV 20–29,9%) | Peso 5 (incidencia de ETV 30–39,9%) |
| Sedentarismo | Edad >60 años | Encamamiento >4 días en >50 años | EPOC descompensada grave | Embarazo+ETEV previa | TVP previa con trombofilia |
| Marcapasos | |||||
| Raloxifeno a partir del 3.er año | Embarazo | Mieloma múltiple+quimioterapia+talidomida | |||
| Puerperio | |||||
| Trombocitosis | TVP previa | ACV con parálisis EI | |||
| Varices | Anticonceptivos orales | ICC clase iii NYHA | ICC clase iv NYHA | Neoplasia mama+quimioterapia | |
| Catéter epidural | |||||
| DIU | Tratamiento hormonal sustitutivo | Infección aguda grave | |||
| Etilismo | IAM | C. Pulmón+cirugía | |||
| HPN | Síndrome nefrótico | C. Pulmón+quimioterapia | |||
| Hepatopatía | Neoplasias | Mieloma | C. Pulmón+metástasis | ||
| Ranelato estroncio | Enfermedad inflamatoria intestinal activa | Múltiple+quimioterapia | |||
| Síndrome mieloproliferativo | Antipsicóticos | ||||
| Estimuladores ováricos | Traumas EI sin cirugía | ||||
| Ocupación | Inhibidores de la aromatasa | ||||
| Ubicación del paciente | Vasculitis: enfermedad de Behçet, enfermedad de Wegener | ||||
| Riesgo desconocido: | Tamoxifeno | Embarazo+trombofilia | |||
| Dislipemia | |||||
| Insuficiencia renal crónica | Raloxifeno, durante 2 primeros años | 1.er episodio de TVP espontánea | |||
| Género | Trombofilias: | ||||
| Viaje avión <6h | Diabetes mellitus | anticuerpos antifosfolipídicos | |||
| Hiperhomocisteinemia | Déficit antitrombina | ||||
| Déficit proteína C o S | |||||
| Hiperlipoproteinemia (a) | Factor v Leiden en >60 años | ||||
| VIH | |||||
| Obesidad (IMC >30) | |||||
| Tabaquismo: >35 cigarrillos/día | |||||
| Parálisis de EI como secuela de ACV | |||||
| Viaje en avión >6h | |||||
| Trombofilias: | |||||
| Factor viii | |||||
| Factor v Leyden | |||||
ACV: accidente cerebrovascular; DIU: dispositivo intrauterino; EI: extremidades inferiores; EPOC: enfermedad pulmonar obstructiva crónica; ETEV: enfermedad tromboembólica venosa; HPN: hemoglobinuria paroxística nocturna; ICC: insuficiencia cardíaca crónica; IMC: índice de masa corporal; NYHA: New York Heart Association; TVP: trombosis venosa profunda; VIH: virus de la inmunodeficiencia humana.
Los pacientes hospitalizados por procesos médicos adquieren riesgo de ETEV especialmente elevado si pertenecen al grupo de edad avanzada, padecen determinadas afecciones crónicas (como la insuficiencia cardíaca o la enfermedad pulmonar obstructiva crónica) o agudas (como la sepsis), su estado general está deteriorado o se ven sometidos a inmovilización. Pero estas circunstancias se dan también en pacientes que, por su menor gravedad o por hallarse en fase subaguda del proceso, siguen régimen ambulatorio o de hospitalización domiciliaria16. Así concluyen autores como Samama3, afirmando que la incidencia de TVP aumenta a medida que confluyen diversos contingentes (más del 85% de los pacientes con TVP tenía al menos un FR, y más del 50% tenía al menos dos, mientras que más del 80% de los controles presentaba uno o ninguno) y, dado que alrededor del 60% de las ETEV acontecen después de la hospitalización y que el 60% de ellas a su vez incide en pacientes no quirúrgicos, el riesgo de ETEV podría no limitarse al ingreso médico en su fase aguda, sino extenderse al medio ambulatorio y de hospitalización domiciliaria. Los autores recomiendan que se valore el riesgo individual de que se presente una TVP en pacientes con patología médica incluso extrahospitalariamente.
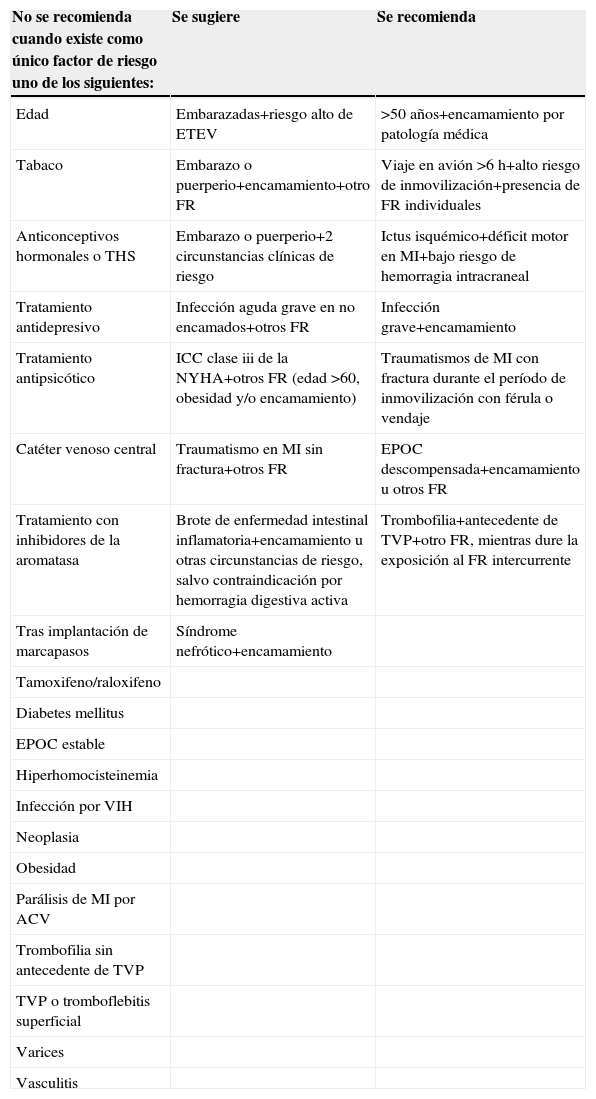
El perfil de riesgo del paciente ambulatorio subsidiario de tromboprofilaxis vendría definido por una situación precipitante que se añade al padecimiento de un proceso o a una situación médica de riesgo. De todas ellas, quizá la inmovilización/encamamiento sea el factor asociado más frecuente en el medio extrahospitalario. Esto habría que aplicarlo también al paciente institucionalizado (residencia de ancianos, hogares de día) y a pacientes con movilidad reducida, como es el caso de aquellos que realizan viajes de más de 6h de duración en cualquier medio de transporte. En la tabla 4 se han definido varios escenarios de riesgo y la recomendación de hacer o no profilaxis de la ETEV.
Algunas situaciones de riesgo en atención primaria y recomendaciones sobre la profilaxis de enfermedad tromboembólica venosa en el paciente médico
| No se recomienda cuando existe como único factor de riesgo uno de los siguientes: | Se sugiere | Se recomienda |
| Edad | Embarazadas+riesgo alto de ETEV | >50 años+encamamiento por patología médica |
| Tabaco | Embarazo o puerperio+encamamiento+otro FR | Viaje en avión >6h+alto riesgo de inmovilización+presencia de FR individuales |
| Anticonceptivos hormonales o THS | Embarazo o puerperio+2 circunstancias clínicas de riesgo | Ictus isquémico+déficit motor en MI+bajo riesgo de hemorragia intracraneal |
| Tratamiento antidepresivo | Infección aguda grave en no encamados+otros FR | Infección grave+encamamiento |
| Tratamiento antipsicótico | ICC clase iii de la NYHA+otros FR (edad >60, obesidad y/o encamamiento) | Traumatismos de MI con fractura durante el período de inmovilización con férula o vendaje |
| Catéter venoso central | Traumatismo en MI sin fractura+otros FR | EPOC descompensada+encamamiento u otros FR |
| Tratamiento con inhibidores de la aromatasa | Brote de enfermedad intestinal inflamatoria+encamamiento u otras circunstancias de riesgo, salvo contraindicación por hemorragia digestiva activa | Trombofilia+antecedente de TVP+otro FR, mientras dure la exposición al FR intercurrente |
| Tras implantación de marcapasos | Síndrome nefrótico+encamamiento | |
| Tamoxifeno/raloxifeno | ||
| Diabetes mellitus | ||
| EPOC estable | ||
| Hiperhomocisteinemia | ||
| Infección por VIH | ||
| Neoplasia | ||
| Obesidad | ||
| Parálisis de MI por ACV | ||
| Trombofilia sin antecedente de TVP | ||
| TVP o tromboflebitis superficial | ||
| Varices | ||
| Vasculitis |
ACV: accidente cerebrovascular; ETEV: enfermedad tromboembólica venosa; FR: factor de riesgo; THS: tratamiento hormonal sustitutivo; ICC: insuficiencia cardíaca crónica; NYHA: New York Heart Association; MI: miembros inferiores; TVP: trombosis venosa profunda.
Es cierto que existen diversos obstáculos a la hora de implementar la tromboprofilaxis del paciente con patología médica en AP (tabla 5) y que los escenarios que se pueden presentar, derivados de las distintas combinaciones de FR, son diversos y variados. Para ello, una de las aportaciones más reseñables de la guía PRETEMED ha sido el diseño de una tabla de cálculo del riesgo de ETEV en procesos médicos. A partir de la ponderación del nivel de riesgo, se ha elegido la necesidad de intervención farmacológica cuando el cómputo global ha sido mayor o igual a 4, que correspondería a una incidencia de ETEV del 20%, riesgo a partir del cual se recomienda anticoagular.
Obstáculos para una adecuada tromboprofilaxis de la enfermedad tromboembólica venosa en atención primaria
|
ETEV: enfermedad tromboembólica venosa.
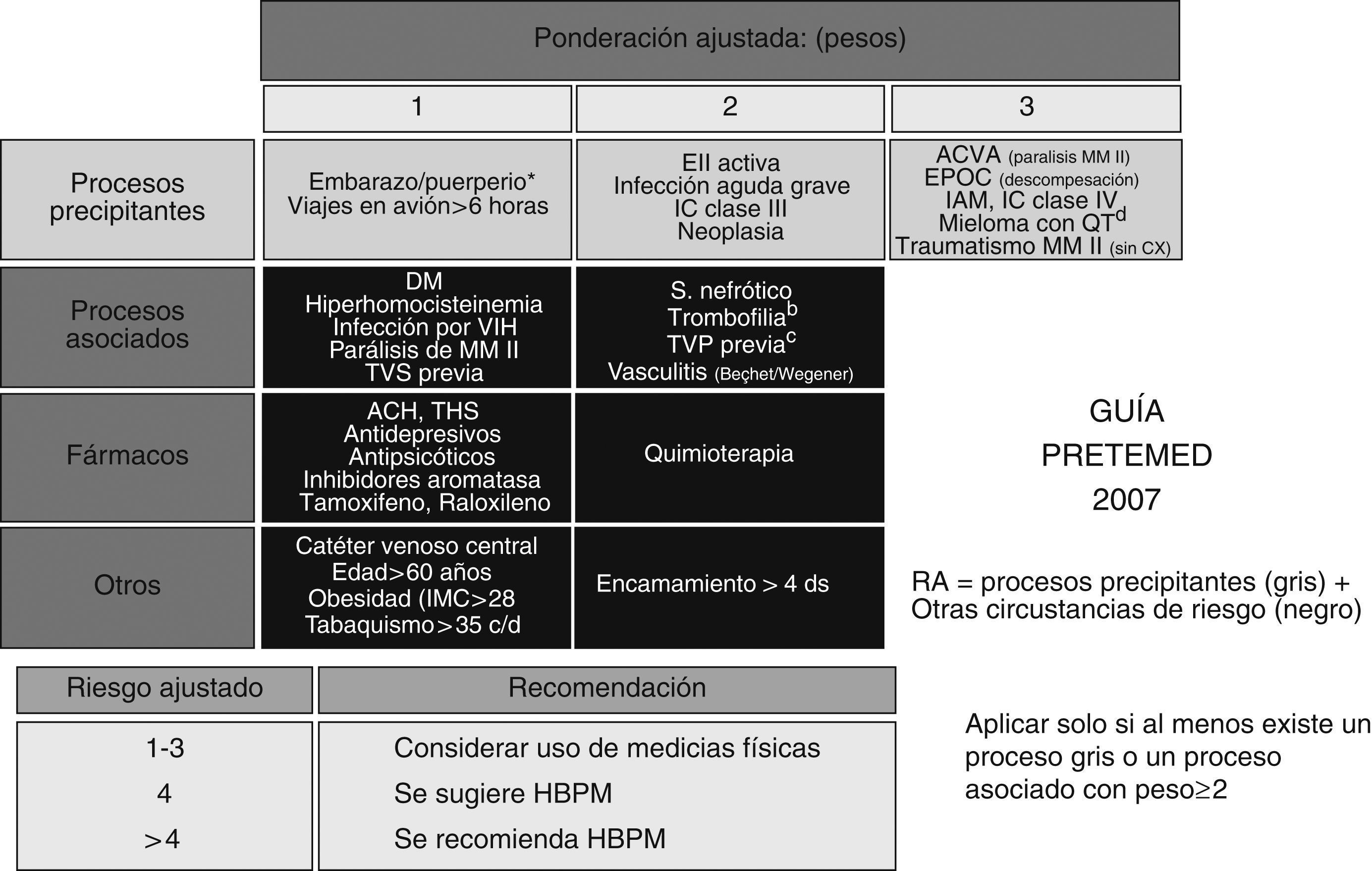
De esta forma, la incertidumbre del balance riesgo-beneficio de la instauración de tromboprofilaxis en el paciente médico ambulatorio ha quedado más clarificada, puesto que la guía PRETEMED no sólo presenta las evidencias sobre el riesgo de ETEV en una tabla en la que se ha adjudicado un peso específico a cada circunstancia de riesgo, sino que también ha elaborado otra en la que se pueden valorar los escenarios que se presentan habitualmente en la práctica diaria como combinación de circunstancias (fig. 3).
Tabla para el cálculo del riesgo ajustado y recomendaciones profilácticas en el paciente médico.
ACH: anticonceptivos hormonales; ACVA: accidente cerebrovascular agudo; CX: cirugía; DM: diabetes mellitus; EII: enfermedad inflamatoria intestinal; HBPM: heparina de bajo peso molecular; IAM: infarto agudo de miocardio; ICC: insuficiencia cardíaca crónica; QT: quimioterapia; RA: riesgo absoluto; THS: tratamiento hormonal sustitutivo; TVP: trombosis venosa profunda; TVS: trombosis venosa superficial.
Para calcular el riesgo ajustado de cada paciente con patología médica, utilizaremos la tabla si el paciente presenta al menos un proceso precipitante (gris) o un proceso asociado con peso ajustado mayor o igual a 2.
A partir de ahí, iremos sumando circunstancias de acuerdo con el peso ajustado otorgado. Cuando la suma de puntuación sea entre 1–3, se considerará el uso de medidas físicas. Si la puntuación es mayor que 4, existe una recomendación fuerte, alta confianza y poca incertidumbre, que indican que los beneficios claramente superan los riesgos al instaurar una profilaxis farmacológica con heparinas de bajo peso molecular (HBPM). Si la puntuación es 4, la recomendación de inicio de profilaxis farmacológica con HBPM es más débil, indicando que los beneficios probablemente superan los riesgos. En este caso, es de esperar variabilidad en la práctica médica, pero la decisión puede tomarse basándose en otros factores individuales.
Medios para realizar tromboprofilaxis de la enfermedad tromboembólica venosa- A.
Medidas generales. La deambulación precoz, la elevación de las extremidades inferiores, la hidratación adecuada del paciente y los ejercicios antiestasis venosa constituyen medidas importantes en la prevención de la ETEV.
- B.
Compresión elástica externa. La terapia compresiva mediante medias o vendajes es un método preventivo seguro y moderadamente eficaz. Las medias de compresión gradual reducen la distensión patológica venosa, mejoran la insuficiencia valvular y reducen el volumen de sangre venosa en las extremidades inferiores acelerando el retorno venoso. También aumentan la actividad fibrinolítica parietal, disminuyendo el riesgo de trombosis. En una revisión sistemática de Roderick et al17, el uso de medias de compresión gradual en monoterapia redujo la incidencia de TVP en un 66% frente al grupo control (p=0,00001). Asimismo, cuando la compresión se asociaba a medidas farmacológicas, se producía una reducción adicional del 60% de TVP. Datos similares fueron también publicados en una revisión Cochrane por Amaragiri et al18.
En pacientes encamados se pueden utilizar medias de compresión normal según la normativa española. En pacientes de alto riesgo se deben utilizar las de compresión fuerte (presión en tobillo de 30mmHg)15,19.
Una de las ventajas de la terapia compresiva es que se puede utilizar en pacientes con alto riesgo de sangrado4.
No debemos olvidar las situaciones en las que está contraindicada la terapia compresiva de forma absoluta, como ocurre en pacientes con isquemia arterial y dermatitis, artritis reumatoide en fase aguda, neuropatía diabética, alergia al tejido o relativa, como es el caso de la insuficiencia cardíaca congestiva descompensada y de la hipertensión arterial19.
- C.
Fármacos anticoagulantes
- a)
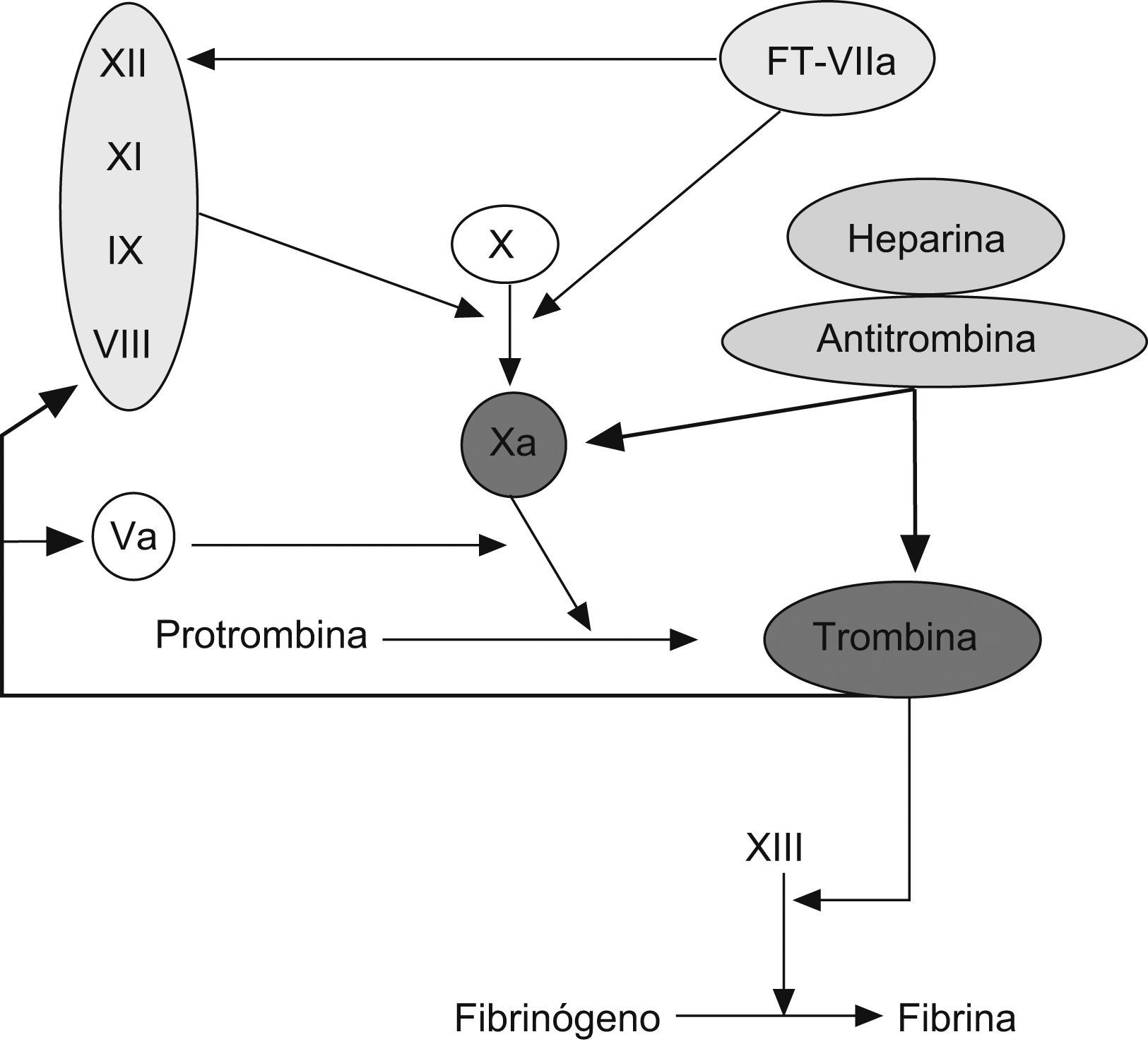
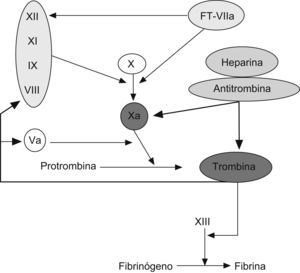
Heparinas. Las heparinas son glucosaminoglicanos constituidos por una mezcla de largas cadenas de unidades de sacáridos. Actúan potenciando la actividad neutralizante de la antitrombina sobre el factor xa, además de los factores ixa, xia y xiia (acción antitrombótica). De forma secundaria, participa en la inactivación de la trombina (factor iia) (acción anticoagulante) (fig. 4). En la actualidad disponemos de la heparina no fraccionada (HNF) y de las HBPM. Estas últimas derivan de la HNF por despolimerización química o enzimática.
Las HBPM poseen una biodisponibilidad cercana al 90% tras inyección subcutánea, con un efecto anticoagulante más predecible que las HNF, por lo que no precisan monitorización plasmática de niveles, salvo circunstancias especiales (obesidad importante o insuficiencia renal). Si se requiere monitorización, se deben solicitar los niveles anti-xa tras 4h de la dosis. Poseen una vida media más larga que las HNF y se pueden administrar cada 12 o 24h; tienen menor riesgo de osteoporosis y de trombocitopenia inducida, así como de hemorragias graves20.
Además, su seguridad y eficacia en la prevención del paciente con patología médica viene avalada por numerosos estudios clínicos4.
Todo ello las hace ser las heparinas de elección para el paciente con patología médica en el medio ambulatorio.
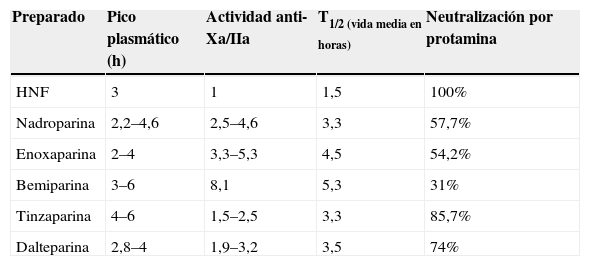
Un concepto importante es que las HBPM son fármacos distintos y no intercambiables y que, con cada producto, varía también su capacidad antitrombótica (aunque posean igual actividad anti-Xa) y su riesgo hemorrágico, por lo que no se recomienda sustituir una por otra una vez iniciado el tratamiento1,20,22. En las tablas 6 y 7 se describen sus características principales y la dosificación en la prevención de la ETEV.
Tabla 6.Características de las heparinas
Preparado Pico plasmático (h) Actividad anti-Xa/IIa T1/2 (vida media en horas) Neutralización por protamina HNF 3 1 1,5 100% Nadroparina 2,2–4,6 2,5–4,6 3,3 57,7% Enoxaparina 2–4 3,3–5,3 4,5 54,2% Bemiparina 3–6 8,1 5,3 31% Tinzaparina 4–6 1,5–2,5 3,3 85,7% Dalteparina 2,8–4 1,9–3,2 3,5 74% HNF: heparina no fraccionada.
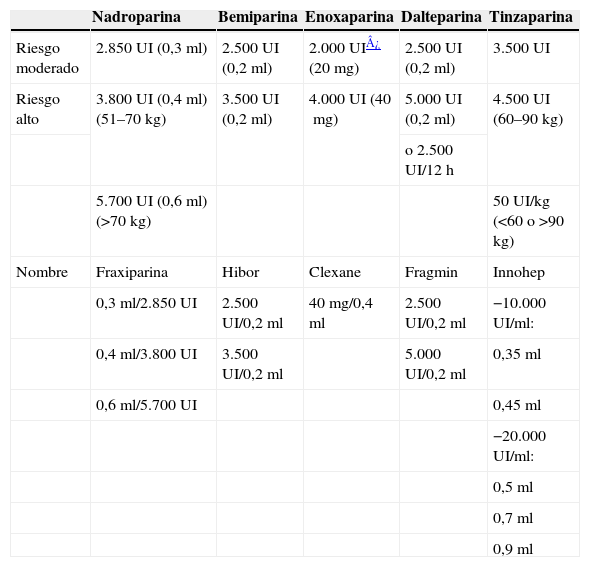
Tabla 7.Profilaxis de la enfermedad tromboembólica venosa. Dosis profilácticas de las distintas heparinas de bajo peso molecular según el riesgo
Nadroparina Bemiparina Enoxaparina Dalteparina Tinzaparina Riesgo moderado 2.850UI (0,3ml) 2.500UI (0,2ml) 2.000 UI¿ (20mg) 2.500UI (0,2ml) 3.500UI Riesgo alto 3.800UI (0,4ml) (51–70kg) 3.500UI (0,2ml) 4.000 UI (40mg) 5.000 UI (0,2ml) 4.500UI (60–90kg) o 2.500 UI/12h 5.700UI (0,6ml) (>70kg) 50UI/kg (<60 o >90kg) Nombre Fraxiparina Hibor Clexane Fragmin Innohep 0,3ml/2.850UI 2.500UI/0,2ml 40mg/0,4ml 2.500UI/0,2ml −10.000UI/ml: 0,4ml/3.800UI 3.500UI/0,2ml 5.000UI/0,2ml 0,35ml 0,6ml/5.700UI 0,45ml −20.000UI/ml: 0,5ml 0,7ml 0,9ml Los efectos adversos más frecuentes de las heparinas son la hemorragia y la trombocitopenia, por lo que se debe hacer un control analítico a la semana de tratamiento. Las hemorragias suelen ser más frecuentes en edad avanzada, insuficiencia renal, cirugía reciente, lesiones locales, traumatismos, alteraciones en la hemostasis, uso de antitrombóticos o ácido acetilsalicílico, aunque su porcentaje es mínimo20. El sulfato de protamina neutraliza totalmente tanto la actividad antitrombina de las heparinas como la actividad anti-Xa de la HNF, pero sólo parcialmente la actividad anti-Xa de la HBPM, que varía en función del compuesto estudiado (tinzaparina al 85,7%; dalteparina al 74%; fraxiparina al 57,7%, y enoxaparina al 54,2%)21.
Las contraindicaciones se describen en la tabla 8.
Tabla 8.Contraindicaciones relevantes de la heparinas
Contraindicaciones absolutas Contraindicaciones relativas - •
Alergia a heparina
- •
Trombopenia
- •
Diátesis hemorrágicas graves
- •
Procesos hemorrágicos activos
- •
Ulcus gastroduodenal activo
- •
Hipertensión grave no controlada
- •
Hemorragia intracraneal reciente
- •
Cirugía neurológica y algunos tipos de cirugía oftálmica reciente; si la evolución es correcta, reiniciar a las dos semanas
- •
Aneurisma intracerebral
- •
Retinopatía hemorrágica (dependiendo de su gravedad)
- •
Mala absorción intestinal
- •
Disminuidos psíquicos
- •
Cirugía o traumatismo reciente, según el riesgo hemorrágico
- •
Epilepsia no controlada
- •
Pericarditis con derrame
- •
Endocarditis bacteriana
- •
Pacientes con pronóstico vital infausto a corto plazo
- •
Alcoholismo activo
- •
Insuficiencia renal
- •
Insuficiencia hepática grave
- •
Gestación: últimas semanas de embarazo o posparto inmediato
- •
- b)
Anticoagulantes orales. Cumarinas. Los dos cumarínicos autorizados en España son acenocumarol y warfarina, que actúan como antagonistas de la vitamina K, impidiendo la síntesis de factores ii, vii, ix y x así como de las proteínas C y S. Su acción máxima se desarrolla a los 3–4 días y cuando se suspenden, su efecto se mantiene durante 2 días en caso de acenocumarol o de 2–5 días en caso de warfarina. El objetivo para la prevención es alcanzar un INR de 2,5 (2–3). Su farmacocinética, efectos secundarios e interacciones son de sobra conocidos y no son objeto de este artículo por limitaciones de extensión, pudiendo acudir a bibliografía de referencia para más información23. Es importante saber que cuando queramos pasar de un tratamiento subcutáneo con HBPM a cumarínicos, ambos fármacos deben administrarse de forma conjunta durante al menos 5 días, tras los que se harán controles del INR. Cuando se alcance el INR objetivo (2–3), se retirará la HBPM.
- c)
Fondaparinux. Es un inhibidor indirecto selectivo del factor xa a través de la potenciación de la antitrombina iii, que se administra de forma subcutánea en dosis de 2,5mg/día20. Se ha aprobado con la indicación, entre otras, de prevención de eventos tromboembólicos venosos (ETV) en pacientes no quirúrgicos inmovilizados considerados de alto riesgo de ETV y que han sido inmovilizados debido a una enfermedad aguda, como insuficiencia cardíaca y/o alteraciones respiratorias agudas y/o alteraciones inflamatorias o infecciosas agudas24. Es un fármaco de uso hospitalario.
- d)
Nuevos anticoagulantes. Numerosos fármacos anticoagulantes están siendo desarrollados para mejorar el perfil de seguridad y eficacia de los ya existentes. Algunos ya han sido comercializados para la prevención de la ETEV en pacientes quirúrgicos y se esperan ensayos clínicos que den resultados en profilaxis de pacientes con patología médica. Tal es el caso de ribarixabán, apixabán y dabigatrán25.
- a)
Claramente, el riesgo de ETEV no desaparece con el alta hospitalaria, pero la duración de la profilaxis en estos pacientes con patología médica permanece incierta26. En el estudio MEDENOX se mantuvo la profilaxis con HBPM durante 10±4 días, si bien se produjeron episodios poco relevantes de tromboembolia venosa varias semanas tras la suspensión de la profilaxis, lo que sugiere que el tratamiento pudo haber sido demasiado corto6. El estudio EXCLAIM (Extended Clinical Prophylaxis in Acutely ill Medical Patients) es el primero controlado y randomizado designado para evaluar la eficacia del tratamiento prolongado de profilaxis en pacientes con procesos médicos agudos inmovilizados de forma prolongada. Tras una dosis inicial de enoxaparina (40mg/día) durante una media de 10 días, los pacientes son randomizados de forma doble ciego para recibir placebo o enoxaparina durante una media de 28 días adicionales. Los resultados preliminares del estudio determinan una reducción significativa de riesgo del 44% de ETEV, el 73% en ETEV sintomática y el 34% en ETEV asintomática, sin diferencia entre grupos para todas las causas de mortalidad y con un exceso de sangrado bajo pero más frecuente en el grupo de enoxaparina (5,7%, 0,6% mayores) frente a placebo (3,8%, 0,15% mayores)27,28. Actualmente, parece apropiado recomendar una duración mínima de 10 días y mantenerla hasta que desaparezca el FR precipitante. La instauración de la profilaxis ha de establecerse de forma precoz (primeras 48h).
Estrategias para la profilaxis de la enfermedad tromboembólica venosa en el paciente ambulatorio con patología médicaLa tromboprofilaxis en AP incluye la continuación domiciliaria de la profilaxis hospitalaria en pacientes posquirúrgicos o sometidos a inmovilizaciones por procesos traumatológicos. No obstante, la población diana del presente artículo son los pacientes subsidiarios de tromboprofilaxis que sólo son valorados en el ámbito extrahospitalario; es decir, aquellos en los que la indicación de la profilaxis corresponde, en exclusiva, al médico de AP.
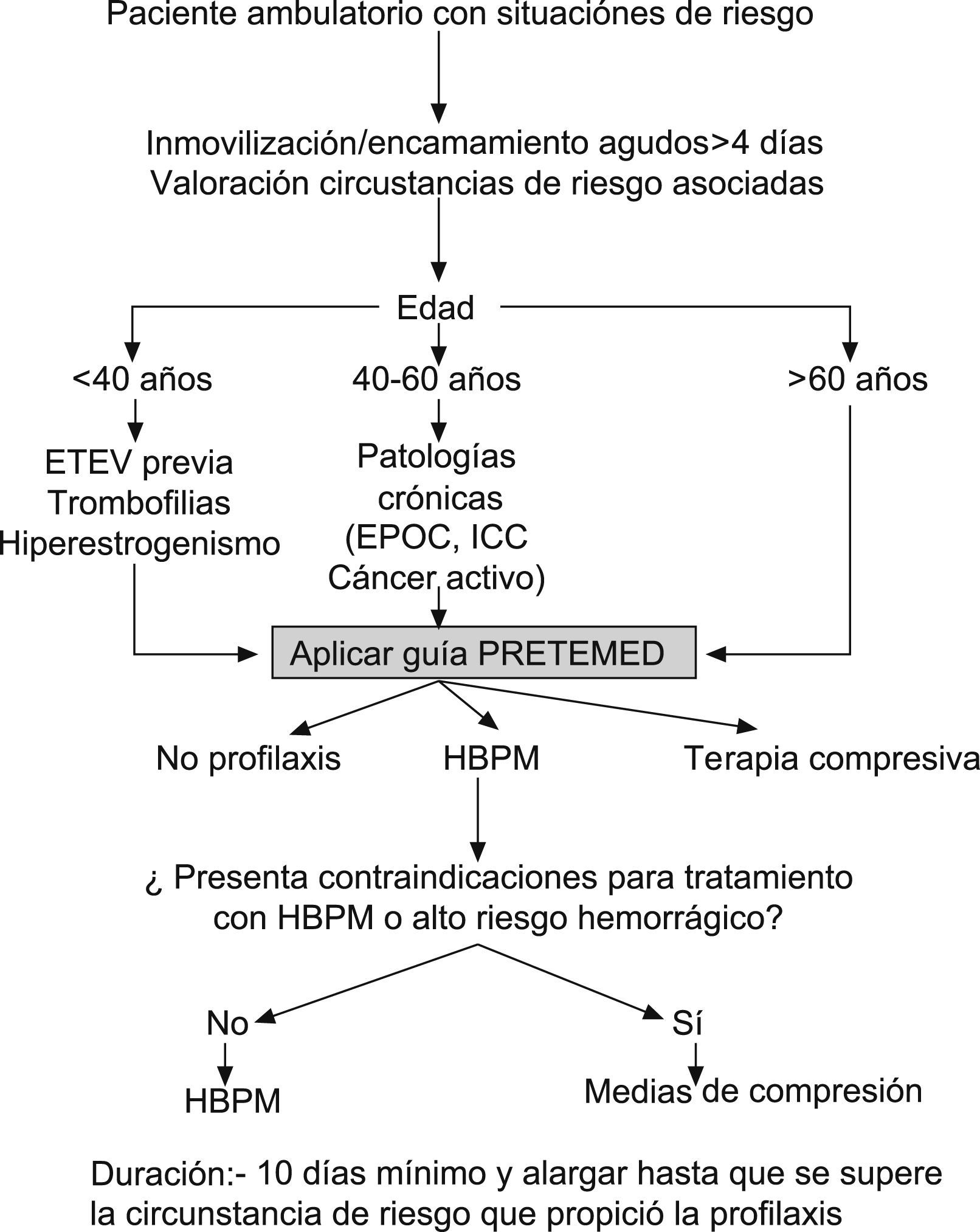
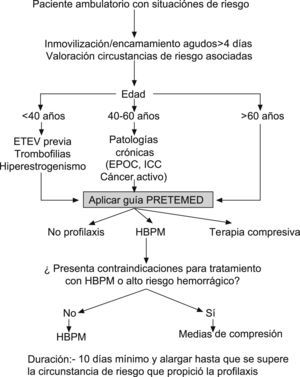
Con objeto de determinar de forma sencilla y clara los perfiles clínicos subsidiarios de tromboprofilaxis farmacológica más frecuentes en AP se propone el algoritmo de la figura 5.
El elemento inicial que plantea la posibilidad de establecer la profilaxis domiciliaria debe ser la certeza o la sospecha fundada de un encamamiento prolongado y reversible. En el ámbito extrahospitalario este hecho constituye el factor precipitante que, de forma más determinante, altera el riesgo de sufrir un posible episodio de ETEV. Las situaciones clínicas que pueden dar lugar a estados de hipercoagulabilidad de la sangre son múltiples. Las de mayor trascendencia o impacto en el ámbito de la AP, ya sea por su importancia o frecuencia, son las siguientes:
Edad. Existe un aumento lineal de la incidencia de la ETEV hasta edades muy avanzadas, con un riesgo relativo en los mayores de 60 años de 4 con respecto a los menores de esa edad. Por tanto, se recomienda que a todo paciente de más de 60 años encamado durante más de 4 días en su domicilio se le ponderen todos los FR de la ETEV y se actúe en consecuencia. En pacientes más jóvenes, la edad y el encamamiento por sí solos no justifican la profilaxis, pero el riesgo de ETEV sí se incrementa de forma evidente si el paciente es portador de ciertas patologías crónicas, por lo que ante su presencia también se recomienda la cuantificación de todos los FR. En los pacientes jóvenes, menores de 40 años, el riesgo de ETEV es muy bajo y la prevalencia de las enfermedades crónicas también, por lo que sólo estaría justificada la ponderación de todos los factores en situaciones de alto riesgo de ETEV, como lo es el antecedente de un episodio previo de TVP o TEP, o de situaciones de menor riesgo pero muy frecuentes, como los estados de hiperestrogenismo.
Patologías relacionadas con un mayor riesgo de ETEV. Son múltiples las enfermedades que se han relacionado con una mayor incidencia de ETV. Dentro de estas patologías crónicas, las descompensaciones de la insuficiencia cardíaca y la enfermedad pulmonar obstructiva crónica son las situaciones prevalentes en AP que más estrechamente se han relacionado con una mayor incidencia de ETEV. La presencia de neoplasias también constituye un FR de ETEV de grado medio, que varía en función del órgano afectado (mayor en el páncreas, el ovario, el cerebro y en linfoma; intermedio en leucemia, enfermedad renal y el estómago; menor en el cuello, la vejiga y la mama) y de otras situaciones clínicas relacionadas con la enfermedad (cirugía, empleo de quimioterapia, presencia de metástasis). En todas estas circunstancias, la profilaxis con HBPM ha demostrado una elevada eficacia.
Dentro de las patologías agudas, se ha demostrado una mayor incidencia de ETEV en los pacientes ingresados por infecciones graves, sobre todo las de origen urinario y respiratorio.
Antecedente de ETEV. La ETEV idiopática no se relaciona con la presencia de ningún FR conocido. Por lo general, suelen obedecer a la presencia de una alteración congénita o adquirida de alguna de las múltiples proteínas que intervienen en el complejo proceso de la hemostasia sanguínea. En estos casos, el riesgo de ETEV no desaparece con el tiempo, sino que se incrementa con la edad.
Estados de hiperestrogenismo. Los niveles elevados de estrógenos modifican cualitativa y cuantitativamente distintos factores de la coagulación y la fibrinólisis, que dan lugar a un estado de hipercoagulabilidad. Por tanto, todas las situaciones que, de forma fisiológica, patológica o terapéutica, cursan con niveles elevados de estrógenos se asocian con un mayor riesgo de padecer un evento tromboembólico. A pesar de ser la TEP una de las primeras causas de muerte durante la gestación, en términos absolutos la ETEV es poco frecuente en el embarazo; no obstante, su incidencia aumenta significativamente en el puerperio y cuando se asocian otros FR (trombofilia, amenaza de parto prematuro con reposo prolongado, presencia de varices y edad mayor de 35 años). El tratamiento hormonal sustitutivo y los anticonceptivos hormonales microdosis tienen un efecto trombogénico bajo si no se asocian a otros FR; no obstante, sí se ha documentado una mayor incidencia de ETEV en mujeres que toman anticonceptivos con gestágenos de tercera generación (desogestrel y gestodeno) respecto de las que emplean levonorgestrel, en obesas, en fumadoras y en portadoras de trombofilias (siendo la más frecuente la presencia del factor v Leiden).
Otras enfermedades reconocidas como procesos asociados a la ETEV, pero no indicadoras por sí mismas de tromboprofilaxis, son la diabetes mellitus, la hiperhomocisteinemia, la infección por el VIH o la presencia de una trombosis venosa superficial. Todos estos procesos deberán ser cuantificados en un paciente determinado, pero no son puntos críticos a la hora de establecer la profilaxis.
Una vez decidida la tromboprofilaxis, ésta debe ser instaurada en las primeras 48h. Todavía no está totalmente definida la duración óptima de la profilaxis en los pacientes encamados por causa médica. Los últimos datos apuntan a que ésta debería ser más prolongada tanto en los pacientes quirúrgicos como en los ingresados por causa médica, por lo que, hasta que no se disponga de datos más concluyentes, se recomienda mantenerla hasta que no esté totalmente superada la situación de riesgo.
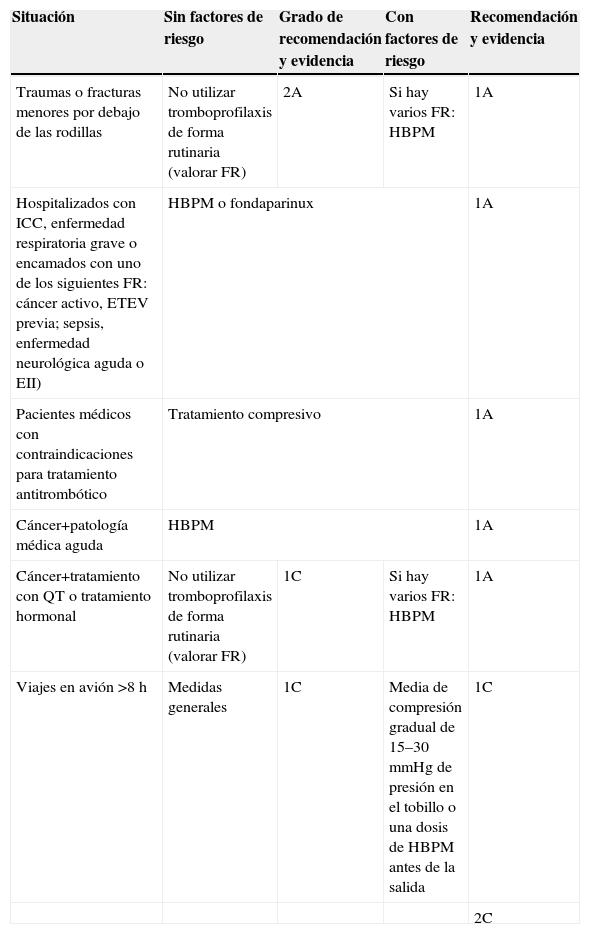
En la tabla 9 se describen las últimas recomendaciones en situaciones no quirúrgicas según Geerts et al4.
Directrices para el establecimiento de la profilaxis en la enfermedad tromboembólica venosa según Geerts et al4
| Situación | Sin factores de riesgo | Grado de recomendación y evidencia | Con factores de riesgo | Recomendación y evidencia |
| Traumas o fracturas menores por debajo de las rodillas | No utilizar tromboprofilaxis de forma rutinaria (valorar FR) | 2A | Si hay varios FR: HBPM | 1A |
| Hospitalizados con ICC, enfermedad respiratoria grave o encamados con uno de los siguientes FR: cáncer activo, ETEV previa; sepsis, enfermedad neurológica aguda o EII) | HBPM o fondaparinux | 1A | ||
| Pacientes médicos con contraindicaciones para tratamiento antitrombótico | Tratamiento compresivo | 1A | ||
| Cáncer+patología médica aguda | HBPM | 1A | ||
| Cáncer+tratamiento con QT o tratamiento hormonal | No utilizar tromboprofilaxis de forma rutinaria (valorar FR) | 1C | Si hay varios FR: HBPM | 1A |
| Viajes en avión >8h | Medidas generales | 1C | Media de compresión gradual de 15–30mmHg de presión en el tobillo o una dosis de HBPM antes de la salida | 1C |
| 2C | ||||
EII: enfermedad inflamatoria intestinal; ETEV: enfermedad tromboembólica venosa; FR: factores de riesgo; HBPM: heparina de bajo peso molecular; ICC: insuficiencia cardíaca crónica; QT: quimioterapia.
- 1.
La ETEV constituye una enfermedad de alta incidencia y morbimortalidad.
- 2.
La mejor forma de evitar la carga sociosanitaria de la ETEV es la profilaxis adecuada.
- 3.
Los pacientes con patología médica y otros FR presentan mayor riesgo de padecer una ETEV que los quirúrgicos o traumatológicos. Además, los episodios suelen presentar un peor pronóstico.
- 4.
El paciente encamado por causa médica en su domicilio posee un riesgo de ETEV similares al hospitalario.
- 5.
La guía PRETEMED permite ponderar de forma individual el riesgo de ETV y establece recomendaciones de profilaxis cuando el riesgo es alto.
- 6.
El médico de AP es el responsable de la ponderación del riesgo de ETV en los pacientes extrahospitalarios, y debe implementar la profilaxis cuando esté indicada.
- 7.
Se puede establecer un perfil de riesgo tributario de profilaxis que debe ser reconocido de forma sencilla por el médico de AP (fig. 5).
- 8.
La seguridad y eficacia de las HBPM ha sido establecida en numerosos ensayos clínicos en el ámbito de la AP.
- 9.
Faltan estudios para el establecimiento definitivo de la eficacia de la tromboprofilaxis en el ámbito de la AP.